吳茱萸堿磷脂復合物自乳化藥物遞送系統的制備、表征及胃黏膜滲透性研究
宋朔堯 楊貴前 陶玲 沈祥春 張環 李和蓉 王守莉 石惠云 劉文







中圖分類號 R944 文獻標志碼 A 文章編號 1001-0408(2022)09-1056-06
DOI 10.6039/j.issn.1001-0408.2022.09.06
摘 要 目的 制備吳茱萸堿磷脂復合物自乳化藥物遞送系統(EVO-PC-SMEDDS),并對其進行表征及胃黏膜滲透性考察。方法 制備EVO-PC-SMEDDS,檢測其粒徑、多分散系數(PDI)和Zeta電位,并進行顯微觀察。考察該制劑在不同pH(1.2、2.0、4.0、7.0)模擬胃液中的穩定性。測定該制劑的包封率和載藥量,并進行體外釋放考察。將大鼠胃黏膜組織和尤斯灌流室技術相結合,考察該制劑的胃黏膜滲透性。結果 EVO-PC-SMEDDS的粒徑為(53.63±1.51) nm、PDI為0.217±0.017、Zeta電位為(-12.20±0.15) mV、包封率為(95.25±0.97)%、載藥量為(19.30±1.21) mg/g。在透射電子顯微鏡下,EVO-PC-SMEDDS呈大小均勻的類球形乳滴。穩定性實驗結果顯示,EVO-PC-SMEDDS在不同pH的模擬胃液中,粒徑、PDI、Zeta電位均無明顯變化,穩定性良好。體外釋放實驗結果顯示,與吳茱萸堿(EVO)原料藥比較,EVO-PC-SMEDDS的體外累積釋放率提高了6.83倍,符合一級動力學釋放模型。胃黏膜滲透性實驗結果顯示,EVO-PC-SMEDDS的累積滲透轉運量、滲透速率、滲透通量及累積滲透曲線下面積均高于EVO原料藥。結論 本研究成功制得EVO-PC-SMEDDS,且該制劑穩定性良好,可明顯改善EVO的體外釋放行為和胃黏膜滲透性。
關鍵詞 自乳化藥物遞送系統;吳茱萸堿;表征;胃黏膜;釋放
Preparation,characterization and gastric mucosal permeability of evodiamine phospholipid complex self- microemulsifying drug delivery system
SONG Shuoyao1,2,YANG Guiqian1,2,TAO Ling1,2,SHEN Xiangchun1,2,ZHANG Huan1,2,LI Herong1,2,WANG Shouli1,2,SHI Huiyun1,2,LIU Wen1(1. School of Pharmacy,Guizhou Medical University,Guiyang 550025,China;2. Guizhou Province Key Laboratory for Optimal Utilization of Natural Medicine Resources, Guiyang 550025, China)
ABSTRACT ? OBJECTIVE To prepare and characterize evodiamine phospholipid complex self-microemulsifying drug delivery system (EVO-PC-SMEDDS), and to investigate its gastric mucosal permeability. METHODS EVO-PC-SMEDDS was prepared, and particle size, polydispersity (PDI) and Zeta potential were tested,and microscopic observation was carried out. The stability of EVO-PC-SMEDDS in simulated gastric liquid with different pH (1.2, 2.0, 4.0, 7.0) was investigated. The entrapment efficiency and drug-loading amount of the preparation were determined, and the in vitro release was investigated. The gastric mucosal permeability of EVO-PC-SMEDDS was studied by combining rat gastric mucosal tissue and Ussing Chamber technology. RESULTS The particle size of EVO-PC-SMEDDS was (53.63±1.51) nm, PDI and Zeta potential were 0.217±0.017 and ? ? ? ? (-12.20±0.15) mV, entrapment efficiency was (95.25±0.97)% and drug-loading amount was (19.30±1.21) mg/g. EVO-PC- SMEDDS exhibited a uniformly dispersed round spherical shape under transmission electron microscope. Stability experiments showed that EVO-PC-SMEDDS exhibited no significant change in particle size,PDI and Zeta potential under the simulated gastric fluid with different pH and showed excellent stability. Results of in vitro release test showed that compared with evodiamine (EVO), in vitro accumulative release of EVO-PC-SMEDDS were enhanced 6.83-fold, which was in line with the first-order kinetic release model. Results of gastric mucosal permeability showed that gastric mucosal permeation transport,permeation rate,permeation flux and area under curve of cumulative permeability of EVO-PC-SMEDDS were higher than those of EVO,respectively. CONCLUSIONS EVO-PC-SMEDDS is prepared successfully and shows good stability. It could significantly improve the release behavior and gastric mucosal permeability of EVO.
KEYWORDS ? self-microemulsifying drug delivery system;evodiamine; characterization; gastric mucosal; release
口服遞送給藥是治療慢性胃炎、胃潰瘍和胃癌等胃部疾病最有效的給藥方式。但患者年齡、胃部結構、給藥時間等因素會影響胃酸分泌,引起胃液酸度波動,導致藥物的胃內穩定性差[1]。此外,胃黏膜屏障也會阻礙藥物滲透,減少藥物在胃部病灶部位的富集[2]。因此,在復雜的胃內環境中,藥物常規劑型的治療效果往往不太理想。
吳茱萸堿(evodiamine,EVO)是從中藥吳茱萸中提取分離出來的吲哚生物堿,也是治療“肝火犯胃證”的經典名方左金丸的藥效物質基礎之一[3]。現代藥理研究表明,EVO具有鎮痛抗炎、抗菌、抗腫瘤、抗胃潰瘍、保護胃黏膜等多重藥理活性,尤其對胃部疾病的治療效果顯著;但其水溶性極差,口服生物利用度低,體內消除迅速,按生物藥劑學分類系統(biopharmaceutics classification system,BCS)分類屬于Ⅳ類藥物(即低溶解度、低滲透性類藥物)[4]。
自乳化藥物遞送系統(self-microemulsifying drug delivery system,SMEDDS)是由油相、乳化劑和助乳化劑組成的液體制劑,口服后經胃液分散可自發乳化形成粒徑小于100 nm的乳滴,被廣泛應用于BCS Ⅲ類和Ⅳ類藥物的口服遞送[5]。SMEDDS粒徑小、吸收表面積大,且具有良好的黏膜滲透性和生物相容性,特別有利于藥物的跨胃黏膜遞送[6]。此外,SMEDDS的油相可提高難溶性藥物的溶解度,并通過增強藥物的旁路轉運,避免首過效應[7]。研究表明,自乳化形成油水界面屏障可以保護藥物免受胃酸的破壞,在增加藥物穩定性的同時還可降低藥物的刺激性,且SMEDDS可通過降低表面張力和改變上皮細胞連接緊密度來增加藥物的膜滲透性[8]。相關研究發現,磷脂復合物(phospholipid complexes,PC)和SMEDDS中的脂質成分均與人消化道上皮細胞的細胞膜成分相似,因此,將PC和SMEDDS結合可進一步提高難溶性藥物的穩定性、載藥量和跨生物膜轉運,減少藥物的消除以延長作用時間并提高口服生物利用度[9-10]。因此,本研究擬制備吳茱萸堿磷脂復合物自乳化藥物遞送系統(EVO-PC-SMEDDS),并以粒徑、多分散系數(polydispersity index,PDI)和Zeta電位為指標,評價其在胃內的穩定性及釋放行為;另外,將大鼠胃黏膜組織和尤斯灌流室技術相結合[11-13],研究該制劑的胃黏膜滲透性,以期為胃部疾病治療藥物的開發提供參考。
1 材料
1.1 主要儀器
本研究所用主要儀器包括VWD/1260 Infinity ⅡPrime型液相色譜系統(美國Agilent公司)、Nano-brook 90Plus PALS型 Zeta電位及粒度分析儀(美國Brookhaven Instruments公司)、UPW-UP-10型純水儀(四川成都天莘寧科技有限公司)、EO-CVUC型尤斯灌流系統(北京金工鴻泰科技有限公司)、ME104/02型電子天平(瑞士Mettler Toledo公司)、HB ECO S096型旋轉蒸發儀(德國IKA公司)、JEM-1400PLUS型透射電子顯微鏡(日本JEOL公司)。
1.2 主要藥品與試劑
本研究所用主要藥品與試劑有15-羥基硬脂酸聚乙二醇酯(HS15,德國BASF公司,批號20189322),聚山梨酯80(國藥集團化學試劑有限公司,批號20191211),油酸乙酯、卵磷脂(上海阿拉丁生化科技股份有限公司,批號分別為G1508008、20195724),EVO原料藥(成都德思特生物技術有限公司,質量分數≥98%,批號2018061321),EVO對照品(中國食品藥品檢定研究院,批號110802-201606,純度99.6%),甲醇(美國TEDIA公司,色譜級);其余試劑為實驗室常用規格,水為雙蒸水。
1.3 動物
本研究所用動物為SPF級雄性SD大鼠,體質量(200±20) g,由貴州醫科大學動物中心提供,實驗動物生產許可證號為SCXK(黔)2021-0021。本研究動物實驗方案經貴州醫科大學動物倫理委員會批準通過(編號1900154)。
2 方法與結果
2.1 EVO-PC-SMEDDS的制備
2.1.1 EVO-PC的制備 在實驗室前期研究和已有的文獻基礎上進行改進,采用溶劑揮發法制備EVO-PC[14-15]。將2.0 g EVO原料藥與2.0 g 卵磷脂置于50 mL乙醇-四氫呋喃(1 ∶ 1,V/V)混合有機溶液中進行復合反應,反應溫度為55 ℃,時間為3 h;反應結束后,采用旋轉蒸發儀減壓回收有機溶劑,并將殘余混合物于真空條件下冷凍干燥48 h;將干燥后的混合物加入150 mL氯仿中復溶,直至其完全溶解,再抽濾過0.22 μm有機膜以去除未復合的雜質;所得濾液采用旋轉蒸發儀減壓回收氯仿,再于真空條件下冷凍干燥48 h,即得EVO-PC。本研究所制EVO-PC的外觀均勻,復合率為95.8%;于-20 ℃條件下保存30 d后再次復溶,亦無沉淀析出,表明EVO-PC的穩定性良好。
2.1.2 EVO-PC-SMEDDS的制備 根據實驗室前期研究優化后的處方[16],固定SMEDDS總質量為1 g,其中油酸乙酯25%(油相),聚山梨酯80和HS15組成的混合乳化劑(兩者質量比為2 ∶ 1)55%,無水乙醇(助乳化劑)20%。然后將EVO-PC(總質量40 mg)加入SMEDDS中,超聲(功率300 W,頻率40 kHz,下同)30 min助溶,再置于37 ℃水浴條件下攪拌,直至獲得穩定的透明液體,即得EVO-PC-SMEDDS。本研究所制EVO-PC-SEDDS的外觀澄清透明,略帶淡藍色乳光;于室溫條件下放置7 d后,仍無沉淀、轉相和渾濁現象,表明EVO-PC- SMEDDS的穩定性良好。
2.2 EVO-PC-SMEDDS的表征
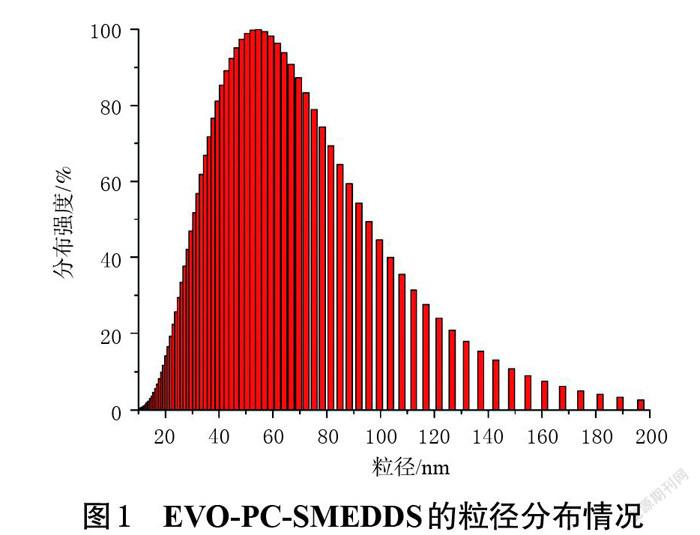
2.2.1 EVO-PC-SMEDDS的粒徑及Zeta電位 取適量EVO-PC-SMEDDS加水稀釋100倍,使用Zeta電位及粒度分析儀測定其粒徑及Zeta電位,實驗平行3次。結果顯示,EVO-PC-SMEDDS粒徑分布均勻,粒徑為(53.63±1.51) nm,RSD為1.25%(n=3);PDI為0.217±0.017,RSD為2.06%(n=3);Zeta電位為(-12.20±0.15)mV,RSD為1.38%(n=3)。EVO-PC-SMEDDS的粒徑分布情況見圖1。
2.2.2 EVO-PC-SMEDDS的顯微觀察 取適量EVO- PC-SMEDDS置于銅網上,加入5%磷鎢酸溶液染色5 min,風干后置于透射電子顯微鏡下觀察。結果顯示,EVO-PC-SMEDDS為大小均勻的類球形乳滴,詳見圖2。
2.3 EVO-PC-SMEDDS的胃內穩定性考察
將EVO-PC-SMEDDS分散于不同pH(pH值根據人胃酸的動態變化范圍設置[11-13])的模擬胃液中,以考察其在胃內的穩定性。具體方法如下:稱取胃蛋白酶3.2 g、NaCl 2.0 g溶于1 000 mL水中,平行制備4份,分別使用鹽酸調節pH為1.2、2.0、4.0、7.0,即得不同pH的模擬胃液。將“2.1.2”項下制得的EVO-PC-SMEDDS分散于上述模擬胃液中,室溫靜置24 h后,采用Zeta電位及粒度分析儀分析其粒徑、PDI、Zeta電位的變化情況,實驗平行3次。結果顯示,EVO-PC-SMEDDS在模擬胃液中粒徑為50.12~58.08 nm,PDI為0.220~0.250,Zeta電位為-16.43~-11.98 mV。由此可知,EVO-PC-SMEDDS在不同pH的模擬胃液中,粒徑、PDI和Zeta電位均無顯著變化。結果見圖3、圖4。
2.4 EVO-PC-SMEDDS的包封率、載藥量和體外釋放考察
2.4.1 色譜條件 色譜柱為Agilent ZORBAX XDB-C18(250 mm×4.6 mm,5 μm);流動相為甲醇-水(75 ∶ 25, ? ? V/V);檢測波長為225 nm;流速為1.0 mL/min;柱溫為30 ℃;進樣量為20 μL[17]。
2.4.2 溶液的制備 (1)對照品溶液:精密稱取EVO對照品10.0 mg,置于50 mL量瓶中,以甲醇溶解并定容,即得EVO質量濃度為200 μg/mL的對照品溶液。(2)供試品溶液:取EVO-PC-SMEDDS適量,置于10 mL量瓶中,加入適量甲醇超聲破乳并定容,過0.22 μm微孔濾膜后,即得供試品溶液。
2.4.3 標準曲線的繪制 精密量取“2.4.2”項下對照品溶液適量,以甲醇稀釋定容,分別制成EVO質量濃度為0.4、1.0、2.0、5.0、10.0、20.0 μg/mL的系列溶液,然后按“2.4.1”項下色譜條件進樣分析。以峰面積為縱坐標(y)、EVO質量濃度為橫坐標(x),進行線性回歸,得回歸方程y=102.31x-11.52(R2=0.999 9),EVO的檢測質量濃度線性范圍為0.4~20.0 μg/mL。
2.4.4 精密度試驗 精密量取“2.4.3”項下質量濃度為0.4、5.0、20 μg/mL的EVO對照品溶液適量,每個樣品分別連續進樣6次,按“2.4.1”項下色譜條件進樣分析,計算日內精密度RSD;重復操作2 d,計算日間精密度RSD。結果顯示,上述3種樣品中EVO峰面積的日內精密度和日間精密度的RSD均小于2%(n=6),表明該方法精密度良好。
2.4.5 重復性試驗 精密量取同一批次的EVO-PC- SMEDDS適量,按“2.4.2”項下方法平行制備6份供試品溶液,按“2.4.1”項下色譜條件進樣分析,記錄峰面積,并根據標準曲線計算EVO含量。結果顯示,EVO-PC- SMEDDS中EVO的平均含量為196.4 μg/mL,RSD為0.72%(n=6),表明該方法的重復性良好。
2.4.6 穩定性試驗 精密量取“2.4.2”項下供試品溶液適量,于室溫放置0、2、6、8、12、24、36、48 h后,按“2.4.1”項下色譜條件進樣分析,記錄峰面積。結果顯示,EVO峰面積的RSD均小于2%(n=8),表明供試品溶液在室溫放置48 h內的穩定性良好。
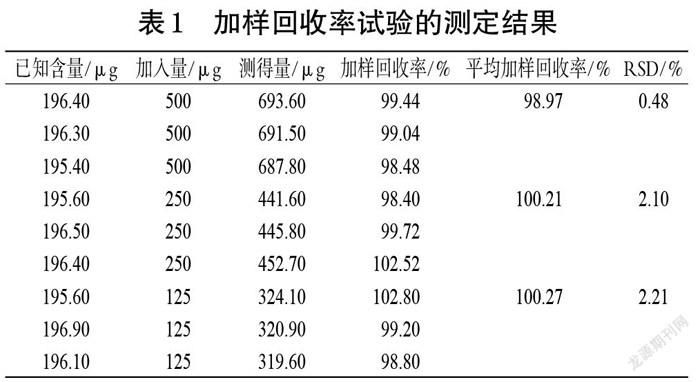
2.4.7 加樣回收率試驗 精密量取“2.4.2”項下已知EVO含量的供試品溶液,共9份,置于50 mL量瓶中,分為3組;每組分別加入“2.4.2”項下EVO對照品溶液 2.5、1.25、0.625 mL,然后加甲醇定容,按“2.4.1”項下色譜條件進樣分析,并計算加樣回收率。結果顯示,EVO的平均加樣回收率為98.97%~100.27%,RSD為0.48%~2.21%(n=3),結果見表1。
2.4.8 EVO-PC-SMEDDS載藥量和包封率的測定 采用超濾離心法測定EVO-PC-SMEDDS的載藥量和包封率[18]。分別精密量取EVO-PC-SMEDD 1 mL于超濾管內(截留相對分子質量為50 000 Da),以3 500 r/min離心30 min,取超濾液,按“2.4.1”項下色譜條件進樣分析,并計算EVO的含量(Wfree)。另取EVO-PC-SMEDDS適量,置于10 mL量瓶中,加適量甲醇超聲破乳并定容,再按“2.4.1”項下色譜條件進樣分析,計算EVO的含量(Wadd)。根據公式計算EVO-PC-SMEDDS的載藥量和包封率。其中,包封率(%)=(Wadd-Wfree)/Wadd×100,載藥量(%)=(Wadd-Wfree)/Wall×100(Wall表示EVO-PC-SMEDDS的總質量)。結果顯示,EVO-PC-SMEDDS的載藥量為(19.30±1.21) mg/g,包封率為(95.25±0.97)%。
2.4.9 EVO-PC-SMEDDS的體外釋放考察 以0.1 mol/L鹽酸溶液為釋放介質,采用動態透析法進行EVO-PC- SMEDDS體外釋放考察[19]。取EVO原料藥適量,以空白釋放介質制成EVO混懸液。分別取EVO混懸液和EVO-PC-SMEDDS適量(EVO含量均為2 mg),置于透析袋(截留相對分子質量為35 000 Da)中,兩端扎緊;然后分別置于100倍體積的釋放介質中(加入10%無水乙醇助溶),于37.0 ℃、100 r/min恒溫振蕩器中振蕩0、1、2、4、6、8、16、24、48 h后取樣(同時補充同溫等量的釋放介質)。將取樣液過0.22 μm微孔濾膜,取續濾液按“2.4.1”項下色譜條件進樣分析,根據標準曲線計算EVO的含量,并計算累積釋放率,繪制累積釋放曲線(見圖5);利用Origin 9.0軟件擬合EVO-PC-SMEDDS的體外釋放模型(見表2)。
由圖5可知,與EVO原料藥相比,EVO-PC- SMEDDS的體外累積釋放率提高了6.83倍;EVO-PC- SMEDDS在4 h時的累積釋放率為80.16%,遠高于EVO原料藥(累積釋放率為14.56%)。由表2可知,EVO- PC-SMEDDS一級動力學釋放模型的R2值為0.975 2,相較于其他模型,其擬合度更好、可信度更高。這提示該制劑在胃液中的釋放更符合一級動力學模型。
2.5 EVO-PC-SMEDDS體外胃黏膜滲透性實驗
2.5.1 胃黏膜滲透裝置的構建 實驗前將3只大鼠禁食不禁水12 h,用異氟烷麻醉后處死,取出胃,并沿外側胃大彎剖開,收集胃內容物;將胃內側朝上展開固定在手術臺上,用37 ℃生理鹽水清洗干凈后,先向胃黏膜層淺層帶與胃肌固有層中間注射適量生理鹽水(以形成水墊,便于兩層剝離),再用微型手術刀分離得到大鼠胃黏膜層。將大鼠胃黏膜層無縫隙地嵌入夾片中,插入尤斯灌流室的中間槽,備用。另外,將上述胃內容物置于離心管中,以2 000 r/min離心10 min,取上清液,備用。
2.5.2 體外胃黏膜滲透性實驗 分別在尤斯灌流室的供體室和接受室中加入胃內容物上清液與磷酸鹽緩沖液的混合溶液(體積比為1 ∶ 1)10 mL作為釋放介質,并加入10%無水乙醇助溶;將溫度維持在37 ℃,以模擬胃內環境。將兩室通入95%O2和5%CO2混合氣體以模擬胃蠕動,平衡后,在供體室中分別加入EVO原料藥混懸液和EVO-PC-SMEDDS溶液(EVO含量均為0.2 mg);于1、2、4、6、8 h時,在接收室中取1 mL樣品(同時補充同溫等量介質),置于10 mL量瓶中,加適量甲醇超聲溶解并定容,再按“2.4.1”項下色譜條件進樣分析,計算各時間點的藥物質量濃度(Cn)。按公式(1)(2)(3)分別計算EVO的胃黏膜累積滲透轉運量(Qn)、滲透通量(F)和滲透速率(S),并利用Origin 9.0軟件計算EVO的累積滲透曲線下面積(AUC0-8 h)[20-21]。
Qn=(10Cn+[∑][i=1][n-1]Ci)/A…(1)
F=Qn/h…(2)
S=(10Cn+[∑][i=1][n-1]Ci)/h…(3)
上述公式中,Cn為第n個取樣時間點的藥物質量濃度(μg/mL),Ci為第i個取樣時間點的藥物質量濃度(μg/mL),A為胃黏膜通過面積(本研究取1.25 cm2)。
結果如圖6A所示,EVO-PC-SMEDDS 8 h的Qn為106.33 μg/cm2,遠高于EVO原料藥的28.93 μg/cm2。圖6B顯示,EVO-PC-SMEDDS的S在2 h時即到達最高點(27.12 μg/h),為EVO原料藥的11.4倍。此外,EVO- PC-SMEDDS的F和AUC0-8 h分別為12.69 μg/(cm2·h)和24.30 μg·h/mL,為EVO原料藥的7.01倍和3.64倍。由此可知,EVO-PC-SMEDDS具有較高的胃黏膜滲透速率,提示該制劑可增加EVO在胃部的吸收。
3 討論
片劑、膠囊劑等常規劑型受胃酸、胃黏膜屏障以及胃排空效應的影響,故而對胃部疾病治療藥物的遞送作用有限[22]。同時,常見的胃部疾病治療藥物(如胃黏膜保護劑、抑酸劑和抗幽門螺桿菌藥物等)也存在體內非特異性分布、溶解度低和生物利用度差等問題[23]。SMEDDS由于粒徑小、生物相容性好以及黏膜滲透性強,從而具備增強藥物治療效果的潛力[6]。
本研究在前期研究的基礎上,將磷脂復合物與自乳化技術相結合,制得EVO-PC-SMEDDS,從而克服了EVO溶解度低的缺點。EVO-PC-SMEDDS的粒徑為(53.63±1.51) nm、PDI為0.217±0.017、Zeta電位為 ? (-12.20±0.15)mV;進一步顯微觀察發現,該制劑為大小均勻的類球形乳滴。以粒徑、PDI和Zeta電位為評價指標,考察該制劑的穩定性,結果發現,EVO-PC- SMEDDS在不同pH模擬胃液中粒徑、Zeta 電位和PDI均無顯著變化,這表明該制劑可在胃內均勻分散,且能保持結構穩定。
由于EVO是水溶性極差的藥物,因此進行EVO- PC-SMEDDS體外釋放考察時,在釋放介質中加入10%乙醇來助溶。結果顯示,EVO-PC-SMEDDS的體外累積釋放率遠高于EVO原料藥,這表明該制劑可改善EVO的溶解性。
胃黏膜屏障是胃部疾病特異性遞送的難題之一,通過功能化的遞送材料來提高藥物的胃黏膜滲透能力,是實現胃部深層病灶靶向遞藥的有效手段[24]。本研究將大鼠胃黏膜組織和尤斯灌流室技術相結合,建立了EVO-PC-SMEDDS體外胃黏膜滲透轉運模型。結果顯示,EVO-PC-SMEDDS的胃黏膜Qn、F、S和AUC0-8 h均高于EVO原料藥,具有較強的胃黏膜滲透能力。
綜上所述,本研究成功制得了EVO-PC-SMEDDS;該制劑穩定性較好,可明顯改善EVO的釋放行為和胃黏膜滲透性。
參考文獻
[ 1 ] CAI X Q,XU Y T,ZHAO L N,et al. In situ pepsin-assis- ted needle assembly of magnetic-graphitic-nanocapsules for enhanced gastric retention and mucus penetration[J]. Nano Today,2021,36:101032.
[ 2 ] ANGEL L,FRANCIS K C. Peptic ulcer disease[J]. The Lancet,2017,390(10094):613-624.
[ 3 ] 李艷英,黃能聽,韓馥蔓,等.左金丸的古代文獻分析[J/OL].中國實驗方劑學雜志,2022[2022-03-22]. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname= CAPJLAST&filename=ZSFX20210811000&uniplatform=NZKPT&v=ZoxzmtHRskyq5dwUEd9F87v9kzHgqxHsyR_ QNqlUnOpm_zF56DXOOqHt95Ol0ZFM. DOI:10.13422/j.cnki.syfjx.20211854.
[ 4 ] SUN Q,XIE L,SONG J W,et al. Evodiamine:a review of its pharmacology,toxicity,pharmacokinetics and preparation researches[J]. J Ethnopharmacol,2020,262:113164.
[ 5 ] MAHMOOD A,BERNKOP-SCHNüRCH A. SEDDS:a game changing approach for the oral administration of hydrophilic macromolecular drugs[J]. Adv Drug Deliv Rev,2019,142:91-101.
[ 6 ] ABDULKARIM M,SHARMA P K,GUMBLETON M. Self-emulsifying drug delivery system:mucus permeation and innovative quantification technologies[J]. Adv Drug Deliv Rev,2019,142:62-74.
[ 7 ] 馬巧芳,曾佳,沙康,等.口服自微乳給藥系統的研究進展[J].藥學進展,2020,44(6):466-475.
[ 8 ] XIA F,CHEN Z J,ZHU Q G,et al. Gastrointestinal lipolysis and trans-epithelial transport of SMEDDS via oral route[J]. Acta Pharm Sin B,2021,11(4):1010-1020.
[ 9 ] NOURAEI M,COLLYMORE C,DIOSADY L,et al. HLD-NAC design and evaluation of a fully dilutable lecithin-linker SMEDDS for ibuprofen[J]. Int J Pharm,2021,610:121237.
[10] WU H Y,LONG X Y,YUAN F,et al. Combined use of phospholipid complexes and self-emulsifying microemulsions for improving the oral absorption of a BCS class Ⅳ compound,baicalin[J]. Acta Pharm Sin B,2014,4(3):217-226.
[11] MAMADOU G,CHARRUEAU C,DAIROU J,et al. Increased intestinal permeation and modulation of presystemic metabolism of resveratrol formulated into self-emulsifying drug delivery systems[J]. Int J Pharm,2017,521(1/2):150-155.
[12] BABADI D,DADASHZADEH S,OSOULI M,et al. Nanoformulation strategies for improving intestinal permeability of drugs:a more precise look at permeability assessment methods and pharmacokinetic properties changes
[J]. J Control Release,2020,321:669-709.
[13] 胡詠梅,張珊珊,張磊,等. Ussing chamber技術評價P-糖蛋白及有機陽離子轉運體對左氧氟沙星跨胃黏膜轉運的影響[J].中國臨床藥理學雜志,2015,31(17):1732- 1735.
[14] 柳珊,譚群友,王紅,等.吳茱萸堿磷脂復合物的制備、表征及體外抗腫瘤活性的研究[J].中國藥學雜志,2012,47(7):517-523.
[15] 王益,李婉蓉,楊佳佳,等.氧化苦參堿磷脂復合物自乳化釋藥系統的研制[J].中草藥,2018,49(18):4277-4283.
[16] JIANG F,WU G P,LI W R,et al. Preparation and protective effects of 1,8-cineole-loaded self-microemulsifying drug delivery system on lipopolysaccharide-induced endothelial injury in mice[J]. Eur J Pharm Sci,2019,127:14-23.
[17] 楊婕,劉宏明,陳云,等.吳茱萸堿脂質納米粒的藥代動力學和在體腸吸收特性研究[J].中國藥科大學學報,2020,51(6):696-701.
[18] TIMUR S S,Y?YEN-ERMI? D,ESENDA?LI G,et al. Efficacy of a novel LyP-1-containing self-microemulsi- ?fying drug delivery system(SMEDDS)for active targeting to breast cancer[J]. Eur J Pharm Biopharm,2019,136:138-146.
[19] 楊佳佳,韋世權,李婉蓉,等.星點設計-效應面法優化丹皮酚脂微球處方工藝及其體外釋藥機制研究[J].中草藥,2020,51(15):3901-3910.
[20] 陳蓓,文麗梅,鞏月紅,等.基于Ussing Chamber技術評價阿苯達唑納米晶體在大鼠不同腸段的吸收特性[J].中國醫院藥學雜志,2021,41(12):1192-1196.
[21] 朱蘊,顧星,張兵,等.基于尤斯灌流室技術的澤瀉湯大鼠腸吸收研究[J].天津中醫藥大學學報,2017,36(4):299- 302.
[22] ALEXANDER A,AJAZUDDIN,PATEL R J,et al. Recent expansion of pharmaceutical nanotechnologies and targeting strategies in the field of phytopharmaceuticals for the delivery of herbal extracts and bioactives[J]. J Control Release,2016,241:110-124.
[23] YAN X M,HUANG Z C,WU Y Y,et al. Sequential loa- ding of inclusion complex/nanoparticles improves the ? gastric retention of Vladimiriae Radix essential oil to ? ?promote the protection of acute gastric mucosal injury[J]. Int J Pharm,2021,610:121234.
[24] O’NEIL D H R,LEONARD A. Gastric disorders:modifications of gastric content,antacids and drugs influencing gastric secretions and motility[J]. Anaesth Intensive Care Med,2012,13(2):67-70.
(收稿日期:2021-12-23 修回日期:2022-03-24)
(編輯:唐曉蓮)

