植物細胞內膜運輸調控機制及相關前沿電子顯微鏡技術應用的研究進展
李彥斌,齊 青,鄭曉慧,徐一月,崔 勇*
(1.廈門大學生命科學學院,細胞應激生物學國家重點實驗室,福建 廈門 361102;2.香港中文大學生命科學學院,香港 999077)
與大多數真核細胞一樣,植物細胞含有一套由核膜、細胞膜以及多種細胞器組成的內膜系統,包括內質網(ER)、高爾基體(Golgi)、反式高爾基體網絡(TGN)、液泡前體/多囊泡體(PVC/MVB)、液泡和自噬體等.蛋白質等物質在植物細胞內經該內膜系統運輸,完成細胞內物質及信息的傳遞和交換;同時,精確和高效的物質運輸對生物體的正常生長發育和環境應答都十分重要,因此了解掌握植物蛋白在細胞內運輸的調控機制顯得尤為關鍵[1].
蛋白質在不同細胞器之間的運輸主要經囊泡介導,而這些囊泡大部分直徑都小于200 nm,用普通光學顯微鏡無法清晰觀察,這令此領域研究者長期在一些關鍵問題上存在爭議[2].而隨著電子顯微鏡技術的發展,這些精細的物質運輸過程逐漸得以呈現,不僅幫助厘清了此領域中一些長期存在的爭議,還讓研究者們發現了全新的運輸模式,極大地推動了內膜運輸在植物細胞研究中的進展.本文重點闡述當前植物蛋白運輸途徑的研究成果,結合近期研究展示前沿電子顯微鏡技術在植物細胞內膜運輸研究中的應用,并對本領域研究存在的機遇與挑戰進行展望.
1 植物細胞內囊泡介導的蛋白運輸途徑
在植物細胞內膜系統中,一方面,新合成的蛋白質需要先被運送到不同細胞器完成蛋白修飾后才能被運送到目標位置行使功能;另一方面,一些在細胞膜定位的膜蛋白在感知環境變化后會被運送到細胞內的特定部位完成信號的傳遞.細胞內眾多通路彼此高效協作,共同調控蛋白質在細胞內的靶向運輸,維持細胞內環境的穩態.下文主要介紹植物細胞內囊泡介導的最重要且常見的3條運輸途徑:蛋白分泌途徑、靶向液泡的運輸途徑和內吞途徑,圖1所示為經典分泌途徑和內吞途徑.
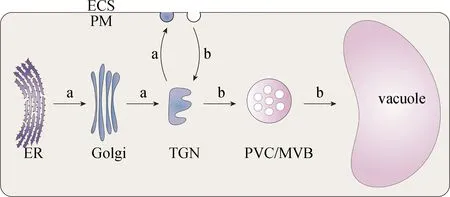
a.經典分泌途徑:ER-Golgi-TGN-細胞膜(PM)/細胞外(ECS);b.內吞途徑:ECS/PM-TGN-PVC/MVB-液泡.
1.1 植物蛋白分泌途徑
在分泌途徑中,新合成的蛋白質在完成加工之后會被運輸到PM或ECS行使功能,對維持細胞內環境穩定、促進細胞間信息交流以及應答生物或非生物脅迫等有重要的生理意義.植物蛋白分泌途徑主要分為經典分泌途徑和非經典分泌途徑.
1.1.1 經典分泌途徑
在經典分泌途徑中,對于多數分泌蛋白而言,其氨基端(N端)會含有一段疏水的氨基酸序列,稱為信號肽(SP),當肽鏈在核糖體上開始合成后,SP序列會指引其進入ER腔內進行后續的翻譯以及折疊修飾等[3-4].除經典的共翻譯轉運外,最近的研究還發現了一些翻譯后轉運的分泌蛋白.此類蛋白尾部含有一個膜錨定結構(TA),通過特定的TA蛋白指引復合物幫助其插入ER膜[5].無論是共翻譯還是翻譯后轉運,肽段進入ER腔內都需要借助Sec轉運體系.在釀酒酵母(Saccharomycescerevisiae)中Sec轉運體系由形成轉運通道的Sec61異源三聚體(Sec61p、Sbh1p和Sss1p)以及Sec62p、Sec63p、Sec71p、Sec72p組成的異源四聚體復合體所構成[6-7].Sec61異源三聚體和Sec63p參與共翻譯和翻譯后蛋白轉位,而Sec62p、Sec71p和Sec72p僅與翻譯后轉運相關[8].在擬南芥(Arabidopsisthaliana)基因組中有3個基因編碼Sec61p的同源蛋白,其中兩個與Sec63p同源,另一個與Sec62同源,且最新研究表明sec62突變體表現出生長受阻、花粉敗育[9],但具體機制仍有待闡明.
在ER完成加工后,包被蛋白(COPⅡ)囊泡會介導蛋白貨物從ER傳遞至Golgi.這一過程最早在酵母中被發現,此后證明其在動物和植物中都是保守的[10].COPⅡ囊泡的形成首先是將胞質中小G蛋白Sar1招募到ER膜上,然后Sec12作為其特異的鳥苷酸交換因子(GEF)使得Sar1變成結合三磷酸鳥苷(GTP)的激活形式,隨后激活態Sar1招募一個由GTPase激活蛋白Sec23和接頭蛋白Sec24所組成的異源二聚體,形成一個出芽的復合體,其中Sec24可以結合可溶性貨物的受體蛋白或跨膜的貨物蛋白,從而捕獲貨物[11];此復合體又招募Sec13-Sec31異源四聚體,作為COPⅡ最外層的包被蛋白,最終形成完整的COPⅡ囊泡[12-13].通過生物信息學分析,COPⅡ囊泡的某些蛋白組分的表達水平還會隨著各種脅迫條件和發育階段的變化而改變,表明植物中COPⅡ囊泡的數量處于動態變化中[14].
貨物蛋白被運輸至Golgi后,大多數會通過TGN分泌至PM或ECS,但最近研究也發現存在由Golgi直接產生的分泌囊泡[15].研究分泌蛋白運輸途徑最直接的方式就是監測PM上新合成的膜蛋白運動,如利用免疫熒光技術觀察細胞膜表面受體激酶(BRI1)蛋白的分布,發現在被運輸至PM之前,BRI1還有TGN的定位,說明BRI1的分泌是由TGN衍生的囊泡所介導的[16].除分泌單個的囊泡外,研究還發現TGN衍生的分泌囊泡能聚集成束,形成由5~12個囊泡組成的不規則大囊泡,直徑為50~100 nm,極大地提高了運輸效率,如分泌載體相關膜蛋白2(SCAMP2)就是通過此種途徑運輸的[17].
1.1.2 非經典分泌途徑
近些年來,越來越多的研究表明很多分泌型蛋白并不含SP序列,其分泌是通過非經典分泌途徑完成的.前期在動物和酵母的研究中就已經證明了非經典分泌途徑的存在,如動物中成纖維細胞生長因子2(FGF2)蛋白和白介素-1α(IL-1α)蛋白都是在疏水性釋放復合物的協助下,通過跨膜通道直接穿過PM[18-19].
在植物中,非經典分泌途徑也被慢慢發現.布雷菲德菌素A(BFA)是一種特異性阻斷蛋白質從ER轉運至Golgi的大環內酯類抗生素,且用BFA處理后的細胞會產生Golgi衍生囊泡聚集體,稱為“BFA體”[20],因此BFA常被用于非經典分泌途徑的研究.HYGR是一種缺乏SP的植物胞質蛋白,可以被分泌到ECS,且BFA處理后并不會影響該分泌過程[21];此外,甘露糖脫氫酶在水楊酸誘導下的分泌也表現出BFA不敏感性,表明非經典分泌途徑在植物應答脅迫過程中也發揮作用[22].然而在這兩種蛋白的運輸過程中,并未鑒定到任何囊泡狀結構,暗示著植物可能存在非囊泡介導的Golgi旁路分泌途徑.事實上,在動物細胞中確實發現PM上孔狀結構的形成有利于蛋白的直接整合,但這一結構在植物中還未被發現[23].
此外,非經典分泌途徑也介導了植物胞外囊泡(EV)的形成.EV這一概念在2011年才被正式提出,用來定義細胞向外分泌的各種具有脂質層包被的囊泡,如外泌體、凋亡小體和微泡等[24].最初EV被認為是細胞向外排出代謝廢物的一種途徑,但最近研究發現哺乳動物細胞分泌的外泌體還包裹著抗原物質和信使RNA(mRNA)[25-26],可以促進細胞間信息交流,具有很高的臨床應用價值,對外泌體等EV的研究在生物學界掀起了熱潮.早在20世紀60年代,研究者們用透射電鏡觀察胡蘿卜(Daucuscarota)細胞時就發現了植物中的EV[27],但受限于當時的分離純化技術,EV在植物中的研究遠滯后于動物中的研究.直至2017年,研究者們利用優化的差速離心法結合碘克沙醇密度梯度離心,才首次在植物葉片中分離出純度較高的EV[28].進一步通過生化分析鑒定出植物EV中含有核酸、蛋白質、脂質等活性物質,而這其中就包括很多參與細胞壁重塑和降解的酶[29],以及可以沉默病原菌基因表達的小分子RNA[30].上述證據說明,EV對植物正常生理活動的進行以及防御病原菌等方面都具有重要意義.植物中的EV主要包括exocyst亞基EXO70E2標記的EXPO(exocyst positive organelle)、四跨膜蛋白8(TET8)標記的外泌體和PEN1(plant syntaxin)標記的EV.
EXPO是一種新型的雙層膜包被的細胞器,膜上含有特殊的exocyst復合體,可以介導分泌囊泡與質膜的拴系和融合.在對擬南芥EXO70E2蛋白進行亞細胞定位研究時,研究者們發現其定位既不受BFA、ConA、wortmannin等經典分泌途徑抑制劑的影響,也不與自噬體、Golgi、TGN、PVC/MVB和液泡膜標記蛋白共定位[31].利用免疫電鏡技術,觀察到其標記的一種雙層膜結構與PM融合后可以釋放單層內膜包裹的囊泡(直徑為200~500 nm),使胞外也能檢測到EXO70E2蛋白,由此將此種新發現的雙層膜細胞器稱為EXPO[32].S-腺苷甲硫氨酸合成酶2是一種維持細胞壁結構的木質素生物合成酶,正是通過此種途徑分泌的[33].
對動物中分離出來的外泌體進行分析時,研究者們發現其膜上有很多TET,如CD9、CD37、CD63等[34],這些TET可以用作動物外泌體的標記物.擬南芥中有17個TET家族成員,通過序列比對和表達分析發現TET8與動物中CD家族同源性最高[35].且通過熒光共定位發現TET8與植物中Rab5蛋白(ARA6和RHA1)在胞內共定位[36],即TET8在胞內定位于MVB上.結合TET8有PM和ECS的定位,可以認為TET8是植物外泌體特有的一個標記物.當用灰霉菌(Botrytiscinerea)侵染植物時,TET8的表達豐度還會顯著提高,暗示植物分泌外泌體很有可能也是抵御病原菌入侵的一種防御手段.事實證明這種TET8標記的EV中含有的小分子RNA可以有效沉默病原菌特定基因的表達,從而達到防御目的[30].
PEN1是一種具有病原菌滲透抗性的蛋白,在擬南芥中亦稱為SYP121,屬于PM定位的Qa-可溶性N-乙基馬來酰亞胺敏感性因子附著蛋白受體Qa-SNARE;其分布在PM和ECS,但并不與Rab5共定位,也不與TET8共定位,由此認為PEN1標記的EV不同于TET8標記的EV[36].且在分離純化時,這兩種EV位于不同的密度梯度組分中,驗證了二者的差異[28].
此外,液泡也可以介導非經典分泌途徑的發生.植物細胞的液泡有較低的pH值且含各種水解酶,其功能類似于動物細胞中的溶酶體,是細胞中物質降解的中心.通常細胞中需要被降解的蛋白、代謝廢物等都會被運送到液泡降解,但植物在抵御病原菌入侵時,也需要這些水解酶或是其他具有抗性的次生代謝產物,此時就需要液泡再向外分泌這些物質.當用病原菌Pst(Pseudomonassyringaepathovartomato)菌株DC3000侵染擬南芥時,在電鏡下可以觀察到液泡膜與PM的融合過程,同時此過程需要病原菌的抗原蛋白AvrRpm1與植物抗斑生假單胞菌(P.maculicola)蛋白RPM1的互作[37].關于植物如何觸發液泡與PM的融合以及具體的膜融合機制仍有待進一步研究.
1.2 植物蛋白靶向液泡的運輸途徑
1.2.1 Rab5和Rab7雙依賴型靶向液泡的運輸途徑
在經典的蛋白分泌途徑中,新合成的蛋白會從ER運輸至Golgi,再進入TGN進行分選,對于含有液泡分選序列的蛋白來說,它們會靶向液泡[38].液泡貨物蛋白在TGN上被特有的液泡分選受體(VSR)所識別并結合,VSR與貨物蛋白結合后并非獨立地將蛋白運輸至液泡,而是以網格蛋白包被囊泡(CCV)的形式不斷與中間過程的細胞器融合,最終到達液泡.因此對VSR的鑒定,最初是通過純化CCV來實現的[39].現已證明接頭蛋白1(AP-1)/AP-4復合體參與CCV的形成[40].當貨物被運輸至MVB后,MVB進而與液泡融合.在擬南芥中,MVB也有兩種狀態,分別由Rab5和Rab7標記.通過尋找動物中的同源蛋白,發現莫能菌素敏感性1(MON1)/鈣咖啡因鋅敏感性1(CCZ1)復合體可以與GTP結合的Rab5互作,亦可與二磷酸鳥苷(GDP)結合的Rab7互作,從而揭示了植物中Rab5與Rab7轉換的分子機制[41].此條途徑可以簡單概括為:Rab5首先招募C類核心液泡內體束縛(CORVET),亦可招募MON1/CCZ1作為Rab7的GEF,從而激活Rab7,激活態的Rab7又可以招募同型融合和蛋白質分選復合體(HOPS)等效應蛋白,最終介導MVB與液泡的融合(圖2-a).擬南芥中運輸至蛋白儲存型液泡的12S球蛋白,以及運輸至溶解型液泡的液泡硫基蛋白酶(aleurain),均是通過此種方式運輸的.
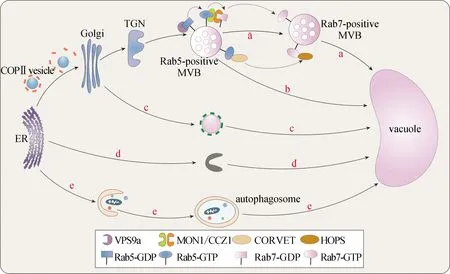
a.Rab5和Rab7依賴途徑,Rab5招募MON1/CCZ1復合體激活Rab7,最終由Rab7介導MVB與液泡的融合;b.Rab5依賴途徑;c.AP-3復合體依賴途徑;d.從ER直接運輸到液泡途徑;e.自噬途徑.
1.2.2 僅依賴Rab5靶向液泡的運輸途徑
擬南芥中共有3個編碼Rab5的同源蛋白ARA7、RHA1和ARA6.其中ARA7和RHA1負責介導蛋白靶向液泡的運輸;而ARA6為植物特有,負責介導MVB向PM的運輸[42].盡管它們發揮不同的功能,但都有一個共同的GEF(VPS9a),可以使得Rab5以GTP結合的方式錨定在MVB膜上[43].最近的研究發現VPS9a的羧基端(C端)結構域可以與ARA6互作,但并不與ARA7或RHA1互作,暗示此區域的互作位點可用于區分不同的Rab5[44].vps9a突變體表現出生長缺陷,也證明Rab5在植物液泡運輸中發揮不可或缺的作用[45].雖然多數液泡蛋白通過經典途徑靶向液泡,但是也存在只依賴于Rab5的蛋白靶向液泡運輸途徑(圖2-b).SYP22是一個靶向液泡膜的SNARE蛋白,在vps9a-2突變體中SYP22的運輸受到抑制,但在mon1-2突變體中卻表現正常,證明SYP22的運輸不依賴Rab7而只依賴Rab5[46].
1.2.3 依賴AP-3復合體靶向液泡的運輸途徑
AP-3復合體介導的液泡運輸最初在酵母中發現,被鑒定為堿性磷酸酶的運輸途徑[47],后續在動物中也被證明介導溶酶體的靶向運輸[48],且均無需再經過中間細胞器,通過Golgi后可直接將貨物運輸至液泡或溶酶體[49].AP-3復合體是一個異源四聚體,由兩個大亞基(δ和β3)、一個中亞基(μ3)以及一個小亞基(σ3)構成[50].在擬南芥中,跨膜蛋白PAT10已被證明是AP-3復合體介導的蛋白靶向液泡運輸途徑中的貨物[51](圖2-c).在ap-3β突變體中,發現一種靶向液泡的貨物蛋白SUC4被滯留在Golgi而非TGN中.
1.2.4 ER直接靶向液泡的運輸途徑
上述幾種植物蛋白靶向液泡的運輸途徑都需要經過Golgi.而在2013年,有研究者利用遺傳學結合光學和電子顯微鏡成像等多種技術,在擬南芥根分生組織細胞中發現H+三磷酸腺苷(ATP)酶VHA-a3可以從ER直接靶向液泡[52](圖2-d),但具體的分子機制尚不明確.
1.2.5 自噬途徑
自噬在真核生物中高度保守,是受損的蛋白質和細胞器循環再利用的重要途徑,在植物細胞中通過自噬體與液泡融合完成,是靶向液泡運輸的一種類型,對植物維持細胞穩態和響應各種環境脅迫(如營養缺陷、逆境、病原體感染等)必不可少(圖2-e).自噬由一系列核心的自噬相關基因(ATG)蛋白起始和調控(圖3).ATG蛋白根據其功能可分為4組:ATG1/ATG13激酶復合體、磷脂酰肌醇-3-激酶(PI3K)復合體、ATG9包含囊泡、ATG8/ATG12類泛素化結合系統[53].ATG1/ATG13激酶復合體負責響應細胞營養信號以起始自噬體的形成;PI3K復合體在自噬體膜上催化產生磷脂酰肌醇-3-磷酸(PI3P),通過招募不同的PtdIns3P結合蛋白來調控自噬過程,包含VPS34、VPS15、ATG6、ATG14共4個亞基;ATG9包含囊泡穿梭于不同膜來源的細胞器,運輸膜脂以促進自噬泡的擴張;ATG8/ATG12類泛素化結合系統促進自噬體的擴張和成熟.首先ATG5與ATG12共價連接以形成復合體,然后該復合體進一步與ATG16互作以產生ATG5-ATG12/ATG16多聚體.該多聚體作為E3連接酶發揮作用,將ATG8連接到自噬體的磷脂酰乙醇胺(PE)上.

植物自噬體膜來源眾多,包括ER、ATG9囊泡和COPⅡ囊泡等.這些膜結構首先形成前自噬體結構(PAS),然后在需要降解的貨物(如線粒體、葉綠體)周圍形成杯狀雙層的吞噬體膜;接著吞噬體膜伸長并密封形成自噬體;最后自噬體與液泡融合,其內容物被液泡水解酶分解,完成自噬過程.
自噬的誘導受細胞營養狀態的調節.在營養豐富的條件下,雷帕霉素靶蛋白(TOR)和其他激酶誘導ATG13亞基過磷酸化和ATG1激酶低磷酸化,促使ATG1/ATG13激酶復合體解離.最近研究表明,擬南芥腫瘤壞死因子受體相關因子(TRAF)家族蛋白中的TRAF1a和TRAF1b可作為支架蛋白,與RING E3泛素蛋白連接酶SINAT1、SINAT2互作,通過泛素化途徑降解ATG13或ATG6,將自噬維持在適當水平[54-55].然而,在饑餓等營養缺乏時,蔗糖非發酵相關蛋白激酶1(SnRK1)會抑制TOR活性,導致ATG13去磷酸化以及ATG1/ATG13激酶復合體的結合以啟動自噬.
自噬體的膜起源是植物自噬領域長期研究的問題.近年研究發現,擬南芥中ATG9的缺失可導致在自噬過程中擴大的自噬體相關小管連接到ER,為ER作為植物自噬體的膜來源提供了結構學證據[56].此外,COPⅡ囊泡不但介導蛋白質從ER到Golgi的正向運輸,還可在自噬過程中作為自噬體生物發生的膜來源之一[57](圖3).
一些非ATG蛋白也參與自噬過程,如乳腺癌 1號基因鄰近基因1(NBR1)、SH3結構域蛋白2(SH3P2)等.NBR1和ATG8-PE互作,作為選擇性自噬受體在蛋白質聚集體的清除中發揮重要功能[58].SH3P2是一種膜相關蛋白,與擬南芥中PI3K復合體結合并與ATG8互作,協同促進膜擴張或成熟[59].最新研究表明自噬受體蛋白NBR1的數量增減會影響ATG8與SH3P2的互作[59],細胞以此來調節選擇性自噬途徑的活躍程度,即按需要將自噬貨物運送至植物液泡降解,維持營養和能量的平衡.
自噬體在完成貨物裝載后會與液泡融合,其內容物被液泡水解酶分解,完成自噬過程(圖3).然而在植物細胞中,自噬體膜的閉合過程以及與液泡的融合機制還不是很清楚.通常認為多種Rab蛋白、拴系復合物和SNARE蛋白等都可能參與自噬體與液泡的融合.
1.3 植物內吞途徑
與分泌途徑相對,內吞作用也是真核生物維持胞內環境穩定、應答外界環境信號的重要方式.相比于動物細胞,植物細胞特有的細胞壁和液泡結構使其多了一道天然屏障,并大大提高了膨壓,但同時在一定程度上阻礙了PM內陷.植物細胞是否會發生內吞作用曾引發學界的激烈討論.
深入的研究發現植物細胞不僅會發生內吞作用而且內吞作用還具有重要的生理意義.在植物細胞中,根據貨物蛋白在PM上凹陷出芽形成的小泡類型,將內吞途徑分為網格蛋白介導的內吞(CME)途徑和非網格蛋白介導的內吞(CIE)途徑.
1.3.1 CME途徑
CME是植物中主要的內吞途徑,也是研究得較為清楚的途徑.生長素極性運輸載體PIN2、水通道蛋白PIP、鐵轉運蛋白IRT1等均通過此種內吞途徑進入細胞[60].CME發生的過程包括以下5個步驟.1)內吞貨物的募集:此步驟需要AP復合體.在真核生物中共鑒定到5種AP復合體,其中AP-2復合體在內吞途徑中發揮重要作用.AP-2復合體也是一個異源四聚體,由兩個大亞基(α和β2)、一個中亞基(μ2)和一個小亞基(σ2)構成.其中AP-α可以與PM上二磷酸磷脂酰肌醇或三磷酸磷脂酰肌醇結合穩定內吞裝置,AP-μ2可以特異識別內吞貨物將其分選募集[61].2)網格蛋白的招募:AP-2復合體的作用類似橋梁,一端連接著內吞貨物,另一端則通過AP-β2招募網格蛋白,并在PM形成內陷的小窩(CCP).此過程還需要其他輔助蛋白以促進網格蛋白的招募和膜內陷,如Epsin1和AP180[62]等.3)CCP從膜上縊裂形成CCV.縊裂的過程需要膜縊裂相關蛋白(DRP),這是一類大GTPase蛋白家族,通過纏繞在CCP莖上水解GTP,釋放能量以促進CCP從膜上脫落[63].DRP的招募由含有Bin/兩性蛋白/Rvs(BAR)結構域的endophilin和SNX9蛋白完成,在擬南芥中DRP1和DRP2表現出對內吞過程的調控[64].4)CCV 脫去包被蛋白:auxilin、熱激同源蛋白70(HSC70)等蛋白會破壞AP-2與網格蛋白間的連接[65],從而促進網格蛋白的釋放.5)最終內吞囊泡與內體融合,完成貨物運輸.
內吞作用很大程度上會影響PM表面的分子分布,進而觸發信號轉導等過程,因此也會受到生物或非生物因子的調控.最新的一項研究發現,三價稀土元素鑭[La(Ⅲ)]可以調控CME:用低劑量La(Ⅲ)處理葉片后,可以激活葉細胞的CME過程,且還會將此信號長距離傳導至根;而這種長距離運輸的機制是La(Ⅲ)激活葉細胞CME后,觸發AtrbohD(一種產生活性氧的還原型輔酶Ⅱ氧化酶)和茉莉酸的協同作用,使信號得以傳遞[66].
1.3.2 CIE途徑
在動物細胞中,CIE途徑主要包括脂筏蛋白介導的內吞、巨胞飲以及非網格蛋白、脂筏蛋白依賴的胞吞等,例如IL-2受體就是由endophilin所介導的CIE途徑進行內吞的貨物.研究表明endophilin通過小G蛋白Cdc4招募Formin結合蛋白17(FBP17)和Cdc42相互作用蛋白4(CIP4)蛋白在PM上富集,FBP17和CIP4又招募磷酸酶SHIP2和lamellipodin,使得PM上局部產生二磷酸磷脂酰肌醇,最終endophilin被富集在PM上特定區域引發內吞作用[67].最近關于植物CIE的研究日益增多,如有研究證明煙草BY-2(NicotianatabacumL.cv.Bright Yellow 2)細胞被CME途徑的抑制劑斑鳩霉素(ikarugamycin)處理后仍能吸收外界環境中的葡萄糖[68],暗示植物體內也存在CIE途徑.此外,通過對擬南芥質膜內在蛋白2;1(PIP2;1)的研究發現,在不同狀態下該蛋白可以依賴不同途徑進行內吞作用[69]:在正常情況下,細胞通過CME途徑進行PIP2;1蛋白的內吞作用;而在高滲脅迫時,脂筏介導的內吞途徑被激活,共同參與該蛋白的內吞過程.進一步研究發現,PIP2;1蛋白的內吞過程部分與脂筏標記蛋白1(Flot1)介導的PM微區內吞有關,抑制Flot1的表達會對植物的生長發育造成影響.另外呼吸爆發氧化酶同系物D(RbohD)蛋白的內吞作用也同時受網格蛋白和PM微區的調控,特別是受到鹽脅迫時,由Flot1富集的PM微區內吞作用變強[70].除了葡萄糖、蛋白質可以經CIE途徑進入植物細胞外,植物激素如油菜素內酯(BR)也被CIE途徑調控.施加BR可以促進其受體BRI1進入Flot1富集的PM微區并由其介導內吞[71].由此可見,當植物經受外源刺激時,CIE在植物體內發揮重要調控作用[72-73].
2 前沿電子顯微鏡技術在植物內膜系統研究中的應用
在過去的20年中,研究者們借助于顯微鏡技術直接明確地觀察到植物內膜系統中的囊泡運輸過程,并解析出不同蛋白在其中發揮的作用,極大地加快、加深了人們對植物內膜系統精準調控的理解.激光共聚焦掃描顯微鏡作為一種高端的光學顯微鏡,被廣泛應用于觀察細胞內囊泡的實時動態運輸過程.相較于傳統光學顯微鏡,電子顯微鏡的分辨率達到0.2 nm左右,可以提供分子甚至原子水平的信息.特別是隨著科技的發展,越來越多前沿電子顯微鏡技術在提高觀察分辨率的同時,也最大限度地保留了樣品真實的生理狀態.這些電子顯微鏡技術的使用令人們逐步看清了這些看似滄海一粟的熒光點的廬山真面目,極大地推動了本領域的研究進展,為更深入地理解分子機制提供了不可估量的幫助.根據研究對象和目的,下文將具體介紹在植物內膜系統研究中逐漸開始應用的4種前沿電子顯微鏡技術,分別為用于解析蛋白結構的冷凍電子顯微鏡技術(cryo-EM)、著重進行細胞器三維重構的電子斷層掃描技術(ET)、用來減薄冷凍樣品的冷凍聚焦離子束技術(cryo-FIB),以及將光學顯微鏡與電子顯微鏡聯用的光電聯用技術(CLEM).
2.1 cryo-EM
目前解析蛋白結構的方法主要有X射線晶體衍射、核磁共振(NMR)和cryo-EM 3種.X射線晶體衍射是解析蛋白質大分子和晶體結構的主流手段,NMR技術則在小分子量的蛋白質結構解析中發揮重要作用,然而這兩種技術都有一定的局限性.當蛋白質無法形成高質量晶體且分子量較大時,就需要用cryo-EM來解析蛋白結構,其主要原理是利用透射電鏡在低溫下觀察包埋于玻璃態冰中的樣品,然后通過軟件對數據進行處理,從而得到樣品的精細結構.1975年,Henderson等[74]首次利用cryo-EM和電子晶體學解析出細菌視紫紅質膜蛋白的結構,開啟了cryo-EM在結構學中的應用;Lepault等[75]于1983年發明了將樣品速凍于玻璃態冰中的方法,使cryo-EM變得更為實用.自此,cryo-EM成為揭示蛋白結構的一個強有力工具.
cryo-EM最初主要用于結構生物學,隨著技術的不斷進步和革新,如今已廣泛應用于微生物學、神經生物學、免疫學、細胞生物學等多個學科研究領域[76-78].在植物學研究中,應用cryo-EM在亞納米水平解析了擬南芥自噬蛋白中唯一跨膜蛋白ATG9的三維結構,發現ATG9組成一個同源三聚體,每個單體至少有6個跨膜的α-螺旋,在三聚體的中心,相鄰單體通過C端細胞質區域和膜嵌入區域的互作形成三聚體界面;結合使用序列共同進化信息對蛋白質結構的預測,該結構提供了ATG9分子水平的解析,并為ATG9調節自噬進展的分子機制提供了可檢驗的假設[79].類似地,研究者們通過cryo-EM方法解析出玉米(Zeamays)花粉中F-肌動蛋白的結構,顯示其為一個右旋、雙鏈(兩條平行鏈)和交錯的結構,該結構通過鏈內和鏈間的互作得以穩定,這對理解肌動蛋白如何作為長距離囊泡和細胞器運輸的軌道至關重要[80].
對于體積和厚度較小的樣品(如上述蛋白),利用直插式冷凍固定,對包被在冰膜中分散的、取向隨機的成千上萬的同一種蛋白分子進行拍照,將獲得的蛋白照片進行疊加,即可獲得這個蛋白接近于原子尺度分辨率的三維結構,該過程稱作單顆粒分析(SPA).隨著直接探測電子相機的出現和新算法的開發,SPA可達到原子分辨率水平[81].而當研究對象不具備周期性或全同性,如生物大分子復合體或細胞器、細胞骨架、囊泡運輸系統時,樣品不僅在體積和厚度上大過蛋白質且異質性高,直插式冷凍無法固定樣品,且無法用SPA方式對圖像進行疊加,研究者們于是開始尋求另一套冷凍固定、電子顯微鏡成像技術和三維重構的算法.
2.2 ET
ET是對樣品中同一物體沿著垂直軸通過不同的傾斜角度進行拍攝,獲得一系列二維投影圖像后再重構其三維結構的方法.一般傾斜角度在-60°~+60°范圍內,每1°~2°拍攝一次.根據樣品的特性,ET又細分為樹脂包埋樣品的常溫ET和非樹脂包埋的冷凍ET(cryo-ET),常溫ET的應用較為廣泛,cryo-ET的應用則是近期的熱點,尤其在植物中的應用才剛開始.通常為了最大限度地保存細胞器結構,在固定植物細胞時,相對于傳統的化學固定,優選采用高壓冷凍法(HPF)和冷凍替代法(FS)來制備樣品.使用此方法固定的植物材料已被證明可以很好地應用于后續ET[82].目前在植物內膜系統研究中主要為常溫ET,應用于細胞器起源以及新型細胞器的鑒定.在對擬南芥自噬體的研究中,研究者利用ET首次揭示了自噬體小管和ER膜之間的直接聯系,為植物自噬體起源于ER膜提供了關鍵證據[83].而同樣利用ET,在重構出的植物根細胞三維圖像中,研究證實植物細胞中存在多個互相獨立的液泡,并首次鑒別出一個直徑400~1 000 nm的小液泡(SV),其中包含很多腔內囊泡;結合統計分析及對MVB形成或融合缺陷突變體的分析,最終證明植物中央大液泡是通過MVB融合形成SV,SV再進一步融合而來[79].由此解答了植物液泡的起源之謎,揭示了擬南芥根細胞中液泡形成的過程,結束了40多年關于液泡起源的爭論[84-86].除此之外,研究者還利用ET鑒定出苜蓿(Medicagosativa)根緣細胞中一種源于TGN獨特的介導半乳糖醛酸分泌的囊泡[87].在酵母和哺乳動物細胞等其他真核生物系統中,ET還成功應用于膜接觸位點的研究,幫助闡明不同細胞器之間的連接機制[88-89].
為將樣品更好地保持在其生理狀態,cryo-ET提供了解析更接近自然狀態的細胞器的方法.在樣品制備方面,根據樣品的厚度可以采用直插式冷凍法(樣品厚度小于10 μm)或HPF(樣品厚度小于300 μm).由于電子的穿透能力有限,通常要對樣品進行減薄處理,雖然可以通過冷凍超薄切片完成,但是這些冷凍切片常出現因切割導致的壓縮、折皺等假象[90],結果并不穩定且對操作者技術能力要求高,工序費時.于是研究者們將目光轉向了材料學中常見的雙束聚焦離子束(FIB)減薄法,嘗試將其應用于ET的樣品制備,并拓展至冷凍條件下的cryo-ET的樣品減薄.另外,目前針對cryo-ET圖像處理的子斷層圖像平均(STA)技術也正在悄然崛起.雖然目前其最終圖像分辨率(0.3 nm)不及上述的SPA[91],但是該技術可以對較大、較厚、缺乏重復性的生物樣品在其原位進行研究,這些優勢都是SPA不可比擬的,有望成為日后研究細胞結構與功能的重要技術手段[76-78].
2.3 cryo-FIB
FIB技術是利用靜電透鏡將高能離子束聚焦成非常小的束斑,對材料表面進行轟擊,從而達到材料的剝離、沉積和改性的一種方法,主要應用于材料學領域[92].目前FIB通常配置在掃描電鏡(SEM)上,使加工過程可以實時觀察,令操作更加精準.但FIB-SEM設備速度較慢,運行的時間有限,如果收集大體積樣品,中途停頓會導致圖像堆棧缺乏連續性.針對較大體積的生物樣品,為了使FIB-SEM在數月的連續運行中變得更快、更可靠,研究者們改進FIB-SEM信號的檢測方式,在合理的時間范圍內對完整的果蠅(Drosophilamelanogaster)大腦進行成像,并使堆棧中各圖像的間隙僅為8 nm[93].此外,高能離子束對樣品具有很高的破壞性[94],但cryo-FIB技術的發展減少了離子束對樣品的損傷[95-96].
在植物內膜系統研究中,FIB-SEM已應用于本氏煙草(Nicotianabenthamiana)葉細胞和大豆(Glycinemax)根瘤細胞的細胞器觀察.在煙草葉片細胞中,研究者觀察到緊密堆積的細胞器可能形成膜接觸[97].利用ET重構出的大豆根瘤細胞的三維模型表明,與二維電子顯微鏡超薄切片顯示的許多單獨的共生體不同,受感染細胞中的類菌體全部包含在一個大的膜結構中[97].雖然cryo-FIB已在線蟲、酵母、細菌、哺乳動物細胞、小鼠腦組織中有所應用[98-100],但是在植物領域條件仍未優化,其應用還鮮有報道.
2.4 CLEM
借助高分辨率重構的三維植物細胞模型,可以看到植物細胞內環境復雜且擁擠,內膜系統包含的細胞器眾多[84].如上所述,為了更好地分析各細胞器,研究者們通常利用多種熒光蛋白或染料對數個細胞器或細胞結構進行標記,在光學顯微鏡下進行成像觀察.然而受限于熒光顯微鏡約200 nm的分辨率限制,標記部分的超微結構無法看清.隨著科技的發展,現在已經可以將觀察得到的光學顯微鏡信號(通常是熒光)和EM圖像相結合,從而獲得感興趣區域的高分辨率結構信息,并把這兩種技術結合的方法稱為CLEM.在CLEM發展早期,由于光學顯微鏡分辨率較低,光學顯微鏡與EM關聯的準確性并不非常高.隨著超高分辨率光學顯微鏡(SR-LM)的發展,也產生了如基于單分子成像技術的光激活定位顯微術與常溫透射EM結合[101]或與SEM結合的應用[102].這些工作預示著CLEM已進入SR-CLEM的發展階段.隨后,研究者們又成功地推動常溫CLEM向冷凍方向發展,利用cryo-CLEM/cryo-ET觀察了黃色黏球菌(Myxococcusxanthus)的第六分泌系統的結構[103]以及線粒體膜上轉位酶TOM20的精細定位分布[104].與常溫CLEM相比,cryo-CLEM的熒光強度大幅提高,且冷凍樣品更接近細胞的自然狀態.目前在冷凍條件下應用CLEM可幫助ET定位,大部分都應用于動物細胞和細菌[105].在植物中,常溫下應用此技術的研究主要集中在TGN[106],而冷凍條件下CLEM和cryo-ET結合應用的條件仍需優化,一旦成功,其應用潛力將會非常大.
3 總結與展望
內膜系統是細胞中結構和功能的重要組成部分,負責將生物大分子等選擇性運送到目標部位并發揮功能.植物蛋白運輸主要通過囊泡介導,主要運輸途徑包括蛋白分泌途徑、靶向液泡的運輸途徑和內吞途徑,而細胞器則是這些運輸途徑的中轉站并發揮多種功能.囊泡運輸的調控和細胞器的生物發生一直以來都是細胞生物學研究的熱點和難點.植物細胞含有不同于動物細胞的細胞壁,這對研究者在植物細胞中開展研究提出了更多的挑戰.盡管越來越多的分子、新的運輸途徑甚至未知的細胞器被鑒定出來,人們對植物細胞內膜系統運輸調控機制的理解仍處于初級階段,對這些井然有序過程的調控機制還知之甚少,仍有大量重要的問題等待回答.例如:植物細胞內不同運輸途徑之間是否存在交叉互作?如果有,哪些蛋白介導了這些互作?互作的生物學意義是什么?當植物受到生物或非生物脅迫時,植物細胞內不同運輸途徑又是如何協調運作使植物在逆境中進行抵抗最終得以生存?能否利用基因工程的手段通過優化各蛋白運輸途徑以達到增加糧食產量、提高品質的目的?想要回答上述問題,多學科交叉(如與生物物理、計算機等學科)和新技術發展(如前沿電子顯微鏡成像技術)都是不可或缺的.在實驗條件優化和自動化大數據高分辨率圖片處理的配合下,有望逐步實現對植物細胞內囊泡運輸、細胞器生成等生理過程的原位分析,在分子甚至原子層面闡明其調控機制,將結構與功能有機結合,進一步加深對本領域的認識;同時為內膜系統在動物細胞、真菌等不同系統的運作機制提供線索,最終實現在農業、醫療等領域的應用,助力可持續發展.

