經皮耳迷走神經刺激對患者術后早期認知功能的影響
王娟,劉佩蓉,劉春亮,彭生
(上海中醫藥大學附屬第七人民醫院,上海 200137)
術后認知功能障礙(postoperative cognitive dysfunction, POCD)是發生在手術后的一種中樞神經系統并發癥,常表現為焦慮和語言理解、記憶力及社交能力下降等,其中老年患者高發。重度者可表現出躁狂癥狀,甚至呈類似阿爾茲海默癥病(AD)極端癡呆癥狀,自殺傾向,導致死亡率增加[1-3]。有研究顯示應用藥物減輕中樞神經系統炎癥及營養中樞神經細胞對 POCD具有改善作用,但是藥物均有一定的副作用。有研究發現通過物理治療的方法,在副作用忽略不計的情況下,可以取得類似的效果,其中耳迷走神經刺激是常用的方法之一[4]。而通過迷走神經刺激是否能改善 POCD,目前報道較少。因此,本研究擬采用經皮耳迷走神經刺激,觀察其對老年患者術后早期認知功能障礙的影響。
1 臨床資料
1.1 一般資料
120例擬擇期全麻下手術的老年患者,隨機分為經皮耳迷走神經刺激(transcutaneous auricular vagus nerve stimulation, TAVNS)組、假刺激組和空白對照組,每組40例。3組一般資料比較,差異無統計學意義(P>0.05)。詳見表1。
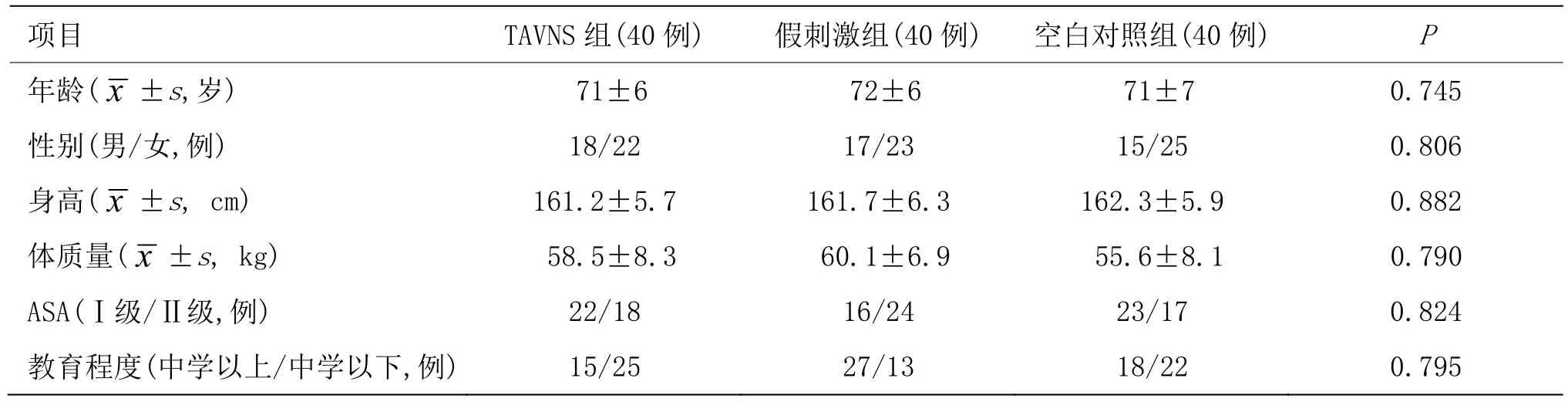
表1 3組一般資料比較
1.2 納入標準
①年齡≥65歲,性別不限;②術前麻醉評估 ASAⅠ~Ⅱ級;③無高血壓、糖尿病等系統病變,無精神類藥物服用史、藥物成癮史;④能理解并配合完成簡易智能量表(MMSE)篩查和蒙特利爾認知評估量表(MoCA)測定;⑤自愿參加本項試驗,簽署知情同意書。
1.3 排除標準
①術前MMSE<27分者;②處于妊娠期、哺乳中或計劃懷孕者;③合并有心、腦、肝、腎和造血系統嚴重原發性疾病,以及急性病、傳染病、惡性腫瘤者;④曾參加過電刺激治療的臨床試驗者;⑤電刺激部位皮膚有破損或皮膚病者。
2 治療方法
2.1 TAVNS組
常規乙醇消毒后,于耳甲迷走神經分布區[解剖學定位為耳甲腔和耳甲艇,耳甲艇后下緣為耳甲 12區(肝);耳甲腔后上緣為耳甲 13區(脾);對耳輪下腳臀穴直對的耳甲艇為耳甲10區(腎),肝腎之間為耳甲11區(胰膽);耳甲腔中心為耳甲 15區(心);心穴周圍為耳甲14區(肺);心穴到外耳道口為耳甲16區(氣管);屏間切跡內緣為耳甲 17區(三焦);外緣為耳甲 18區(內分泌)]放置電極片后,采用低頻脈沖治療儀(G6805-2)進行 30 min的刺激,強度 1 mA,頻率 20~30 Hz,脈沖持續時間1 ms,刺激間隔時間10 s。每日1次。術前1 d至術后3 d進行治療。
2.2 假刺激組
予以相同參數的電刺激,但電極刺激位置為耳郭非迷走神經分布區域,詳見圖1。
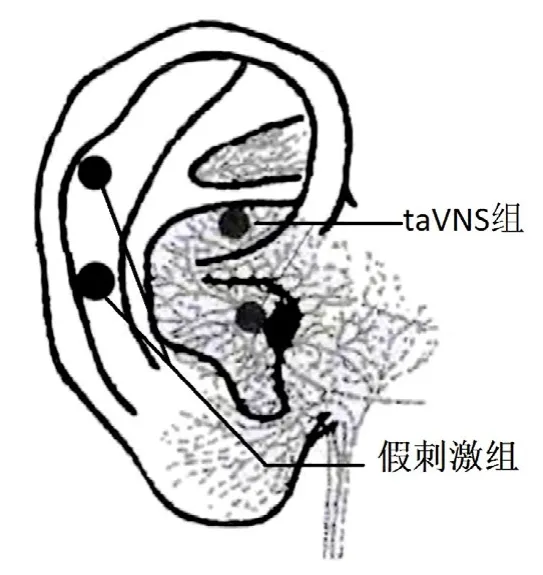
圖1 刺激部位示意圖
2.3 空白對照組
不做任何處理。
3 治療效果
3.1 觀察指標
3.1.1 行為學指標
術前 1 d采用簡易智力狀態檢查(MMSE)進行篩選,MMSE<27分者剔除。入組后,由經過培訓的專人評估,記錄所有患者術前1 d,術后1 d、3 d、7 d的MoCA評分。MoCA內容包括注意與集中、執行功能、記憶、語言、視空間技能、抽象思維、計算和定向力8個認知領域的11個檢查項目。完成MoCA檢查大約需要10 min。總分為30分,<26分被認為有認知功能障礙。
3.1.2 血清生化指標
用酶聯免疫吸附法(ELISA)測定術前、術畢及術后1 d、3 d的神經元特異性烯醇酶(NSE)、S100β、腫瘤壞死因子(TNF)-α、白細胞介素(IL)-6及 IL-1β表達水平。
3.2 統計學方法
所有數據均采用 SPSS21.0統計學軟件進行統計分析。符合正態分布的計量資料以均數±標準差表示,不同時間點的組間比較采用單因素方差分析,組內不同時間點比較采用配對t檢驗。不符合正態分布的資料比較采用Wilcoxon秩和檢驗。檢驗水準為α=0.05。
3.3 治療結果
3.3.1 3組不同時間MoCA評分比較
術前3組患者MoCA評分比較,差異無統計學意義(P>0.05)。術后1 d、3 d、7 d,TAVNS組的評分高于假刺激組和空白對照組(P<0.05),假刺激組和空白對照組比較差異無統計學意義(P>0.05)。詳見表2。
表2 3組不同時間MoCA評分比較 (±s,分)
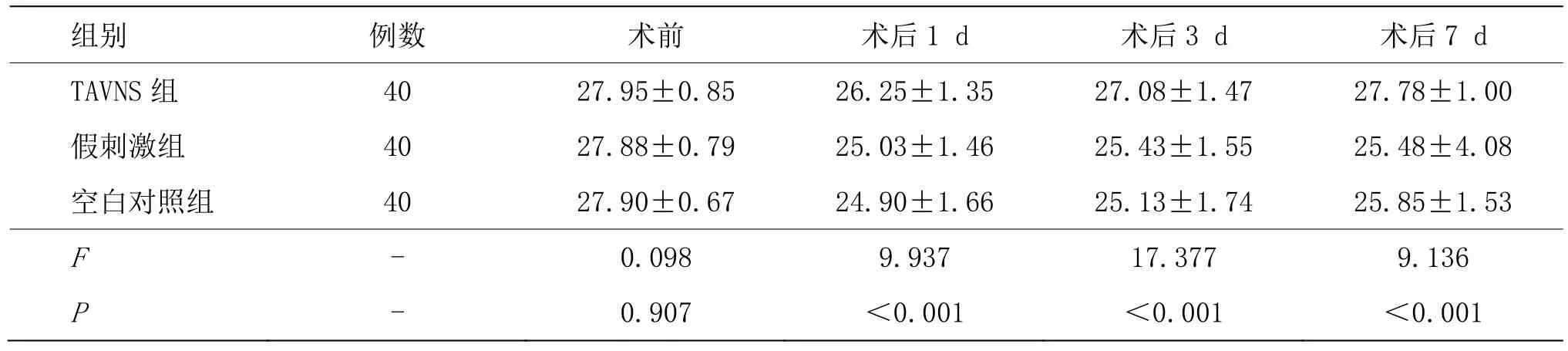
表2 3組不同時間MoCA評分比較 (±s,分)
組別 例數 術前 術后1 d 術后3 d 術后7 d TAVNS 組 40 27.95±0.85 26.25±1.35 27.08±1.47 27.78±1.00假刺激組 40 27.88±0.79 25.03±1.46 25.43±1.55 25.48±4.08空白對照組 40 27.90±0.67 24.90±1.66 25.13±1.74 25.85±1.53 F - 0.098 9.937 17.377 9.136 P - 0.907 <0.001 <0.001 <0.001
3.3.2 3組不同時間血清NSE和S100β水平比較
3組術前和術畢血清 NSE、S100β比較,差異無統計學意義(P>0.05)。與空白對照組和假刺激組比較,TAVNS組術后1 d、術后3 d的NSE、S100β水平降低(P<0.05);假刺激組和空白對照組比較差異無統計學意義(P>0.05)。詳見表3。
表3 3組不同時間血清NSE和S100β水平比較 (±s, ng/mL)
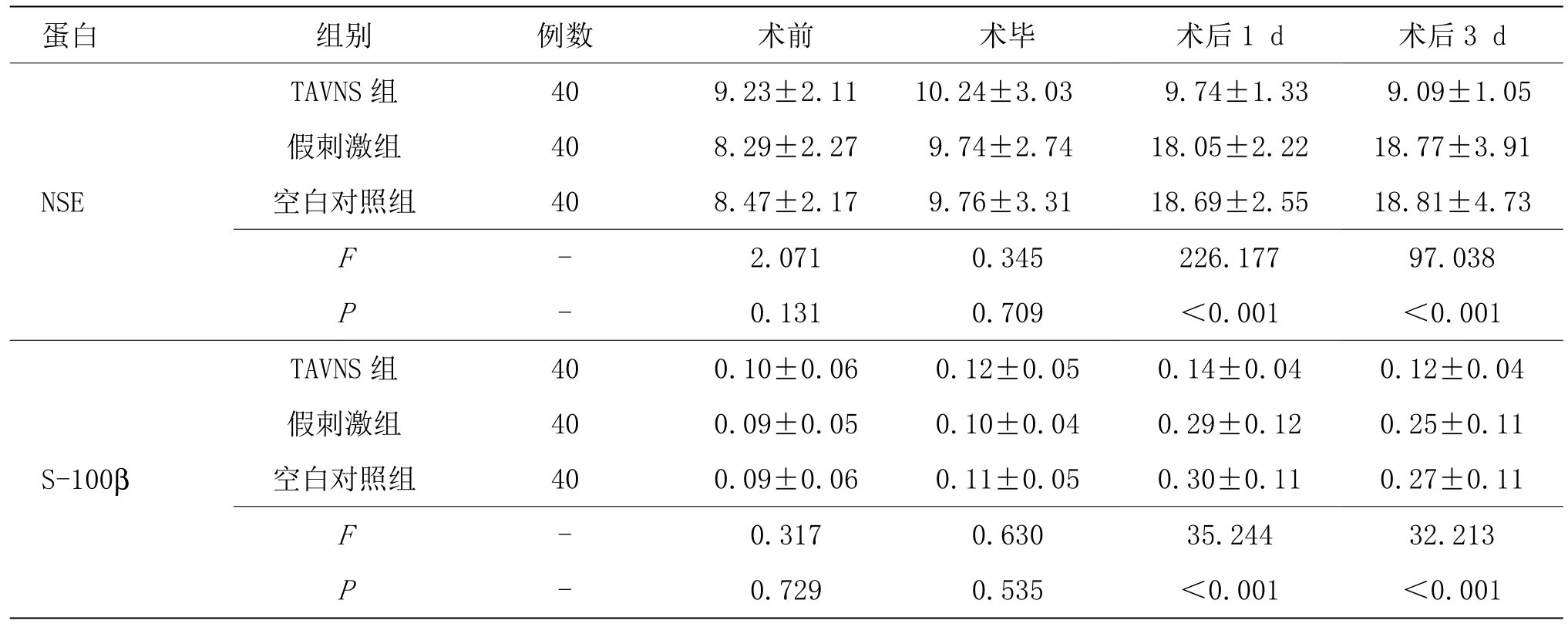
表3 3組不同時間血清NSE和S100β水平比較 (±s, ng/mL)
蛋白 組別 例數 術前 術畢 術后1 d 術后3 d NSE TAVNS 組 40 9.23±2.11 10.24±3.03 9.74±1.33 9.09±1.05假刺激組 40 8.29±2.27 9.74±2.74 18.05±2.22 18.77±3.91空白對照組 40 8.47±2.17 9.76±3.31 18.69±2.55 18.81±4.73 F - 2.071 0.345 226.177 97.038 P - 0.131 0.709 <0.001 <0.001 S-100β TAVNS 組 40 0.10±0.06 0.12±0.05 0.14±0.04 0.12±0.04假刺激組 40 0.09±0.05 0.10±0.04 0.29±0.12 0.25±0.11空白對照組 40 0.09±0.06 0.11±0.05 0.30±0.11 0.27±0.11 F - 0.317 0.630 35.244 32.213 P - 0.729 0.535 <0.001 <0.001
3.3.3 3組不同時間血清 TNF-α、IL-6、IL-1β水平比較
3組術前和術畢血清TNF-α、IL-6、IL-1β水平比較,差異無統計學意義(P>0.05)。與空白對照組和假刺激組比較,TAVNS組術后 1 d、術后 3 d患者血清TNF-α、IL-6、IL-1β水平降低(P<0.05);假刺激組與空白對照組比較差異無統計學意義(P>0.05)。詳見表4。
表4 3組不同時間血清TNF-α、IL-6、IL-1β水平比較 (±s, ng/mL)
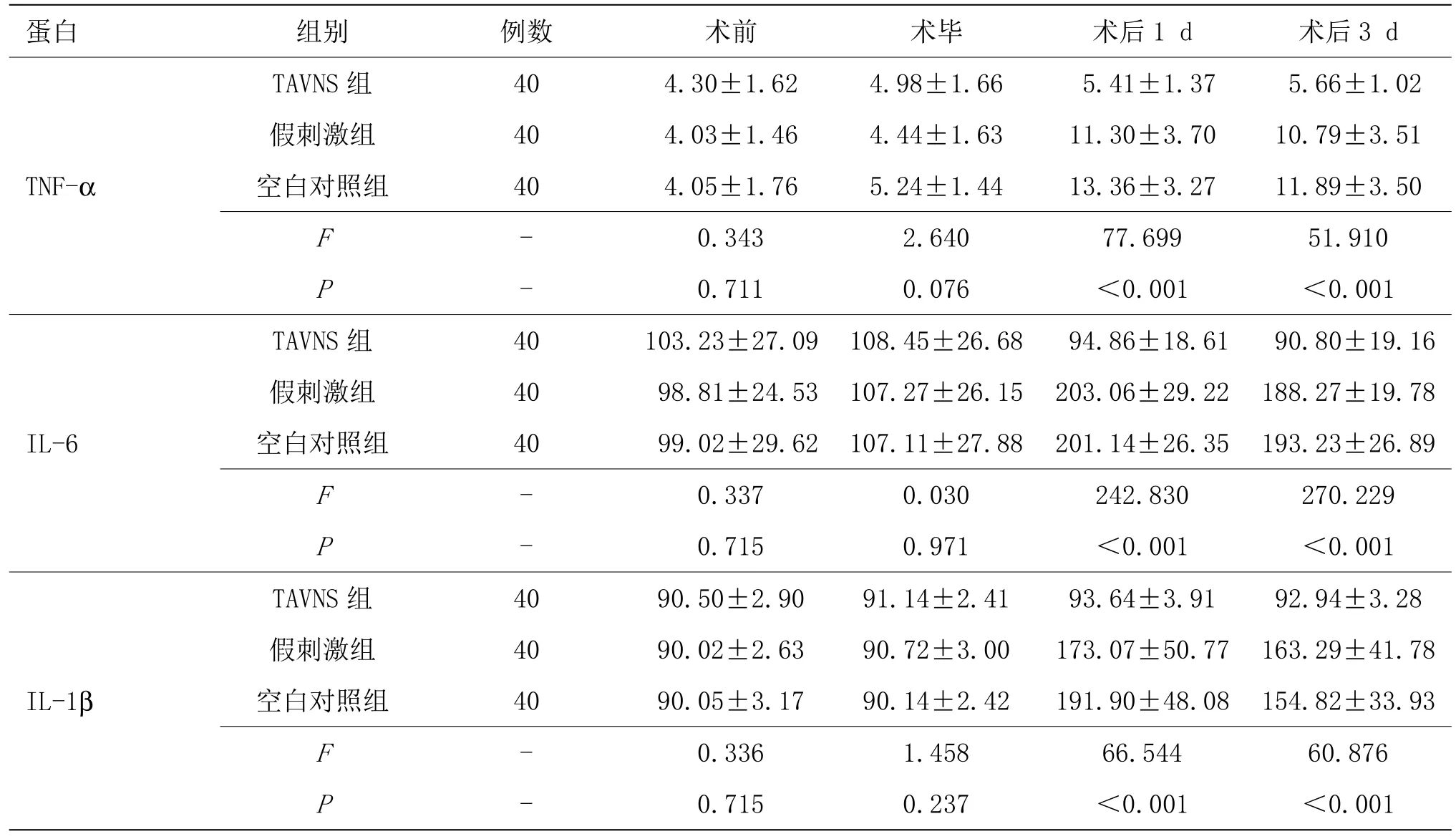
表4 3組不同時間血清TNF-α、IL-6、IL-1β水平比較 (±s, ng/mL)
蛋白 組別 例數 術前 術畢 術后1 d 術后3 d TNF-α TAVNS 組 40 4.30±1.62 4.98±1.66 5.41±1.37 5.66±1.02假刺激組 40 4.03±1.46 4.44±1.63 11.30±3.70 10.79±3.51空白對照組 40 4.05±1.76 5.24±1.44 13.36±3.27 11.89±3.50 F - 0.343 2.640 77.699 51.910 P - 0.711 0.076 <0.001 <0.001 IL-6 TAVNS 組 40 103.23±27.09 108.45±26.68 94.86±18.61 90.80±19.16假刺激組 40 98.81±24.53 107.27±26.15 203.06±29.22 188.27±19.78空白對照組 40 99.02±29.62 107.11±27.88 201.14±26.35 193.23±26.89 F - 0.337 0.030 242.830 270.229 P - 0.715 0.971 <0.001 <0.001 IL-1β TAVNS 組 40 90.50±2.90 91.14±2.41 93.64±3.91 92.94±3.28假刺激組 40 90.02±2.63 90.72±3.00 173.07±50.77 163.29±41.78空白對照組 40 90.05±3.17 90.14±2.42 191.90±48.08 154.82±33.93 F - 0.336 1.458 66.544 60.876 P - 0.715 0.237 <0.001 <0.001
4 討論
有研究[5]顯示,POCD的發生率可高達15.66%,且一旦發生,會導致患者死亡率增加,喪失工作能力的風險增高,并增加家庭社會負擔。在老年患者發生率更高,研究顯示老年患者術后早期認知功能障礙在術后1周發生率為23%,70歲以上的為29%,術后3個月超過70歲的患者發生率仍有14%,提示POCD的風險隨著年齡的增加而增加[6]。針對POCD,目前尚沒有療效確切的藥物或改善措施。因此,尚需要臨床進一步的探討。
迷走神經刺激術(VNS)是近年來興起的用于治療某些頑固性疾病的物理治療方法,美國 FDA分別于1997年2005年先后批準了頸部VNS作為難治性癲癇及抑郁癥的一種可行療法[7]。有一個小樣本的臨床試驗,用VNS治療10例老年性癡呆(AD)患者,經治療后患者的認知功能得到了明顯改善。直接的迷走神經刺激術需要暴露迷走神經并放置刺激器,手術風險高,并發癥多,臨床開展并不廣泛。近年來大量學者研究顯示經皮耳迷走神經刺激(TAVNS)是無需手術,費用較低,幾乎沒有不良反應,并能保證與傳統VNS有相近功效[8-9]。已有研究發現TAVNS在治療癲癇[10]、抑郁癥[11]、意識障礙[12]等多種腦及相關疾病中發揮著重要的作用。
耳針是中醫針灸學的一個重要組成部分,“耳者,宗脈之所聚也”。耳甲區有耳穴心、耳穴肝、耳穴腎、耳穴神門等分布,稱為“內臟代表區”。神經解剖學研究表明,耳甲是體表唯一有迷走神經分布的區域,刺激耳甲區可激活迷走神經耳支,其傳入纖維到達中樞神經系統,傳出纖維支配心血管系統、呼吸系統、胃腸道系統等外周器官。理論上,經皮耳迷走神經刺激能夠通過激活耳甲區傳入性迷走神經進而促使傳出性迷走神經傳出沖動增加,從而激活膽堿能抗炎通路,最終抑制炎癥反應。
中樞神經系統炎癥是POCD發生的重要原因,POCD的發生與術后外周血炎癥標記物濃度有關[13],因此減輕炎癥反應理論上可以改善POCD。TNF-α、IL-6、IL-1β是反映機體炎癥水平的常用指標,因此本研究中其表達水平被選擇用于代表術后的炎癥水平。結果顯示,手術結束后,由于創傷、應激和麻醉等原因,TNF-α、IL-6、IL-1β顯著上調。手術結束后,采用耳穴迷走神經刺激的TAVNS組患者TNF-α、IL-6、IL-1β表達水平顯著低于空白對照組,同時其MoCA評分也顯著高于空白對照組,提示,耳穴迷走神經刺激通過抑制術后炎性細胞因子的表達參與了POCD的改善。而假刺激組無顯著效果。參照RONG P等[11]研究,本試驗的假刺激采用的是將電極部位移動到耳郭非耳甲區部位,結果顯示,同樣的刺激參數下,假刺激組抑制炎性細胞因子TNF-α、IL-6、IL-1β的上調效果較TAVNS組明顯較差,提示耳甲區刺激有特定的治療效果。楊歡等[14]研究表明電針刺激可以降低糖尿病患者術后認知功能障礙的發生,并降低血清IL-6、IL-1β水平。李小嬌等[15]研究也發現連續8周的耳甲電針刺激可以顯著改善難治性抑郁的認知評分,和筆者的結果相一致。
NSE和S100β表達均是腦損傷的外周血反映指標,腦損傷后NSE和S100β表達上升后,可以透過血腦屏障滲出到外周血,因此通過測量外周血NSE和S100β的表達可以反映出腦損傷水平。POCD的發生的實質是手術中多種原因造成的腦損傷,因此術后外周血 NSE和S100β表達具有不同程度上調。RUSLIN M等[16]研究發現腦損傷患者腦神經元發生損傷,NSE就會釋放入細胞間隙和腦脊液,導致腦脊液和血清中 NSE的含量升高,血漿 NSE水平與患者腦損傷的嚴重程度呈顯著性相關。MERCIER E等[17]研究表明,檢測血清S100β蛋白可判斷顱腦損傷嚴重程度,腦損傷后 S100β蛋白水平與患者預后不良有顯著相關。徐靜等[18]研究表明,S100β和 NSE在腦內分別代表神經膠質細胞和神經元的損傷程度,二者聯合檢測具有互補的診斷價值,能更全面、準確地反映腦損傷程度。而林之薇[19]研究表明術前使用烏司他丁,可降低老年患者手術后出現圍術期神經認知紊亂的發生率,該保護作用與其抗炎作用有關,其抑制炎性細胞因子的表達后,可以顯著抑制外周血NSE、S100β和IL-6的上調。饒瑾等[20]研究表明高壓氧治療可以減少患者外周血 TNF-α、IL-6水平,抑制炎性反應,可以改善老年患者手術后認知功能。
炎性細胞因子導致認知功能障礙可能的機制是①炎癥導致血腦屏障受損,使外周血的有害物質更容易通過血腦屏障進入中樞[21-23]。②炎癥能促進神經細胞凋亡,導致神經細胞數量減少。③炎癥導致神經膠質細胞激活增加,進一步放大炎癥反應,導致細胞水腫,細胞間信息傳導障礙,表現為認知功能受損。近年來大量臨床及實驗研究[24-29]證實了TNF-α、IL-6等炎癥因子可以參與學習、記憶的生理過程,并在認知功能障礙的病理生理過程中發揮一定的作用,各種促炎細胞因子水平顯著升高,進一步激活小膠質細胞并破壞血腦屏障的通透性,從而引起腦損傷和認知功能障礙。
因此本試驗觀察了經皮耳迷走神經刺激治療前后患者外周血NSE和S100β的表達水平和TNF-α、IL-6、IL-1β的表達水平。研究發現,與空白對照組和假刺激組比較,TAVNS組術后1 d、3 d患者血清NSE、S100β和 TNF-α、IL-6、IL-1β水平降低;而假刺激組與空白對照組比較無明顯差異。術前3組患者MoCA評分組間比較,差異無統計學意義;而術后1 d、3 d、7 d, TAVNS組的評分顯著大于假刺激組和空白對照組。因此可以推斷出隨著時間的延長,多次經皮耳迷走神經刺激可以緩解老年患者術后早期認知功能障礙。
綜上所述,經皮耳迷走神經刺激可以顯著改善老年患者術后的認知評分,同時抑制NSE和S100β水平和炎性細胞因子TNF-α、IL-6、IL-1β水平的上調。

