龜鹿二仙膠加味方聯合潑尼松片治療Duchenne型肌營養不良的療效觀察
喻緒恩,余亞運,汪 昌,周 潔,歐夢迪,張亮亮,徐 銀,胡紀源,韓詠竹
(安徽中醫藥大學神經病學研究所附屬醫院,安徽 合肥 230061)
Duchenne型肌營養不良(Duchenne muscular dystrophy, DMD)屬于X連鎖隱性遺傳性肌病,是以四肢近端為主,緩慢進展的肌肉變性疾病,該病的發病機制關鍵是抗肌萎縮蛋白(dystrophin, Dys)的完全缺失,故其診斷的“金標準”是肌肉組織中Dys的免疫組織化學染色結果完全陰性[1-2]。DMD患者由于先天稟賦不足,精虧血少不能濡養肌肉筋骨,逐漸出現肌無力、肌萎縮,DMD的中醫相關研究比較匱乏[3-4]。目前,DMD仍無有效的治療方法,而其病情進展迅速,隨時有致死致殘可能,因此尋找對DMD患者有效的治療方法依然是臨床醫師亟待解決的難題[5-6]。眾多學者認為西醫治療DMD的療效甚微且不良反應突出,不能長期使用,而中醫藥治療DMD具有部分有效且不良反應少的優勢[7-8],中西醫結合治療可能是DMD有效治療方法的優化選擇。筆者采用龜鹿二仙膠加味方聯合潑尼松片治療DMD,取得較好的臨床療效,現報道如下。
1 臨床資料
1.1 診斷標準 參照中華醫學會神經病學分會制的《神經系統疾病診療指南及檢查技術操作規范》[2],依據患者性別、發病年齡、臨床癥狀和體征(Gowers征、腓腸肌肥大等)、顯著升高的血清肌酸激酶(creatine kinase, CK)以及X連鎖隱性遺傳的家族史,應高度懷疑DMD可能,確診依賴于Dys的免疫組織化學染色結果陰性[1-2]。
1.2 納入標準 ①均符合DMD的診斷標準;②肌電圖提示肌源性損害為主;③肌肉組織的Dys免疫組織化學表達完全缺失;④非過敏體質或者對方劑內已知藥物或已知成分過敏;⑤患兒及監護人知情同意。
1.3 排除標準 ①病情嚴重,合并嚴重并發癥,出現呼吸衰竭或心臟循環系統衰竭;②肌電圖以神經源性損害為主;③肌肉的病理學檢查結果提示炎癥改變為主,且使用皮質類固醇有明顯療效。
1.4 一般資料 本研究選擇2018年1月至2019年12月在安徽中醫藥大學神經病學研究所附屬醫院住院的DMD患者,均符合納入標準,共49例,均為男性。將患者分為觀察組和對照組。觀察組19例,發病年齡1~8歲,平均就診年齡(7.16±1.80)歲;病程6個月至7年,平均病程(3.16±1.68)年。對照組30例,發病年齡1~7歲,平均就診年齡(7.87±2.71)歲;病程6個月至12年,平均病程(4.40±2.52)年。兩組患者就診年齡、病程比較,差異均無統計學意義(就診年齡:t=-1.005,P=0.320;病程:Z=-1.843,P=0.065)。
2 方法
2.1 治療方法 觀察組患者采用龜鹿二仙膠加味方聯合潑尼松片治療,對照組患者采用單純潑尼松片治療。以龜鹿二仙膠為底方加味做成濃縮丸,其中鹿角片、人參、龜板、枸杞子的質量比為10∶1∶5∶2,每10丸約相當于原方9 g。脾腎虛弱者,加熟地黃、山茱萸、茯苓、山藥、陳皮;肝腎不足者,加杜仲、熟地黃、芍藥。兩組患者均服用潑尼松0.4 mg/(kg·d),每日1次,早餐后頓服。兩組療程均為3個月。
2.2 結局指標
2.2.1 癥狀評分 根據DMD的主要臨床癥狀和文獻[9]的病情分級標準,制定臨床癥狀評分標準(見表1),按“正常”“輕度”“中度”“重度”分別計10、9、6、3分。患者在治療前和治療3個月后分別檢測一次。
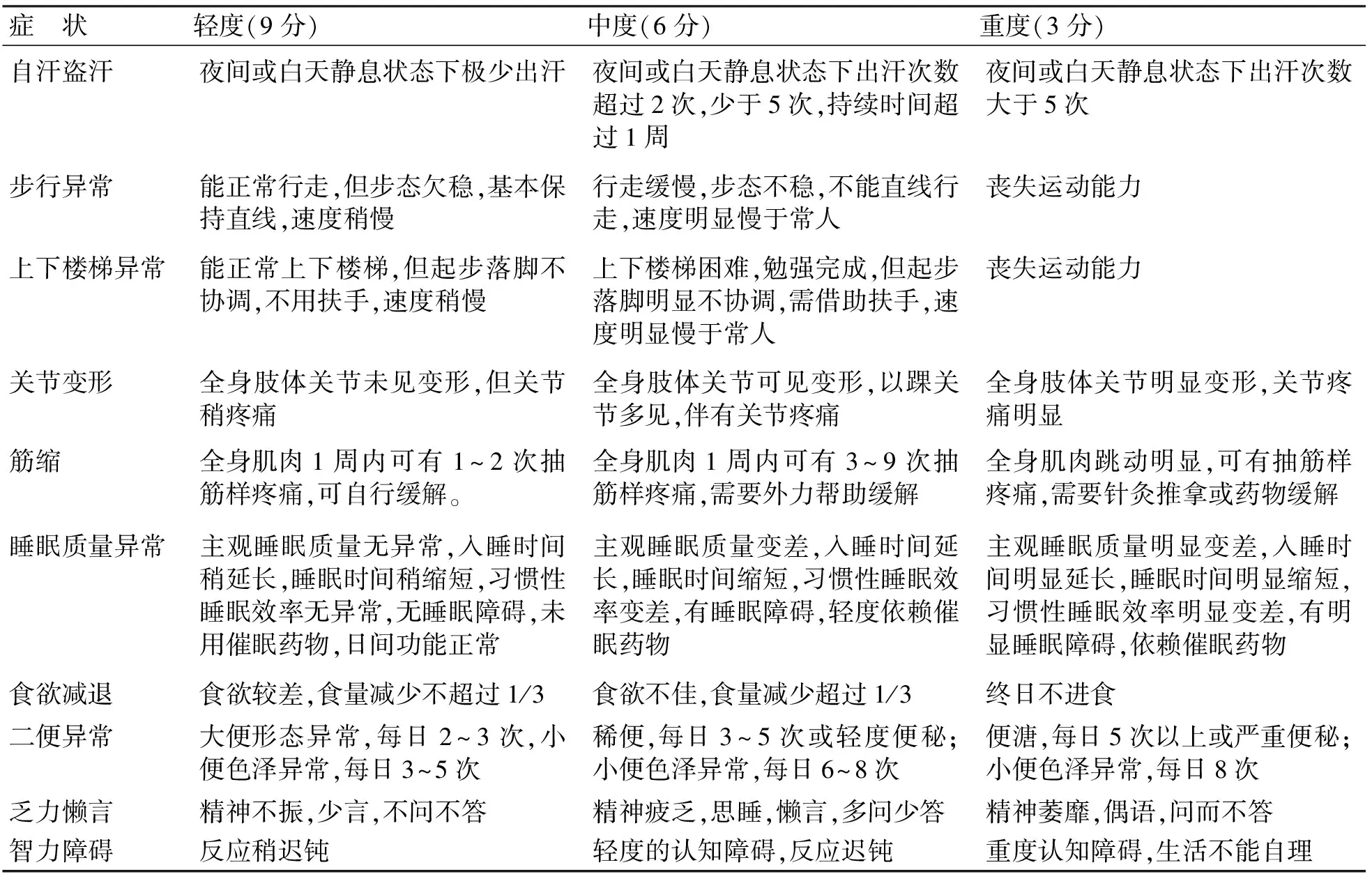
表1 臨床癥狀評分標準
2.2.2 血清特異性酶學指標 治療前和治療3個月后,分別采用連續監測法檢測血清CK水平,采用速率法檢測乳酸脫氫酶(lactic dehydrogenase,LDH)水平,采用免疫抑制法檢測肌酸激酶同工酶(creatine kinase-MB, CK-MB)水平。
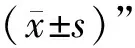
3 結果
3.1 兩組患者治療前后臨床癥狀評分比較 與治療前比較,對照組治療后自汗盜汗、睡眠質量、食欲減退、二便異常、乏力懶言評分顯著降低(P<0.05),而觀察組治療后自汗盜汗、步行異常評分顯著升高(P<0.05),兩組治療前后自汗盜汗、步行異常、睡眠質量異常、乏力懶言評分差值的差異具有統計學意義(P<0.05)。見表2。
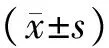
表2 兩組患者治療前后臨床癥狀評分比較
3.2 兩組治療前后血清CK、LDH、CK-MB水平比較 與治療前比較,對照組治療后血清CK、LDH、CK-MB水平均顯著降低(P<0.05);觀察組治療后CK、CK-MB水平均顯著降低(P<0.05)。觀察組治療后LDH和CK-MB水平降低程度明顯低于對照組(P<0.05)。見表3。
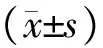
表3 兩組治療前后CK、LDH、CK-MB水平比較
4 討論
DMD的病理機制關鍵在于Dys蛋白的缺失,其功能不能正常表達,無法使肌纖維膜處于穩定狀態,并且增加了肌纖維膜所構建的肌細胞骨架脆性,在肌肉正常的收縮牽拉運動時,肌纖維極易受到牽拉、撕裂等損傷[10-11]。DMD患者血清CK、LDH、CK-MB均有不同程度升高,直接反映肌纖維壞死程度及患者病情輕重,尤以血CK升高具有特異性[10]。
DMD相當于中醫學“痿證”,是由先天稟賦異常所致。脾主肌肉四肢,為胃行其津液,中醫治療DMD相關痿證多從脾腎論治[12-13]。研究[14-15]表明,單用激素治療DMD的療效甚微,并且不良反應明顯。龜鹿二仙膠加味方聯合潑尼松片治療DMD是經過廈門大學周海虹及安徽中醫藥大學韓詠竹、胡紀源等反復論證的中西醫結合治療方法,符合臨床診療規范,是治療DMD的新途徑、新方法。龜鹿二仙膠源自羅美的《古今名醫方論》,為陰陽雙補之良方[7]。本方以鹿角片、龜板、人參、枸杞子等為主組方。方中重用鹿角片、龜板以補腎益氣、養血填精,補先天之本。精血旺則氣盛血行,肉得血榮則豐滿,骨得血榮則堅;人參補元氣,枸杞子補腎益精、養肝明目。本方陰陽氣血并補,先天后天兼顧。中醫藥可不同程度緩解DMD的癥狀[16-17],各版本DMD治療指南均推薦使用激素[6,18],因此中醫藥和激素都屬于DMD的有效治療方法。兩組患者的發病年齡及病程差異無統計學意義,本研究的一般資料結果與既往文獻報道一致[11]。
DMD患者臨床癥狀是反映其病情的重要指標,可以評判其病情的嚴重程度,直接反映DMD患者的預后,臨床癥狀包括步行障礙等運動功能的異常,以及自汗盜汗、睡眠質量降低等非運動功能的異常,這些癥狀的評分均是反向評分,直接或間接反映患者病情嚴重程度[9]。本研究結果顯示,觀察組治療后自汗盜汗、步行評分較治療前顯著升高(P<0.05),而對照組治療后自汗盜汗、睡眠質量、食欲、乏力懶言評分反而較治療前顯著降低(P<0.05)。結果提示龜鹿二仙膠加味方聯合潑尼松片可明顯改善DMD患者的臨床癥狀,其機制可能與促進DMD患者肌肉損傷的修復或延緩病情進展有關,但其具體機制尚需進一步研究。
血清CK、LDH、CK-MB水平的變化能直接反映DMD患者肌肉損傷的程度。研究[18-19]表明,激素治療后DMD患者血清CK水平的明顯下降可能會延緩病情。本研究結果顯示,與治療前比較,對照組治療后CK、CK-MB、LDH水平均顯著下降,而觀察組治療后CK、CK-MB水平顯著下降,且觀察組血清LDH、CK-MB下降程度不及對照組。血清CK水平升高是反映四肢肌肉尤其是四肢近端肌肉壞死的靈敏指標,而血清LDH、CK-MB水平升高則是反映心臟肌肉損傷的靈敏指標。觀察組血清LDH、CK-MB水平下降程度不及對照組,提示龜鹿二仙膠加味方對DMD患者四肢肌肉損傷的修復效果較優,而對心肌損傷的修復效果不佳。
綜上所述,龜鹿二仙膠加味方聯合潑尼松片治療DMD具有較好的療效,不僅可以改善自汗盜汗、步行異常等癥狀,而且可以修復CK、CK-MB等血清酶學指標的異常。

