經尿道前列腺剜除術在良性前列腺增生治療中的效果及對患者BUN、Scr、NSE、S100 β 蛋白水平的影響
薛金雄
福建醫科大學附屬福州市第一醫院泌尿外科,福建福州 350009
良性前列腺增生是老年男性群體多發的泌尿外科常見疾病之一,該病以尿路尿急、排尿不暢等癥狀為主要表現,病情輕者可服藥治療,待病情進展至重度時,則需要通過手術切除增生腺體,以促進病情的改善[1]。目前,電切鏡經尿道前列腺電切術、電切鏡經尿道前列腺剜除術均是良性前列腺增生的常用治療術式,前者的應用優勢在于創傷輕、恢復快,但在重度前列腺增生患者治療中難以改善其下尿路癥狀,而后者屬于新型微創手術,可結合電切系統與內窺鏡為一體,達到徹底切除增生前列腺的效果[2-4]。 基于此, 該院回顧性分析2018 年12 月—2020 年12 月收治的70 例良性前列腺增生患者的臨床資料,對經尿道前列腺剜除術的臨床效果進行分析,現報道如下。
1 資料與方法
1.1 一般資料
回顧性分析該院接受治療的70 例良性前列腺增生患者的臨床資料, 以治療術式的不同作為分組依據, 應用電切鏡經尿道前列腺電切術治療的患者設為對照組(35 例),應用電切鏡經尿道前列腺剜除術治療的患者設為觀察組(35 例)。 納入標準:患者符合 《2019 版中國泌尿外科和男科疾病診斷治療指南》[5]制定的相關診斷標準;患者臨床資料完整。排除標準:合并其他泌尿系統合并癥或免疫系統疾病者;合并巨大膀胱憩室者。 對照組年齡55~73 歲, 平均(65.35±3.20)歲;病程2~8 年,平均(6.84±1.73)年;前列腺增生程度:輕度11 例,中度13 例,重度11例。觀察組年齡55~73 歲,平均(65.43±3.11)歲;病程2~8 年,平均(6.73±1.50)年;前列腺增生程度:輕度10 例,中度10 例,重度15 例。 兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。 該研究經醫院醫學倫理委員會批準。 患者及其家屬均已簽署知情同意書。
1.2 方法
對照組應用電切鏡經尿道前列腺電切術治療:予以患者全麻, 取膀胱截石位后應用F24、F27 尿道探子擴張患者尿道,經尿道將F26 電切鏡插入膀胱,觀察前列腺增生情況。針對前列腺三葉增生患者,首先切除中葉,然后切除兩側葉,沿著5 點至7 點方向將中葉切割至前列腺外科包膜。 需注意兩側葉切割時作切口標志于精阜部, 待電切鏡轉至頸部后再切除增生組織與外科包膜,以此水平逆向切割右側葉,順向切割左側葉, 最后處理精阜部。 以上操作結束后,應用普通電切電極修整粗糙面,將絮狀壞死組織完全清除后沖洗膀胱。
觀察組應用電切鏡經尿道前列腺剜除術治療:予以患者全麻, 取膀胱截石位后應用F24、F27 尿道探子擴張患者尿道,經尿道將F26 電切鏡插入膀胱,觀察前列腺增生情況。針對前列腺中葉增生,切開膀胱經后作標志于雙側輸尿管, 由下至上切開至膀胱三角區, 通過橫切口連結患者膀胱三角區與精阜上緣,并沿著外科包膜進行分離。在兩側葉切除時分別朝著左、右兩個方向旋轉電切鏡鞘做切割處理,術中持續沖洗患者膀胱。
1.3 觀察指標
記錄兩組治療前后臨床指標[尿素氮(blood urea nitrogen,BUN)、血肌酐(serum creatinine,Scr)、神經元特異性烯醇化酶 (neuron-specific enolase,NSE)、S100β 蛋白]水平、圍術期指標(膀胱造瘺管留置時間、尿管留置時間)與并發癥(膀胱頸痙攣、包膜穿孔、暫時性尿失禁)發生情況。臨床指標檢測方法:分別于術前、術后24 h 取兩組空腹外周血5 mL,經過離心處理后保存上層血清于-80℃冰箱內,應用全自動生化分析儀(型號:iChem-540,深圳市奧特庫貝科技有限公司) 檢測BUN、Scr 水平,NSE 與S100β 蛋白水平測定時則分別應用NSE 試劑盒(上海將來實業股份有限公司)、S100β 蛋白試劑盒 (上海瑞番生物科技有限公司),方法均采用酶聯免疫吸附法。
1.4 統計方法
采用SPSS 22.0 統計學軟件分析數據, 符合正態分布的計量資料用(±s)表示,比較采用t檢驗;計數資料采用頻數或率(%)表示,比較采用χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 兩組治療前后臨床指標水平比較
術前,兩組BUN、Scr、NSE 與S100β 蛋白水平基本一致,差異無統計學意義(P>0.05);術后24 h,兩組BUN、Scr、NSE 與S100β 蛋白水平均高于術前,觀察組BUN、Scr 水平低于對照組,差異有統計學意義(P<0.05), 兩組NSE 與S100β 蛋白水平基本一致,差異無統計學意義(P>0.05),見表1。
表1 兩組治療前后臨床指標水平比較(±s)Table 1 Comparison of clinical index levels between the two groups before and after treatment (±s)
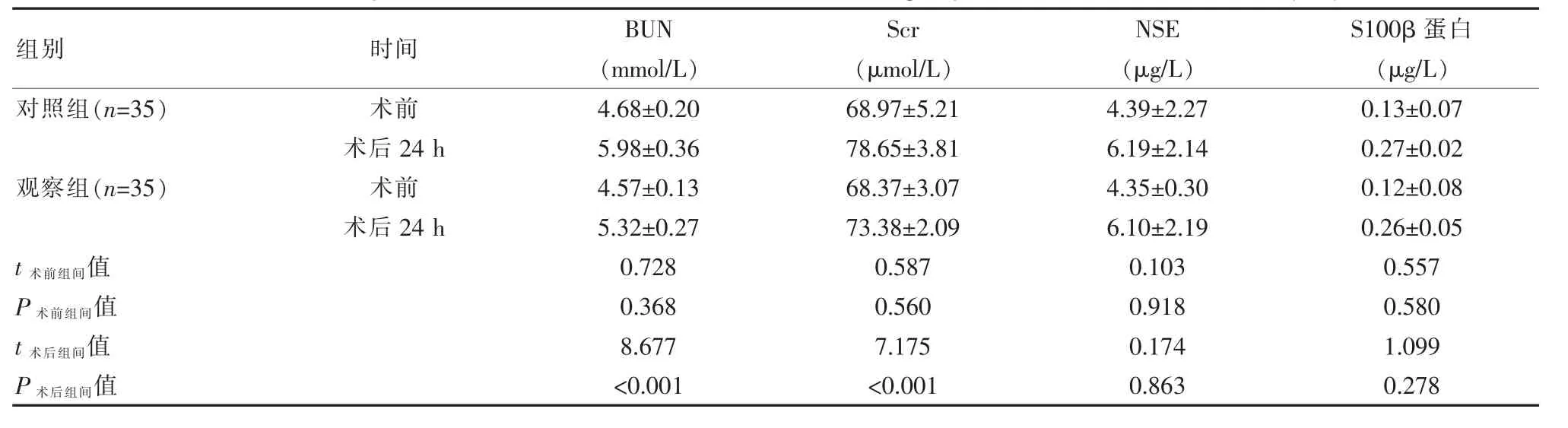
表1 兩組治療前后臨床指標水平比較(±s)Table 1 Comparison of clinical index levels between the two groups before and after treatment (±s)
?
2.2 兩組圍術期指標比較
觀察組膀胱造瘺管、尿管留置時間均短于對照組,差異有統計學意義(P<0.05),見表2。
表2 兩組圍術期指標比較[(±s),h]Table 2 Comparison of perioperative indicators between the two groups [(±s),h]

表2 兩組圍術期指標比較[(±s),h]Table 2 Comparison of perioperative indicators between the two groups [(±s),h]
?
2.3 兩組并發癥發生情況比較
對照組、 觀察組并發癥發生率分別為28.57%、8.57%,觀察組并發癥發生率低于對照組,差異有統計學意義(P<0.05),見表3。
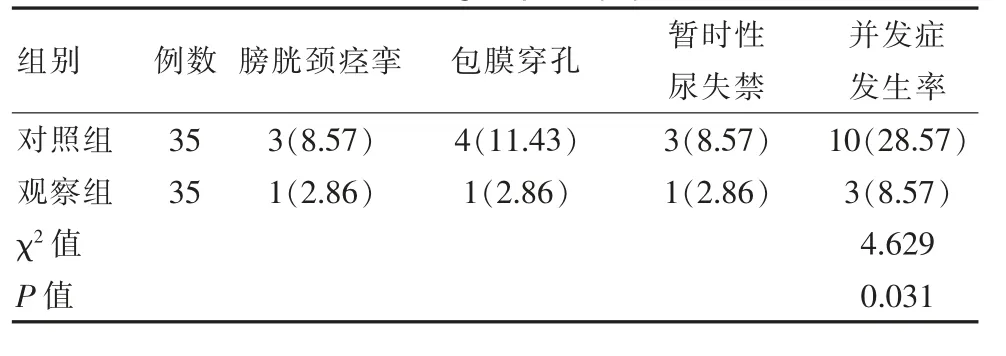
表3 兩組并發癥發生率比較[n(%)]Table 3 Comparison of the incidence of complications between the two groups [n(%)]
3 討論
電切鏡經尿道前列腺電切術是臨床上治療前列腺增生患者的一種常用術式, 術中高溫切割操作易對前列腺血管、海綿體神經造成損傷,影響患者術后性功能[6]。經尿道前淚腺剜除術則是基于男性解剖生理學角度開展各項操作的新型微創手術, 其可提供清晰的術野,提升增生前列腺的切除效果[7-8]。
該研究結果顯示, 術后24 h, 觀察組BUN、Scr水平低于對照組(P<0.05),兩組NSE 與S100β 蛋白水平基本一致(P>0.05),說明經尿道前列腺剜除術對患者腎功能的影響較輕。 術中直接在患者外科包膜進行止血,阻斷增生腺體的血管,可減輕手術操作的創傷性,避免反復出血[9-10]。 經尿道前列腺剜除術對患者周圍組織并不會造成熱損傷效應, 醫護人員沿著外科包膜將增生進行剝離,可保護包膜[11-12]。 有研究指出, 良性前列腺增生患者在侵入性手術治療后會繼發纖溶亢進或纖溶過度激活癥狀的原因多與前列腺本身組織結構以及術中操作對前列腺腺體的破壞有關,前列腺體本身富含纖維蛋白溶酶,而手術操作破壞腺體結構會導致纖維蛋白大量流入血循環,表現為術后大量出血[13-14]。 經尿道前列腺剜除術符合微創治療的理念,醫護人員首先鑒別外科包膜、增生腺體之間分界面,以此剝離、分離與剜除增生腺體,整體操作的封閉性較顯著,可減少手術操作對患者纖溶酶原的影響, 避免纖維蛋白原因過度激活而流入血液循環的情況,促進患者癥狀與病情改善[15]。除手術累及范圍較小以外, 該術式相應操作創傷性小,對患者組織并不會造成嚴重損傷,患者術后纖溶亢進或凝血機制過度激活的可能性、 出血風險均會因此降低。 研究結果顯示,對兩組膀胱造瘺管、尿管留置時間進行比較,觀察組均短于對照組(P<0.05);對照組、 觀察組并發癥發生率分別為28.57%、8.57%,觀察組并發癥發生率更低(P<0.05),與莊緒平等[14]研究結果相近。 莊緒平等對經尿道雙極等離子電切術(對照組)與剜除術(觀察組)治療良性前列腺增生的并發癥發生率進行對比得出,觀察組、對照組并發癥發生率分別為4.50%、18.20%,其中觀察組發生率較低(P<0.05),說明患者行經尿道前列腺剜除術治療后并發癥發生率低。 術后發生尿道感染或其他不適癥狀的原因多與術中操作方式及患者前列腺體積大小有關;若手術無法保證操作的精準度,多依靠經驗和感覺去探查患者前列腺病變情況則難以獲取前列腺切除體積的準確參考資料[15-16]。經尿道前列腺剜除術實施過程中是通過電切鏡觀察患者前列腺增生情況,隨后根據精阜明確前列腺外科包膜,以此為標志切開前立腺, 最后通過鏡鞘向膀胱頸方向逆行于中葉與兩側葉腺體進行剝離、剜除,以上操作接近于解剖結構的開放手術摘除,故安全性高,再加上無熱損傷效應, 患者術后無需長時間留置膀胱造瘺管與尿管,能夠加快恢復速度,避免切口長期不愈合而引發并發癥[17-18]。
綜上所述, 應用經尿道前列腺剜除術對良性前列腺增生患者進行治療,不會對患者腎功能造成嚴重影響,有助于降低其術后出血風險,且術后患者無需長時間留置膀胱造瘺管、尿管,并發癥發生率較低。

