L-色氨酸-Hg2+-青霉胺體系的熒光光譜及分析應用
閆晶晶, 張甜, 胡詠梅, 李政, 劉劍雄, 胡小莉
1.西南大學 化學化工學院,重慶 400715;2.成都市第二人民醫院,成都 610017
青霉胺(3,3-二甲基半胱氨酸,PA)是青霉素的代謝產物,也是一種含巰基氨基酸[1].同時青霉胺也是一種具有藥理作用的手性化合物,用于治療多種疾病,如威爾遜氏病、類風濕性關節炎、硬皮病及重金屬中毒等[2].青霉胺作為手性化合物,存在D-青霉胺(D-PA)和L-青霉胺兩種對映異構體,它們的藥效及毒理作用差別很大,其中L-PA有一定毒副作用,只有D-PA有治療疾病的作用.世界衛生組織已經將D-PA列為基礎醫療中的必備藥品.因此,建立簡單、快速、高靈敏、高選擇檢測D-PA的方法具有重要意義.目前報道的檢測D-PA的主要方法有電化學發光[3]、電化學法[4]、分光光度法[5]、HPLC法[6]、圓二色性法[7]和離子色譜法[8].此外,熒光光譜法相比于其他方法更簡單、高效,且靈敏度更高.近年來,已有較多測定D-PA的熒光法報道[9-11],但是有的熒光探針合成步驟復雜繁瑣,限制了方法的使用.本研究利用一種簡單易得的熒光探針來檢測D-PA.研究發現,L-色氨酸(L-Trp)在352 nm處有很強的熒光發射峰,隨著Hg2+的加入,L-Trp熒光被猝滅.接著加入D-PA,L-Trp的熒光得到恢復,據此建立了一種“開-關”模型來檢測D-PA,其反應機理見圖1.
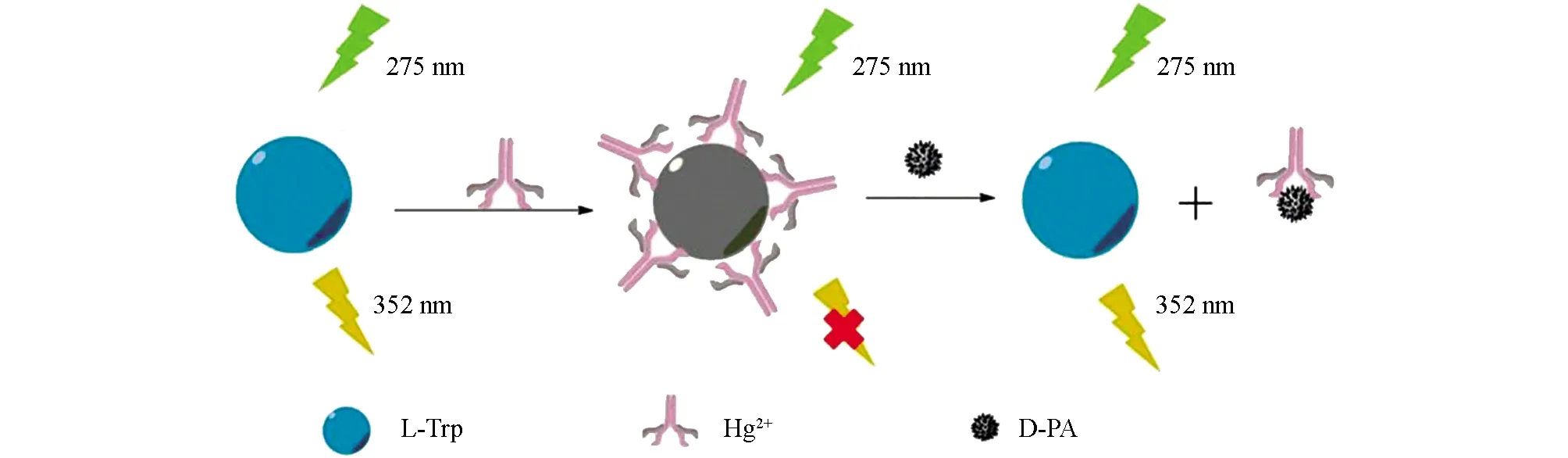
圖1 L-Trp測定D-PA的反應機理
1 實驗部分
1.1 實驗儀器與材料
Hitachi F-2500型熒光分光光度計(日立科學儀器有限公司,日本);UV-2450型紫外-可見分光光度計(島津公司,日本);pHSJ-4F酸度計(上海儀電科學儀器股份有限公司,上海).
L-Trp、D-PA(阿拉丁試劑有限公司,上海);HgCl2(四川科倫醫藥貿易有限公司,成都);Britton-Robinson緩沖溶液:2.71 mL 85% 磷酸(重慶北碚化學試劑廠,重慶),2.36 mL 冰醋酸(重慶川東化工有限公司,重慶)和2.47 g 硼酸(重慶北碚化學試劑廠,重慶)溶于1.0 L蒸餾水中,用0.2 mol/L NaOH調節不同pH值.實驗過程中所用水均為超純水.
1.2 實驗方法
在10.0 mL的比色管中依次加入pH=4.8的BR緩沖溶液1.0 mL,0.5 mL 4.0 × 10-4mol/L L-色氨酸,0.5 mL 1.0 × 10-2mol/L Hg2+和一系列不同濃度的D-PA,用蒸餾水定容至刻度后搖勻,在室溫下靜置15 min.在熒光分光光度計上以λex=275 nm激發,進行波長掃描,記錄體系的熒光光譜,并在波長352 nm處測定樣品和試劑空白的熒光強度,ΔF=F-F0.狹縫寬度為10 nm.
2 結果與討論
2.1 熒光光譜
以最大激發波長275 nm對L-Trp溶液進行熒光光譜掃描,發現其最大熒光峰位于352 nm處(圖2中曲線1),而Hg2+和D-PA均無熒光.L-Trp與D-PA溶液混合,L-Trp的熒光強度幾乎沒有變化(圖2中曲線2).然而,在一定濃度的L-Trp中加入適量Hg2+后,由于Hg2+與L-Trp 結構中的羧基結合,使得L-Trp在352 nm的熒光猝滅[12](圖2中曲線4),接著向溶液中加入與Hg2+結合能力更強的D-PA,L-Trp被釋放出來,溶液熒光逐漸得到恢復(圖2中曲線3).
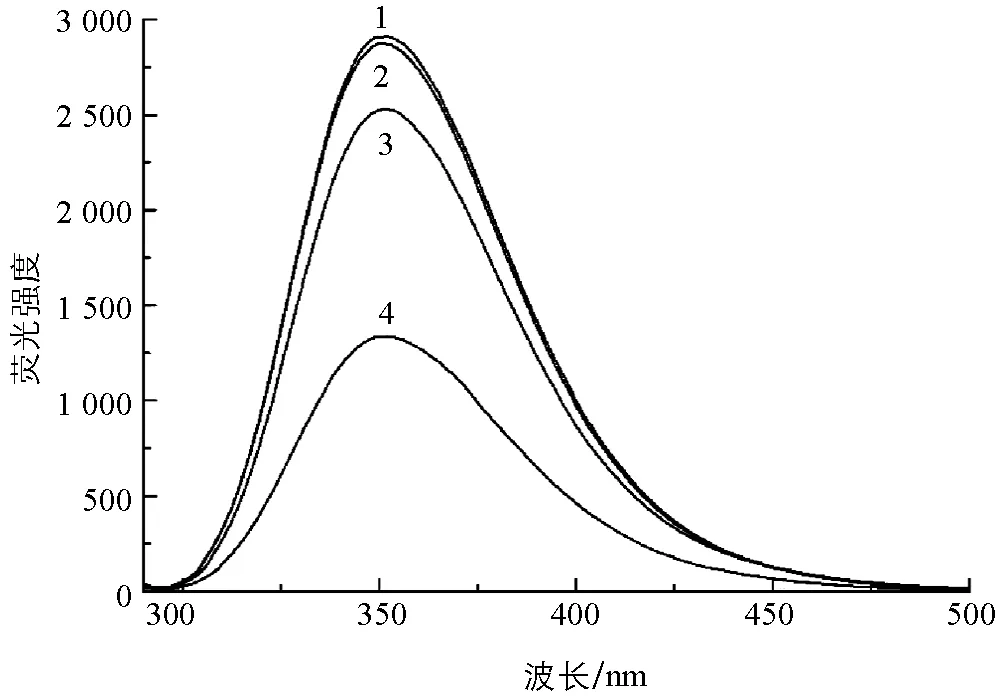
1.L-Trp;2.L-Trp+D-PA;3.L-Trp+Hg2++D-PA;4.L-Trp+Hg2+;cL-Trp=2.0×10-5 mol/L; mol/L;cD-PA=5.0×10-5 mol/L;pH=4.8.
2.2 反應條件優化
2.2.1 pH值的影響
實驗探究了不同pH值的BR緩沖溶液對反應體系的影響.由圖3可知,L-Trp-Hg2+和L-Trp-Hg2+-D-PA兩個反應體系的熒光強度在pH=2.0~3.1范圍逐漸增強,pH=3.1~7.2之間熒光逐漸減弱,但熒光恢復值(ΔF)在pH=4.0~5.0時最大(圖3插圖).因此本實驗選用pH=4.8的BR溶液為反應介質.
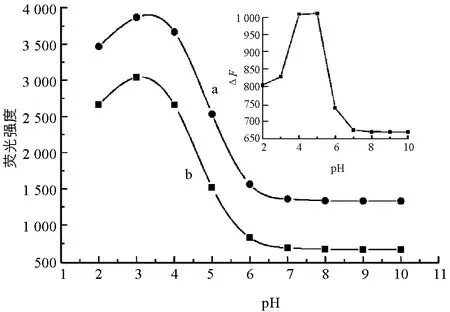
a.cD-PA=2.0×10-5 mol/L;b.cD-PA=0.
2.2.2 Hg2+濃度的影響
L-Trp作為一種常見天然氨基酸,已有文獻報道Hg2+可以與羧基螯合從而猝滅L-Trp的熒光[13].如圖4所示,在Hg2+濃度為4.0×10-4mol/L時,L-Trp熒光猝滅程度最大,且隨著Hg2+繼續加入,熒光強度保持不變.故本實驗選擇5.0×10-4mol/L為Hg2+后續實驗濃度.
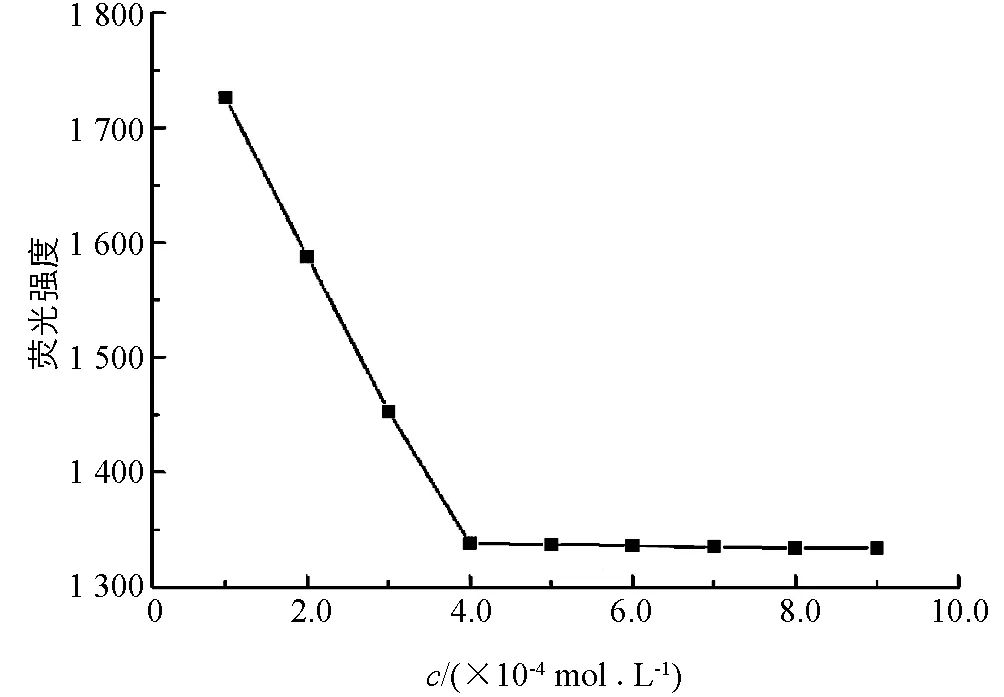
cL-Trp=2.0×10-5 mol/L;pH=4.8.
2.2.3 離子強度和反應時間的影響
研究了離子強度對三元反應體系的影響(圖5),當NaCl濃度低于4.0×10-4mol/L時,反應體系熒光強度較穩定;當NaCl濃度高于4.0×10-4mol/L時,熒光強度有所增加,因此,在實際樣品檢測過程中要注意控制離子強度,避免高濃度鹽類的引入.此外,實驗發現L-Trp的熒光在15 min恢復到最大值并且在1 h內保持穩定,因此選擇15 min為反應時間.
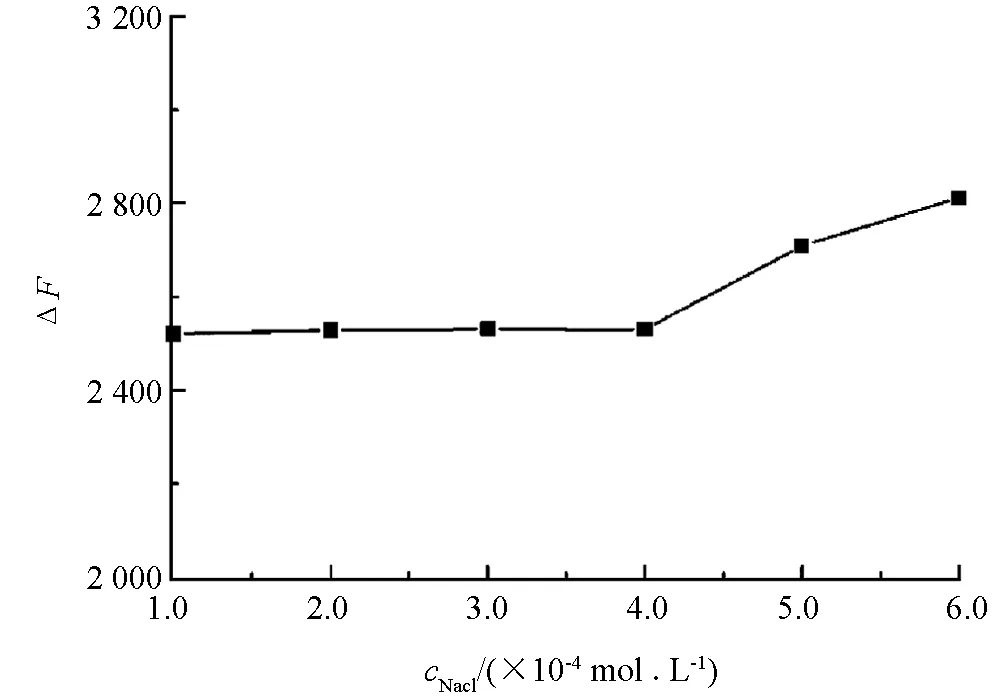
cL-Trp=2.0×10-5 mol/L, mol/L,cD-PA=5.0×10-5 mol/L,pH=4.8.
2.3 方法的選擇性
為了考察該方法的選擇性,在優化的實驗條件下,探究了20種常見物質對測定D-PA的影響.當共存物質引起的熒光強度改變在相對誤差±5%之內,通常認為不會對檢測造成影響.由表1可知,常見的金屬離子、氨基酸、糖類對D-PA的檢測幾乎沒有影響,表明本法具有較好的選擇性,可以應用于實際樣品的檢測.
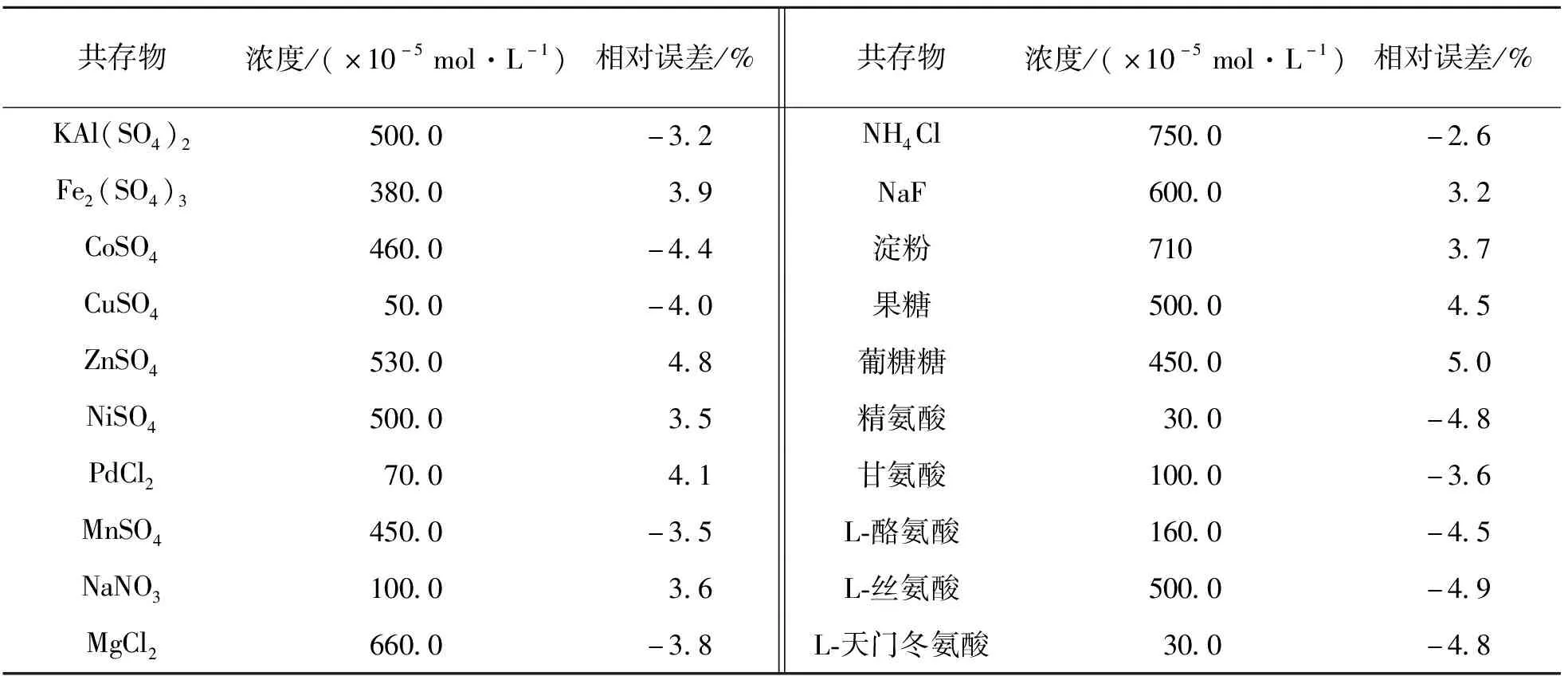
表1 共存物質的影響(cD-PA=5.0×10-5 mol/L)
2.4 標準曲線
按照前述實驗方法,測定不同D-PA濃度下反應體系的熒光強度.如圖6所示,隨著D-PA的加入,L-Trp的熒光逐漸恢復,熒光恢復程度(ΔF)與D-PA濃度在0.44~50.0 μmol/L范圍內呈現良好的線性關系(圖6插圖),線性回歸方程為ΔF=226.6C+51.8,相關系數為0.999 3,檢出限(3σ/K)達0.13 μmol/L.表2列出了本法與其他方法測定D-PA的比較,由此可以看出,本法靈敏度高,操作簡單,更具有實用價值.
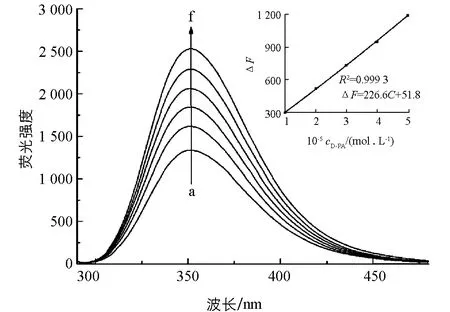
cL-Trp=2.0×10-5 mol/L, mol/L,cD-PA×10-5 mol/L/a-f=0.0,1.0,2.0,3.0,4.0,5.0.
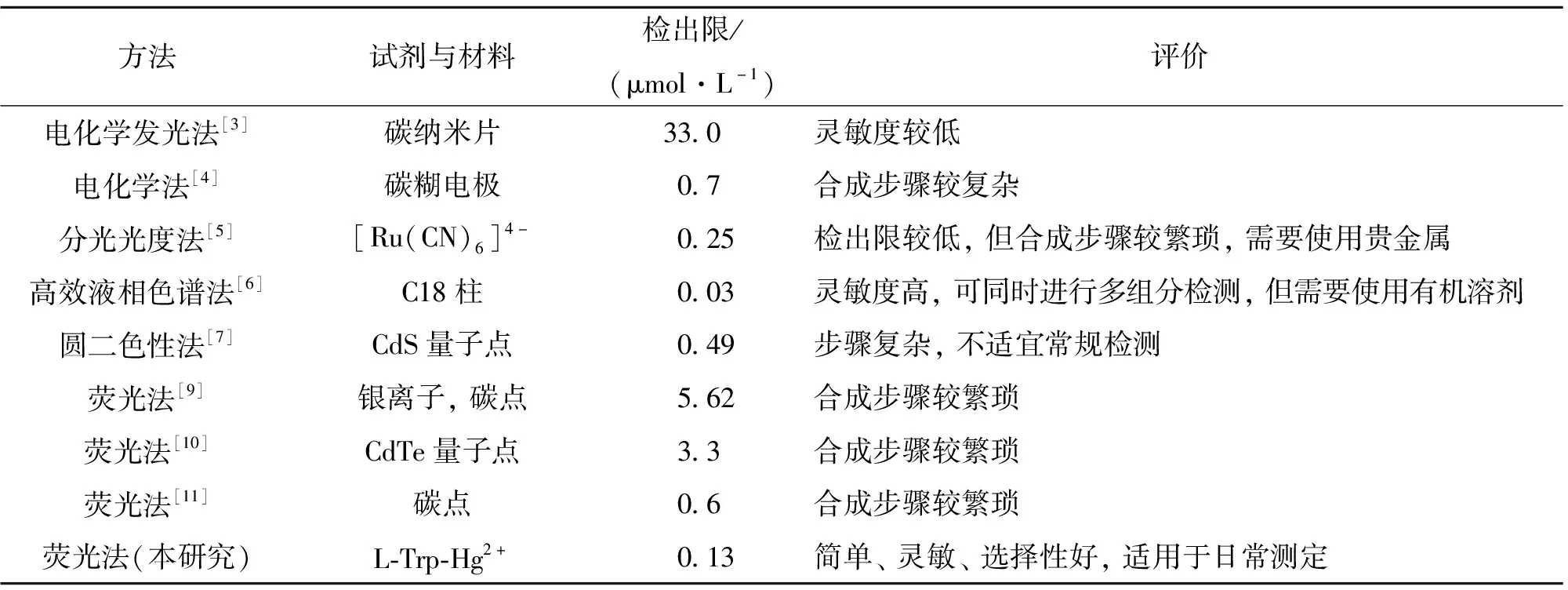
表2 測定D-PA的不同方法的比較
2.5 邏輯門的模擬應用
分子傳感器與目標分析物協同作用,對反應條件進行信息處理,將一個或多個反應條件作為輸入信號,熒光信號的改變作為輸出信號[14].基于熒光響應可以通過Hg2+和D-PA的加入來回切換,體系熒光強度進入“on-off-on”模式,為此構建了IMPLICATION邏輯門[15].以 L-Trp作為一種邏輯門裝置,設定Hg2+(輸入1)和D-PA(輸入2)為輸入信號,352 nm處熒光強度為輸出信號,0和1分別代表熒光猝滅和未猝滅.無信號輸入(0,0)或只有D-PA輸入(0,1),352 nm處熒光吸收很強,輸出為1;單獨Hg2+輸入(0,1)時,熒光猝滅,輸出為0.當兩者同時輸入(1,1)時,L-Trp熒光恢復,輸出為1.表3為邏輯門對應的真值表,圖7為熒光輸出IMPLICATION邏輯圖.
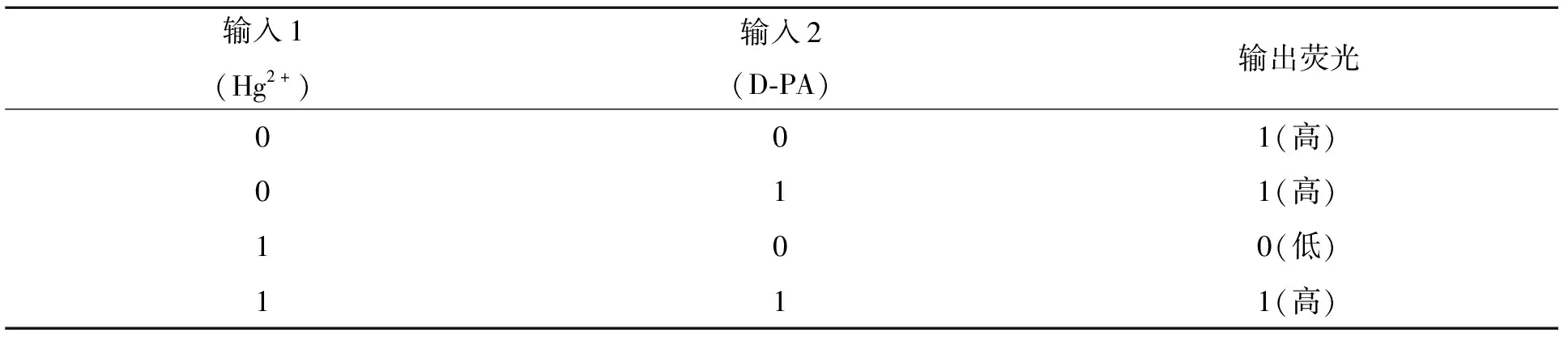
表3 邏輯門真值表
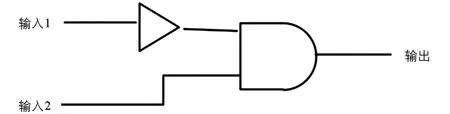
圖7 IMPLICATION邏輯圖
2.6 實際樣品的測定
為了評價本方法的適用性和有效性,將本方法用于青霉胺藥片中D-PA含量檢測.隨機選10片藥片(上海信誼藥廠有限公司),研細.稱取相當于0.25片質量的樣品,溶解、過濾、除去不溶物,最后定容至500.0 mL容量瓶中,備用.吸取0.5 mL待測液于10.0 mL比色管中進行檢測,結果見表4.通過標準加入法測得回收率和相對標準偏差分別為96.0%~103.8% 和2.8%~4.0%,表明本方法具有較高的準確度和較好的重復性,可以用于實際樣品的測定.
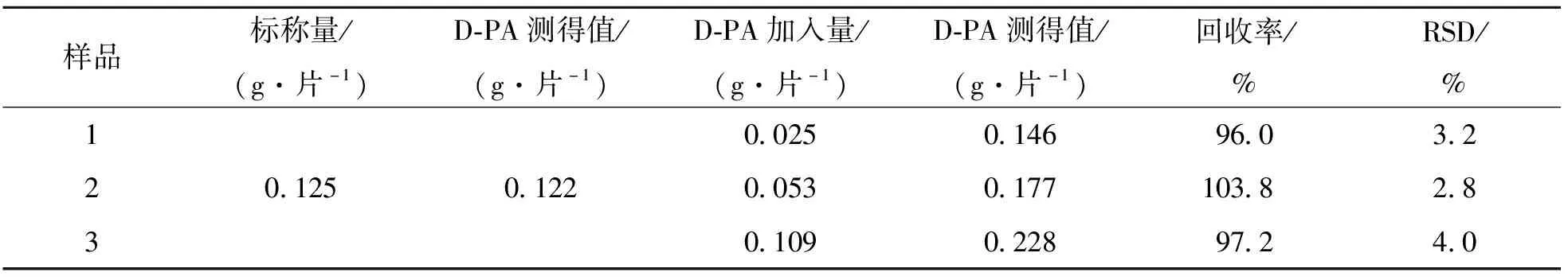
表4 藥片中D-PA的測定結果
3 結論
利用Hg2+與D-PA之間的強螯合作用,使得Hg2+脫離L-Trp,L-Trp熒光得到恢復,從而設計了分子邏輯門,并建立了D-PA的熒光檢測新方法.本方法相較于其他方法,簡單易行、選擇性好、靈敏度高,無需精密的儀器和復雜的合成步驟,適用于青霉胺藥片含量的測定.

