氧化應激對豬前體脂肪細胞分化及PPARγ選擇性剪接的影響
魏 芳,李帥兵,宋蘇堤,苗 健,張國華,盧建雄
(西北民族大學 生命科學與工程學院,甘肅 蘭州 730030)
脂肪細胞分化是脂肪形成的基礎,影響動物胴體品質和肉質性狀。揭示脂肪細胞分化機制,對于提高畜禽生產效益和改善肉品質具有重要意義。機體內、外環境多種因素影響脂肪細胞分化,其中氧化還原平衡是維持細胞各種生物學功能的基礎。體外環境變化及體內物質代謝產生的超氧陰離子(O2-)、過氧化氫(H2O2)和一氧化氮(NO)等各種活性氧(ROS)均可造成機體及組織細胞氧化應激,影響細胞發育、分化、凋亡及代謝。脂肪細胞攝取能量物質后產生活性氧,改變細胞氧化還原電位,促進脂肪生成[1]。脂肪細胞的氧化應激會影響脂肪細胞增殖分化、脂肪合成及分解、細胞因子的分泌以及胰島素敏感性等,進而對脂肪沉積產生影響[2]。
過氧化物酶體增殖物激活受體γ(PPARγ)作為配體激活的轉錄因子,在脂肪細胞分化中起著樞紐作用[3]。PPARγ激活后啟動脂肪細胞分化及脂肪生成基因表達,導致甘油三酯合成與持續積累,調控脂肪細胞從發育到代謝的各個生物學過程[4],包括脂肪細胞分化、胰島素敏感性、脂肪生成和細胞生存[5]。PPARγ編碼基因富含外顯子和內含子順式調控元件,因而可以產生嚴格的選擇性剪接調控[6]。研究表明,PPARγ外顯子6中有絲氨酸/精氨酸富集剪接因子1(serine/arginine-rich splicing factor 1,SRSF1)的結合位點[7],SRSF1與PPARγ外顯子6結合可能有助于跳過外顯子5產生PPARγ選擇性剪接亞型PPARγΔ5[8]。PPARγ外顯子5跳躍是一種自然發生的選擇性剪接事件,在人類皮下和內臟脂肪組織、脂肪細胞、APCs和HEK239等細胞均檢測到PPARγΔ5[9-10]。RNA免疫沉淀實驗也證實,剪接因子SRSF1與PPARγ的前體及成熟mRNA結合促進外顯子5跳躍。PPARγ外顯子5跳躍導致蛋白質編碼框移位,產生缺失配體結合域的PPARγ亞型PPARγΔ5。PPARγΔ5對野生型PPARγ活性具有顯性負性影響[8],可能通過影響PPARγ的作用調控脂肪細胞的分化。因此,本文就氧化應激對豬前體脂肪細胞分化及PPARγ選擇性剪接的影響做了初步研究,為深入了解豬脂肪形成的調控機制提供參考。
1 材料與方法
1.1 材料
3~6日齡杜×長×大雜交仔豬由蘭州瑞源農業科技有限公司提供;DMEM/F12 1:1培養基(HyClone公司);胎牛血清FBS(浙江天杭生物科技股份有限公司);注射用青霉素鈉和硫酸鏈霉素、0.25% EDTA胰酶、油紅O和DMSO、I型膠原酶(Solarbio公司);牛血清白蛋白(Gibco公司);地塞米松(DEX)、3-異丁基-1-甲基黃嘌呤(IBMX)、胰島素(INS)、葡萄糖(Sigma公司);細胞總RNA抽提試劑盒、反轉錄試劑盒和熒光定量PCR試劑盒(TaKaRa公司,大連);無水乙醇(天津市富宇精細化工有限公司)、DEPC水(大連美侖生物技術有限公司)。
1.2 方法
1.2.1原代豬前體脂肪細胞培養 將仔豬麻醉處死、體表消毒后,在無菌狀態下分離皮下脂肪組織,PBS清洗后剪碎,用0.1% Ⅰ型膠原酶消化液于37 ℃水浴鍋中消化1 h左右,終止消化并過濾,濾液離心10 min,棄上清,加入培養液吹打均勻,然后用含FBS 10%的DMEM/F12培養液重懸,接種于6孔板中,于37 ℃、5 %CO2培養箱中培養,隔天換液[11-12]。細胞生長至80%匯合后,用5 g/L胰蛋白酶37 ℃消化,接種至12孔細胞培養板。
1.2.2過氧化氫處理12孔板培養的前體脂肪細胞生長至80%匯合后,用含0.5 mm IBMX、1 μm DEX和5μg/ml胰島素的DMEM/F12誘導分化培養液培養72 h,然后用DMEM/F12維持培養液培養,隔天換液。分別在誘導分化后2 d、4 d和6 d,用H2O2終濃度為500 μmol/L的培養液培養24 h構建氧化應激細胞模型,檢測細胞分化及提取總RNA。
1.2.3油紅O染色提取法檢測細胞分化12孔板培養的細胞H2O2處理24 h后,按于淇等[13]報道的油紅O染色提取法檢測細胞分化,并在顯微鏡下觀察、拍照。
1.2.4基因mRNA表達檢測 吸出培養液,PBS清洗細胞后,提取細胞R N A。提取的R N A用超微量紫外分光光度計(Nanodrop One)檢測R N A純度和濃度,按照逆轉錄試劑盒說明書,反轉錄合成c D N A。反轉錄反應體系(10 μl):5×Primer 2 μl,1~3 μl RNA,ddH2O補至10 μl。反應程序:37 ℃、15 min,84 ℃、5 s,4 ℃、30 min。cDNA于-20 ℃冰箱保存。按TaKaRa公司GreenTM Premix Ex TaqTM II(Tli RNaseH Plus)試劑盒使用說明書,用實時熒光定量PCR儀(CFX96,BIO-RAD公司,美國)檢測相關基因的表達量,所用引物(由湖南艾科瑞生物工程有限公司合成)見表1,反應體系:cDNA 1 μl,上、下游引物(5 μmol/L)各0.4 μl,SYBR?Premix Ex TaqTMⅡ (2×) 5 μl,ddH2O 3.2 μl,共10 μl。參考岳小婧等[12-14]反應程序進行PCR反應。采用2-ΔΔCt法計算基因mRNA相對表達量。

表1 PCR引物
1.2.5統計分析 試驗數據采用SPSS 25.0軟件統計處理,用One-Way ANOVA進行單因素方差分析,用最小顯著極差法(LSD)進行多重比較。結果用平均值±標準差表示。
2 結果
2.1 氧化應激抑制豬脂肪細胞分化
豬前體脂肪細胞成脂誘導后,用H2O 2處理24 h造成細胞氧化應激,油紅O染色提取法檢測誘導后3 d、5 d和7 d細胞的分化。從圖1可以看出,與對照組相比,H2O2處理顯著降低成脂誘導第5 d和第7 d前體脂肪細胞的分化(P<0.05),成脂誘導第3 d細胞的分化僅有降低趨勢(P>0.05)。圖2顯示成脂誘導后7 d脂肪細胞油紅O染色結果。H2O2處理后,油紅O染色細胞數減少,脂滴較小。可見,H2O2處理誘導的氧化應激可抑制豬前體脂肪細胞分化。
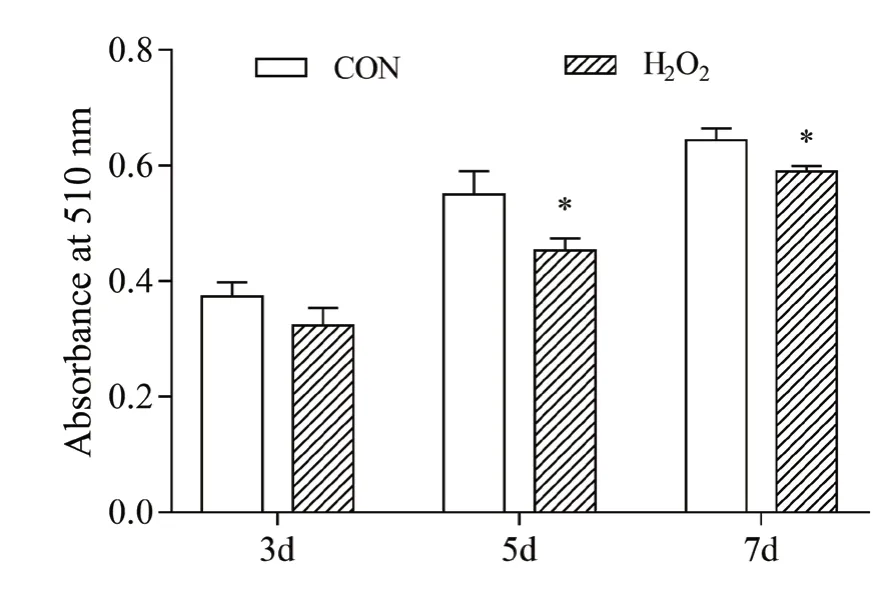
圖1 H2O2處理對豬前體脂肪細胞分化的影響
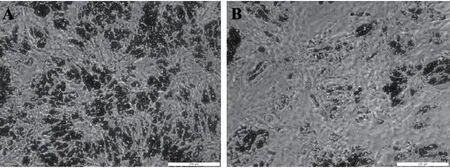
圖2 成脂誘導后7d豬前體脂肪細胞油紅O染色結果
2.2 H2O2處理對豬脂肪細胞成脂分化基因表達的影響
成脂誘導6 d的脂肪細胞用H2O2處理24 h后,提取RNA,檢測分化相關基因mRNA表達的變化,結果如圖3所示。與對照組相比,H2O2處理極顯著降低細胞FABP4、C/EBPα、SCD和PPARγ mRNA表達(P<0.01),但Txnip和LPL表達極顯著提高(P<0.01),表明氧化應激通過影響細胞成脂分化相關基因表達抑制豬前體脂肪細胞分化。

圖3 H2O2處理對豬脂肪細胞基因表達的影響
2.3 氧化應激抑制脂肪細胞PPARγ選擇性剪接
如圖4所示,H2O2處理24 h,脂肪細胞選擇剪接異構體PPARγΔ5和剪接因子SRSF1 mRNA表達均極顯著降低(P<0.01)。可見,氧化應激可以抑制PPARγ的選擇性剪接。
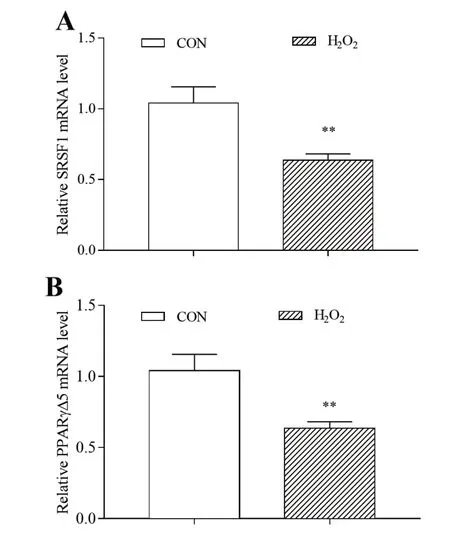
圖4 氧化應激對豬脂肪細胞SRSF1、PPARγΔ5 mRNA表達的影響
3 討論
氧化應激(Oxidative Stress)是指生物體內氧化與抗氧化作用失衡的一種狀態。許多因素如動物生理階段改變、環境變化和外源致病菌及毒素等都會破壞機體氧化還原平衡,引發氧化應激。營養物質在體內代謝過程中也可以產生大量超氧陰離子、過氧化氫和一氧化氮等活性氧。體內積累的過多活性氧破壞組織器官黏膜屏障,導致機體功能和代謝損傷,引起疾病發生[15]。機體超氧化物歧化酶(SOD)、過氧化氫酶(CAT)、谷胱甘肽過氧化物酶(GSH-Px)等抗氧化酶及非酶抗氧化系統與氧自由基相互作用,維持機體適度的氧化還原平衡。研究表明,氧化還原平衡影響脂肪細胞分化及脂質代謝。細胞內氧化還原電位在脂肪細胞分化過程中經歷了顯著變化[16],細胞外氧化還原環境通過影響細胞內活性氧的產生影響細胞過程[17]。然而,氧化應激對脂肪細胞分化的影響還存在爭議。過氧化氫誘導的氧化應激促進3T3-L1細胞PPARγ表達及成脂分化[18],增強機體脂肪積累[19-20]。在小鼠OP9前體脂肪細胞分化過程中,隨著細胞內活性氧的積累,脂滴增加[21]。然而,Pessler等[22]報道,氧化應激通過降低C/EBP的DNA結合活性抑制3T3-L1前體脂肪細胞分化。同樣,Nitta等[23]也發現,H2O2處理誘導的氧化應激可下調3T3-L1細胞PPARγ表達,降低C/EBP DNA結合活性,抑制細胞分化。與此一致,本研究用H2O2處理原代培養豬前體脂肪細胞時,細胞分化顯著減弱,成脂分化關鍵轉錄因子C/EBPα和PPARγ及其下游生脂基因FABP4和SCD表達降低,而脂解基因LPL表達提高。研究證明,氧化還原環境通過影響細胞內活性氧的產生影響細胞過程[17],C/EBPα和PPARγ是介導活性氧影響脂肪生成的主要因子[24]。由此可見,H2O2誘導的氧化應激通過下調C/EBPα和PPARγ表達抑制豬前體脂肪細胞分化。
作為一種氧化還原調節蛋白,硫氧還蛋白互作蛋白(Txnip)參與許多細胞生理過程[25],可通過抑制硫氧還蛋白(thioredoxin,Trx)的還原活性調節細胞的氧化還原狀態[26]。Txnip是PPARγ的負調控因子,過表達Txnip可抑制豬前體脂肪細胞分化、下調PPARγ表達[13];相反,Txnip表達沉默上調PPARγ表達、促進分化[12]。本研究用過氧化氫處理豬前體脂肪細胞,Txnip表達顯著提高。與此一致,H2O2處理引起細胞氧化應激、生長停滯,Txnip表達提高[27-28]。這些結果也支持了氧化應激抑制豬前體脂肪細胞分化的觀點。
前體mRNA(pre-mRNA)選擇性剪接是真核生物基因表達的重要調控方式,95%以上的人類基因存在選擇性剪接[29]。通過選擇性剪接可形成結構與功能多樣的蛋白質,精密調控組織類型和細胞發育。PPARγ蛋白含有不依賴配體激活的N-端結構域、DNA結合域(DNA binding domain,DBD)和依賴配體激活的C端-配體結合域(ligand binding domain,LBD)。經天然或合成的配體激活后,PPARγ與其分子伴侶RXR形成異二聚體,轉運到細胞核,與反應元件PPREs序列結合,以配體應答方式依賴LBD反式激活靶基因表達[8,30]。剪接因子SRSF1是一種非典型的SR蛋白,作為序列依賴性剪接激活因子發揮作用,是脂肪細胞分化必需的調節因子[31]。PPARγ第6外顯子上有SRSF1的結合位點,SRSF1與之結合促進外顯子5跳躍,產生缺失配體結合域的PPARγ亞型PPARγΔ5[8]。用PPARγ和PPARγΔ5過表達質粒共轉染細胞后,配體誘導的PPARγ反式激活活性降低約50%,說明PPARγΔ5對野生型PPARγ的活性具有抑制作用,是PPARγ的顯性負性亞型[8],可能在脂肪細胞分化和脂質代謝調控中發揮作用。用H2O2處理豬前體脂肪細胞后,剪接因子SRSF1與剪接異構體PPARγΔ5的表達水平均顯著降低,即PPARγΔ5的表達可能因氧化應激抑制SRSF1表達而降低。因此,PPARγΔ5也可能參與了氧化應激對豬前體脂肪細胞分化的影響,但其功能作用有待進一步研究。
4 結論
氧化應激可通過抑制轉錄因子C/EBPα和PPARγ表達及促進Txnip表達減弱豬前體脂肪細胞分化,并抑制PPARγ基因選擇性剪接。研究結果為進一步探討豬脂肪形成的調控機制提供了基礎。

