阿司匹林干預腦膠質細胞瘤相關巨噬細胞表達VEGF、bFGF 和YKL-40 成血管生長因子
陳麗麗,王涵,武蕾蕾,展濤,郭素芬,于建渤,吳影,高丹
(牡丹江醫學院附屬紅旗醫院 皮膚科,黑龍江 牡丹江 157011)
0 引言
腫瘤血管生成為腫瘤組織提供必需的營養成分和氧氣,同時也是腫瘤組織擴散和轉移的必要條件。靶向阻擊腫瘤血管生成一直是抗腫瘤轉移或抗腫瘤復發的熱點。但是,臨床研究發現,應用抗腫瘤血管生成類的藥物,卻沒有完全達到抗腫瘤轉移的預期效果[1]。
腫瘤微環境(tumor microenvironment,TME)包含腫瘤細胞和非腫瘤細胞、炎癥細胞以及多種促血管生成因子等,這些成分構成了腫瘤生長、轉移的局部微環境,TME對腫瘤血管的生成起到重要的促進作用[2]。血液中的單核細胞/巨噬細胞,被炎癥因子募集到腫瘤組織中,經細胞因子刺激極化為腫瘤相關巨噬細胞,該細胞能夠分泌基質金屬蛋白酶(matrix metalloproteinase,MMP)、巨噬細胞源性腫瘤壞死因子(tumor necrosis factor,TNF)及白細胞介素-1(interleukin-1,IL-1)等細胞因子而促進血管的生成[3],并有助于腫瘤細胞擺脫免疫系統的攻擊,促進腫瘤生長或轉移,是血管生成因子的主要來源[4]。
膠質瘤是常見的顱內原發腫瘤,具有新生血管較多并且雜亂的特點[5]。雖然目前以放化療或者手術治療為主,但是膠質瘤具有易侵襲、轉移等特點,治療效果并不十分理想。證據表明高腫瘤相關巨噬細胞浸潤與腫瘤患者的疾病進展和總生存率有關[6]。
研究發現:膠質瘤相關巨噬細胞與膠質瘤的惡性程度密切相關,即膠質瘤級別越高,腫瘤相關巨噬細胞越多[7]。又發現膠質瘤中腫瘤相關巨噬細胞與微血管密度呈正相關,且級別越高越顯著[8]。目前關于膠質瘤相關巨噬細胞的研究,多集中在膠質瘤相關巨噬細胞對膠質瘤細胞的凋亡、侵襲和遷移方面的影響,而膠質瘤相關巨噬細胞是否通過影響成血管因子的表達而調控膠質瘤的生長和轉移研究卻較少。
環氧合酶-2(cyclooxygenase-2,COX-2)對腫瘤血管的生成有促進作用。阿司匹林具有選擇性抑制COX-2的重要作用[9],在阿司匹林的干預下,是否可能影響膠質瘤相關巨噬細胞分泌VEGF、bFGF以及YKL-40等成血管因子,是本課題所要解決的問題,研究結果將對揭示膠質瘤相關巨噬細胞與膠質瘤發生發展關系探尋靶點,并為抗膠質瘤做好研究基礎。
1 材料與方法
1.1 材料
1.1.1 細胞株
人白血病THP-1單核細胞(購于中國科學院典型培養物保藏委員會細胞庫);人腦星形膠質母細胞瘤U-87MG細胞(由沈陽萬類生物科技公司惠贈)。
1.1.2 主要試劑和儀器
RPMI-1640或DMEM高糖培養基和胎牛血清(美國Hyclone公司),佛波酯(Phorbol ester,PMA;美國sigma公司),人重組白細胞介素-4蛋白(Interleukin-4,IL-4;美國BD公司),免抗人CD163(武漢博士得公司),免抗人VEGF單克隆抗體、免抗人FGF2單克隆抗體和山羊抗免IgG(美國Proteintech公司),超敏型二步法檢測試劑盒(北京中衫金橋公司),濃縮型DAB試劑盒(北京中衫金橋公司)。人VEGF、bFGF和YKL-40的ELISA試劑盒(美國R&D公司)。日本OLYMPUS倒置顯微鏡,西班牙Biological超凈工作臺。
1.2 實驗方法
1.2.1 細胞培養
含10%胎牛血清的RPMI-1640完全培養液培養THP-1細胞。含10%FBS的DMEM高糖完全培養基培養U-87MG細胞。
1.2.2 細胞誘導和分組
3×105/mL人白血病THP-1單核細胞,添加含PMA的RPMI-1640完全培養基,37℃,5%CO2培養24h后,更換含白細胞介素-4(Interleukin-4,IL-4)的DMEM高糖完全培養基;37℃,5%CO2培養48h,誘導為M2型巨噬細胞,單獨培養M2型巨噬細胞為M2組。單獨培養U-87MG細胞為U-87M組。U-87MG細胞與M2型巨噬細胞非接觸共同培養為共培養M2組,共培養細胞用2mmol/L、4mmol/L、8mmol/L阿司匹林進行干預分別為2mM、4mM、8mM阿司匹林組。
1.2.3 非接觸共培養體系
3×105/mL人M2型巨噬細胞接種在孔徑0.4μm的Transwell培養板下室,DMEM高糖完全培養基培養。2×105/mL U-87MG細胞用DMEM高糖完全培養基重懸,接種至Transwell培養板上室;37℃,5%CO2培養12h后,待U-87MG細胞完全貼壁,Transwell培養板上室內添加0mmol/L、2mmol/L、4mmol/L、8mmol/L阿司匹林,37℃,5%CO2培養24h。
1.2.4 人M2 型巨噬細胞的鑒定
1×104THP-1細胞種植于附有玻片的24孔板內,然后經PMA和人重組IL-4誘導THP-1細胞至貼壁并融合達70%以上;4%多聚甲醛固定30min;3%BSA工作液封閉,室溫放置20min;添加免抗人CD163抗體(1:200),4℃孵育過夜;0.01mmol/l PBS磷酸鹽緩沖液清洗3次,每次3min;山羊抗免IgG(1:300),37℃孵育40min;0.01mmol/l PBS磷酸鹽緩沖液清洗3次,每次2min;滴加DAB工作液,蘇木素輕度復染3min。顯微鏡觀察并照相。
1.2.5 免疫組化法檢測VEGF、bFGF 的表達
取上述各組中單獨培養的細胞和共培養M2型巨噬細胞及阿司匹林作用的M2型巨噬細胞,經固定、沖洗、封閉等處理后加入VEGF、bFGF一抗,4℃過夜;余步驟同M2型巨噬細胞的鑒定。
1.2.6 ELISA
3.5×104各組細胞,37℃,5%CO2培養12h,提取各組細胞的上清液。使用人VEGF、bFGF地ELISA試劑盒檢測各組細胞VEGF、bFGF的含量。
1.3 觀察指標
需要與結果2.1,2.2,2.3對應。
1.4 統計學分析
2 結果
2.1 THP-1細胞形態學特征
THP-1從血液中被募集到組織中,被細胞因子激活,轉化為TMAs。THP-1細胞經2-3次傳代,狀態穩定良好的情況下,細胞懸浮呈圓形,大小均勻,折光度較好。在培養液中添加含濃度為100ng/mL PMA的RPMI-1640完全培養基24h,細胞完全貼壁,形態由圓形轉變為卵圓形或梭形有隆起。添加含濃度為20ng/mL IL-4的RPMI-1640完全培養基24h,部分細胞伸出偽足,形態變長。48h后,細胞形態明顯改變,偽足延長變細,圖1。
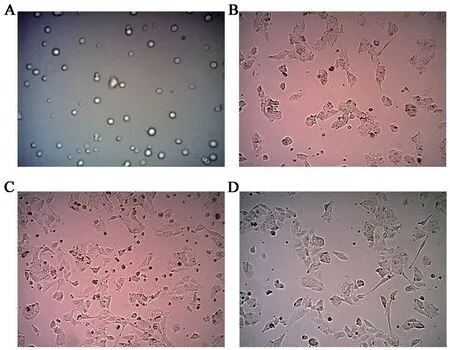
圖1 各組THP-1細胞培養24h的形態學特征(×100)
2.2 M2型巨噬細胞的表型鑒定
免疫組化結果表明:與THP-1細胞誘導之前CD163表達(0.37%)相比,THP-1細胞經PMA及IL-4逐級誘導后出現高表達的M2型巨噬細胞特異性抗原CD163(93.7%),兩組數據相比具有顯著差異(P<0.01),圖2。

圖2 THP-1細胞經PMA及IL-4誘導后CD163的表達(×400)
2.3 ELISA檢測各組細胞VEGF、bFGF和YKL-40含量
單獨培養的M2型巨噬細胞及與U87MG細胞共同培養的M2型巨噬細胞均見VEGF,bFGF和YKL-40的表達,但共培養的M2型巨噬細胞VEGF,bFGF和YKL-40表達明顯增多,數據相比具有統計學有意義(P<0.01)。與共同培養的M2型巨噬細胞相比較,當在共培養體系中加入2mm、4mm、8mm不同濃度阿司匹林后,阿司匹林組VEGF,bFGF和YKL-40含量逐漸降低,數據相比具有統計學有意義(P<0.01)。當阿司匹林濃度達8mm時,共培養體系M2型巨噬細胞VEGF,bFGF和YKL-40含量較2mm和4mm阿司匹林干預的M2型巨噬細胞明顯最低,數據相比具有統計學有意義(P<0.01),表1。
表1 ELISA檢測各組細胞VEGF、bFGF含量(,n=16,pg/mL)

表1 ELISA檢測各組細胞VEGF、bFGF含量(,n=16,pg/mL)
注:*P<0.01,與U-87M組和M2組比較;#P<0.01,與共培養M2組比較
3 討論
膠質瘤是一種頑固、常見的顱內原發腫瘤,具有新生血管較多并且雜亂的特點[5]。臨床目前主要進行放化療或者手術治療,但膠質瘤具有易侵襲、轉移等特點,導致以上治療效果一直不理想,因此我們需要不斷地尋找新的治療方法,為臨床治療膠質瘤提供新思路。
在腫瘤組織中可以發現各種免疫細胞。血液中的單核細胞/巨噬細胞,被炎癥因子募集到腫瘤組織中,經細胞因子刺激極化為腫瘤相關巨噬細胞(TAMs)。從功能表型上,巨噬細胞大致分為:經典(M1)型和替代(M2)型巨噬細胞。M1型巨噬細胞能夠被γ-干擾素等誘導,主要抗感染,抑制腫瘤細胞生長。M2型巨噬細胞分泌多種因子,有助于腫瘤細胞擺脫免疫系統的攻擊,從而促進腫瘤生長轉移。研究發現,M2型巨噬細胞經腫瘤誘導更接近TAMs。有資料顯示:TAMs在腫瘤微環境中扮演重要角色,TAMs是血管生成因子的主要來源[10],如M2型巨噬細胞可以釋放血管內皮生長因子(Vascular endothelial growth factor,VEGF)、基質金屬蛋白酶(Matrix metalloproteinase,MMP)等直接促進血管的生成[3],還可以釋放巨噬細胞源性腫瘤壞死因子(Tumor necrosis factor,TNF)及白細胞介素-1(Interleukin-1,IL-1)等促進黑色素瘤中白細胞介素-8(Interleukin-8,IL-8)和VEGF的釋放,從而間接促進腫瘤的血管生成[11]。越來越多的證據表明高TAMs浸潤與腫瘤患者的疾病進展和總生存率有關。
VEGF和bFGF是最常見的成血管因子,其促進血管形成的機制已有大量報道,如它們可以促進內皮細胞有絲分裂,也可以動員內皮祖細胞遷移并摻入到成熟內皮細胞中而發揮促血管生成作用[12]。YKL-40是一種分泌型糖蛋白,通常由多種細胞如巨噬細胞,軟骨細胞和血管平滑肌細胞表達[13]。大量證據表明YKL-40不僅是急性及慢性炎癥標志物,而且參與細胞的增殖、分化、凋亡、血管生成及組織重構等過程[14]。
阿司匹林是經典的非甾體抗炎藥,具有選擇性抑制環氧合酶-2(cyclooxygenase-2,COX-2)的作用。已有研究表明COX-2對腫瘤血管的生成有促進作用。COX-2對腫瘤血管形成的機制為:①促進血管內皮類生長因子的表達如VEGF;②前列腺素類產物如血栓素A2、前列腺素E2、前列環素能促進內皮細胞的遷移及血管形成;③通過上調Bcl-2的表達或Akt基因的活性,促進血管內皮細胞的形成。Kale和Gan的研究證實:M2型巨噬細胞可以產生COX-2。那么,在阿司匹林的干預下,是否可能通過抑制COX-2來影響TAMs成血管因子VEGF、bFGF以及YKL-40的表達呢?這也是本課題所要解決的問題。
鑒于以上原因,實驗中我們采用共培養系統首先設計了常見的VEGF、bFGF以及YKL-40影響血管形成因子研究。結果發現:與單獨培養的M2型巨噬細胞比,同U87MG膠質瘤細胞共培養的M2型巨噬細胞表達和分泌VEGF、bFGF以及YKL-40明顯增加。結果顯示:與U87MG膠質瘤細胞共培養的M2型巨噬細胞可以高表且與單獨培養的M2型巨噬細胞比具有明顯的統計學意義。以上這些成血管因子的變化說明膠質瘤細胞可能參與誘導M2型巨噬細胞大量表達和分泌VEGF、bFGF以及YKL-40,但具體的機制還不清楚。當阿司匹林濃度達8mm時,共培養體系中的M2型巨噬細胞表達VEGF較空白對照組的M2型巨噬細胞明顯減少。因此,如果采用阿司匹林可以起到重要的抗血管新生作用,阿司匹林不但可以直接抑制腫瘤細胞成血管因子的表達,同時也可以對腫瘤微環境中M2型巨噬細胞成血管因子的生成起到抑制作用,從而為腫瘤的抗血管治療提供更多可靠依據,也可為阿司匹林的進一步藥用價值開發帶來新希望。
這項研究初步探索了阿司匹林干預腦膠質細胞瘤相關巨噬細胞表達VEGF、bFGF和YKL-40成血管生長因子的影響,關于阿司匹林干預血管新生的靶點機制研究還需要借助基因組學、代謝組學等手段深入探索。

