長鏈非編碼RNA FOXC2-AS1在腫瘤中的研究進展
李 靜,李里香
長鏈非編碼RNA(long nocoding RNA, lncRNA)是一類長度大于200 nt的非編碼RNA,lncRNA已被證實參與腫瘤多種復雜的生物學過程,如細胞生長、增殖、分化、侵襲、轉移等[1-3]。FOXC2-AS1(又稱ODRUL)是一種新發現的lncRNA,是由FOXC2負鏈轉錄的單條反義寡核苷酸RNA。研究表明,FOXC2-AS1在骨肉瘤、黑色素瘤、肺癌、前列腺癌等中的表達存在差異,其不僅促進腫瘤的發生、發展,還參與腫瘤的多種生物學過程。本文現對FOXC2-AS1在不同腫瘤中的研究進展進行綜述,并對其研究前景進行展望。
1 FOXC2-AS1簡述
多個研究結果顯示反義寡核苷酸RNA可通過調節其內源基因的表達,參與細胞的生理和病理過程[4-5]。FOXC2-AS1定位于人類基因組16號染色體q24.1上,全長為319個核苷酸。現有研究表明,FOXC2-AS1在不同腫瘤中存在差異表達,其在骨肉瘤中通過FOXC2-AS1/miR-3182/MMP途徑發揮致癌作用;在肺癌和黑色素瘤中通過p15發揮致癌作用;在前列腺癌中通過FOXC2-AS1/miR-1253/EZH2途徑發揮致癌作用;在結直腸癌中通過Ca2+-FAK信號途徑發揮致癌作用。因此,FOXC2-AS1被認為是未來腫瘤的治療靶點標志物。
2 FOXC2-AS1與腫瘤的關系
隨著lncRNA的研究不斷深入,其與腫瘤的關系逐漸被認知。研究發現,FOXC2-AS1在一些腫瘤中表達上調,特別是在骨肉瘤、肺癌、黑色素瘤、前列腺癌、乳腺癌等中表達上調(表1)。
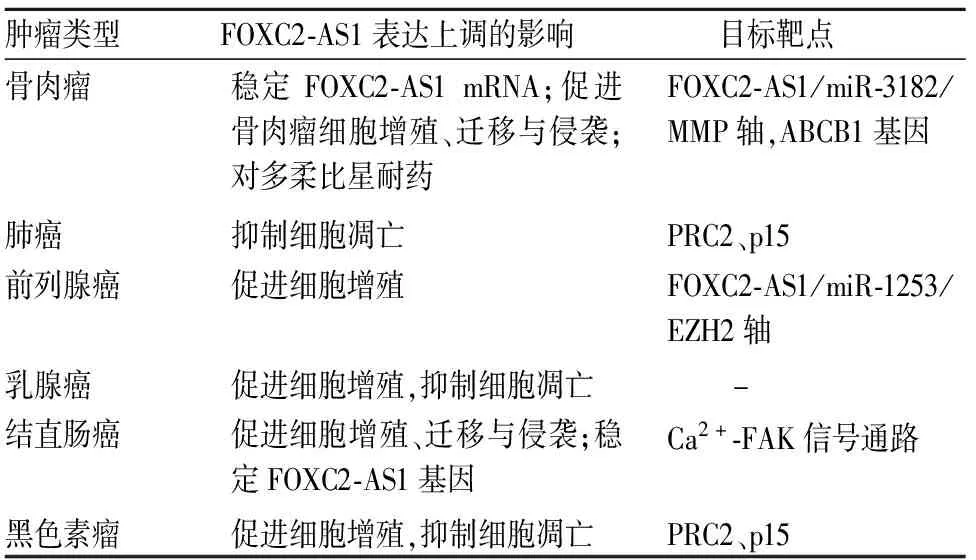
表1 不同腫瘤中FOXC2-AS1的作用
2.1 FOXC2-AS1與骨肉瘤骨肉瘤是兒童和青少年最常見的原發性惡性腫瘤[6]。新輔助化療的標準化應用增加了患者保肢治療的可能性。然而,化療耐藥性的出現極大地阻礙患者5年生存率的提高[7]。Zhang等[8]通過qRT-PCR檢測骨肉瘤細胞系及組織中FOXC2-AS1的表達水平,發現在多柔比星耐藥的骨肉瘤細胞系和組織中,FOXC2-AS1與FOXC2共同上調。與FOXC2-AS1相似,FOXC2也通過調節ABCB1的表達促進骨肉瘤對多柔比星的耐藥性。Kaplan-Meier生存分析發現,骨肉瘤組織中FOXC2-AS1高表達與較低的疾病進展率和總生存期顯著相關。CCK-8及集落分析實驗表明FOXC2-AS1可以促進骨肉瘤對多柔比星的耐藥。此外,作者還發現FOXC2-AS1與其編碼有義配偶體FOXC2的外顯子有重疊區域,進一步的生物信息學分析和FISH檢測結果顯示,這兩種分子主要定位于細胞質,FOXC2-AS1敲除顯著降低FOXC2的基因水平,Western blot法檢測結果亦顯示敲除FOXC2-AS1表達亦降低FOXC2蛋白水平。相比之下,敲除FOXC2后,FOXC2-AS1的表達水平未見明顯下降。此外,進一步的機制研究表明,FOXC2-AS1通過其重疊區域的保護作用,形成一個防止FOXC2 mRNA被RNase降解的RNA-RNA雙鏈結構,隨后在轉錄和轉錄后水平穩定FOXC2表達,進而刺激ABCB1的表達,從而導致骨肉瘤對多柔比星的耐藥。因此,作者推測FOXC2-AS1可能是一個候選的預后生物學標志物和逆轉多柔比星耐藥性的目標。Zhu等[9]研究發現FOXC2-AS1在骨肉瘤組織和細胞系中上調,并可以誘導MMP-2和MMP-9的表達進而促進骨肉瘤細胞遷移和侵襲。研究發現下調FOXC2-AS1表達水平可降低MMP的表達,體外和體內實驗結果顯示其抑制骨肉瘤細胞增殖、遷移、侵襲和腫瘤生長。微陣列篩選結合在線數據庫分析顯示,在表達sh-FOXC2-AS1的MG63細胞中,miR-3182上調、MMP-2下調,并且miR-3182具有FOXC2-AS1和MMP-2的mRNA 3’UTR潛在結合位點。此外,miR-3182的表達和功能與體外和體內的FOXC2-AS1表達呈負相關。熒光素酶報告基因實驗結果進一步表明FOXC2-AS1直接與miR-3182競爭性結合,并上調MMP-2的表達。該研究首次闡明了FOXC2-AS1/miR-3182/MMP-2通路在骨肉瘤中的作用,并揭示FOXC2-AS1可能為骨肉瘤新的潛在治療靶點。
2.2 FOXC2-AS1與非小細胞肺癌非小細胞肺癌是一種常見的惡性腫瘤,多數患者確診時已為晚期,預后差。因此,探究非小細胞肺癌的分子機制及有價值的生物學標志物和腫瘤治療靶點具有重要意義[10]。Sun等[11]的研究結果顯示,非小細胞肺癌組織中FOXC2-AS1的表達水平明顯高于癌旁正常組織,且FOXC2-AS1高表達與非小細胞肺癌患者的總生存期密切相關。CCK-8實驗及細胞周期分析結果顯示,敲除FOXC2-AS1可顯著抑制非小細胞肺癌細胞系(A549、H460)的增殖,加速細胞凋亡,并誘導細胞周期停滯在G0/G1期。機制實驗進一步表明,FOXC2-AS1通過將PRC2募集到p15的啟動子上抑制p15的表達。PRC2是個多亞基復合物,包括EZH2、EED和SUZ12。回復實驗驗證了FOXC2-AS1和p15之間的相互作用。總之,此研究結果證實FOXC2-AS1可通過相互作用EZH2抑制p15的表達而加重非小細胞肺癌的發生,可為非小細胞肺癌的治療策略提供新思路。
2.3 FOXC2-AS1與前列腺癌Chen等[12]研究發現FOXC2-AS1在前列腺癌組織和細胞中表達上調。CCK-8實驗、集落形成實驗、流式細胞術的周期分析及體內異種移植試驗等結果表明,FOXC2-AS1在體外和體內均有促進前列腺癌細胞增殖和生長的作用。為研究FOXC2-AS1在前列腺癌中的分子作用機制,作者首先使用生物信息學分析,預測miR-1253與FOXC2-AS1的3’UTR具有共同的結合位點,此外,兩者的相互作用通過熒光素酶報告分析得到證實。Pearson相關分析表明,FOXC2-AS1表達與miR-1253表達呈負相關,而miR-1253表達與EZH2表達呈正相關。隨后Western blot、CCK-8和集落形成實驗證實,FOXC2-AS1/miR-1253/EZH2軸對前列腺癌細胞增殖和進展的重要調節功能。因此,作者推斷FOXC2-AS1可通過作為miR-1253的競爭性內源性RNA來調節增殖和腫瘤生長,與EZH2蛋白互補結合,從而加速前列腺癌細胞的致癌作用。
2.4 FOXC2-AS1與乳腺癌乳腺癌是女性常見的癌癥之一,屬于復雜的異質性疾病。近年發現lncRNA在乳腺癌的發生、發展中起重要作用,其在腫瘤免疫逃逸的調控作用也備受關注[13-14]。Yang等[15]首先通過qPCR實驗對56例乳腺癌組織和相應正常組織進行分析,發現FOXC2-AS1在乳腺癌組織中表達明顯增加,且乳腺癌細胞系中FOXC2-AS1的表達明顯高于正常人乳腺細胞系。研究發現FOXC2-AS1表達與乳腺癌分化程度、淋巴結轉移、HER-2/neu狀態和TNM分期顯著相關,與患者年齡、腫瘤大小、ER以及PR表達無關。Kaplan-Meier生存分析顯示,FOXC2-AS1高表達與乳腺癌患者的不良預后有關。采用特定的siRNA沉默內源性水平的FOXC2-AS1后,MTT實驗結果顯示沉默FOXC2-AS1明顯降低相對細胞活力,細胞增殖被明顯抑制。集落形成實驗結果表明,轉染sh-FOXC2-AS1可降低乳腺癌細胞的增殖能力。流式細胞分析結果顯示,沉默FOXC2-AS1引起細胞周期停滯并誘導凋亡。此外,敲除FOXC2-AS1還導致乳腺癌細胞在G1期停滯并誘導細胞凋亡。為更深入地了解FOXC2-AS1對乳腺癌的影響,我們需要進一步分析其在乳腺癌中的具體分子作用機制。
2.5 FOXC2-AS1與結直腸癌Pan等[16]研究發現FOXC2-AS1在結直腸癌組織中表達上調。同時,轉移的結直腸癌組織中FOXC2-AS1表達高于非轉移的腫瘤組織,且FOXC2-AS1高表達與TNM分期和轉移顯著相關。qPCR檢測結腸癌細胞系(HCT116、HT-29、SW620和LoVo)和正常結腸細胞系NCM460中FOXC2-AS1的內源性表達,FOXC2-AS1在腫瘤細胞系中表達明顯上調,其中SW620和LoVo細胞系的表達高于HCT116和HT-29細胞系。因此,選擇SW620和LoVo進行功能喪失試驗。實驗結果證實,通過轉染FOXC2-AS1 siRNA-1和siRNA-2,FOXC2-AS1表達被有效抑制。MTT和克隆形成實驗結果顯示,FOXC2-AS1的減少顯著阻礙細胞的增殖和生長。值得注意的是,敲除FOXC2-AS1明顯抑制裸鼠皮下異種移植物的腫瘤體積、生長率和重量。劃痕實驗和Transwell實驗結果亦表明敲除FOXC2-AS1明顯損害結直腸癌細胞的遷移和侵襲。上述結果證實:FOXC2-AS1在體內外均可促進結直腸癌細胞的生長、侵襲和轉移。此外,FOXC2-AS1可與相鄰基因FOXC2形成雙鏈體,正向調節并穩定FOXC2基因。回復試驗及系列功能實驗結果表明,FOXC2-AS1可通過增強FOXC2基因的穩定性,在體內外促進結直腸癌細胞的增殖、侵襲和轉移。為進一步探討FOXC2-AS1/FOXC2介導的結直腸癌進展的分子機制,對TCGA數據集中的GSEA進行分析,發現FOXC2表達與鈣信號通路和局部粘連呈正相關。敲除FOXC2-AS1可降低細胞內FOXC2的表達水平,細胞內Ca2+水平也進一步降低,最后抑制黏著斑形成和FAK信號傳導。該結果進一步表明,FOXC2-AS1通過激活Ca2+-FAK信號增強FOXC2基因的穩定性,以促進結直腸癌的增殖、遷移和侵襲,作者推測FOXC2-AS1可能是結直腸癌進展的潛在有效治療靶點。
2.6 FOXC2-AS1與其他腫癌Xu等[17]的研究結果顯示,轉移或II~IV期黑色素瘤組織中FOXC2-AS1表達異常升高,且FOXC2-AS1高表達的黑色素瘤患者比低表達患者生存率更低。敲除FOXC2-AS1可抑制A375和sk-mel-110細胞的活力,并刺激其凋亡。此外,轉染si-FOXC2-AS1的黑色素瘤細胞中p15水平上調,主要分布于細胞質。RNA-RIP法分析驗證了FOXC2-AS1與EZH2和SUZ12的相互作用。ChIP法分析結果亦證實FOXC2-AS1通過募集EZH2調節p15轉錄的作用。實驗進一步發現FOXC2-AS1/p15軸對黑色素瘤細胞活力和凋亡具有調節作用。劉偉等[18]的研究結果顯示,FOXC2-AS1在彌漫大B細胞淋巴瘤組織中呈高表達,其可能與彌漫大B細胞淋巴瘤惡性增殖、侵襲、治療、預后有關。因此,作者猜測FOXC2-AS1可能作為腫瘤癌基因,參與腫瘤的發生,但仍需深入分析FOXC2-AS1在腫瘤中的分子機制。
3 結語
非編碼RNA在生命調控過程中扮演重要角色,其可與蛋白質、DNA、RNA相互作用并調控相關基因的表達,參與原癌基因活化調節、免疫細胞分化和免疫系統調控等一系列重要過程。越來越多的證據表明lncRNA起著癌基因或抑癌基因的作用,它們在正常情況下保持平衡[19-20]。目前,FOXC2-AS1的重點腫瘤研究領域局限于骨肉瘤、黑色素瘤、肺癌、前列腺癌及乳腺癌,在其他腫瘤中的研究仍在起步階段,隨著對FOXC2-AS1的不斷深入探究,其有望為腫瘤的診斷和靶點治療帶來新進展。

