腸道微生態(tài)與慢性腎臟疾病研究進(jìn)展
王艷萍,王德華,何江業(yè),李欣媛
(天津科技大學(xué) 食品科學(xué)與工程學(xué)院,天津 300457)
慢性腎臟疾病(chronic kidney disease,CKD)指腎臟結(jié)構(gòu)、持續(xù)性功能異常超過(guò)3個(gè)月[1],其發(fā)病率呈現(xiàn)出日益升高,年輕化的趨勢(shì)。據(jù)2019年發(fā)布的《中國(guó)腎臟病網(wǎng)絡(luò)(CK-NET)年度數(shù)據(jù)報(bào)告》顯示,中國(guó)CKD患者中男性占比達(dá)58.9%,且CKD高齡患者(60歲及以上)達(dá)到50%以上。
腎小球過(guò)濾能力下降、腎小管間質(zhì)炎癥等都會(huì)造成腎臟重吸收以及排泄有害物質(zhì)等功能受損,體內(nèi)有毒廢物開(kāi)始蓄積,腎臟排泄壓力逐步加重,CKD逐步發(fā)展,長(zhǎng)期以往最終會(huì)發(fā)展為終末期腎臟疾病(end-stage renal disease,ESRD)(尿毒癥)。治療及消除導(dǎo)致腎臟功能衰退的因素,是改善CKD的基礎(chǔ)和前提,也是有效緩解腎臟功能衰退以及保護(hù)剩余腎臟功能的重中之重[2]。針對(duì)CKD,現(xiàn)有的治療手段大致包括以下幾個(gè)方面(見(jiàn)圖1):(1)針對(duì)原發(fā)疾病和加重因素的治療;(2)飲食、藥物等一體化治療[3](低蛋白飲食治療、降低血壓及其他方面治療);(3)代替腎臟功能治療[4](血液透析、腹膜透析、腎臟移植)。但是,以上治療手段仍存在不少問(wèn)題,如CKD患者在經(jīng)過(guò)長(zhǎng)時(shí)間的低蛋白飲食等一體化治療后,會(huì)出現(xiàn)營(yíng)養(yǎng)攝入不均衡的問(wèn)題;吸附劑具有生物相容性差、吸附量少、成本高的劣勢(shì);腹膜透析容易引起傷口感染;腎臟移植后產(chǎn)生免疫反應(yīng),且沒(méi)有可靠的方法來(lái)解決,只能通過(guò)長(zhǎng)時(shí)間的使用免疫抑制劑,其結(jié)果也導(dǎo)致患者抵抗感染和腫瘤的免疫力降低;供體腎臟匱乏。

圖1 慢性腎臟疾病常用治療方式Fig.1 Common treatment methods of chronic kidney disease
鑒于現(xiàn)有治療和預(yù)防慢性腎病的現(xiàn)狀,醫(yī)學(xué)、營(yíng)養(yǎng)學(xué)和食品科學(xué)等不同領(lǐng)域的專(zhuān)家學(xué)者,從不同的角度尋求更加安全可靠、毒副作用小、成本低的治療和預(yù)防方法。近些年,通過(guò)益生菌調(diào)整腸道菌群結(jié)構(gòu)治療CKD的方法被人們逐步重視,因而本文總結(jié)了近些年來(lái)國(guó)內(nèi)外通過(guò)調(diào)整腸道菌群結(jié)構(gòu)治療CKD的研究進(jìn)展。
1 腸道內(nèi)環(huán)境紊亂對(duì)人體腎臟的影響
正常人體的腸道包含了超過(guò)千種微生物種類(lèi),主要為約64%的厚壁菌門(mén)(Firmicutes)和23%的擬桿菌門(mén)(Bacteroidetes)。腸道菌群中的微生物互相生存與制約,形成了一種微生態(tài)平衡[5],并發(fā)揮著重要作用,主要包括(1)維持腸道緊密連接結(jié)構(gòu),與病原菌競(jìng)爭(zhēng)腸道表皮細(xì)胞結(jié)合位點(diǎn);(2)促進(jìn)腸道免疫功能,促進(jìn)免疫調(diào)節(jié)及細(xì)胞分化;(3)產(chǎn)生大量對(duì)腸道健康及機(jī)體健康發(fā)揮重要作用的代謝產(chǎn)物,如對(duì)人體有益的乳酸,以及丁酸等短鏈脂肪酸(short chain fattyacids,SCFAs),還有對(duì)人體有害的硫酸吲哚酚(indoxylsulfate,IS)、硫酸對(duì)甲酚(p-cresol sulfate,pCS)等腸源性尿毒癥毒素。
腸道菌群的生態(tài)平衡與人類(lèi)健康息息相關(guān)。不良飲食習(xí)慣、濫用抗生素以及感冒或者經(jīng)常性憋尿等因素都會(huì)破壞腸道菌群的生態(tài)平衡,使得人體腸道內(nèi)環(huán)境紊亂[6],而腸道內(nèi)環(huán)境紊亂往往會(huì)促進(jìn)CKD的發(fā)生及發(fā)展。
1.1 腸道內(nèi)環(huán)境紊亂導(dǎo)致機(jī)體微炎癥
腸道菌群平衡被打破,不僅會(huì)造成腸上皮屏障通透性增加,還會(huì)造成腸道蠕動(dòng)不規(guī)律,從而導(dǎo)致清除有毒廢物能力降低,通過(guò)腸道排泄的尿酸、尿素、肌酐等尿毒癥毒素蓄積,然后以其為底物的條件致病菌數(shù)量增加。伴隨條件致病菌的增加,脂多糖透過(guò)腸上皮屏障進(jìn)入血液循環(huán)形成內(nèi)毒素[7],內(nèi)毒素是革蘭氏陰性細(xì)菌外膜的主要成分,其可以通過(guò)依賴(lài)Toll樣受體-4(toll-like receptor 4,TLR4)激活核因子κB(nuclear factor kappa-B,NF-KB)通路,促進(jìn)更多的炎癥因子釋放(見(jiàn)圖2),使得人體處于一種微炎癥狀態(tài)。長(zhǎng)期以來(lái),脂多糖進(jìn)入血液形成內(nèi)毒素引起炎癥反應(yīng)被認(rèn)為是造成腎臟負(fù)擔(dān)逐漸加的重要原因。呂晨蕭等[8]對(duì)69名健康人群以及29名CKD 5期透析人群和24名CKD 5期非透析人群的糞便進(jìn)行脫氧核糖核酸(deoxyribonucleic acid,DNA)測(cè)序發(fā)現(xiàn),與健康對(duì)照組的腸道菌群相比,CKD5-NHD組在門(mén)水平上,厚壁菌門(mén)豐富度高;在屬水平上,雙歧桿菌屬(Bifidobacterium)、鏈球菌屬(Streptococcus)、瘤胃球菌屬(Ruminococcus)、柯林斯氏菌屬(Collinsella)等豐富度高;CKD5-HD組在門(mén)水平上,厚壁菌門(mén)、放線菌門(mén)豐富度高,而這些細(xì)菌的增多,導(dǎo)致了丁酸鹽產(chǎn)生菌的顯著減少,而丁酸鹽可以為腸壁細(xì)胞供能維持腸道黏膜屏障,這也意味著CKD患者腸道通透性增加,尿毒素以及菌群移位引發(fā)機(jī)體炎癥以及腎臟負(fù)擔(dān)加重。同時(shí)炎癥反應(yīng)還與Treg細(xì)胞有關(guān),有學(xué)者[9]利用白色假絲酵母菌喂養(yǎng)小鼠,使其腸道菌群發(fā)生紊亂,然后觀察空白組與服用白色假絲酵母菌組小鼠的腎臟免疫細(xì)胞Treg的變化,得出實(shí)驗(yàn)組小鼠腎臟Treg細(xì)胞數(shù)量顯著提高,而腎臟Treg細(xì)胞數(shù)量與腎臟炎癥有關(guān)。

圖2 腸道菌群改變對(duì)慢性腎臟疾病發(fā)展的影響Fig.2 Effect of gut microflora change on the development of chronic kidney disease
1.2 腸道內(nèi)環(huán)境紊亂導(dǎo)致菌群及腸源性尿毒癥毒素移位
伴隨條件致病菌比例增加,人體攝入的蛋白質(zhì)被其酵解產(chǎn)生有機(jī)代謝廢物包括酚類(lèi)、吲哚類(lèi)、氨類(lèi)等的數(shù)量也會(huì)增加(見(jiàn)圖2),這些有機(jī)代謝廢物統(tǒng)稱(chēng)為腸源性尿毒癥毒素。其中氨類(lèi)物質(zhì)增加,導(dǎo)致腸道內(nèi)pH的增加,使得腸道黏膜蛋白主要包括occurludin、claudin及ZO蛋白的表達(dá)下降,腸道上皮細(xì)胞緊密連接結(jié)構(gòu)破壞[8],腸道黏膜屏障受損,有研究表明,不僅腸道內(nèi)存在細(xì)菌,而且血液循環(huán)中也存在相同種類(lèi)細(xì)菌[10](見(jiàn)圖2),從而猜測(cè)細(xì)菌可以通過(guò)受損的腸道屏障進(jìn)入血液循環(huán),在被人體免疫系統(tǒng)攻擊分解后形成內(nèi)毒素,產(chǎn)生大量促炎因子,刺激腎小球表面黏膜細(xì)胞產(chǎn)生炎癥因子,進(jìn)一步導(dǎo)致腎小球炎癥反應(yīng),加快腎小管上皮細(xì)胞凋亡及腎間質(zhì)纖維化程度;同時(shí)還有研究表明,除了常見(jiàn)的尿素、肌酐等尿毒癥毒素,像硫酸吲哚酚(IS)和硫酸對(duì)甲酚(pCS)等酚類(lèi)、吲哚類(lèi)腸源性尿毒癥毒素也可通過(guò)受損的腸道屏障進(jìn)入血液循環(huán),引起人體炎癥反應(yīng),并且由于兩者是蛋白結(jié)合毒素均不能通過(guò)透析去除,BARRIOS C等[11]通過(guò)對(duì)4 439例CKD早期患者體內(nèi)的尿毒癥毒素水平研究,發(fā)現(xiàn)其體內(nèi)pCS和IS水平與腎功能下降呈正相關(guān)。
2 慢性腎臟疾病對(duì)腸道菌群的影響
腎臟作為人體重要的排泄代謝廢物的器官,起著至關(guān)重要的作用,血液經(jīng)過(guò)腎小球時(shí),血液中的水、無(wú)機(jī)鹽以及含氮代謝廢物會(huì)被過(guò)濾到腎小囊中,借此將代謝廢物排出體外;同時(shí),腎臟還可以分泌激肽,血液中的α-球蛋白經(jīng)專(zhuān)一蛋白酶作用后釋放出的活性多肽,對(duì)于維持人體正常血壓和血流通暢起重要作用,腎臟的這些功能,保證了人體新陳代謝的順利進(jìn)行[12]。
慢性腎臟疾病發(fā)生時(shí),一方面,人體的新陳代謝功能降低,腎臟的代謝功能受損,腎臟功能逐步衰退減弱,導(dǎo)致排泄代謝廢物的能力逐步減弱,人體內(nèi)代謝廢物在血液中蓄積,代謝廢物在血液中濃度逐步升高,產(chǎn)生大量促炎因子,進(jìn)而引起機(jī)體炎癥反應(yīng),破壞腸道黏膜屏障,然后通過(guò)腸道表皮毛細(xì)血管進(jìn)入腸道內(nèi)部,破壞腸道菌群的生態(tài)平衡,微生物數(shù)量、組成、分布上發(fā)生明顯改變(見(jiàn)圖3),例如,乳酸桿菌(Lactobacillus)、雙歧桿菌(Bifidobacterium)等有益菌的數(shù)量明顯減少,腸桿菌科(Enterobacteriaceae)等致病菌數(shù)量顯著增加[13]。

圖3 慢性腎臟疾病的發(fā)生對(duì)腸道菌群的影響Fig.3 Effect of chronic kidney disease on gut microflora
另一方面,由于CKD患者的腎臟功能不完整,為防止腎臟功能進(jìn)一步遭到破壞,飲食需要調(diào)整和控制,因而需要限制蛋白質(zhì)以及K+的攝入,減少包含膳食纖維在內(nèi)的部分營(yíng)養(yǎng)素的攝入,長(zhǎng)此以往導(dǎo)致膳食纖維攝入量不足,使得體內(nèi)攝入的蛋白利用率增加,進(jìn)一步增加腸道內(nèi)含氮代謝廢物的蓄積,腸道菌群生態(tài)平衡由此受到影響而改變。已有研究表明,低蛋白攝入量會(huì)導(dǎo)致入球小動(dòng)脈的收縮,降低腎小球壓力,保護(hù)殘余腎功能損壞[14],同時(shí)低蛋白攝入量還會(huì)降低含氮廢物如尿素的產(chǎn)生,但是還有研究發(fā)現(xiàn),通過(guò)攝入膳食纖維可以改善CKD患者體內(nèi)炎癥狀態(tài)以及減弱蛋白質(zhì)分解[15],同時(shí),膳食纖維除了被腸道細(xì)菌糖酵解產(chǎn)生乙酸、丁酸等SCFAs,SCFAs可以為腸壁細(xì)胞提供能量維持腸道黏膜屏障的正常功能;膳食纖維還可以通過(guò)被腸道細(xì)菌分解與結(jié)腸中氨基酸結(jié)合到細(xì)菌蛋白質(zhì)中從糞便排出,而不是發(fā)酵為腸源性尿毒癥毒素,以此改善腸道菌群的組成,減少吲哚類(lèi)和酚類(lèi)等腸源性尿毒癥毒素的產(chǎn)生與蓄積[16],如JIANG S等[17]通過(guò)對(duì)65名CKD患者和20名健康人群糞便菌群進(jìn)行研究發(fā)現(xiàn),羅氏菌屬(Rothia)和普拉氏梭桿菌(Faecalibacterium prausnitzii)與腎臟功能呈負(fù)相關(guān),得出產(chǎn)生丁酸鹽的微生物消耗可能與CKD炎癥以及進(jìn)展有關(guān),丁酸鹽可以作為CKD進(jìn)展的“微生物標(biāo)志物”。WANG S等[18]對(duì)127名CKD患者和63名健康人群的SCFAs水平進(jìn)行對(duì)比研究,發(fā)現(xiàn)健康人群血清中SCFAs水平顯著高于CKD患者(P<0.05),同時(shí)健康人群體內(nèi)丁酸鹽含量[(3.44±2.12)μmol/L]達(dá)到CKD患者體內(nèi)丁酸鹽含量[(1.48±0.60)μmol/L]的2倍多;還通過(guò)對(duì)CKD小鼠模型補(bǔ)充丁酸鹽的實(shí)驗(yàn),驗(yàn)證了丁酸鹽在延緩CKD發(fā)展中發(fā)揮重要作用。
3 基于調(diào)節(jié)腸道菌群治療CKD的益生菌療法
現(xiàn)有的研究表明,CKD發(fā)展程度與腸道菌群生態(tài)變化相互聯(lián)系,相互影響(見(jiàn)圖4)。當(dāng)CKD發(fā)生時(shí),除了腎臟損傷引起的血液中尿毒癥毒素的積累會(huì)通過(guò)受損腸道黏膜屏障進(jìn)入腸道,改變菌群微生態(tài),治療藥物的使用以及飲食結(jié)構(gòu)的改變也會(huì)引起腸道菌群結(jié)構(gòu)的改變;反之,當(dāng)菌群結(jié)構(gòu)改變,以尿酸等尿毒癥毒素為底物的條件致病菌大量繁殖,條件致病菌以及腸源性尿毒癥毒素通過(guò)受損腸道黏膜屏障進(jìn)入血液,引起腎臟炎癥反應(yīng),最終加重CKD患者殘余腎臟功能代謝壓力。
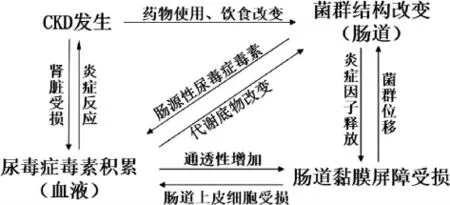
圖4 慢性腎臟疾病與腸道菌群相互影響Fig.4 Chronic kidney disease interacts with intestinal flora
正常人體腸道中含有一定比例的益生菌,而CKD患者因腸道菌群結(jié)構(gòu)被破壞,益生菌的比例降低,同時(shí),鑒于益生菌具有可以促進(jìn)有益菌生長(zhǎng)、釋放生物活性物質(zhì)和免疫調(diào)節(jié)因子[19],在營(yíng)養(yǎng)物質(zhì)消化、調(diào)節(jié)腸道功能中發(fā)揮作用的有益功能[20-21]。因此,通過(guò)補(bǔ)充益生菌或益生元(促進(jìn)益生菌生長(zhǎng)繁殖)改善CKD患者疾病逐漸被關(guān)注。益生菌在CKD的發(fā)展過(guò)程中發(fā)揮著重要的益生作用。
3.1 調(diào)節(jié)腸道菌群
腸道內(nèi)環(huán)境紊亂往往會(huì)促進(jìn)CKD的發(fā)生及發(fā)展,補(bǔ)充益生菌可以通過(guò)改善慢性腎臟疾病患者的腸道菌群的構(gòu)成來(lái)緩解慢性腎臟疾病的發(fā)展[22],LEE Y J等[23]通過(guò)研究Pm1(副干酪乳桿菌(Lactobacillus paracasei)BCRC12188、嗜熱鏈球菌(Streptococcus thermophilus)BCRC 13869、植物乳桿菌(Lactobacillus plantarum)BCRC 12251)對(duì)順鉑誘導(dǎo)的慢性腎臟疾病蘭嶼豬模型盲腸中菌群的調(diào)節(jié)作用,發(fā)現(xiàn)模型組中類(lèi)桿菌和梭桿菌的豐度顯著增加,而經(jīng)Pm1干預(yù)治療后,盲腸中微生物組成朝著空白組的菌群結(jié)構(gòu)發(fā)展,強(qiáng)調(diào)了通過(guò)調(diào)節(jié)宿主、微生物群和代謝物之間的關(guān)系來(lái)預(yù)防慢性腎病的特殊益生菌干預(yù)的重要性;除此之外,HUANG H等[24]在腺嘌呤誘導(dǎo)的慢性腎臟疾病小鼠模型中應(yīng)用體外降解IS、pCS等腸源性尿毒癥毒素能力強(qiáng)的乳酸桿菌(植物乳桿菌MFM30-3、副干酪乳桿菌MFM18)進(jìn)行體內(nèi)驗(yàn)證,同樣得出了篩選得到的乳酸菌可以通過(guò)逆轉(zhuǎn)腸道生態(tài)失調(diào),進(jìn)一步改變腸道內(nèi)共生細(xì)菌,尤其是SCFAs產(chǎn)生菌的豐度,減少尿毒癥毒素的產(chǎn)生。
3.2 調(diào)節(jié)免疫功能
益生菌還可通過(guò)腸上皮細(xì)胞與腸道免疫系統(tǒng)發(fā)生相互作用[25-27],如激活免疫細(xì)胞(樹(shù)突狀細(xì)胞、巨噬細(xì)胞、自然殺傷細(xì)胞、淋巴細(xì)胞)引發(fā)宿主機(jī)體對(duì)病原微生物產(chǎn)生免疫反應(yīng)[28];增強(qiáng)免疫耐受性[29];調(diào)節(jié)腸黏膜表面的修飾作用等[30]。已有研究表明,益生菌可以通過(guò)調(diào)節(jié)炎癥反應(yīng)以此緩解CKD,起到保護(hù)腎臟功能的作用[31-32]。姚穎等[33]通過(guò)研究益生菌L.casei Zhang對(duì)小鼠腎臟缺血再灌注損傷所引起的慢性腎損傷模型中細(xì)胞簇的影響,得出益生菌L.casei Zhang可以通過(guò)其相關(guān)代謝產(chǎn)物免疫調(diào)節(jié)巨噬細(xì)胞和腎小管上皮細(xì)胞,減少炎癥反應(yīng)發(fā)生。ZHU H等[34]通過(guò)研究服用益生菌干酪乳桿菌(Lactobacillus casei)Zhang后小鼠腎臟缺血再灌注損傷所引起的慢性腎損傷模型中代謝物的變化,發(fā)現(xiàn)服用益生菌L.casei Zhang后可以促進(jìn)腎臟中煙酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide,NAD+)生物合成的激活,從而達(dá)到保護(hù)小鼠缺血性腎臟損傷。胡文興等[35]通過(guò)對(duì)78例維持性血液透析慢性腎臟疾病患者進(jìn)行隨機(jī)臨床雙盲試驗(yàn),對(duì)照組進(jìn)行原有治療,實(shí)驗(yàn)組在原有治療的基礎(chǔ)上服用益生菌顆粒,結(jié)果表明實(shí)驗(yàn)組內(nèi)毒素水平較對(duì)照組下降水平更加顯著,同時(shí),有研究表明CKD患者腎臟衰竭程度與內(nèi)毒素水平呈正相關(guān),內(nèi)毒素可以通過(guò)激活相關(guān)通路產(chǎn)生白細(xì)胞介素1(interleukin-1,IL-1)激活巨噬細(xì)胞,加重對(duì)腎臟的免疫損失,因而降低體內(nèi)內(nèi)毒素的含量對(duì)于保護(hù)CKD患者殘余腎臟功能具有重要作用[36]。
3.3 增強(qiáng)腸上皮細(xì)胞屏障作用
對(duì)于慢性腎臟疾病患者,補(bǔ)充益生菌,一方面可以通過(guò)益生菌細(xì)胞壁的特殊組分磷壁酸同腸道黏膜細(xì)胞緊密結(jié)合,形成一個(gè)保護(hù)腸道以防止條件致病菌入侵及定植的生物學(xué)屏障,賀麗娟等[37]通過(guò)對(duì)5/6腎切除小鼠分別灌胃108CFU/d雙歧桿菌和104CFU/d乳酸桿菌測(cè)定血液中D-乳酸含量的變化,得出雙歧桿菌和乳酸桿菌可以維持慢性腎衰竭腸黏膜的正常通透性,從而達(dá)到抑制病原菌在腸道中的生長(zhǎng)繁殖的效果。
另一方面,腸道益生菌產(chǎn)生的細(xì)胞外糖苷酶可降解腸黏膜上皮細(xì)胞的復(fù)雜多糖產(chǎn)生乙酸、丁酸等SCFAs[38],SCFAs可以為腸壁細(xì)胞供能,提供營(yíng)養(yǎng),維持腸道黏膜屏障,還可通過(guò)代謝產(chǎn)生乳酸降低腸道pH[39],或者產(chǎn)生某些抗菌化合物[40](抗菌肽),既可以抑制條件致病菌生長(zhǎng)繁殖,減少致病菌利用蛋白發(fā)酵產(chǎn)生IS、pCS等腸源性尿毒癥毒素,也可以降低腸道內(nèi)氨的吸收,從而減少腸道內(nèi)尿素的生成(見(jiàn)圖5),促進(jìn)腸道蠕動(dòng),有利于腸道內(nèi)代謝產(chǎn)物排泄[41]。如GUIDA B等[42]通過(guò)對(duì)30例未經(jīng)透析的終末期腎病患者進(jìn)行隨機(jī)雙盲臨床試驗(yàn),實(shí)驗(yàn)組口服益生菌制劑,對(duì)照組口服安慰劑,結(jié)果表明,口服益生菌制劑可以顯著降低血液中pCS以及IS的水平;NATARAJAN R等[43]通過(guò)對(duì)經(jīng)過(guò)接受透析治療的終末期腎病(end-stage renal disease,ESRD)患者進(jìn)行了一項(xiàng)隨機(jī)、雙盲、安慰劑對(duì)照交叉研究實(shí)驗(yàn),實(shí)驗(yàn)組口服特異性益生菌制劑,對(duì)照組口服安慰劑,結(jié)果表明,口服特異性益生菌制劑的ESRD患者血液中炎癥因子水平下降以及氧化應(yīng)激反應(yīng)減輕;HUANG H等[24]在腺嘌呤誘導(dǎo)的慢性腎臟疾病小鼠模型中進(jìn)行驗(yàn)證,得出了乳酸菌可以調(diào)整SCFAs產(chǎn)生菌的豐度來(lái)調(diào)節(jié)代謝產(chǎn)物丁酸的產(chǎn)生防止腸屏障破壞,還可以通過(guò)減少腎損傷和纖維化相關(guān)蛋白、調(diào)節(jié)氧化應(yīng)激、促炎活性和免疫反應(yīng),顯著改善腎功能。

圖5 益生菌干預(yù)的優(yōu)點(diǎn)Fig.5 Advantages of probiotics intervention
4 結(jié)論
以腸道菌群為切入點(diǎn)通過(guò)補(bǔ)充益生菌、益生元調(diào)節(jié)腸道菌群,可以恢復(fù)腸道運(yùn)動(dòng),促進(jìn)SCFAs的產(chǎn)生修復(fù)受損的腸道黏膜屏障,以及刺激抗炎因子的產(chǎn)生,均能有效延緩CKD發(fā)展,為臨床治療CKD提供了新的治療思路與方式。但是還應(yīng)該強(qiáng)調(diào)腸道菌群的局限性以及具體作用機(jī)制、研究樣本量小及基線水平的差異、臨床試驗(yàn)中的具體數(shù)據(jù)反映等,有待更加深入和系統(tǒng)的研究。
同時(shí),未來(lái)的研究不僅要關(guān)注益生菌能否通過(guò)胃腸道存活的數(shù)量發(fā)揮效果,還更應(yīng)該關(guān)注益生菌的菌株特異性,深入探索不同益生菌發(fā)揮作用的具體機(jī)制,通過(guò)基因組學(xué)技術(shù)驗(yàn)證并確定CKD患者和腸道菌群的相互關(guān)系,明確不同益生菌相關(guān)基因的上下游通路機(jī)制,以此進(jìn)行CKD患者的治療以及預(yù)后。

