間充質干細胞治療早產兒支氣管肺發育不良的研究進展
黃高展,劉春華
(汕頭大學醫學院第一附屬醫院新生兒科,廣東 汕頭 515041)
隨著圍產醫學及新生兒醫學技術的進步,早產兒尤其是超早產兒的存活率不斷提高。支氣管肺發育不良(bronchopulmonary dysplasia,BPD)作為一種早產兒常見的嚴重并發癥,其發病率也在逐年上升。我國幾項多中心研究表明超低出生體重兒或超未成熟兒BPD發生率差異較大,2006—2008年僅19.3%,2011年為48.1%,2019年則高達72.2%[1]。合并BPD的早產兒病死率高,且伴有不同程度的后遺癥,給患者家庭及社會帶來了巨大的經濟負擔。臨床上通過預防早產,使用溫和的機械通氣模式,降低吸入氧濃度,肺表面活性物質的治療和營養支持等一系列措施在BPD的防治上取得一定成效,但目前仍未能有效治愈BPD[2]。間充質干細胞 (mesenchymal stem cells,MSCs)療法可以調節免疫,減輕肺部纖維化和炎癥,增強肺部細胞的再生和修復,降低肺動脈高壓,給BPD的治愈帶來了希望。本文從BPD的發病機制出發,通過查閱MSCs治療BPD相關機制研究的文獻,結合當前的臨床試驗對MSCs治療BPD進行綜述與展望。
1 BPD的發病機制
早產兒肺部發育常處于小管晚期或囊狀早期,早產使正常肺泡和遠端血管發育中斷,在產前因素(如胎兒宮內生長受限、宮內感染等)及產后因素(如細菌感染、機械正壓通氣、氧療等)的影響下[3],對未發育完全的肺造成進一步損傷,激活了免疫反應[4],引起肺部炎癥因子和抗炎因子的紊亂,造成肺部干細胞損傷或耗竭[5],導致肺泡結構簡單化和異常肺血管生成,出現了肺部纖維化[6]和動脈高壓[7],最終形成BPD,這是一個動態、復雜的過程。
2 MSCs的來源及其治療機制
MSCs屬于多能成體干細胞,具有自我更新、多向分化及低免疫原性的特點,在妊娠組織(胚胎、臍帶、胎盤、臍帶血)、骨髓、皮膚等組織均有存在[8]。MSCs發揮治療的機制主要包括以下幾方面。(1)MSCs具有定向增殖分化能力,可通過歸巢作用促進組織的愈合。MSCs遷移進入損傷的組織、修復損傷組織的機制尚未完全明確,但很可能與MSCs表達的黏附分子與炎癥趨化因子通過局部或全身循環遷移到達靶器官并相互作用有關[9]。(2)研究發現MSCs分泌的可溶性蛋白(細胞因子、趨化因子、生長因子、蛋白酶)、外泌體、細胞外囊泡在BPD肺組織的修復和再生中也起了關鍵作用[10]。Willis等[11]研究發現通過靜脈給予MSC外泌體可以改善肺動脈的發育及肺纖維化;Braun等[12]的研究也顯示MSC細胞外囊泡可通過抗炎和促血管生成機制促進肺泡發育。MSCs分泌的產物具有免疫原性低、半衰期長、在體內穩定、遞送效率高等特性,并且更易于隔離、存儲和管理[13],在治療BPD上有著巨大潛力。(3)MSCs可通過細胞間的相互作用及細胞因子抑制T細胞、B細胞等免疫細胞的增殖發揮免疫調節作用[14]。人類白細胞抗原(human leukocyte antigen,HLA)又稱移植抗原,低水平的HLA可規避免疫識別。MSCs表達HLA-Ⅰ類分子(與排斥反應相關)和Ⅱ類分子(與免疫反應相關)的水平較低,可使MSCs更好地逃脫免疫監視[15],降低異體移植的排斥反應。
3 MSCs治療BPD的臨床試驗
BPD動物實驗研究證實了MSCs治療能有效改善肺泡結構和血管生成,減輕肺纖維化和肺脈高壓等[16]。動物實驗的成功對MSCs的臨床應用有著較大的啟發,目前在美國國家衛生研究院數據庫(https://clinicaltrials.gov)上注冊的應用MSCs治療BPD臨床試驗共有14項(表1)。
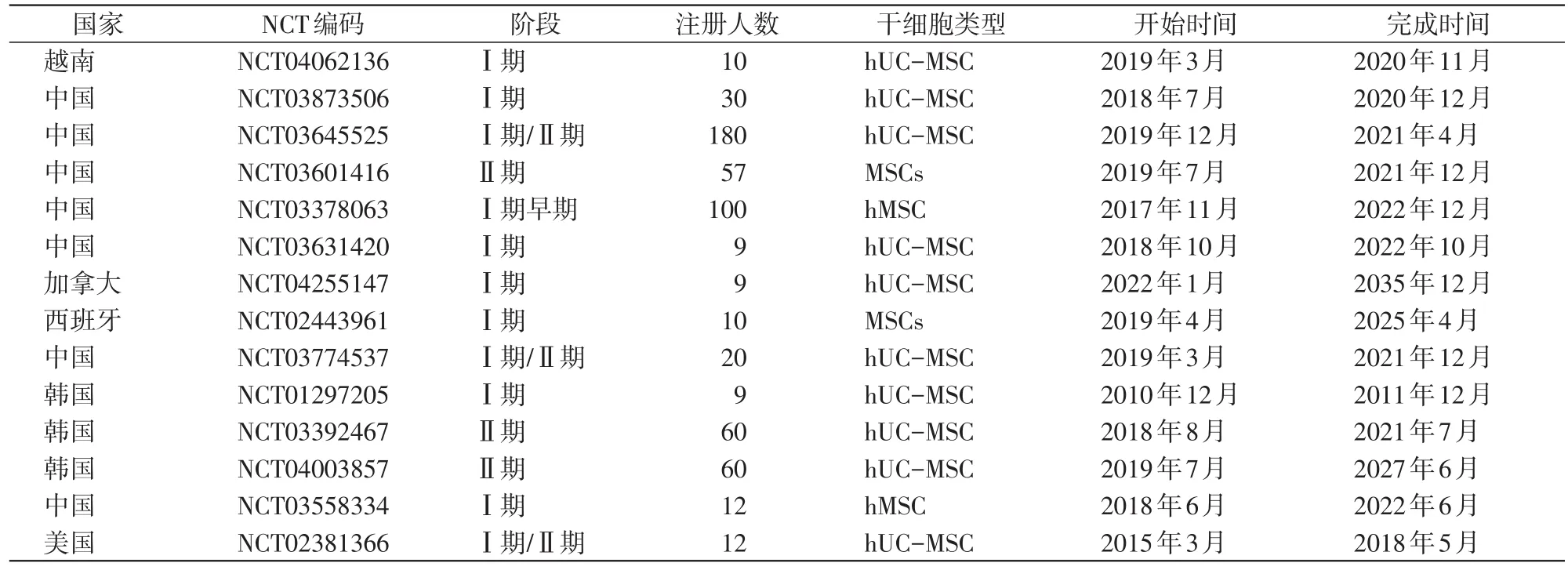
表1 14項MSCs治療BPD臨床試驗信息
Chang等[17]在Ⅰ期臨床研究中使用不同劑量MSCs治療BPD患兒以驗證其安全性及可行性,在9例高危BPD患兒氣管內注入MSCs,其中3例為低劑量MSCs(細胞數為1×107個/kg),6例為高劑量MSCs(細胞數為2×107個/kg),治療84 d后結果顯示,患兒治療的耐受性良好,且沒有嚴重的副作用;Ahn等[18]在對該9例患兒長達2年的隨訪中,未發現接受MSCs治療的患兒有致瘤、致畸等不良后果。王燕等[19]使用hUC-MSC治療BPD的一項臨床研究中,將高危早產兒(共18例)分為試驗組(8例)和對照組(10例),試驗組患兒出生后7 d、14 d分別給予氣管內滴入hUC-MSC(細胞數為1×107個/kg),對照組給予同體積生理鹽水,結果顯示試驗組患兒BPD發生率、平均住院時間、平均用氧時間及1歲內肺炎發生率均比對照組低(P值均<0.05),且肺泡灌洗液中抑制性炎性因子水平也低于對照組(P<0.05)。Powell等[20]也進行了一項類似的臨床試驗,在12例BPD高危早產兒氣管內使用MSCs治療,其中6例為低劑量MSCs(細胞數為1×107個/kg),6例為高劑量MSCs(細胞數為2×107個/kg),結果也顯示患兒的耐受性良好,未發現不良反應。隨后Ahn等[21]在Ⅰ期臨床研究的基礎上,對66例23~28周的高危早產兒進行雙盲、隨機、安慰劑對照的Ⅱ期臨床試驗,這些早產兒在出生后第5天至第14天期間伴有呼吸惡化,接受機械呼吸機支持。將66例高危早產兒按胎齡分為23~24周組(n=31)和25~28周組(n=35),按1∶1隨機分配接受MSCs治療(細胞數為1×107個/kg,n=33)或安慰劑治療(等體積的生理鹽水,n=33)。結果顯示雖然接受MSCs治療的患兒氣管吸出液中炎性因子顯著降低,但MSCs組(17/33,52%)與對照組(18/33,55%)出現死亡或中重度BPD的結局并未得到顯著改善;在23~24周患兒的亞組分析中(MSCs組16例,對照組15例),MSCs組出現嚴重BPD的結局(3/16,19%)較對照組(8/15,53%)則有了顯著改善,而在25~28周的亞組分析中出現嚴重BPD結局并無明顯改善。因此,進行一項更大樣本量的研究(NCT03392467),旨在了解關于23~24周早產兒使用MSCs治療的效果。
4 目前的不足及未來展望
MSCs治療BPD在臨床試驗中已初步證實其效果是顯著的,是最具革命性的下一代治療手段,在轉化應用于臨床前需要明確其安全性、適宜的患兒及用藥參數。MSCs來源廣泛,雖然從自體妊娠組織中提取的MSCs具有低成本,低免疫原性及高生物活性的特點且不涉及倫理問題[22],但仍有部分患兒無相應的條件,需行異體干細胞移植,因此倫理學討論是必要的[23]。而且制定一個標準化方法收集安全有效的MSCs非常重要,目前已有臨床試驗使用符合藥品生產管理規范的人誘導多能干細胞[24],未來這可能是MSCs來源的最佳方式。超早產(胎齡<27周)及超低出生體重(出生體重<1 000 g)是BPD的獨立高危因素[1],這個階段的患兒肺部處于原始肺泡發育的關鍵時期,對外界因素極度敏感,出生后需要機械通氣等高級生命支持,且目前治療手段有限,因此更適合使用MSCs進行治療。MSCs在臨床上的用藥參數需要個體化,氣管內給藥較靜脈給藥副作用少,且對于有創通氣的患兒操作方便,這可能是最佳的給藥方式;臨床試驗結果顯示不同劑量的MSCs治療效果良好,最佳的劑量需要結合肺部損傷的程度來決定,伴隨著MSCs的消耗,部分患兒可能需要多次使用MSCs治療才能達到最佳治療效果;多項動物實驗中提示在高氧造成的肺部損傷炎癥到達高峰或穩定階段之前使用MSCs移植效果更好[25],臨床試驗的結果也支持這一結論,因此臨床中治療BPD越早使用MSCs可能效果越好。隨著多中心、大規模、前瞻性臨床隨機對照試驗的進行,未來MSCs療法將給BPD患兒帶來更多福音。

