CuO/ZnO/Al2O3改性催化劑上CH3OH重整制氫的研究
王 康, 李 濤, 張海濤
( 華東理工大學大型工業反應器工程教育部工程研究中心,上海 200237)
氫作為一種新能源,能夠降低CO2的排放,從而減緩全球變暖問題[1]。氫主要用于合成氨、甲醇等工業領域[2]。近年來,氫作為一種清潔能源被用于燃料電池行業,但其中的一個難題是氫氣的便攜性問題,解決方案之一是利用甲醇進行車載制氫[3]。
甲醇水蒸氣重整(Methanol Steam Reforming, MSR)反應體系十分復雜,反應機理也不統一,MSR體系主要包含甲醇水蒸氣重整(SR)、甲醇分解(DE)和水汽變換(WGS)3個反應。從催化劑和反應活化能角度分析,有研究人員提出DE-WGS反應機理,但是實驗測得的CO濃度遠遠低于WGS反應計算的理論值[4-5]。Choi等[6]提出了SR-DE反應機理,但仍不能預測CO含量。文獻[7-8]提出SR-RWGS(逆水汽變換)反應機理,認為CO來自RWGS反應,解決了實驗測得的CO含量低于理論計算值的問題。
根據MSR反應體系中所包含的方程數,MSR動力學模型分為單速率模型、雙速率模型和三速率模型。Tesser等[9]在低溫(160~200 ℃)下發現了幾種單速率動力學模型,但是其適用范圍有限,實驗值與模型預測值的偏差較大。Idem等[10]提出了能夠適用不同溫度區間的反應動力學模型,以此來提高模型的準確性。單速率反應動力學模型簡化了MSR反應體系,雖然能夠快速地預測CH3OH、H2、CO2等關鍵組分的含量,但是無法預測CO含量,不能應用到對CO含量較敏感的燃料電池中。Purnama等[11]認為CO可能來自于RWGS反應,從而提出SR-RWGS雙速率模型。Peppley等[12]提出了包含3個反應的三速率反應動力學模型,能夠完整地預測產物中各組分的含量,但是該模型復雜,求解困難。上述3種MSR動力學模型中,雙速率模型能夠預測CO含量,并且參數少,適合推廣使用。本文推導并驗證了Langmuir-Hinshelwood型雙速率動力學模型,為催化劑的工業化應用提供實驗依據。
相比于Pd、Pt、Ni型催化劑,Cu系催化劑的失活研究比較少。Twigg等[13]提出了Cu系催化劑失活的原因主要是燒結、積碳、中毒等。本文通過對催化劑進行表征,找出催化劑失活的具體原因,有助于延長催化劑使用壽命。
1 實驗部分
1.1 實驗原料
甲醇:w≥99%,上海阿拉丁生化科技股份有限公司;超純水系統(DZG-303A),上海礫鼎水處理有限公司;石英砂(SiO2):超純砂,上海阿拉丁生化科技股份有限公司;氮氣(N2):φ≥99.9%,液化空氣(上海)有限公司;氫氣-氮氣混合氣(H2-N2),體積分數H25%、N295%,液化空氣(上海)有限公司。
1.2 測試與表征
低溫氮氣物理吸附儀(美國Micrometrics公司ASAP 2020型):453 K下真空脫氣6 h,然后在77 K液氮中脫附;X射線熒光光譜儀(德國Bruker公司S4 PIONEER型):Rh靶管,最大功率是4 kW;X射線衍射儀(日本Rigaku公司D/MAX2550VB/PC型):射線源是Cu/Kα,測試電壓為40 kV,電流為200 mA,掃描范圍10°~80°,掃描速率為8(°)/min;全自動程序升溫化學吸附儀(美國Micrometrics公司AutochemⅡ2920型):300 ℃下純氫還原1 h,降至室溫后通入CO吸附30 min,再換載氣He吹掃,最后以10 ℃/min升溫至700 ℃。
1.3 實驗流程
在常壓條件下,采用等溫積分反應器(內徑10 mm,長度500 mm)進行CuO/ZnO/Al2O3改性催化劑的MSR反應性能評價。40~60目(250~380 μm)的催化劑顆粒與40~60目(250~380 μm)的石英砂按照體積比1∶1混合稀釋后,放置于底部墊有高溫石英棉的反應器中部恒溫區內。床層底部裝有鎳鉻-康銅熱電偶,用來測量反應床層溫度,反應器內壓力用精密壓力表測量。反應前,反應器內通入H2-N2混合氣(50 mL/min),程序升溫至300 ℃后,保溫2 h,進行催化劑還原。還原結束后,通高純N2將反應器內溫度降至室溫。N2作為反應載氣,配制好的甲醇水溶液通過神舟微科2PB系列平流泵進入預熱器中,汽化后進入反應器中反應。反應后氣體經冷凝器冷凝得到甲醇和水,不凝性氣體通過氣液分離器后進入Agilent 7890B氣相色譜儀中,分析氣體組成,反應尾氣通入皂膜流量計測量后放空。甲醇轉化率(X)和CO選擇性(S)分別按式(1)和式(2)計算。

式中,Fi,in、Fi,out分別表示i組分(CH3OH、CO或CO2)在反應器進口和出口處的摩爾流率。
1.4 內、外擴散影響的消除
甲醇水蒸氣重整制氫反應為氣-固非均相催化反應,研究其反應動力學時,需要先消除內、外擴散對反應體系的影響。
對于氣-固非均相催化反應,影響內擴散的主要因素是催化劑的顆粒大小,其可以通過減小催化劑粒徑來消除。當催化劑粒徑減小到一定程度時,甲醇轉化率不會隨著粒徑的改變而變化,內擴散影響被消除。本實驗在常壓和240 ℃的條件下,采用5組不同粒徑(即20~40目(380~830 μm)、40~60目(250~380 μm)、60~80目(180~250 μm)、80~100目(150~180 μm)、100~120目(120~150 μm))的催化劑。由圖1可知,當催化劑粒徑減小至250~380 μm時,甲醇轉化率不再隨著粒徑的變化而變化,證明內擴散影響已消除。因此,在進行動力學實驗時,催化劑粒徑為250~380 μm。

圖1 催化劑粒徑對內擴散的影響Fig. 1 Effect of particle size of catalyst on internal diffusion
提高進料的液時空速(Liquid Hourly Space Velocity, LHSV)、增加催化劑用量均可以減弱外擴散影響。選用兩組不同裝填量(1 g和2 g)的催化劑,通過調整LHSV(0.1~6.0 h?1)來考察消除外擴散影響的條件,結果如圖2所示。圖2表明,當LHSV大于或等于0.6 h?1時,兩組催化劑的甲醇轉化率幾乎相同,說明外擴散影響已經消除,因此動力學實驗的液時空速不低于0.6 h?1。
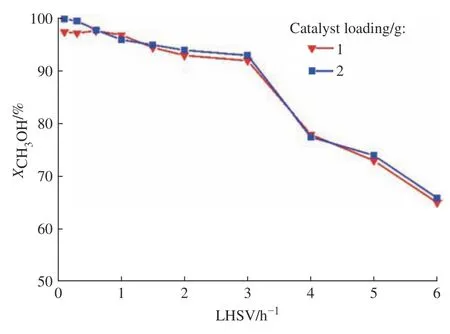
圖2 進料液時空速對外擴散的影響Fig. 2 Effect of LHSV on external diffusion
2 結果與討論
2.1 操作條件對反應的影響
在水與甲醇物質的量之比為1.2、LHSV為3.0 h?1、常壓的反應條件下,考察了反應溫度(200~300 ℃)對CH3OH轉化率和CO選擇性的影響,結果如圖3所示。由圖3可知,CH3OH轉化率和CO選擇性都隨著反應溫度的升高而增加,當溫度超過240 ℃時,甲醇轉化率接近100%。SR反應和DE反應都屬于吸熱反應,溫度升高,CH3OH轉化率會升高;WGS反應是放熱反應,溫度升高有利于RWGS和DE反應,所以CO選擇性會升高。溫度為240~250 ℃時,CH3OH轉化率很高,此時CO選擇性還沒有急劇升高,所以,MSR反應的適宜溫度為240~250 ℃。
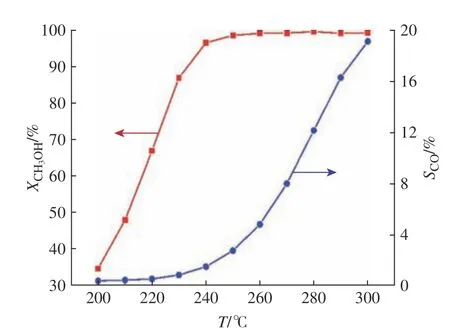
圖3 溫度對反應結果的影響Fig. 3 Effect of the temperature on reaction results
在溫度為240 ℃、LHSV為3.0 h?1、壓力為常壓的反應條件下,考察了甲醇水溶液進料中水與甲醇物質的量之比(1.0~2.0)對CH3OH轉化率和CO選擇性的影響(圖4)。由圖4可知,CH3OH轉化率隨著水與甲醇物質的量之比的增大而增加,CO選擇性則相反,隨著水與甲醇物質的量之比的增大而減小,當水與甲醇物質的量之比達到1.2時,CH3OH轉化率在95%以上。水與甲醇物質的量之比的增大,有利于SR和WGS反應,但是氣化甲醇水溶液會消耗較高的能量。因此本實驗適宜的水與甲醇物質的量之比為1.2。
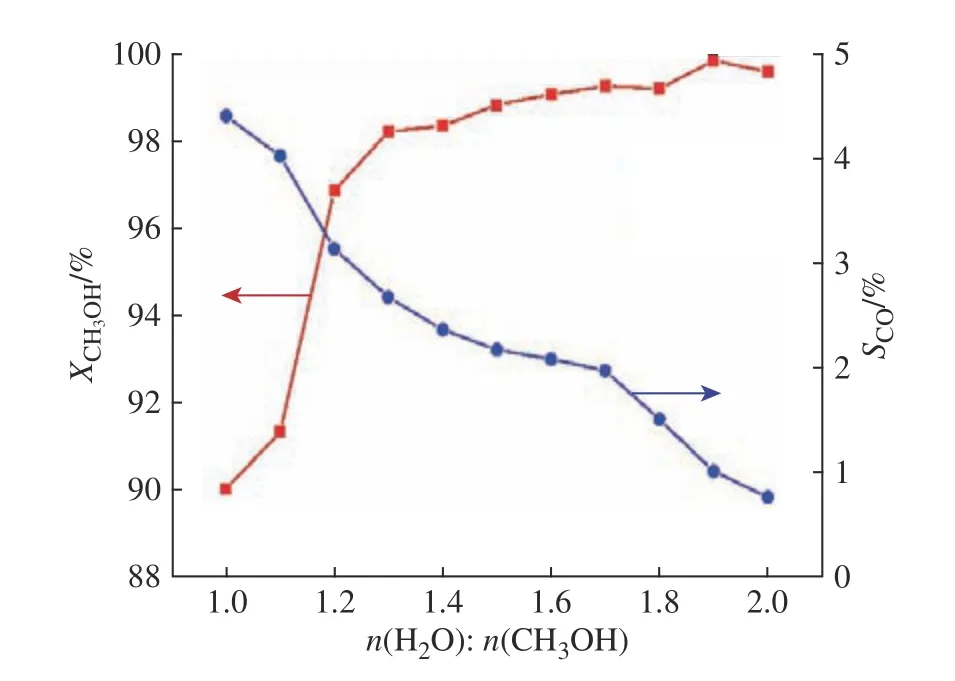
圖4 水與甲醇物質的量之比對反應結果的影響Fig. 4 Effect of H2O/CH3OH molar ratio on reaction results
在溫度為240 ℃、水與甲醇物質的量之比為1.2、壓力為常壓的反應條件下,考察了LHSV(0.3~11.1 h?1)對CH3OH轉化率和CO選擇性的影響。由圖5可知,CH3OH轉化率和CO選擇性隨著LHSV的增大而減小。LHSV增加,反應物在反應器床層內的停留時間變短,使得反應不完全,所以CH3OH轉化率和CO含量都會下降。LHSV太大,反應不完全,會浪費原料;LHSV太小,反應速率太慢,產氫速率太慢,所以要根據不同的生產要求選擇合適的LHSV。
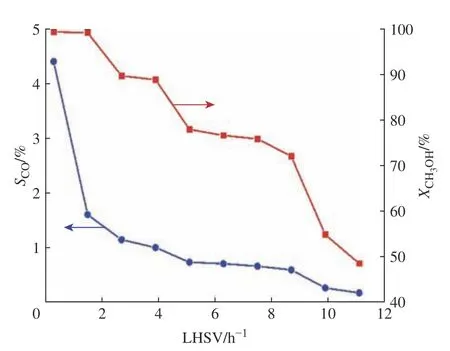
圖5 液時空速對反應結果的影響Fig. 5 Effect of LHSV on reaction results
2.2 本征反應動力學模型
甲醇水蒸氣重整制氫反應體系主要由SR反應、DE反應和WGS反應組成,反應式及焓變分別如式(3)~式(5)所示。

本文采用的是Sandra等[14]提出的SR-RWGS雙速率模型,其既能預測主要產物H2和CO2的含量,也能預測副產物CO的含量,并且求解過程相對來說比較簡單。本文涉及到的Langmuir-Hinshelwood型雙速率動力學模型方程中SR反應速率表達式和RWGS反應速率表達式分別如式(6)和式(7)所示。
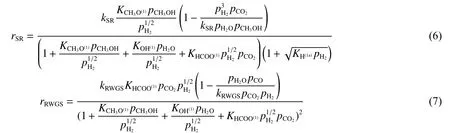
式中,kSR為SR反應的速率常數,kRWGS為RWGS反應的速率常數,Ki為組分i的吸附常數(其中括號中符號表示催化劑的活性位),pj為j組分的分壓。其中與溫度有關的反應速率常數和吸附常數可以用阿侖烏尼斯方程表示,具體公式如下:

對于CuO/ZnO/Al2O3催化劑而言,式(10)中的吸附熱數據在許多研究中已經確定,為了減少待估參數的個數,本文采用Peppley等[12]給出的4個吸附熱數據,具體如下:
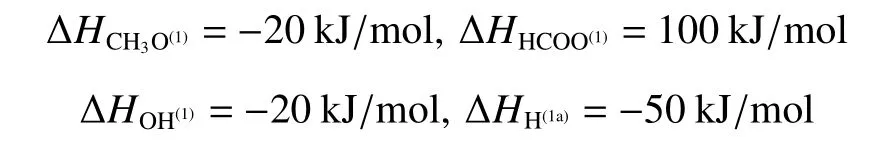
采用某研究所制備的CuO/ZnO/Al2O3催化劑,裝填量2 g,粒徑40~60目(250~380 μm)。反應在常壓下進行,反應溫度范圍473.85~552.65 K,進料甲醇水溶液中水與甲醇物質的量之比1.0~1.8,進料LHSV范圍0.6~10.2 h?1。采用正交試驗方法設計了實驗過程,得到了25組實驗數據,如表1所示。

表1 甲醇水蒸氣重整制氫的本征動力學實驗數據Table 1 Experimental data of the intrinsic kinetics of hydrogen production via methanol steam reforming
對于本實驗中的固定床反應器,CO2和CO的連續性方程如下:

式中,N為反應次數(N=25),下標cal表示模型計算值,下標exp表示實驗值。
運用1STOpt軟件進行編程計算,得到動力學方程參數如表2所示。甲醇水蒸氣重整反應活化能為100.3 kJ/mol,逆水汽變換反應的活化能為79.5 kJ/mol。Peppley等[12]報道甲醇水蒸氣重整和逆水汽變換反應活化能分別為102.8 kJ/mol和87.6 kJ/mol;Agarwal等[15]研究發現在銅基催化劑上甲醇水蒸氣重整和逆水汽變換反應的活化能分別為92 kJ/mol和79.7 kJ/mol;Silva等[16]也報道了甲醇水蒸氣重整反應的活化能是86.9 kJ/mol;Patel等[17]提出甲醇水蒸氣重整反應的活化能是87.7 kJ/mol。通過與上述文獻對比發現,本文得到的SR和RWGS反應活化能與文獻報道值很接近。由表2可知,所有參數的95%置信區間都不包括0,本次參數估值具有統計學意義。
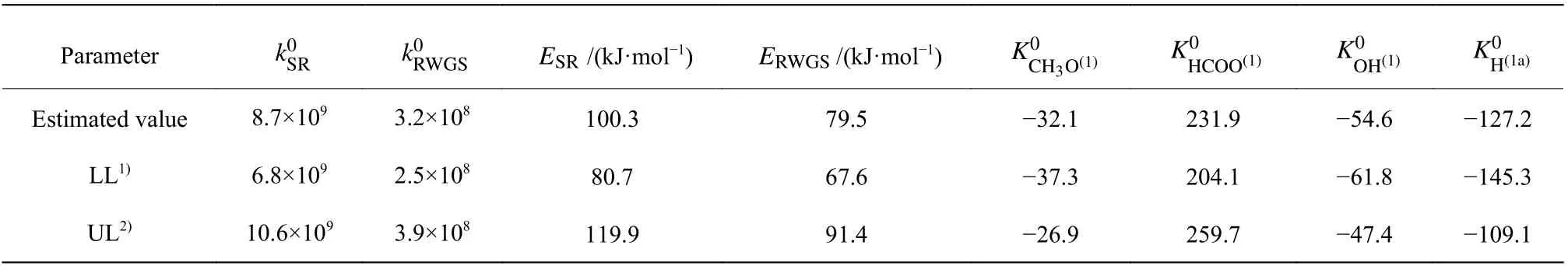
表2 運用ISTOpt軟件得到的動力學模型參數Table 2 Estimated parameters for the kinetic model by ISTOpt software
圖6示出了反應器出口處CO2、CO摩爾流率實驗值與計算值的對比結果,可見實驗值與計算值比較接近,動力學模型中反應器出口處CO2和CO的相對誤差絕對值[18]分別為1.36%和0.93%,擬合效果良好。

圖6 反應器出口處CO2(a)、CO(b)摩爾流率實驗值與計算值的比較Fig. 6 Comparison of experimental and calculated molar flow rates of CO2(a) and CO(b) at reactor outlet
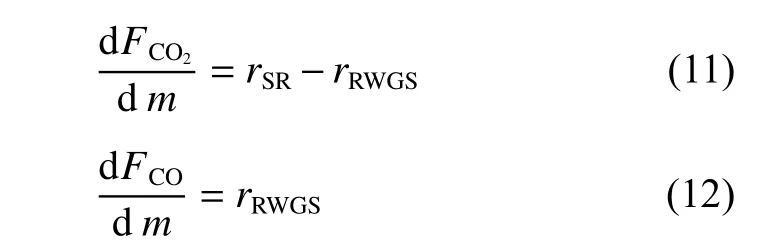
式中,m為催化劑的質量,通過四階Runge-Kutta法求解常微分方程(11)和(12),將25組實驗數據代入速率表達式中,利用最大繼承法(全局+局部搜索)進行參數估值,目標函數為反應器出口處CO2、CO摩爾流率計算值與實驗值的殘差平方和f:
2.3 催化劑失活原因
催化劑在應用時,除了要考慮其活性外,還要考慮其失活問題。對于本實驗中的改性催化劑CuO/ZnO/Al2O3來說,高溫(300 ℃)下MSR反應產生的高含量CO可能會加劇催化劑的失活[19-20]。本文通過對新鮮催化劑(樣品1)、新鮮催化劑在300 ℃下反應20 d后的失活催化劑(樣品2)、新鮮催化劑在200 ℃下反應20 d后的失活催化劑(樣品3)3種催化劑進行表征,探討催化劑失活的具體原因,并驗證300 ℃下反應時產生的高含量CO是否會加劇催化劑失活。所用到的表征手段有N2吸附-脫附測試(BET方程)、X射線熒光光譜(XRF)分析、X射線衍射(XRD)分析、CO程序升溫脫附(CO-TPD)方法。由圖7可知,催化劑經過20 d的使用之后,活性都出現了明顯的下降,其中在300 ℃下反應的催化劑(樣品2)活性下降得更快。
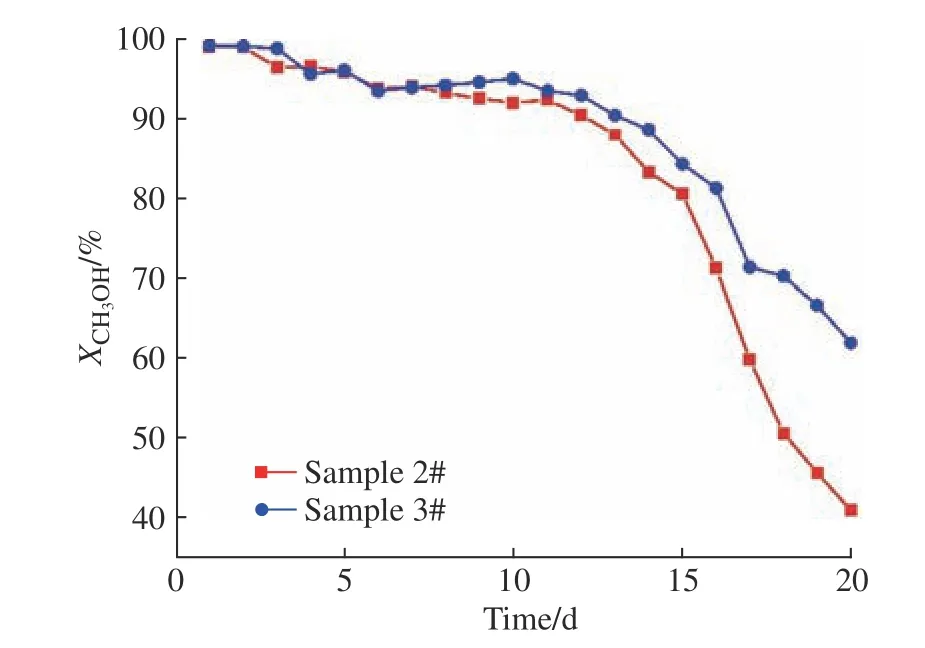
圖7 催化劑活性與時間關系Fig. 7 Relationship between catalyst activity and time
BET方程主要用來表征催化劑的比表面積、孔容和孔徑,反映催化劑的表面形態。一般來說,比表面積越大,反應物與催化劑的接觸面積越大,越有利于活性組分的分布,催化劑的活性越好。但催化劑在高溫下反應,因積碳和大孔道孔壁不穩定而坍塌會造成催化劑比表面積降低,從而使得高溫(300 ℃)下催化劑的活性下降得更快。由表3可知,使用后的催化劑(樣品2和樣品3)比表面積減小,其中樣品2的比表面積減少得更多,這與實驗結果一致。值得注意的是,反應后催化劑平均孔徑變大,這可能是因為反應產生的積碳堵塞微孔,使得大孔的比例增加,同時積碳會形成一些大的機械孔,使得催化劑孔徑增加。
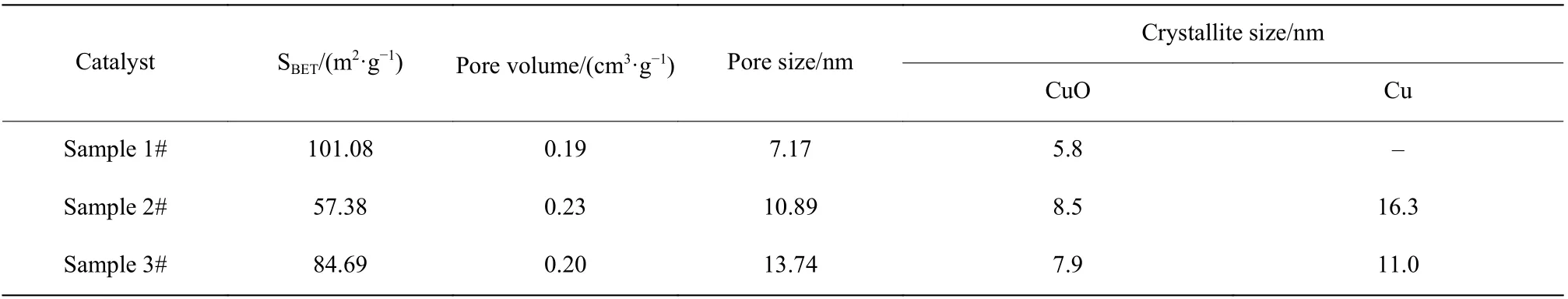
表3 催化劑的結構參數Table 3 Structure parameters of catalysts
如圖8所示,3種催化劑的等溫吸附-脫附曲線都屬于Ⅳ型等溫線,發生介孔毛細凝聚現象,都有H1滯后環。其中樣品1的滯后環明顯更大,說明樣品1比樣品2和樣品3的介孔數量更多。當相對壓力(p/p0)為0.60~0.90時,樣品1的吸附量激增;當p/p0為0.70~0.90時,樣品2的吸附量激增;當p/p0為0.75~0.90時,樣品3的吸附量激增。p/p0的位置反映催化劑孔徑的大小,上述結果說明催化劑樣品2和樣品3的孔徑變大。但如前所述,相比樣品1,樣品2和樣品3的介孔數量減少,說明這兩種催化劑的大孔比例增加,由于一部分大孔是機械孔,不能提升催化劑的活性,因此介孔減少會影響催化劑的活性。
圖9所示是催化劑的孔徑分布曲線,可見樣品1的孔徑主要分布在5~12 nm,樣品2的孔徑主要分布在6~22 nm,樣品3的孔徑主要分布在5~20 nm。很明顯,樣品1的孔徑分布更加集中,這說明新鮮催化劑的介孔比例較高,使用后催化劑的介孔比例減少。同時,樣品2和樣品3的孔徑變大,說明催化劑活性降低,這與圖8中的分析結果一致。
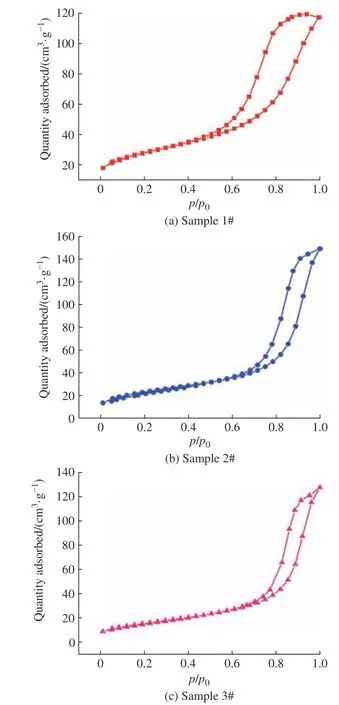
圖8 催化劑的等溫吸附-脫附曲線Fig. 8 Adsorption-desorption isotherms of catalysts

圖9 催化劑的孔徑分布曲線Fig. 9 Pore size distribution curve of catalysts
運用XRF方法表征了催化劑中主要元素的質量分數,結果如表4所示。由表4可知,催化劑中主要金屬元素Cu、Zn、Al的質量分數在催化劑使用之后都出現了下降。本實驗中,樣品2在空氣中暴露的時間比較長,因而Cu大部分被氧化為CuO;樣品3在空氣中暴露的時間較短,因而Cu主要以單質Cu的形式存在。Twigg等[13]認為催化劑中Cu的損失是催化劑失活的一個原因。因此推斷,活性組分CuO的流失是催化劑失活的一個原因。
圖10所示為不同催化劑樣品的XRD譜圖,可見新鮮催化劑(樣品1)中CuO的衍射峰較多、峰較窄、峰面積較大,說明該催化劑中CuO含量高、結晶好。樣品2催化劑中36°和38°處CuO的衍射峰面積變小,說明CuO含量下降,這與表4的分析結果一致。
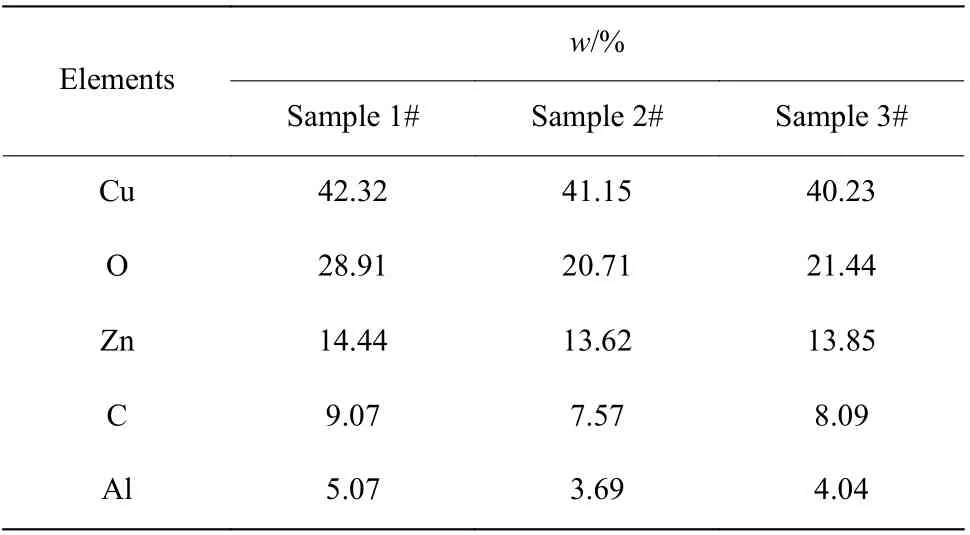
表4 催化劑中主要元素質量分數Table 4 Mass fraction of main elements in catalysts

圖10 催化劑的XRD圖Fig. 10 XRD diagram of catalysts
應用Scherrer公式(式(14)所示)計算晶粒尺寸,并對樣品催化劑中CuO和Cu的晶粒尺寸進行計算,結果如表3所示。

式中,d為晶粒尺寸,Ks為Scherrer常數,λ為X射線波長,B為樣品衍射峰半寬高,θ為衍射角。
樣品2和樣品3的CuO晶粒尺寸相較新鮮催化劑有所增加,樣品2中Cu的晶粒尺寸比樣品3中Cu晶粒尺寸大。Twigg等[13]的研究表明Cu顆粒增大也是催化劑失活的一個原因。催化劑使用后,CuO晶粒尺寸增大,不利于CuO的均勻分散。圖7中樣品2比樣品3的催化活性更差,這與XRD分析結果一致。
CO-TPD可以測試催化劑表面金屬活性中心的數量,也可以測定催化劑對CO的吸附能力。圖11所示為催化劑的CO-TPD圖。由圖11可知,催化劑使用后對CO的吸附能力大大降低,說明催化劑表面上金屬活性中心的數量減少了。MSR反應在高溫(300 ℃)下會產生大量CO,但是樣品2和樣品3的CO吸附能力相差不大。CO的脫附溫度在300 ℃左右,該溫度下的MSR反應雖然生成了大量CO,但是只會有很少一部分吸附在催化劑上。因此,高溫下反應生成的高含量CO對催化劑的失活沒有產生明顯影響。
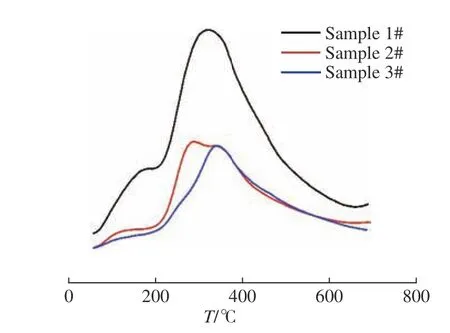
圖11 催化劑的CO-TPD圖Fig. 11 CO-TPD diagram of catalysts
3 結 論
(1) MSR反應的適宜溫度在240 ℃左右,高溫會使得CO選擇性較高,低溫會使得CH3OH轉化率不高;甲醇水溶液進料中水與甲醇物質的量之比增大,CH3OH轉化率變大,CO選擇性變小,但是水與甲醇物質的量之比太大,會消耗更多的能量;在保證CH3OH轉化率的前提下,適當提高進料的液時空速,能夠提高反應效率。
(2) 以Langmuir-Hinshelwood理論為基礎,采用SR-RWGS型雙速率反應動力學模型對甲醇水蒸氣重整反應動力學進行參數估值,動力學模型中反應器出口處CO2和CO的相對誤差絕對值分別為1.36%和0.93%,擬合效果良好。
(3) 催化劑的主要失活原因除熱燒結外,催化劑比表面積減小、介孔比例減少、活性組分CuO或Cu的流失、CuO或Cu晶粒變大也是催化劑失活的具體原因,高溫反應中產生的高含量CO對催化劑的失活沒有明顯影響。

