甲烷催化雙重整過程模擬
莊煒杰, 仇 鵬, 曾澤李, 代正華, 王輔臣
( 華東理工大學資源與環境工程學院,上海市煤氣化工程技術研究中心, 上海 200237)
天然氣作為一種優質、清潔的能源,對于我國優化能源結構、保護生態環境、提高人民生活質量、促進國民經濟和社會可持續發展具有重要意義。在2019年,我國天然氣消費量在一次能源消費總量中的占比達8.1%,同比增長9.1%[1]。
目前,有多種可有效利用天然氣等氣態烴制取合成氣的重整工藝[2],其中,甲烷水蒸氣重整工藝在1926年已經實現工業化應用[3],是龐大的合成氨和甲醇等工業的基礎。工業中通常采用高水碳比(n(H2O)∶n(CH4),2.5~3.0)以減少積碳的生成,所得合成氣的n(H2)/n(CO)遠大于理論值3[4]。富氫的合成氣可用于制氫和合成氨[5],但需要補充額外的CO才能得到合適的n(H2)∶n(CO),以用于費托合成及甲醇合成等其他重要的化工生產。甲烷二氧化碳重整反應能夠充分利用甲烷和二氧化碳這兩種溫室氣體來生產合成氣,該合成氣通常具有較低的n(H2)∶n(CO),可直接用于羰基合成、二甲醚合成、費托合成等反應[6],但由于反應溫度較高,催化劑容易發生積碳、燒結現象而降低壽命[7-8]。
甲烷水蒸氣二氧化碳雙重整過程將上述兩種工藝耦合[9],既可以提高催化劑的穩定性[10],減少積碳的生成,又能靈活調節合成氣中的n(H2)∶n(CO)以適應多種工藝和工況需求,具有重要的研究意義和工程價值。在工藝方面,Oezkara[11]和Jang等[12]采用Gibbs自由能最小法對甲烷水蒸氣二氧化碳雙重整過程進行了熱力學平衡分析,認為在氧化劑量(n(CO2)+n(H2O))保持不變的情況下,改變水碳比不會影響甲烷的消耗速率;但隨著壓力增大,二氧化碳的轉化率與n(H2)∶n(CO)都逐漸降低;當(n(CO2)+n(H2O))∶n(CH4)大于1.2時可以抑制高溫區域積碳的生成。Wu等[13]在甲烷水蒸氣二氧化碳雙重整工藝中加入氧氣形成甲烷三重整過程,通過提高n(H2O)∶n(CH4)、降低n(O2)∶n(CH4)與n(CO2)∶n(CH4)以提高n(H2)∶n(CO)。當n(CH4)∶n(O2)∶n(H2O)∶n(CO2)=1.0∶0.5∶1.0∶1.0,進料溫度達到500 ℃以上時,該甲烷三重整反應可自發進行。Minette等[14]提出了一種使用薄涂層結構的Zoneflow反應器用于甲烷雙重整工藝,可在低壓條件下提高產能,改善熱傳遞并降低壓降,與傳統的顆粒填充床相比通量提高達25%。
在催化劑制備方面,Itkulova等[15]研制了一種新型Co-Pt/Al2O3催化劑,可在相對較低的溫度(700~750 ℃)下對甲烷進行雙重整以生產合成氣,其中Pt是形成穩定性強、分散度高的還原性雙金屬納米粒子的主要因素。任盼盼等[16]研制了一種新型的Ni/ZrO2雙重整催化劑,Ni晶粒尺寸小、分散度高并能加強金屬-載體的相互作用,提高了催化劑的抗燒結和抗積碳能力。Shakouri等[17]制備了一種新型Ni-Co催化劑,在進料組成為CH433% (摩爾分數,余同)、CO221.5%、H2O 12%、H23.5%以及N230%的沼氣中,二氧化碳轉化率達到70%,n(H2)/n(CO)為1.8 ~ 2.0。
盡管前人已較為詳盡地研究了工藝條件對甲烷雙重整過程的影響,但大多基于熱力學分析。本文通過Aspen Plus軟件建立了甲烷雙重整過程的動力學模型,并探究了溫度、壓力和進料物質的量之比對反應產物以及n(H2)/n(CO)的影響。
1 模型建立
1.1 結構描述
甲烷雙重整反應示意圖如圖1所示。混合原料氣經過對流段預熱后導入上集氣管中,通過上集氣管分配至各個轉化管。轉化管內填充催化劑,原料氣自上而下流動,經過反應管內的催化劑床層發生重整反應。反應所需熱量由管外燃料氣與空氣燃燒產生的高溫煙氣供給,主要傳熱方式為輻射傳熱。反應完畢后的高溫出口氣在下端出口流出,在集氣管匯合后進入后續工段[18]。
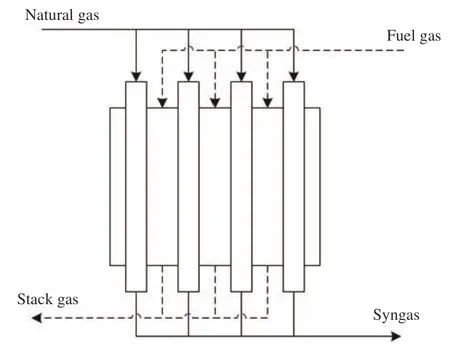
圖1 甲烷雙重整反應器示意圖Fig. 1 Schematic diagram of methane bi-reforming reactor
1.2 數學模型
利用化學計量反應器模擬非甲烷的烷烴與水蒸氣的反應過程和燃料氣的燃燒過程,利用平推流反應器模擬甲烷水蒸氣二氧化碳的雙重整反應,如圖2所示。利用Fortran語言編寫反應動力學模型、壓降模型與傳熱模型。

圖2 甲烷雙重整反應過程模擬圖Fig. 2 Simulation diagram of methane bi-reforming reaction process
1.2.1 雙重整反應的動力學方程 甲烷水蒸氣二氧化碳雙重整過程的催化轉化主要為兩個甲烷水蒸氣重整反應與水氣變換反應,分別如式(1)~式(3)所示。

其動力學模型[19]分別為:

其中:r表示反應速率;Keq和k分別是化學平衡常數和反應速率常數;Kj是組分j的吸附常數,具體數值分別如表1~表3所示,下標1、2、3分別對應式(1)~式(3)。pj是組分j的分壓,單位為Pa。已有研究表明不必考慮特定的二氧化碳重整反應動力學[20]。該動力學模型主要用于甲烷水蒸氣重整反應,但文獻[21]表明該動力學模型在甲烷雙重整反應中也有較好的應用。
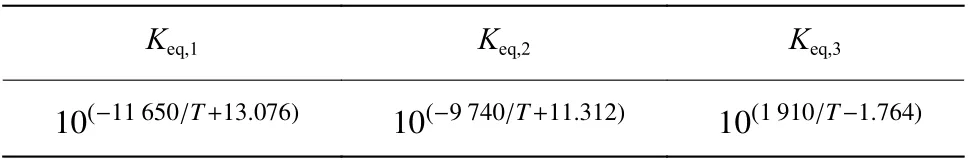
表1 化學平衡常數[12]Table 1 Chemical equilibrium constants[12]

表2 反應速率常數[12]Table 2 Reaction rate constants[12]

表3 組分吸附常數[12]Table 3 Adsorption constants of the components[12]
甲烷、水蒸氣與二氧化碳的轉化率(X)、n(H2)/n(CO)分別根據式(8)~式(11)進行計算。
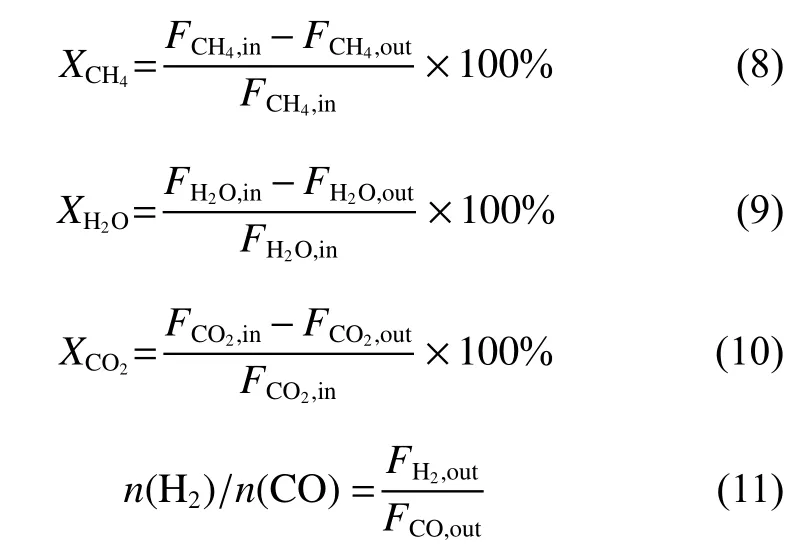
其中:FCH4,in、FH2O,in、FCO2,in為反應器進口氣體的摩爾流量,FCH4,out、FH2O,out、FCO2,out、FH2,out、FCO,out為反應器出口氣體的摩爾流量,單位為kmol/h。
1.2.2 壓降微分方程 平推流反應器的壓降表達式為:
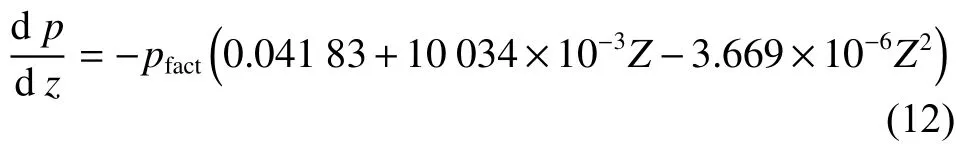
其中:Z為反應器長度,單位為m;pfact為壓降影響因子,取值為0.8。計算結果表明,床層壓降計算值與實際工廠數據較為吻合。
1.2.3 傳熱模型 轉化爐內的主反應為吸熱反應,傳熱速率主要由管內外傳熱系數、煙氣溫度以及管內氣體溫度決定。高溫煙氣與反應管內的主要傳熱方式為輻射傳熱。為便于計算,本文定義了內、外部傳熱系數。
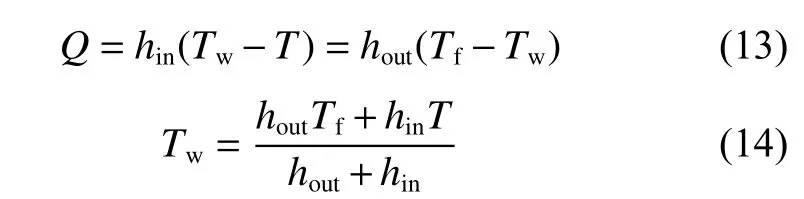
其中:Q為管內區域的熱通量,W/m2;hin和hout分別為內部傳熱系數及外部傳熱系數,W/(m2·K);Tf和Tw分別為高溫煙氣溫度和管壁溫度,單位為K,其中Tf取值為1473 K。內、外部傳熱系數都隨著氣體溫度T的改變而改變。
管內傳熱系數由流體性質決定[22]:
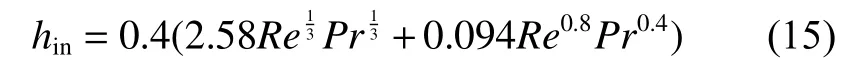
其中:Re為雷諾數;Pr為普朗特常數。
反應管熱通量受輻射傳熱機制的影響:
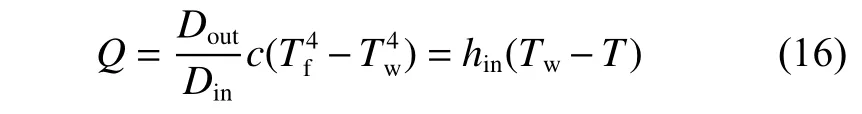
其中:Din和Dout分別為反應管的內徑與外徑;c為Stefan-Boltzman常數與有效發射率的乘積。
2 結果與討論
2.1 模型驗證
2.1.1 甲烷水蒸氣重整模擬驗證 反應器長度11 m,直徑0.17 m,管數88根,進口天然氣壓力3.25 MPa,水碳比2.7,過量空氣系數為1.2,催化劑床層密度2337.9 kg/m3,床層空隙率0.528。進料氣基本條件見表4。
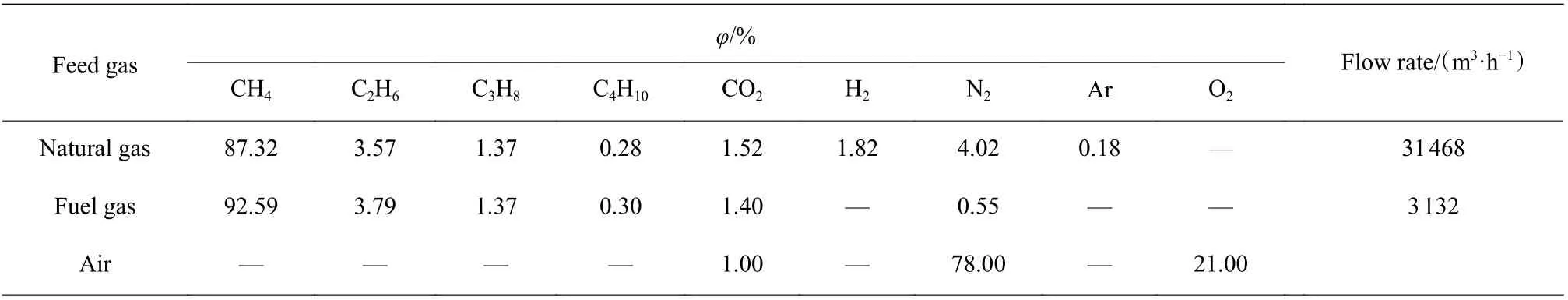
表4 進料氣的基本條件Table 4 Basic conditions of feed gas
甲烷水蒸氣重整模擬驗證結果如表5所示,出口干氣中甲烷體積分數的誤差為6.12%,模擬結果與工廠數據[23]相差較小,說明模型具有較好的準確性。

表5 甲烷水蒸氣重整模擬結果與工廠數據對比Table 5 Comparion of simulation results and plant data of methane steam reforming
2.1.2 甲烷雙重整模擬驗證 甲烷雙重整的工業數據鮮見報道,因此將模擬結果與文獻報道實驗數據[24]進行了比較,反應條件為T=800 ℃、p=0.1 MPa、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4,對比結果如表6所示。模擬結果與文獻數據非常接近,二氧化碳轉化率誤差為5.15%,模型較為準確,可用于進一步討論甲烷雙重整反應過程的影響因素。
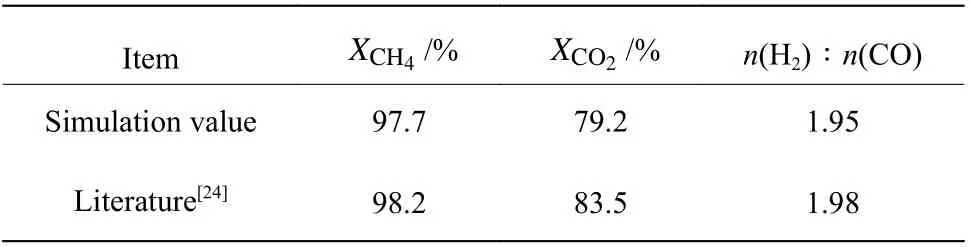
表6 甲烷雙重整模擬結果與實驗數據對比[24]Table 6 Comparion of simulation results and experimental data of methane bi-reforming
2.2 溫度對反應產物的影響
在p=3.2 MPa、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4下考察了反應溫度在550~900 ℃時甲烷雙重整反應中氣體組分的分布情況與甲烷、水蒸氣和二氧化碳的轉化率,結果如圖3所示。由圖3可以看出,甲烷雙重整反應需要較高的溫度才有利于甲烷與二氧化碳發生反應。反應溫度越高,甲烷、水蒸氣和二氧化碳的轉化率越高。當反應溫度為550~650 ℃時,甲烷水蒸氣重整反應為主要反應,二氧化碳在該溫度下不發生反應;當反應溫度為650~750 ℃時,甲烷與水蒸氣的轉化程度有所提高,二氧化碳開始進行轉化,這是因為水氣變換反應為放熱反應,升高溫度有利于促進二氧化碳的轉化,但二氧化碳的轉化率仍低于水蒸氣的轉化率,甲烷水蒸氣重整反應仍為主要反應。當反應溫度為750~900℃時,甲烷、水蒸氣和二氧化碳的轉化率都大幅度提高,且在810℃時,二氧化碳的轉化率超過了水蒸氣的轉化率,表明在較高的反應溫度與壓力下,溫度對甲烷二氧化碳重整反應速率的影響更大。

圖3 溫度對甲烷雙重整反應產物的影響Fig. 3 Effect of temperature on the products of methane bi-reforming reaction
2.3 壓力對反應產物的影響
為提高經濟效益,大多數甲烷雙重整過程都是在高壓下進行的,因此有必要研究壓力對甲烷雙重整反應的影響。在T=800 ℃、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4下考察了壓力在0.1~3.5 MPa范圍內反應產物的轉化率及n(H2)/n(CO),結果如圖4所示。從圖4可以看出,隨著壓力的增大,甲烷、水蒸氣和二氧化碳的轉化率都快速下降。這是因為壓力增大使甲烷水蒸氣重整反應向逆反應方向進行,導致甲烷與水蒸氣的轉化率降低,生成的氫氣也相對減少,因而水氣變換反應中逆反應的反應程度也下降,使得二氧化碳的轉化率降低。當壓力達到3.5 MPa時,甲烷、水蒸氣和二氧化碳的轉化率分別為35.5%、30.3%、28.4%。壓力對n(H2)/n(CO)的影響不顯著,壓力增大,n(H2)/n(CO)緩慢增加。

圖4 壓力對甲烷雙重整反應產物的影響Fig. 4 Effect of pressure on the products of methane bi-reforming reaction
2.4 進料組成對反應產物的影響
通過調節進料組成,可使產物分布更加靈活。在T=800 ℃、p=3.2 MPa條件下考察了不同進料組成對甲烷雙重整反應物甲烷、水蒸氣和二氧化碳轉化率的影響。
2.4.1n(CO2)∶n(CH4)對反應產物的影響 圖5所示為n(CH4)∶n(H2O)=1∶1時不同n(CO2)∶n(CH4)對甲烷、水蒸氣和二氧化碳轉化率及n(H2)∶n(CO)的影響。隨著n(CO2)∶n(CH4)從0升高到2.5,甲烷轉化率由35.35%升高到68.95%。二氧化碳轉化率在n(CO2)∶n(CH4)從0~1.0時快速增加,之后基本不變,說明在高壓下,當n(CO2)∶n(CH4)>1.0時繼續提高n(CO2)∶n(CH4)對二氧化碳轉化率的影響較小。水蒸氣轉化率隨著n(CO2)∶n(CH4)的提高顯著下降,這是因為在高壓下,二氧化碳含量相對增多抑制了甲烷水蒸氣重整反應過程。在n(CO2)∶n(CH4)=2.5時,水蒸氣轉化率僅為2.36%。在n(CO2)∶n(CH4)=0時,700 ℃下n(H2)∶n(CO)遠大于反應式(1)的化學計量比3∶1,說明水氣變換反應起著顯著的作用。隨著溫度升高,n(H2)∶n(CO)逐漸減小,說明溫度升高促進了逆水氣變換反應的進行,消耗了H2并生成了一氧化碳。當n(CO2)∶n(CH4)為1.0或2.0時,溫度對n(H2)∶n(CO)的影響較小。

圖5 不同n(CO2)∶n(CH4)對甲烷雙重整反應產物的影響(n(CH4)∶n(H2O)=1∶1)Fig. 5 Effect of different n(CO2)∶n(CH4) on the products of methane bi-reforming reaction (n(CH4)∶n(H2O)=1∶1)
2.4.2n(H2O)∶n(CH4)對反應產物的影響 圖6所示為n(CH4)∶n(CO2)=1∶1時不同n(H2O)∶n(CH4)對甲烷、水蒸氣和二氧化碳轉化率及n(H2)∶n(CO)的影響。由圖6(a)可知,隨著n(H2O)∶n(CH4)的升高,甲烷和水蒸氣的轉化率均增大,主要原因是n(H2O)∶n(CH4)的增大促進了反應(1)、(2)的進行,當n(H2O)∶n(CH4)大于2.0時,能有效提高反應(2)的反應程度,從而提高甲烷和水蒸氣的轉化率。二氧化碳的轉化率隨著n(H2O)∶n(CH4)的增大而減小,主要原因是水蒸氣含量的相對增多強化了水氣變換反應。增加水蒸氣的量有利于提高生成物中n(H2)∶n(CO)。當n(H2O)∶n(CH4)=0時,n(H2)∶n(CO)隨著反應溫度的升高而增大。當n(H2O)∶n(CH4)=1.0時,溫度對n(H2)∶n(CO)的影響較小,在800 ℃時,n(H2)∶n(CO)為1.35。當n(H2O)∶n(CH4)=2.0時,n(H2)∶n(CO)隨著溫度升高而降低,這是因為升高溫度促進了甲烷二氧化碳重整反應的進行,因而n(H2)∶n(CO)下降趨勢較為明顯。
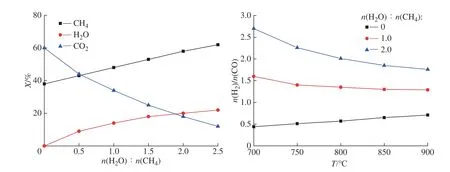
圖6 不同n(H2O)∶n(CH4)對甲烷雙重整反應產物的影響(n(CH4)∶n(CO2)=1∶1)Fig. 6 Effect of different n(H2O)∶n(CH4) on the products of methane bi-reforming reaction (n(CH4)∶n(CO2)=1∶1)
3 結 論
(1) 甲烷、水蒸氣和二氧化碳的轉化率均隨溫度的升高而增大。與甲烷水蒸氣重整反應相比,提高甲烷與二氧化碳的轉化率所需的反應溫度更高,二氧化碳于650 ℃開始轉化。
(2) 隨著反應壓力的增大,甲烷、水蒸氣和二氧化碳的轉化率均快速下降。當壓力達到3.5 MPa時,甲烷、水蒸氣和二氧化碳的轉化率均小于40%。但壓力對n(H2)∶n(CO)的影響不明顯。
(3) 在p=3.2 MPa時,隨著n(CO2)∶n(CH4)的增大,甲烷的轉化率呈線性增加,水蒸氣的轉化率顯著降低,二氧化碳的轉化率呈現先快速增加后穩定的趨勢。可以通過調節溫度和進料中水蒸氣和二氧化碳物質的量之比來調整n(H2)∶n(CO),以進行后續的工業生產。

