HPLC-QAMS法同時測定紫花燒傷軟膏中10種有效成分的含量
張小折,葉曉婭,田廣林
1.平頂山市食品藥品檢驗所,平頂山 467000;2.遂成藥業(yè)股份有限公司,鄭州 451100
紫花燒傷軟膏由紫草、地黃、熟地黃、花椒、黃連、當歸、甘草和冰片8味中藥材加工而成,具有清熱涼血、化瘀解毒、止痛生肌的功效,主要用于Ⅰ、Ⅱ度以下燒傷、燙傷的治療,還可用于壓瘡[1-2]的治療,為《中華人民共和國藥典》(以下簡稱《中國藥典》)2020 年版一部[3]收載品種,是臨床上的常用藥物,現(xiàn)行質(zhì)量標準僅用氣相色譜法對佐藥冰片中龍腦的含量進行檢測,未檢索到與該制劑質(zhì)量控制相關(guān)的文獻,難以全面評價紫花燒傷軟膏的整體質(zhì)量。中藥復方制劑由多味中藥材配伍組方,同時每味中藥材又含有多種藥效成分,具有多靶點、共同奏效等特點,建立多指標成分定量控制模式對提升紫花燒傷軟膏的整體質(zhì)量具有重要意義。高效液相色譜-一測多評(high performance liquid chromatography-quantitative analysis of multi-components by single-marker,HPLCQAMS)法[4]利用中藥藥效組分間的內(nèi)在函數(shù)關(guān)系,通過對1種質(zhì)量穩(wěn)定、易得、價廉的成分進行定量測定來實現(xiàn)對多種成分的同步檢測,現(xiàn)在已越來越多地應用于中藥[5-6]及其制劑[7-8]的研究中。本實驗以乙酰紫草素為內(nèi)參物,用HPLC-QAMS法對紫花燒傷軟膏中10種成分的含量進行同步檢測,首次建立了紫花燒傷軟膏多指標成分質(zhì)量評價方法,為全面、科學地評價該制劑的整體質(zhì)量提供實驗依據(jù)。
1 儀器與試藥
1.1 儀器
1260 Infinity型高效液相色譜儀(美國Agilent公司);Waters 2695型高效液相色譜儀(美國Waters公司);Acclaim 120 C18液相色譜柱(賽默飛世爾科技公司);Phenomenex Luna C18液相色譜柱(廣州同譜實驗儀器有限公司);Waters XBridge C18液相色譜柱(250 mm×4.6 mm,5μm,美國Waters公司);DL-720D 型超聲波清洗器(上海之信儀器有限公司);ME204型電子天平(瑞士Mettler Toledo公司)。
1.2 試藥
對照品:毛蕊花糖苷(批號111530-201914,質(zhì)量分數(shù)為95.2%)和β,β′-二甲基丙烯酰阿卡寧(批號111689-201805,質(zhì)量分數(shù)為98.0%)均購自中國食品藥品檢定研究院;焦地黃苯乙醇苷B1(批號PRF7041822,質(zhì)量分數(shù)為98.5%,成都普瑞法科技開 發(fā) 有 限 公 司);羥 基-α-山 椒 素(批 號 RFSQ11402007006,質(zhì)量分數(shù)為98.2%),羥基-β-山椒素(批號RFS-Q11502007016,質(zhì)量分數(shù)為98.5%),羥基-γ-山椒素(批號RFS-Q11602011013,質(zhì)量分數(shù)為98.3%),乙酰紫草素(批號RFS-Y18811804026,質(zhì)量分數(shù)為98.5%),β-乙酰氧基異戊酰阿卡寧(批號RFS-Y1510210028,質(zhì)量分數(shù)為98.6%),異丁酰紫草素(批號RFS-Y18902102022,質(zhì)量分數(shù)為98.0%),異戊酰紫草素(批號RFS-Y19002102026,質(zhì)量分數(shù)為98.1%),均購自成都瑞芬思生物科技有限公司。乙腈為色譜純;其余試劑為分析純。
紫花燒傷軟膏(規(guī)格:20 g·支-1;批號:20200302、20200501、20200607)購自山東潤澤紫花藥業(yè)有限公司。
2 方法與結(jié)果
2.1 色譜條件
選 用 Acclaim 120 C18色 譜 柱(250 mm ×4.6 mm,5μm)。流動相:乙腈-1 m L·L-1磷酸。梯度洗脫:0~11 min,18.0%乙腈;11~20 min,18.0%→32.0%乙腈;20~32 min,32.0%→58.0%乙腈;32~57 min,58.0%→70.0%乙腈;57~70 min,70.0%→18.0%乙腈)。流速:0.9 m L·min-1。檢測波長:330 nm(0~20 min檢測毛蕊花糖苷和焦地黃苯乙醇苷B1)[9-12]和275 nm(20~70 min羥基-α-山椒素、羥基-β-山椒素、羥基-γ-山椒素、乙酰紫草素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧和異戊酰紫草素)[13-20]。柱溫:30℃。進樣量:10μL。
2.2 溶液的制備
2.2.1 混合對照品溶液的制備 精密稱取毛蕊花糖苷、焦地黃苯乙醇苷B1、羥基-α-山椒素、羥基-β-山椒素、羥基-γ-山椒素、乙酰紫草素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧和異戊酰紫草素對照品適量,用體積分數(shù)50%的甲醇制成 質(zhì) 量 濃 度 依 次 為0.714、0.298、0.576、0.252、0.136、0.982、0.510、0.478、0.634 和1.530 g·L-1的混合對照品儲備液。精密吸取儲備液1.0 m L,用體積分數(shù)50%的甲醇稀釋20倍得混合對照品溶液(10 種 成 分 的 質(zhì) 量 濃 度 分 別 為35.7、14.9、28.8、12.6、6.8、49.1、25.5、23.9、31.7、76.5 mg·L-1)。
2.2.2 供試品溶液的制備 精密稱定紫花燒傷軟膏2.0 g,精密加入體積分數(shù)50%的甲醇25 m L,稱質(zhì)量,超聲10 min,放冷,補足減失的質(zhì)量,搖勻,即得。取按照紫花燒傷軟膏質(zhì)量標準[3]分別制備缺紫草、缺花椒、缺地黃和熟地黃的3個陰性供試品各適量,再按上述方法制得3個陰性供試品溶液。
2.3 系統(tǒng)適用性考察
按照2.1項下色譜條件,取混合對照品溶液和供試品溶液各10μL進樣檢測,記錄色譜圖。結(jié)果見圖1。紫花燒傷軟膏供試品溶液中毛蕊花糖苷、焦地黃苯乙醇苷B1、羥基-α-山椒素、羥基-β-山椒素、羥基-γ-山椒素、乙酰紫草素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧和異戊酰紫草素與相鄰色譜峰的分離度>1.5,理論板數(shù)按所測成分色譜峰計均不低于5 000。陰性供試品對紫花燒傷軟膏中10種成分的同時測定無干擾。
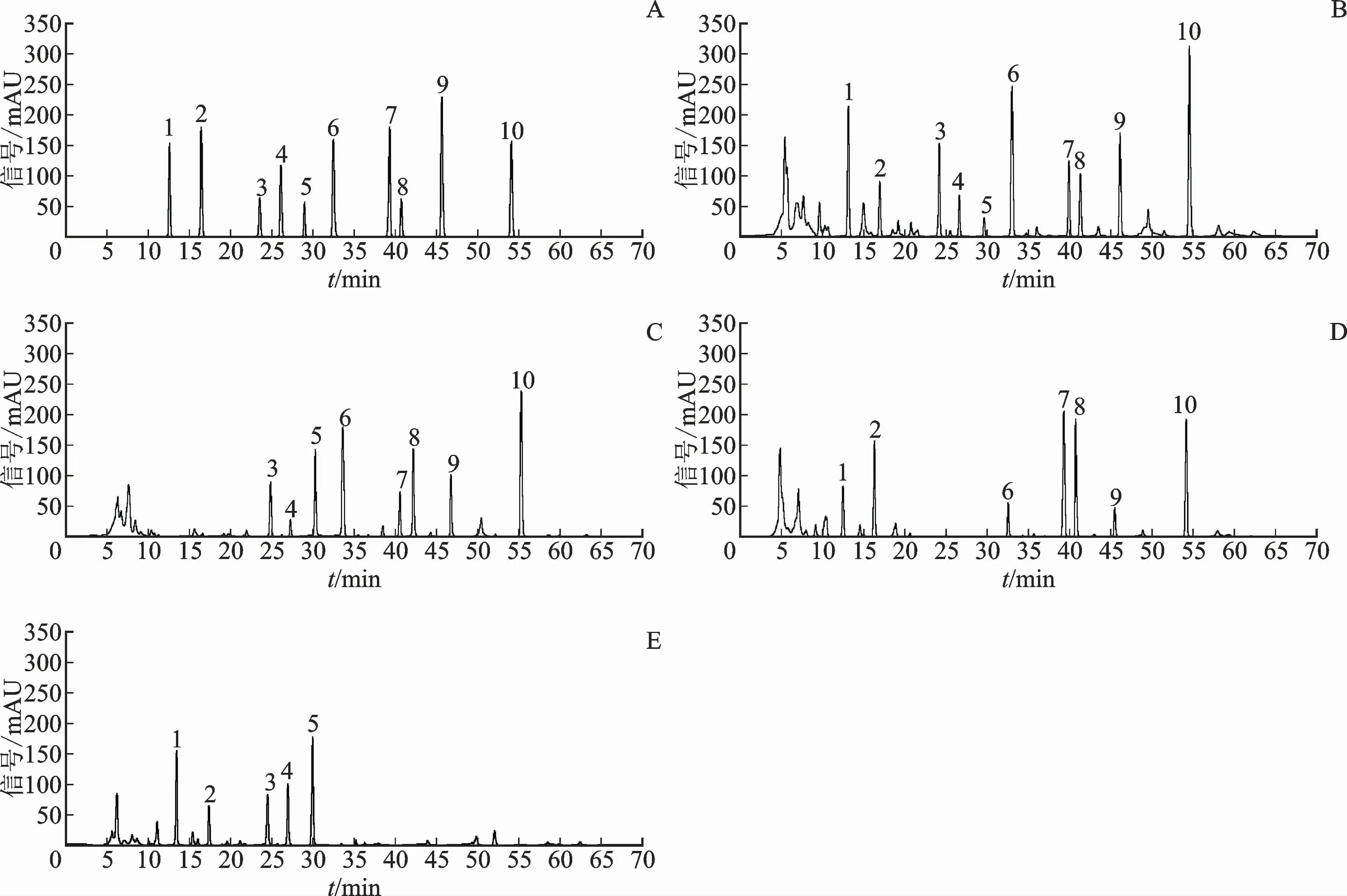
圖1 HPLC圖Fig.1 HPLC chromatograms
2.4 方法學考察
2.4.1 線性關(guān)系考察 精密吸取2.2.1項下儲備液0.1、0.2、0.5、1.0、2.0、5.0 m L,用體積分數(shù)50%的甲醇分別定容至20 m L,得到編號分別為Ⅰ~Ⅵ的混合對照品溶液,按照2.1項下色譜條件進樣檢測,并記錄色譜峰的峰面積,以10種成分的峰面積為縱坐標(y)、質(zhì)量濃度為橫坐標(x)進行線性回歸,結(jié)果見表1。結(jié)果顯示,在各自質(zhì)量濃度范圍內(nèi)10 種成分的線性關(guān)系良好。

表1 10種成分線性關(guān)系測定結(jié)果Tab.1 Results of linear-regression analysis of the 10 constituents
2.4.2 精密度、重復性與穩(wěn)定性實驗 取同一份紫花燒傷軟膏供試品溶液,按照2.1項下色譜條件,重復進樣6次,每次10μL,記錄色譜峰的峰面積。計算得10 種成分峰面積的RSD 值依次為1.06%、1.20%、1.13%、1.27%、1.38%、0.69%、1.08%、1.14%、0.99%、0.52%,表明在上述色譜條件下儀器的精密度良好。
取同一批紫花燒傷軟膏,按照2.2.2項下方法制備6份供試品溶液,各精密吸取10μL,按照2.1項下色譜條件進樣檢測,用外標法計算含量。計算得10種成分含量的RSD 值分別為1.57%、1.71%、1.63%、1.86%、1.92%、1.05%、1.60%、1.58%、1.43%、0.88%,表明建立的方法具有良好的重復性。
分別于0、2、5、9、16、24 h各精密吸取同一份紫花燒傷軟膏供試品溶液10μL,按照2.1項下色譜條件進樣檢測,記錄色譜峰的峰面積。計算得10種成分峰面積的RSD 值依次為1.02%、1.15%、1.19%、1.30%、1.42%、0.66%、1.05%、1.18%、1.02%、0.57%,表明紫花燒傷軟膏供試品溶液在24 h穩(wěn)定性良好。
2.4.3 加樣回收率實驗 取已知10種成分含量的同一批紫花燒傷軟膏,每份精密稱定1.0 g,稱取9份并隨機均分成3 組,精密加入混合對照品溶液(毛蕊花糖苷質(zhì)量濃度為0.607 g·L-1、焦地黃苯乙醇苷B1質(zhì)量濃度為0.243 g·L-1、羥基-α-山椒素質(zhì)量濃度為0.452 g·L-1、羥基-β-山椒素質(zhì)量濃度 為0.169 g·L-1、羥 基-γ-山 椒 素 質(zhì) 量 濃 度 為0.096 g·L-1、乙酰紫草素質(zhì)量濃度為0.817 g·L-1、β-乙酰氧基異戊酰阿卡寧質(zhì)量濃度為0.379 g·L-1、異丁酰紫草素質(zhì)量濃度為0.341 g·L-1、β,β′-二甲基丙烯酰阿卡寧質(zhì)量濃度為0.524 g·L-1、異戊酰紫草 素 質(zhì) 量 濃 度 為1.197 g·L-1)0.8、1.0 和1.2 m L各1組,再按照2.2.2 項下方法制成加樣供試品溶液,按照2.1項下色譜條件檢測并記錄色譜峰的峰面積。計算得10 種成分的平均加樣回收率(RSD 值)分 別 為99.46% (0.73%)、98.27%(1.16%)、97.84% (1.01%)、96.95% (1.45%)、97.18% (1.51%)、100.12% (0.66%)、99.27%(0.92%)、98.56% (1.08%)、99.15% (0.85%)、100.04%(0.78%)。
2.5 相對校正因子的測定及其耐用性考察
2.5.1 相對校正因子的測定 以乙酰紫草素為內(nèi)參物,按照2.1項下色譜條件進樣檢測2.4.1項下編號為Ⅰ~Ⅵ的混合對照品溶液,記錄色譜峰峰面積,計算其他9種成分的相對校正因子(relative correlation factor,RCF)。RCFk/s=(Ak/Wk)/(As/Ws)=(Ak×Ws)/(As×Wk),其中W和A分別表示質(zhì)量濃度和峰面積,k和s分別表示內(nèi)參物和其他待測成分。結(jié)果見表2。
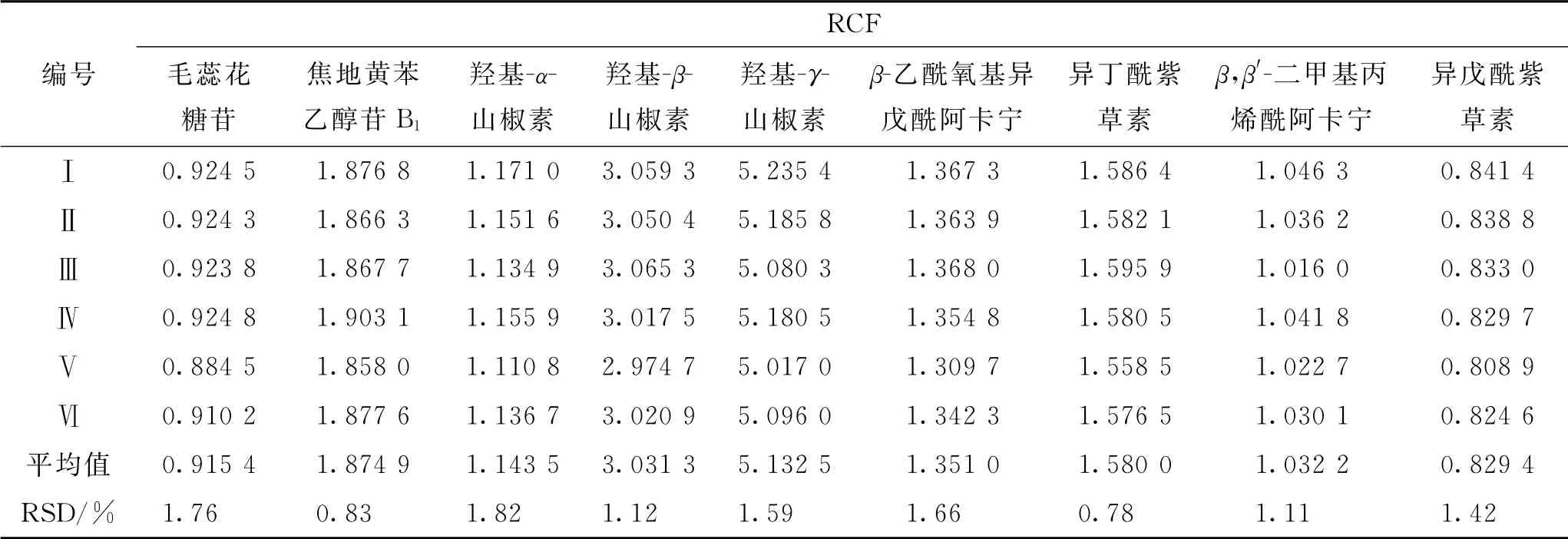
表2 紫花燒傷軟膏中各成分的RCFTab.2 RCFs of various components in Zihua Burn Ointment
2.5.2 RCF耐用性考察
2.5.2.1 儀器與色譜柱 選用不同品牌高效液相色譜儀(Agilent 1260 Infinity型、Waters 2695型)和不同品牌液相色譜柱(Acclaim 120 C18柱、Phenomenex Luna C18柱和Waters XBridge C18柱),考察該條件對各成分RCF 值的影響,按照2.1項下色譜條件進樣檢測2.1.1項下混合對照品溶液,記錄色譜峰的峰面積,計算各成分的RCF 值,結(jié)果見表3。結(jié)果顯示,各成分RCF 的RSD 值在0.83%~1.91%范圍內(nèi),表明儀器及色譜柱對RCF無顯著影響。
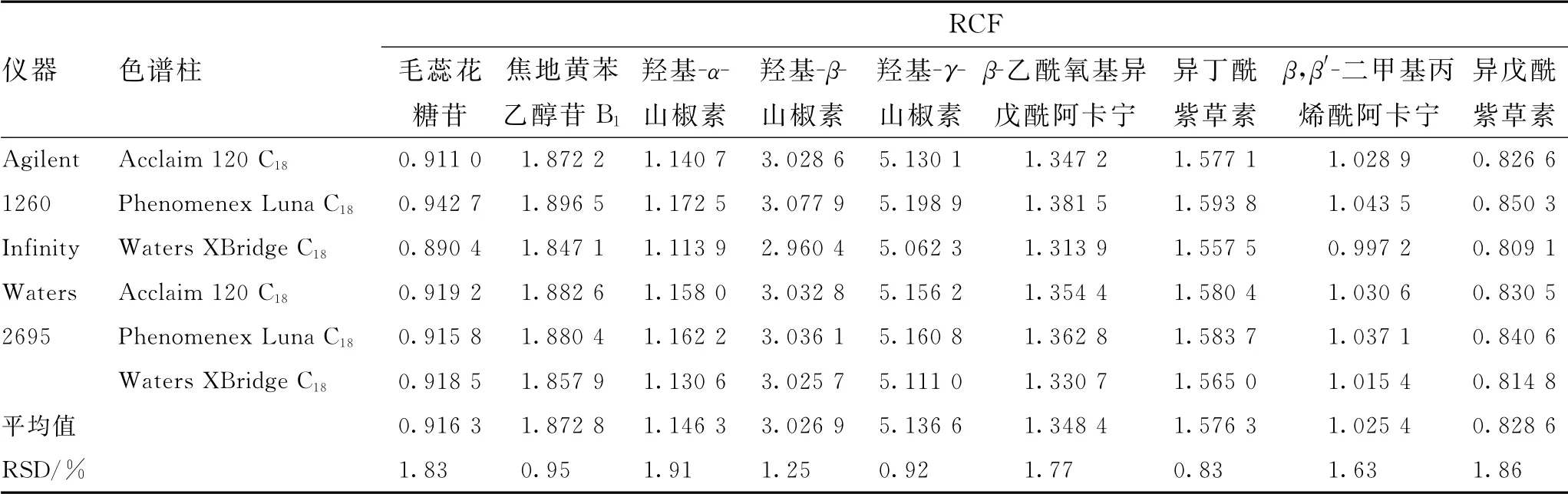
表3 不同儀器及色譜柱條件下的RCFTab.3 RCFs detected with different instruments and under different chromatographic column conditions
2.5.2.2 流 速 在 流 速0.7、0.8、0.9、1.0、1.1 m L·min-1條件下,精密吸取2.1.1項下混合對照品溶液,按照2.1項下色譜條件檢測并記錄色譜峰的峰面積,計算各成分的RCF 值,結(jié)果見表4。結(jié)果顯示,各成分RCF 的RSD 值在1.01%~1.91%范圍內(nèi),表明流速對RCF無顯著影響。
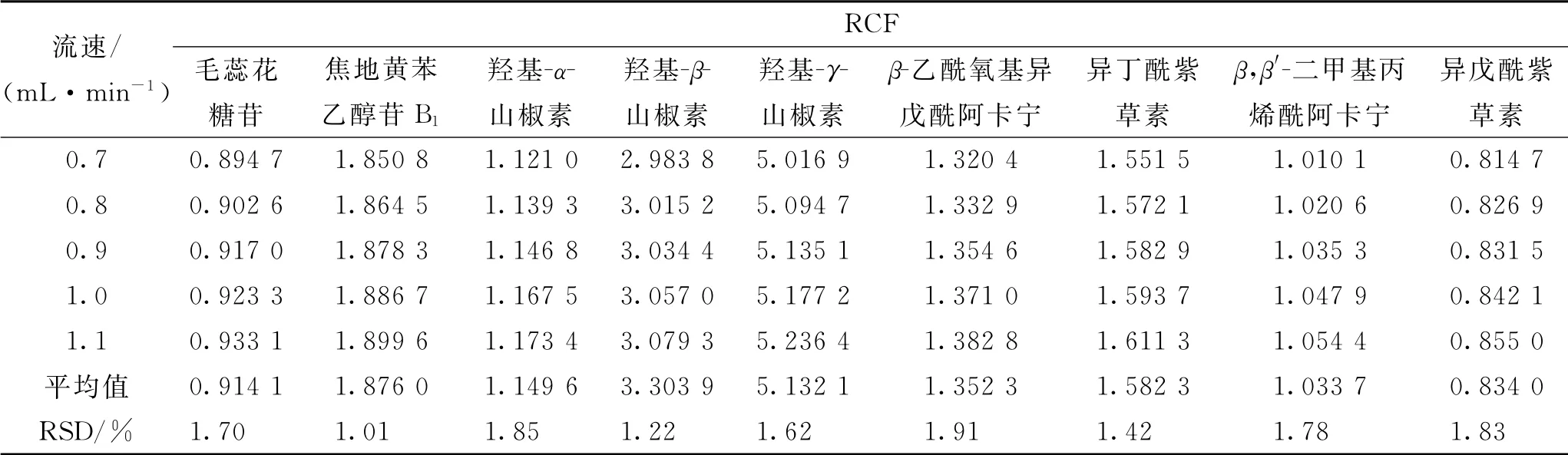
表4 不同流速條件下的RCFTab.4 RCFs detected under different flow rates
2.5.2.3 柱溫 在柱溫20、22、25、28、30℃條件下,精密吸取2.1.1項下混合對照品溶液,按照2.1項下色譜條件檢測并記錄色譜峰的峰面積,計算各成分的RCF值,結(jié)果見表5。結(jié)果顯示,各成分RCF的RSD值在0.97%~1.94%范圍內(nèi),表明柱溫對RCF 無顯著影響。
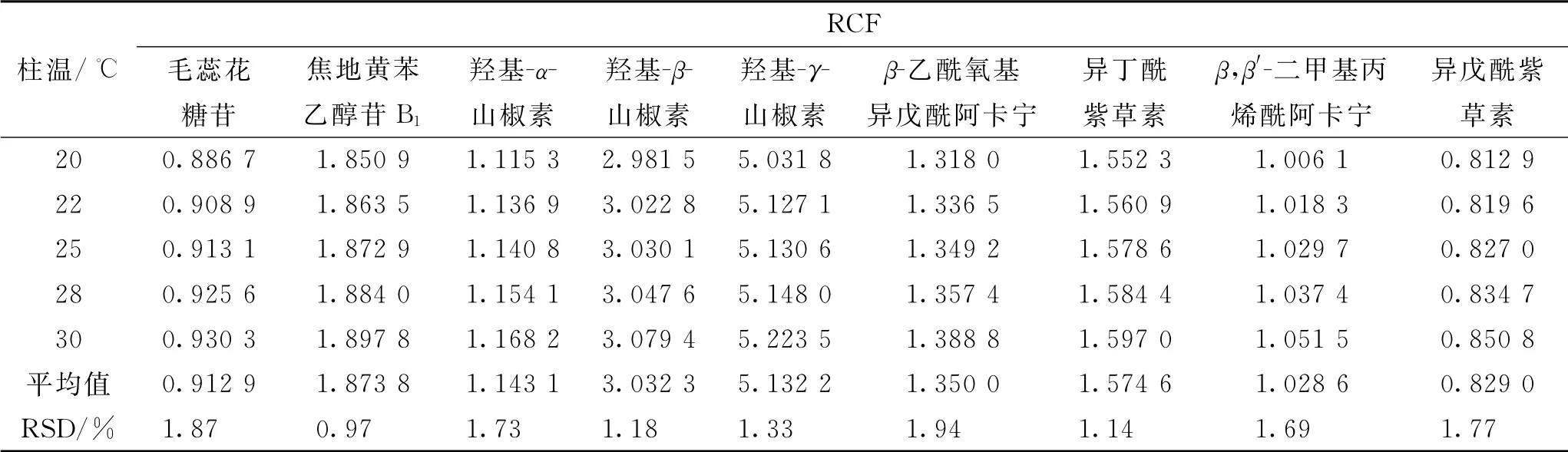
表5 不同柱溫條件下的RCFTab.5 RCFs detected at different column temperatures
2.5.3 色譜峰定位 分別選用不同品牌的高效液相色譜儀(Agilent 1260 Infinity型、Waters 2695型)和不同品牌的液相色譜柱(Acclaim 120 C18柱、Phenomenex Luna C18柱和Waters XBridge C18柱),按照2.1項下色譜條件進樣檢測2.1.1項混合對照品溶液,記錄保留時間,采用相對保留時間(relative retention time,RRT)值法對待測成分色譜峰進行定位,結(jié)果見表6。結(jié)果顯示,毛蕊花糖苷、焦地黃苯乙醇苷B1、羥基-α-山椒素、羥基-β-山椒素、羥基-γ-山椒素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧、異戊酰紫草素和乙酰紫草素RRT 的RSD 值在0.78%~1.78%范圍內(nèi),表明采用RRT 值法可以對目標化合物色譜峰進行準確定位。
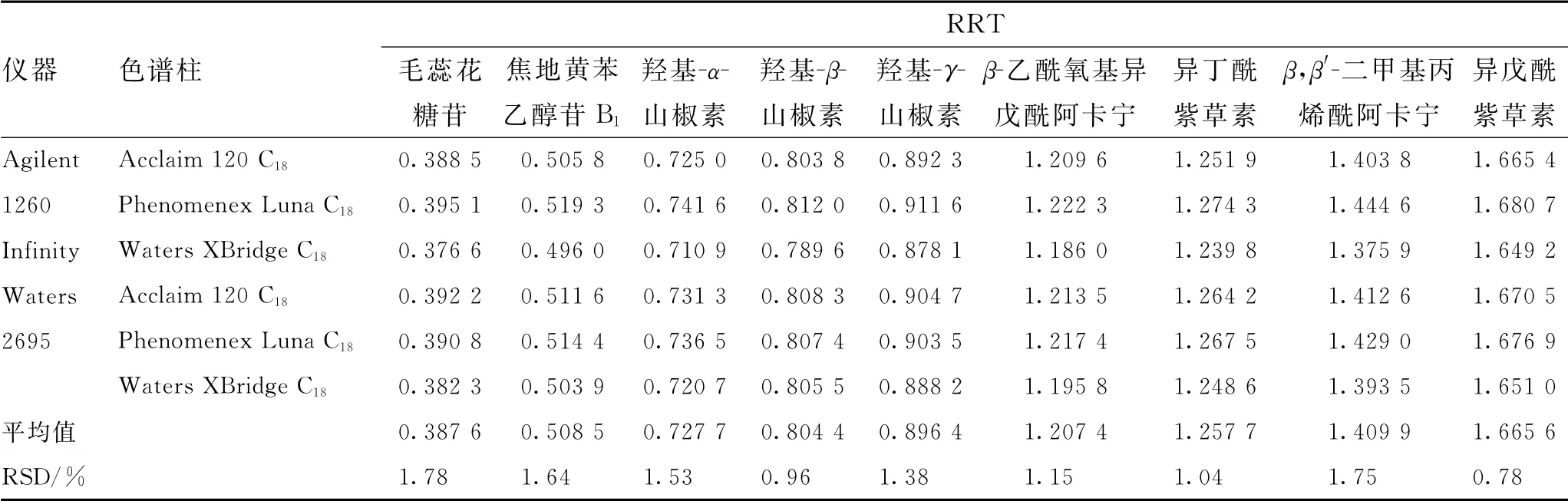
表6 儀器及色譜柱對RRT的影響Tab.6 Effects of instruments and chromatographic columns on RRT
2.6 含量測定
為驗證建立的HPLC-QAMS 法的準確性及可行性,取紫花燒傷軟膏,依法制備供試品溶液并進樣檢測,分別以HPLC-QAMS法和外標法計算各成分的含量,對比2 種方法檢測結(jié)果的差異。結(jié)果見表7。
由表7可知,ESM 和HPLC-QAMS法測得的結(jié)果無顯著差異,表明HPLC-QAMS法可以用于檢測紫花燒傷軟膏中10種成分的含量。
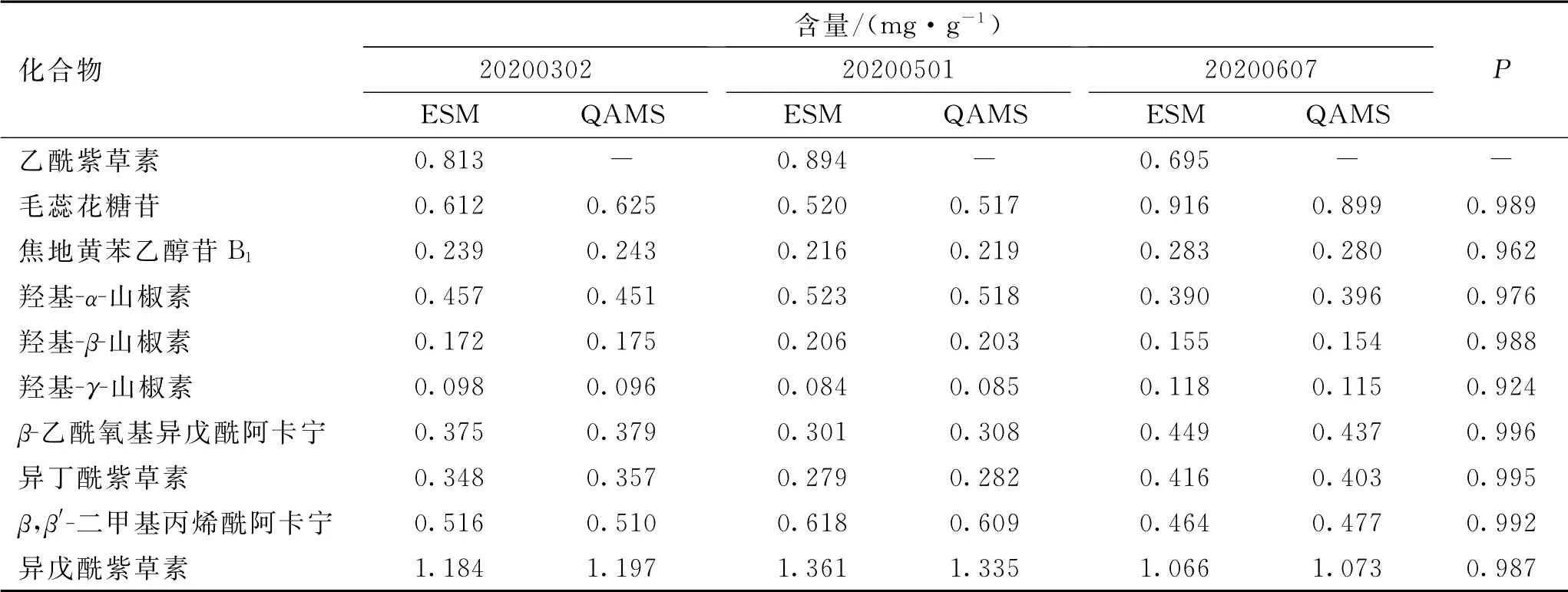
表7 紫花燒傷軟膏中10種成分含量的測定結(jié)果(n=3)Tab.7 Determination results of 10 components in Zihua Burn Ointment(n=3)
3 討論
3.1 指標性成分的選擇
紫花燒傷軟膏由紫草、黃連、地黃、熟地黃、當歸、花椒、冰片和甘草加工而成,處方中紫草具有涼血活血、生肌止痛的功效,黃連具有清熱燥濕的功效,二者合為君藥;生地能夠清熱涼血、瀉火滋陰,熟地能夠填精補髓,與養(yǎng)血活血的當歸共為臣藥;佐藥包括能夠生肌止痛、瀉火的冰片與能夠溫通經(jīng)絡(luò)、止痛止癢的花椒;使藥甘草調(diào)和諸藥、緩急止痛。諸藥合用,清熱涼血、化瘀生肌。為客觀評價紫花燒傷軟膏的內(nèi)在整體質(zhì)量,本實驗以君藥紫草的主要活性成分乙酰紫草素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧和異戊酰紫草素,臣藥生地、熟地的主要代表性成分毛蕊花糖苷和焦地黃苯乙醇苷B1,以及佐藥花椒的主要成分羥基-α-山椒素、羥基-β-山椒素和羥基-γ-山椒素為分析指標,采用HPLCQAMS法測定其含量。
3.2 供試品溶液制備方法的確定
本實驗在確定供試品溶液制備方法時,考察了以體積分數(shù)25%甲醇[10-11]、體積分數(shù)50%甲醇[9]、甲醇[12-14]、體積分數(shù)50%乙醇[16]、石油醚[17-18]為提取溶劑,以超聲和加熱回流方法時10種成分的提取率,結(jié)果顯示,用體積分數(shù)50%甲醇超聲提取時,10種待測成分的響應值較大。繼而以體積分數(shù)50%甲醇為溶劑,考察了提取時間5、10、15、20、40 min對10種成分的含量及雜質(zhì)含量的影響,結(jié)果顯示,提取10 min時,已基本提取完全,故選取體積分數(shù)50%甲醇提取10 min為供試品溶液的制備方法。
3.3 流動相的優(yōu)化篩選
本實驗在優(yōu)化篩選流動相時,分別以乙腈-1 m L·L-1磷酸溶液[9]、乙腈-2 m L·L-1磷酸溶液[12]、乙腈-水[10-11]、甲 醇-水[13]、乙 腈-1 m L·L-1甲 酸 溶液[20]為流動相,按照2.1項下色譜條件進樣檢測供試品溶液,對不同流動相條件下的HPLC 圖進行分析比對,發(fā)現(xiàn)將乙腈-1 m L·L-1磷酸溶液作為流動相時,基線平穩(wěn),峰形較好,各成分響應值大,進而又摸索了有機相與水相的比例,最終確定以2.1項下的色譜條件檢測紫花燒傷軟膏中10種成分的含量。
本實驗以乙酰紫草素作為內(nèi)參物,用HPLCQAMS法對紫花燒傷軟膏中毛蕊花糖苷、焦地黃苯乙醇苷B1、羥基-α-山椒素、羥基-β-山椒素、羥基-γ-山椒素、乙酰紫草素、β-乙酰氧基異戊酰阿卡寧、異丁酰紫草素、β,β′-二甲基丙烯酰阿卡寧和異戊酰紫草素含量進行了檢測分析,考察了RCF 的耐用性,將ESM法與HPLC-QAMS法測定結(jié)果進行了對比,結(jié)果顯示在該色譜條件下RCF具有較好的耐用性,用ESM法與HPLC-QAMS法獲得的結(jié)果間差異無統(tǒng)計學意義,對全面評價紫花燒傷軟膏的質(zhì)量具有重要意義。

