甘草蜜炙前后對小鼠免疫調節的影響△
岳珠珠,姜明瑞,張婧秋,王志成,王慧楠,陳夢雨,魏曉彤,石雙慧,王夢琳,王英姿
北京中醫藥大學 中藥學院,北京 102488
甘草來源于植物烏拉爾甘草Glycyrrhiza uralensisFisch.、脹果甘草G.inflataBat.或光果甘草G.glabraL.的干燥根和根莖,是中醫臨床常用的大宗中藥品種,炙甘草是其常用炮制品,被收載于《中華人民共和國藥典》2020 年版,具有清熱解毒、補中益氣等功效[1]。傳統中醫藥理論認為,甘草蜜炙后補益作用顯著增強。現代研究表明,甘草蜜炙后甘草苷、甘草酸、異甘草素等成分含量發生變化,免疫活性高于生甘草[2-7]。
機體免疫系統由非特異性免疫、體液免疫和細胞免疫三方面組成,能夠識別和清除入侵人體的抗原成分、體內的衰老細胞、凋亡細胞及異常突變細胞等,從而保持機體內環境的相對穩定[8]。目前,蜜炙甘草增強免疫功能的機制尚未清晰,且研究多偏向其中一項,不夠全面。因此,為了更系統地研究蜜炙甘草的免疫功能調節作用,本研究基于課題組前期優化的蜜炙甘草炮制工藝[9],采用環磷酰胺制備小鼠免疫功能低下模型,檢測甘草蜜炙前后對其各類免疫功能相關指標的影響,為其臨床應用提供參考。
1 材料
1.1 實驗動物
無特定病原體(SPF)級BALB/c系小鼠240只,雌雄各半,3~4 周齡,體質量(20±2)g,購于北京斯貝福實驗動物技術有限公司[許可證號:SCXK(京)2019-0010],本研究經北京中醫藥大學倫理委員會審批(編號:BUCM-4-2021112301-4068)。所有動物飼養于北京中醫藥大學動物實驗中心,自由飲水、攝食,實驗過程中嚴格按照實驗動物使用的3R原則給予人道關懷。
1.2 試藥
生甘草飲片由北京華邈藥業有限公司提供(批號為XF1161),經北京中醫藥大學劉春生教授鑒定為豆科植物甘草Glycyrrhiza uralensisFisch.的干燥根和根莖制成的飲片。清炒甘草飲片(不加煉蜜)和蜜炙甘草飲片均按照本課題組前期優化的炮制工藝進行炮制。
環磷酰胺、鹽酸左旋咪唑、綿羊紅細胞(SRBC)、豚鼠血清、都氏試劑、印度墨水、水楊酸緩沖液(SA)、吉姆薩(Giemsa)染色液、乳酸脫氫酶(LDH)基質液、1%雞紅細胞(上海源葉生物科技有限公司,批號分別為X13J11Y115691、Y23M9C56327、H14N11Q131025、H02D11Q133035、H13N11B130941、L17S11G124902、L12N11G130949、R20651、23151、R21234);LDH 細胞毒性檢測試劑盒、CCK-8試劑盒(上海碧云天生物技術有限公司,批號分別為121719200902、E1CK-000208);Hank's液(北京索萊寶科技有限公司,批號:20200921);胎牛血清(杭州四季青公司,批號:110128611);RPMI 1640 完全培養液、臺盼藍染色液(美國Gibco公司,批號分別為1786045、13704);伴刀豆球蛋白A(Con A,美國Sigma公司,批號:C8110);YAC-1細胞(南京科佰生物科技有限公司,批號:CBP60886);1%乙基苯基聚乙二醇(NP-40,上海聯邁生物工程有限公司,批號:LM-0304);2,4-二硝基氟苯[DNFB,薩恩化學技術(上海)有限公司,批號:RXR4 HKE8]。
1.3 儀器
5810R 型高速冷凍離心機(德國Eppendorf 公司);MULTISKAN MK3 型全自動多功能酶標儀、3111 型CO2恒溫細胞培養箱、ECO 型超凈工作臺均購于Thermo Fisher Scientific 公司;756PC 型紫外-可見分光光度計(上海舜宇恒平科學儀器有限公司);M330-HD228S 型光學顯微鏡(深圳市奧斯微光學儀器有限公司)。
2 方法
2.1 樣品的制備
取生甘草飲片、清炒甘草飲片及蜜炙甘草飲片[9]適量,分別加10 倍量的水回流提取3 次,每次1 h,濾過后合并提取液,濃縮至1 g·mL-1(以生藥量計),給藥前用蒸餾水稀釋至所需質量濃度,4 ℃保存備用。
2.2 動物分組與給藥
小鼠適應性喂養7 d 后按體質量隨機分成4 個大組,分別為免疫一組[血清溶血素和抗體生成細胞、遲發型變態反應(DTH)實驗]、免疫二組[淋巴細胞轉化和自然殺傷(NK)細胞活性)]、免疫三組(腹腔巨噬細胞吞噬雞紅細胞)和免疫四組(碳廓清實驗、臟器/體質量比值)[10]。每大組分為6 個小組,即對照組、模型組、陽性藥組和給藥組(生甘草組、清炒甘草組、蜜炙甘草組),每組隨機10 只小鼠。除對照組腹腔注射0.9%氯化鈉溶液外,其余各組連續5 d 腹腔注射環磷酰胺(80 mg·kg-1)構建免疫低下模型;同時對照組、模型組灌胃0.9%氯化鈉溶液,陽性藥組灌胃鹽酸左旋咪唑(40 mg·kg-1),生、清炒、蜜炙甘草組各灌胃1.0 g·kg-1,連續給藥28 d;給藥體積為0.02 mL·g-1。
2.3 檢測指標
根據免疫功能學評價檢驗對小鼠免疫功能進行測定[11],包括淋巴器官/體質量比值測定、血清溶血素測定及抗體生成細胞檢測實驗、脾淋巴細胞轉化實驗、NK 細胞活性測定、DTH 實驗、碳廓清實驗、腹腔巨噬細胞吞噬雞紅細胞實驗。
2.3.1 血清溶血素測定和抗體生成細胞檢測實驗 各組小鼠灌胃至23 d,腹腔注射2%SRBC 懸液0.2 mL進行免疫。5 d后,小鼠稱質量,摘眼球采血于離心管中,做血清溶血素測定;脫頸處死后取脾臟進行抗體生成細胞檢測,計數每1.0×106個脾細胞中溶血空斑數來表示抗體生成水平[12-17]。
血清溶血素測定:離心管靜置約1h后,2000 r·min-1離心10 min(離心半徑為8 cm),取血清備用;小鼠血清用SA 緩沖液稀釋200 倍;吸取1 mL稀釋后血清置試管內,依次加入10%SRBC(用SA緩沖液配制)0.5 mL,豚鼠血清(用SA緩沖液按1∶8稀釋)1 mL。另設不加血清的SA緩沖液為對照管。2000 r·min-1離心10 min(離心半徑為8 cm),取上清液1 mL,加都氏試劑3 mL;同時設半數溶血組,取10% SRBC 0.25 mL,加都氏試劑至4 mL,充分混勻,放置10 min后,于540 nm 處以對照管調零,分別測定各管吸光度(A)。溶血素的量以半數溶血值(HC50)表示,按公式(1)計算。

抗體生成細胞檢測:將小鼠的脾臟在無菌環境下取出,制成細胞懸液,經過200 目的篩網濾過,1000 r·min-1離心10 min(離心半徑為8 cm),采用Hank's 液洗2 遍。表層培養基(1%瓊脂糖)加熱溶解后與等量pH 7.2~7.4 的2 倍濃度Hank's 液混合,分裝于每管0.5 mL,加入脾細胞懸液25 μL、10%SRBC 50 μL,迅速混勻,傾倒于已刷瓊脂糖薄層的玻片上,待瓊脂凝固后,將玻片水平扣放在玻片架上,37 ℃、5%CO2培養箱中溫育1.5 h,然后將SA緩沖液稀釋的補體加入到玻片架凹槽內,繼續溫育1.5 h后,計數溶血空斑數來表示抗體生成水平。
2.3.2 DTH 實驗 第23 天灌胃后,小鼠腹部被毛,面積約3 cm×3 cm,用1% DNFB 溶液50 μL 均勻涂抹致敏,次日再強化重復涂抹1 次,5 d 后用1%DNFB 溶液10 μL 均勻涂抹于小鼠右耳兩面[18-19]。最后一次給藥24 h 后,脫頸處死小鼠,用打孔器取下直徑8 mm 左右耳片稱質量,并計算兩耳質量差值(mg),按公式(2)計算耳腫脹度。

2.3.3 脾淋巴細胞轉化實驗和NK細胞活性測定 末次給藥后,脫頸處死小鼠,無菌環境下取脾,將脾撕碎于盛有適量無菌Hank's 液的平皿中,濾過,制成脾細胞懸液[18,20-22],分為兩部分做如下實驗。
脾淋巴細胞轉化實驗:Hank's液洗滌單細胞懸液2次,每次1000 r·min-1離心10 min(離心半徑為8 cm),后將細胞懸浮于1 mL RPMI 1640 完全培養液中,臺盼藍染色,顯微鏡下活細胞數計數(細胞存活率達95%以上)并調整細胞濃度為3×106個/mL。取96 孔板,對照孔加入上述細胞懸液100 μL,刺激孔加入細胞懸液100 μL 與Con A(終質量濃度為5 μg·mL-1),空白孔加RPMI 1640完全培養液100 μL,設置3個復孔。采用CCK-8 試劑盒說明書檢測小鼠脾淋巴細胞增殖率,使用酶標儀在450 nm下測A。脾淋巴細胞增值率用刺激指數(SI)來表示,按公式(3)計算。

NK細胞活性測定:實驗前24 h將靶細胞YAC-1傳代培養,應用前將Hank's 液洗3 次,調整細胞濃度為4×105個/mL(RPMI 1640完全培養液),Hank's液洗滌脾細胞懸液2 次,每次1000 r·min-1離心10 min(離心半徑為8 cm),調整細胞濃度為2×107個/mL;取靶細胞和效應細胞各100 μL(效靶比50∶1),加入96 孔培養板中,靶細胞自然釋放孔內加入培養液和靶細胞各100 μL、靶細胞最大釋放孔內加入1%NP-40 和靶細胞各100 μL,以上各項均設3 個復孔,于37 ℃、5%CO2培養箱中培養4 h后,1500 r·min-1離心5 min(離心半徑為8 cm),每孔吸取上清液100 μL 置于96 孔培養板中,同時加入LDH 基質液100 μL,反應3 min,加入1 mol·L-1HCl 30 μL,用酶標儀測定490 nm 處A,并計算NK 細胞活性,結果以殺傷率表示,按式(4)計算。

2.3.4 腹腔巨噬細胞吞噬雞紅細胞實驗 各組小鼠灌胃第23天后,給每只小鼠腹腔注射2%SRBC 0.2 mL進行免疫,5 d后脫頸處死小鼠,剪開腹部皮膚暴露腹膜,每只小鼠腹腔注射含5%的胎牛血清的Hank's液4 mL,輕輕按揉腹部,吸取腹腔洗液2 mL 于試管內。吸取腹腔洗液0.5 mL 至裝有0.5 mL 的1%雞紅細胞懸液的離心管,混勻,吸取混合液0.5 mL 至玻片上已晾干的3%瓊脂圈內,37 ℃溫育20 min,甲醇固定,4% Giemsa-磷酸緩沖液染色,顯微鏡觀察計數,每張涂片計數100 個巨噬細胞[18,23],按公式(5)計算吞噬率,公式(6)計算吞噬指數。

2.3.5 碳廓清實驗 末次給藥1 h 后,稱小鼠體質量,以10 mL·kg-1劑量于尾靜脈注入25%印度墨汁,分別于注射后2、10 min從內眥靜脈叢取血30 μL并立即加入到3 mL 0.1%Na2CO3溶液中。Na2CO3溶液作為對照,紫外-可見分光光度計在600 nm 下檢測A[24-25]。采血結束后,將小鼠脫頸處死,剝離肝臟、脾臟,稱質量并分別按式(7)和(8)計算廓清指數(K)和吞噬指數(α)。

式中,K為碳廓清指數(未經矯正的吞噬指數);A1為t1樣品的A;A2為t2樣品的A;t1為注入墨汁后第1次取血時間;t2為注入墨汁后第2次取血時間。
2.3.6 淋巴器官/體質量比值測定 末次給藥后,脫頸處死小鼠并解剖,取出脾臟、胸腺,準確稱質量[26],并按公式(9)和(10)計算脾臟指數和胸腺指數(mg·g-1)。

2.4 統計學方法
采用Excel 2019和SAS 8.2統計軟件對數據進行錄入與統計分析,實驗數據采用()表示,多組間比較采用單因素方差分析(ANOVA),兩組間比較采用t檢驗,P<0.05為差異有統計學意義。
3 結果
3.1 甘草蜜炙前后對免疫低下小鼠血清溶血素和抗體生成細胞的影響
實驗結果見表1,與對照組小鼠比較,模型組小鼠HC50和溶血空斑數均顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠HC50和溶血空斑數均顯著升高(P<0.01);生甘草組小鼠HC50顯著升高(P<0.05),溶血空斑數升高,但差異無統計學意義;清炒甘草組小鼠HC50顯著升高(P<0.01),溶血空斑數顯著升高(P<0.05);蜜炙甘草組小鼠HC50顯著升高(P<0.01),溶血空斑數顯著升高(P<0.05),即清炒甘草組、蜜炙甘草組小鼠的HC50和溶血空斑數均有所升高,且差異均有統計學意義。同時,生甘草組、清炒甘草組小鼠HC50和溶血空斑數差異均有統計學意義(P<0.01),生甘草組、蜜炙甘草組小鼠HC50和溶血空斑數差異均有統計學意義(P<0.01),清炒甘草組、蜜炙甘草組小鼠HC50和溶血空斑數差異無統計學意義。
表1 不同炮制方法對免疫低下小鼠HC50及溶血空斑數的影響(, n=10)

表1 不同炮制方法對免疫低下小鼠HC50及溶血空斑數的影響(, n=10)
注:與對照組比較,*P<0.05,**P<0.01;與模型組比較,#P<0.05,##P<0.01;與生甘草組比較,▲P<0.05,▲▲P<0.01;與清炒甘草組比較,ΔP<0.05,ΔΔP<0.01;表2~6同。
3.2 甘草蜜炙前后對免疫低下小鼠DTH的影響
實驗結果見表2,與對照組小鼠比較,模型組小鼠耳腫脹度顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠耳腫脹度顯著升高(P<0.01);生甘草組小鼠耳腫脹度顯著升高(P<0.05);清炒甘草組小鼠耳腫脹度顯著升高(P<0.01);蜜炙甘草組小鼠耳腫脹度顯著升高(P<0.01),即生甘草組、清炒甘草組、蜜炙甘草組小鼠的耳腫脹度均有升高,且差異均有統計學意義。同時,生甘草組、清炒甘草組小鼠耳腫脹度的差異無統計學意義,生甘草組、蜜炙甘草組小鼠耳腫脹度的差異有統計學意義(P<0.01),清炒甘草組、蜜炙甘草組小鼠耳腫脹度的差異均有統計學意義(P<0.01)。
表2 不同炮制方法對免疫低下小鼠DTH的影響(, n=10)mg

表2 不同炮制方法對免疫低下小鼠DTH的影響(, n=10)mg
3.3 甘草蜜炙前后對免疫低下小鼠脾淋巴細胞增殖率和NK細胞活性的影響
實驗結果見表3,與對照組小鼠比較,模型組小鼠SI、殺傷率均顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠SI 顯著升高(P<0.05)、殺傷率顯著升高(P<0.01);生甘草組小鼠SI、殺傷率均升高,但差異無統計學意義;清炒甘草組小鼠SI 升高,但差異無統計學意義,殺傷率顯著升高(P<0.01);蜜炙甘草組小鼠SI、殺傷率均顯著升高(P<0.01)。同時,生甘草組、清炒甘草組小鼠SI差異有統計學意義(P<0.05),殺傷率差異有統計學意義(P<0.01);生甘草組、蜜炙甘草組小鼠SI、殺傷率差異均有統計學意義(P<0.01),清炒甘草組、蜜炙甘草組小鼠SI、殺傷率差異均有統計學意義(P<0.01)。
表3 不同炮制方法對免疫低下小鼠脾淋巴細胞增殖率和NK細胞活性的影響(, n=10)

表3 不同炮制方法對免疫低下小鼠脾淋巴細胞增殖率和NK細胞活性的影響(, n=10)
3.4 甘草蜜炙前后對免疫低下小鼠腹腔巨噬細胞吞噬功能的影響
實驗結果見表4,與對照組小鼠比較,模型組小鼠吞噬率、吞噬指數均顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠吞噬率、吞噬指數均顯著升高(P<0.01);各給藥組小鼠吞噬率、吞噬指數均顯著升高(P<0.01),即生甘草組、清炒甘草組、蜜炙甘草組小鼠巨噬細胞吞噬功能均有升高,且差異均有統計學意義。同時,生甘草組、清炒甘草組小鼠吞噬率、吞噬指數差異均無統計學意義;生甘草組、蜜炙甘草組小鼠吞噬率差異均有統計學意義(P<0.05),吞噬指數差異有統計學意義(P<0.01);清炒甘草組、蜜炙甘草組小鼠吞噬率差異無統計學意義,吞噬指數差異有統計學意義(P<0.05)。
表4 不同炮制方法對免疫低下小鼠腹腔巨噬細胞吞噬功能的影響(, n=10)

表4 不同炮制方法對免疫低下小鼠腹腔巨噬細胞吞噬功能的影響(, n=10)
3.5 甘草蜜炙前后對免疫低下小鼠碳廓清功能的影響
實驗結果見表5,與對照組小鼠比較,模型組小鼠K、α均顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠K、α均顯著升高(P<0.05);生甘草組小鼠K升高,但差異無統計學意義,α顯著升高(P<0.05);清炒甘草組和蜜炙甘草組小鼠K、α均顯著升高(P<0.01)。同時,生甘草組、清炒甘草組小鼠K、α之間的差異均無統計學意義;生甘草組、蜜炙甘草組小鼠K、α之間的差異均有統計學意義(P<0.01),清炒甘草、蜜炙甘草組小鼠K的差異有統計學意義(P<0.05),α之間的差異有統計學意義(P<0.01)。
表5 不同炮制方法對免疫低下小鼠碳廓清功能的影響(, n=10)
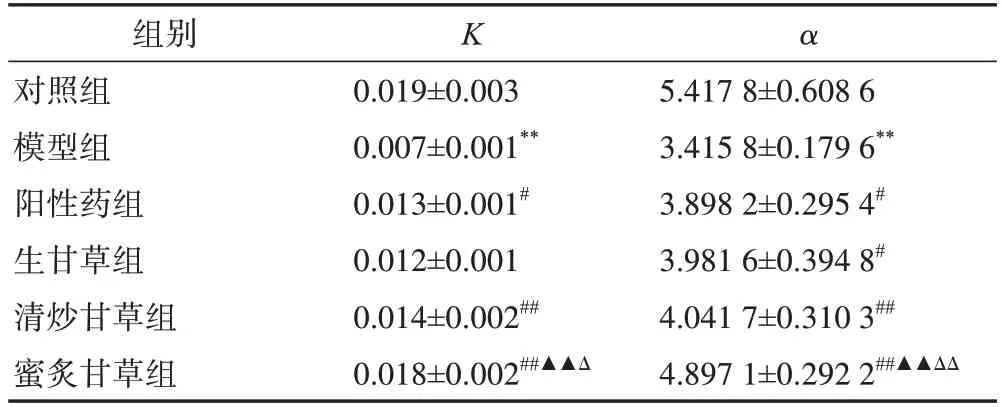
表5 不同炮制方法對免疫低下小鼠碳廓清功能的影響(, n=10)
3.6 甘草蜜炙前后對免疫低下小鼠胸腺指數、脾臟指數的影響
實驗結果見表6,與對照組小鼠比較,模型組小鼠胸腺指數、脾臟指數均顯著降低(P<0.01)。與模型組小鼠比較,陽性藥組小鼠胸腺指數顯著升高(P<0.01),脾臟指數顯著升高(P<0.05);生甘草組小鼠胸腺指數顯著升高(P<0.05),脾臟指數升高,但差異無統計學意義;清炒甘草組小鼠胸腺指數顯著升高(P<0.01),脾臟指數顯著升高(P<0.05);蜜炙甘草組小鼠胸腺指數、脾臟指數均顯著升高(P<0.01)。同時,生、清炒甘草組小鼠胸腺指數、脾臟指數之間差異均無統計學意義,生、蜜炙甘草組小鼠胸腺指數差異無統計學意義,脾臟指數之間差異有統計學意義(P<0.05),清炒、蜜炙甘草組小鼠胸腺指數差異有統計學意義(P<0.05),脾臟指數之間差異無統計學意義。
表6 不同炮制方法對免疫低下小鼠胸腺指數、脾臟指數的影響(, n=10)mg·g-1

表6 不同炮制方法對免疫低下小鼠胸腺指數、脾臟指數的影響(, n=10)mg·g-1
4 討論
脾臟及胸腺是動物體中重要的免疫器官,胸腺指數、脾臟指數可以從整體上評價小鼠體內的免疫功能,反映臟器組織的狀態和功能[27-28];單核巨噬細胞為一種機體非特異性免疫的重要細胞,其吞噬能力是可用于判斷機體非特異性免疫功能,而巨噬細胞的K反映其吞噬功能[29];采用SRBC對小鼠進行免疫,能夠刺激小鼠B 細胞產生抗體,測定免疫后的小鼠血清對SRBC 的溶解能力,反映了抗體分泌細胞分泌抗體的能力,屬于體液免疫應答功能[23];ConA 誘導脾淋巴細胞增殖實驗可以評價T 細胞介導的細胞免疫功能[30];DTH 是抗原誘導機體發生的細胞性免疫應答,特異性抗原在抗原提呈細胞(APC)作用下與致敏T 細胞再次接觸后,使T 細胞活化增殖并分化成為效應T 細胞,效應T 細胞進一步清除抗原,引起局部組織發生炎癥反應[21]。
楊青等[31]通過比較甘草蜜炙前后對小鼠脾淋巴細胞增殖的作用發現甘草蜜炙后相比甘草生品能顯著增加小鼠的免疫功能,并分析得出蜜炙后甘草免疫功能增強與甘草經蜜炙后成分發生的改變、新產生的成分及原有成分含量的變化密切相關。張恒斌等[32]通過甘草生制品與小鼠脾細胞免疫活性增殖實驗發現甘草蜜炙后免疫活性增強且其水提物的免疫活性強于醇提物,并推測甘草免疫活性成分主要為多糖類成分。
本研究通過非特異性免疫、體液免疫、細胞免疫進一步全面探究甘草蜜炙前后對小鼠免疫調節作用的影響,結果表明,同等劑量下,生甘草、清炒甘草、蜜炙甘草均能一定程度上提高免疫低下小鼠的免疫功能,且蜜炙甘草組各指標均有顯著提升,說明蜜炙甘草免疫調節作用優于生甘草和清炒甘草。根據已有文獻報道[33-35],甘草蜜炙后以甘草苷為代表的二氫黃酮類成分含量總體呈下降趨勢,以甘草酸為代表的三萜類成分含量呈下降趨勢,以異甘草素為代表的查耳酮類成分含量呈上升趨勢,與本團隊前期研究結果一致,故推測清炒加熱能使苷類成分的乙酰化產物含量增多,苷元含量降低,苷的含量升高;而蜜炙中蜂蜜對苷的乙酰化具有抑制作用,蜜炙甘草中甘草苷的含量低于生甘草、清炒甘草;而甘草中以甘草酸為代表的三萜類成分發生苷鍵斷裂,不斷生成次級苷及苷元,因此蜜炙后甘草中甘草酸含量有所下降,甘草次酸、異甘草素的含量相對升高;另外,甘草中含有多糖類組分,輔料蜂蜜中含有果糖、葡萄糖等成分,甘草蜜炙后糖類含量升高。綜上,甘草蜜炙免疫調節作用增強,與甘草蜜炙后成分含量、結構的改變及新成分的生成等有密切關聯,后期將對甘草蜜炙后有效成分的變化進行深入探究,為進一步闡明甘草蜜炙后免疫調節作用增強的炮制機制提供參考。

