金線吊烏龜提取物的抗炎鎮痛抗氧化和抑制亞硝化活性研究△
張超,鄒賀康,翟明,莊遠杯,丘波,吳家華,張聲源,羅曉東*
1.嘉應學院 廣東省山區特色農業資源保護與精準利用重點實驗室,廣東 梅州 514015;2.嘉應學院 醫學院 客家藥用生物資源研究所,廣東 梅州 514031;3.嘉應學院 醫學院,廣東 梅州 514031
金線吊烏龜Stephania cepharanthaHayata 為防己科千金藤屬植物,又名頭花千金藤、白藥子,主產于廣西、貴州、云南等地,《中華本草》記載其有清熱解毒、涼血止血、消腫散結的功效,主治咽喉腫痛、熱毒癰腫、風濕痹痛,在民間廣泛用于治療咽喉腫痛、風濕痹痛和腮腺炎等疾病[1-3]。現代藥理學研究表明,千金藤屬植物提取的生物堿千金藤素(cepharanthine,CEP)具有抗炎、清除自由基、抗腫瘤、抑制人類免疫缺陷病毒-1(HIV-1)和免疫調節等生物活性[4-5]。目前,國內外關于金線吊烏龜的研究主要集中于生物堿、黃酮、蒽醌、甾醇和糖類等化學成分和提取方法[6-8],其藥理學相關研究較少。
從民間應用和前人研究基礎出發,為全面評價金線吊烏龜不同提取部位在抗炎、鎮痛、抗氧化及抑制亞硝化的活性差異,本研究以金線吊烏龜的石油醚提取物、乙酸乙酯提取物、正丁醇提取物和水提取物4 個不同極性部位為研究對象,采用二甲苯致小鼠耳廓腫脹法、醋酸扭體法和熱板法評價抗炎、鎮痛活性;采用1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除法和2,2-聯氮基-雙-(3-乙基苯并噻唑啉-6-磺酸)二銨鹽(ABTS)自由基清除法測定抗氧化活性;模擬人體胃酸條件(pH 3.0,溫度37 ℃),采用鹽酸萘乙二胺法和α-萘胺法測定抑制亞硝化活性,以期為金線吊烏龜的制劑開發和臨床應用提供參考。
1 材料
1.1 藥材
金線吊烏龜購于梅州市梅江區藥材市場,經嘉應學院醫學院客家藥用生物資源研究所張聲源副教授鑒定為防幾科千金藤屬多年生藤本植物金線吊烏龜Stephania cepharanthaHayata的塊根。
1.2 動物
無特定病原體(SPF)級昆明種小鼠雄性60 只、雌性150 只,體質量(20±2)g,由南方醫科大學實驗動物管理中心提供,合格證號為44002100026062,實驗動物使用許可證號為SCXK(粵)2021-0041。實驗期間小鼠飼養于嘉應學院醫學院實驗動物房,溫度20~26 ℃,相對濕度40%~70%,自由進食、飲水。
1.3 試藥
雙氯芬酸鈉腸溶片(北京諾華制藥有限公司,批號:X1283);羅通定片(上海金不換蘭考制藥有限公司,批號:H41023917);維生素C(VitC,西隴科學有限公司);DPPH、ABTS(美國Sigma 公司,批號分別為STBB0829V、K1517067);亞硝酸鈉、對氨基苯磺酸、鹽酸萘乙二胺、二甲胺、1-萘胺、過硫酸鉀、無水檸檬酸、磷酸二氫鈉、磷酸氫二鈉、碳酸鈉(上海阿拉丁生化科技股份有限公司);二甲苯(天津市科密歐化學試劑有限公司);乙酸(天津市大茂化學試劑廠);無水乙醇(天津市富宇精細化工有限公司);0.9%氯化鈉注射液(四川科倫藥業股份有限公司);其余試劑均為分析純。
1.4 儀器
RB-200 型智能熱板儀(成都泰盟軟件有限公司);Spark 型酶標儀(瑞士Tecan 公司);UV-1800型紫外-可見分光光度計(日本島津公司)。
2 方法
2.1 金線吊烏龜不同溶劑提取物的制備
金線吊烏龜2.0 kg 干燥后粉碎,用3 倍量95%乙醇加熱回流提取3 次,每次30 min,合并提取液,減壓濃縮得總浸膏225 g(得率11.25%)。取總浸膏200 g 分散于蒸餾水中,依次加入石油醚、乙酸乙酯、正丁醇進行萃取,減壓回收溶劑,得石油醚提取物46 g(得率2.59%)、乙酸乙酯提取物12 g(得率0.67%)、正丁醇提取物59 g(得率3.32%)、水提取物83 g(得率4.67%)。
2.2 抗炎、鎮痛活性考察
2.2.1 二甲苯致小鼠耳廓腫脹法 SPF 級昆明種小鼠60 只,雌雄各半,隨機分為6 組,每組10 只,分別為空白組(0.9%氯化鈉溶液)、陽性組(雙氯芬酸鈉)及4個實驗組(石油醚提取物、乙酸乙酯提取物、正丁醇提取物、水提取物)。陽性組小鼠按照0.01 g·kg-1灌胃雙氯芬酸鈉溶液,經前期開展的預實驗毒性驗證,4個實驗組小鼠灌胃劑量為3 g·kg-1,空白組小鼠灌胃等體積0.9%氯化鈉溶液。連續給藥5 d,末次給藥1 h 后,于小鼠右耳兩面各涂二甲苯10 μL 激發炎癥致腫。4 h 后頸椎脫臼處死,用打孔器沿右耳廓打一直徑為5 mm的圓片,左耳相同部位打孔作對照,分析天平稱質量記錄,根據公式(1)、(2)計算各組腫脹度及腫脹抑制率。

2.2.2 醋酸扭體法 實驗小鼠分組及給藥同2.2.1項下方法。連續給藥5 d,末次給藥1 h后,按0.02 mL·g-1于小鼠腹腔注射0.6%乙酸溶液致痛,記錄注射乙酸后20 min 內小鼠扭體反應(腹部和后肢因疼痛刺激而伸長)次數,并按公式(3)計算扭體反應抑制率。

2.2.3 熱板法 將智能熱板儀調至55 ℃,記錄小鼠開始舔后足的時間,篩選5~30 s 舔后足的雌性昆明種SPF 級小鼠60 只,0.5 h 后再測定1 次,取兩次舔后足的平均時間作為該小鼠的基礎痛閾。分組同2.2.1 項下方法,陽性組小鼠按照0.1 g·kg-1灌胃羅通定溶液,其他組給藥方式不變。連續給藥5 d,末次給藥后的第1、2 小時分別記錄小鼠舔后足的時間作為給藥后的痛閾,并根據公式(4)計算痛閾提高百分率。在熱板上持續60 s 仍無舔足動作的小鼠痛閾按60 s記錄。

2.3 抗氧化活性測定
2.3.1 DPPH 法 以適量無水乙醇充分溶解各實驗組樣品至0.40 mg·mL-1,溶解VitC至0.04 mg·mL-1,逐級稀釋至0.5倍,共5個質量濃度,分別精密吸取不同質量濃度的樣品溶液和VitC 溶液各80 μL 于96孔板中,各加入0.15 mmol·mL-1DPPH 無水乙醇溶液150 μL,混合后避光靜置5 min,在酶標儀517 nm波長處測定各孔的吸光度(A),每個樣品平行操作3 次,根據公式(5)計算各樣品對DPPH 自由基的清除率。以質量濃度為橫坐標(X)、清除率為縱坐標(Y)進行回歸分析,計算半數抑制濃度(IC50),IC50越小,其活性越強。
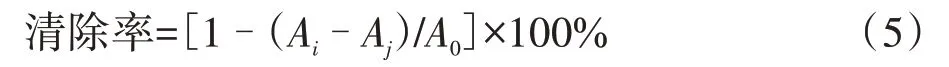
式中Ai為樣品反應體系的吸光度,Aj為對照反應體系的吸光度,A0為空白反應的吸光度。
2.3.2 ABTS法蒸餾水配制7.0 mmol·mL-1的ABTS 溶液與2.45 mmol·mL-1過硫酸鉀溶液等體積混合后,室溫避光靜置12~16 h,制備ABTS母液。分別取10 mmol·L-1磷酸二氫鈉溶液和磷酸氫二鈉溶液19、81 mL,混勻,制備pH 7.4 的磷酸緩沖溶液。用pH 7.4 磷酸緩沖溶液調節ABTS 母液在734 nm 處A為0.70±0.02,即得ABTS 工作液。以無水乙醇充分溶解各組實驗樣品至質量濃度為0.16 mg·mL-1,逐級稀釋至0.5倍,共5個質量濃度;無水乙醇充分溶解VitC 至質量濃度分別為0.01、0.02、0.03、0.04、0.05 mg·mL-1。分別精密吸取不同質量濃度的樣品溶液和VitC溶液各50 μL于96 孔板中,加入ABTS工作液200 μL,混合后避光靜置5 min,在酶標儀734 nm處測定各孔的A,每個樣品平行操作3次。根據公式(5)計算各樣品對ABTS自由基的清除率和IC50。
2.4 抑制亞硝化活性測定
2.4.1 鹽酸萘乙二胺法 分別取0.10 mol·L-1檸檬酸溶液198.63 mL 和0.20 mol·L-1磷酸氫二鈉溶液51.37 mL,混勻,制備pH 3.0 的檸檬酸-磷酸氫二鈉緩沖溶液。以無水乙醇充分溶解各組實驗樣品至質量濃度為20.00 mg·mL-1,逐級稀釋至0.5倍,共5 個質量濃度;無水乙醇充分溶解VitC 至質量濃度分別為1.00、2.00、4.00、6.00、8.00 mg·mL-1。分別精密吸取不同質量濃度的樣品溶液和VitC 溶液1.0 mL 于25 mL 具塞比色管中,依次加入pH 3.0 的檸檬酸-磷酸氫二鈉緩沖液2.0 mL,5 μg·mL-1亞硝酸鈉溶液2.0 mL,充分混勻后37 ℃恒溫反應1 h,加入0.4%對氨基苯磺酸2.0 mL,混勻,靜置5 min后,加入0.2%鹽酸萘乙二胺溶液1.0 mL,定容至刻度,靜置15 min后在紫外-可見分光光度計538 nm處測定A,每個樣品平行操作3 次。根據公式(5)計算各樣品對亞硝酸鹽的清除率和IC50。
2.4.2α-萘胺法 以無水乙醇充分溶解樣品各實驗組樣品溶液至質量濃度分別為4.00、8.00、12.00、16.00、20.00 mg·mL-1,溶解VitC 至質量濃度分別為4.00、8.00、12.00、16.00、20.00 mg·mL-1。分別精密吸取不同質量濃度的樣品溶液和VitC 溶液1.0 mL 于25 mL具塞比色管中,依次加入pH 3.0的檸檬酸-磷酸氫二鈉緩沖液10.0 mL、1 mmoL·L-1亞硝酸鈉溶液1.0 mL、1 mol·L-1的二甲胺溶液1.0 mL,定容至刻度,37 ℃恒溫反應1 h。精密移取反應液1.0 mL 至培養皿,加入0.5%碳酸鈉溶液0.5 mL,紫外燈(254 nm)下反應15 min 后依次加入1%對氨基苯磺酸1.5 mL、0.1%1-萘胺1.5 mL、蒸餾水0.5 mL,靜置15 min后在紫外-可見分光光度計525 nm 處測定A,每個樣品平行操作3 次。根據公式(6)計算各樣品對亞硝胺合成的阻斷率和IC50。
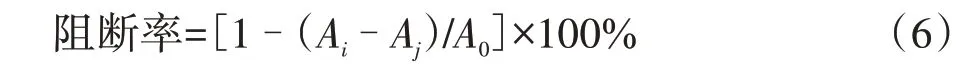
式中Ai為樣品反應體系的吸光度,Aj為對照反應體系的吸光度,A0為空白反應的吸光度。
2.5 數據統計分析
采用SPSS 25.0 和Origin 8.5 軟件對數據進行統計學分析,結果以()表示。采用單因素方差分析進行組間比較,P<0.05表示差異有統計學意義。
3 結果
3.1 金線吊烏龜不同提取物的抗炎、鎮痛活性
3.1.1 小鼠耳廓腫脹度測定結果 各組小鼠耳廓腫脹度及腫脹抑制率見表1。與空白組比較,除乙酸乙酯提取物外,金線吊烏龜各提取部位均能顯著抑制二甲苯引起的小鼠耳廓腫脹(P<0.05),其抑制能力大小依次為水提取物>正丁醇提取物>石油醚提取物>乙酸乙酯提取物。其中水提取物對小鼠耳廓腫脹抑制率高達36.57%,具有較好的抗炎活性。
表1 金線吊烏龜不同提取部位對二甲苯致小鼠耳廓腫脹的影響(, n=10)
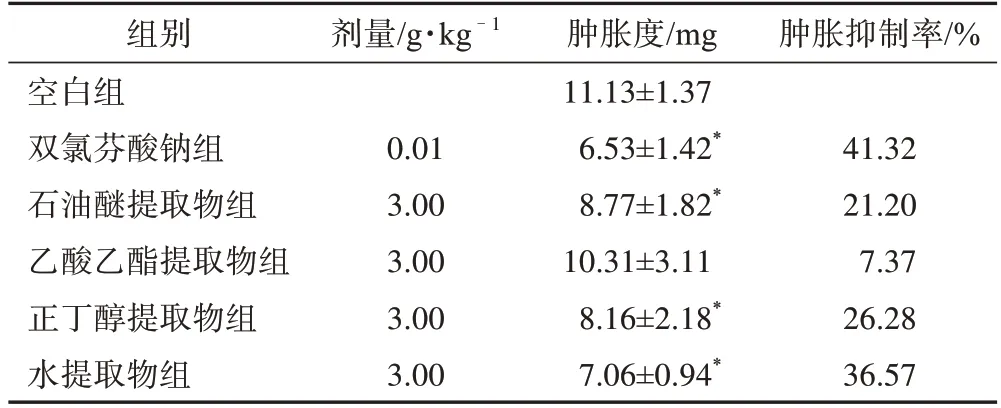
表1 金線吊烏龜不同提取部位對二甲苯致小鼠耳廓腫脹的影響(, n=10)
注:與空白組比較,*P<0.05;表2~3同。
3.1.2 小鼠扭體次數測定結果 各組小鼠扭體次數測定結果見表2。與空白組比較,金線吊烏龜的水提取物和石油醚提取物均能顯著抑制醋酸引起的小鼠扭體反應(P<0.05),而乙酸乙酯和正丁醇作用不明顯。其中,水提取物對小鼠扭體反應的抑制率較高,達到49.14%,優于其他3 個提取部位,顯示出較好的外周鎮痛作用。
表2 金線吊烏龜不同提取部位對醋酸致小鼠扭體反應的影響(, n=10)
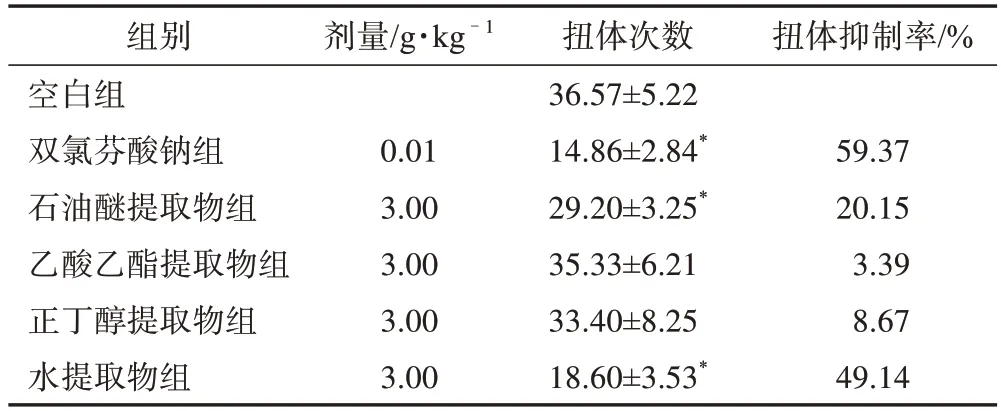
表2 金線吊烏龜不同提取部位對醋酸致小鼠扭體反應的影響(, n=10)
3.1.3 小鼠痛閾測定結果 各組小鼠痛閾測定結果見表3。與空白組比較,金線吊烏龜各提取部位均能提高小鼠對熱板的痛閾,在給藥后1、2 h 都有不同程度的提高(P<0.05)。其中,水提取物給藥后1 h對小鼠痛閾的提高百分率為47.40%,2 h 提高百分率67.35%,且均優于其他3 個提取部位,顯示出較好的中樞鎮痛作用。
表3 金線吊烏龜不同提取部位對小鼠的痛閾提高率(, n=10)
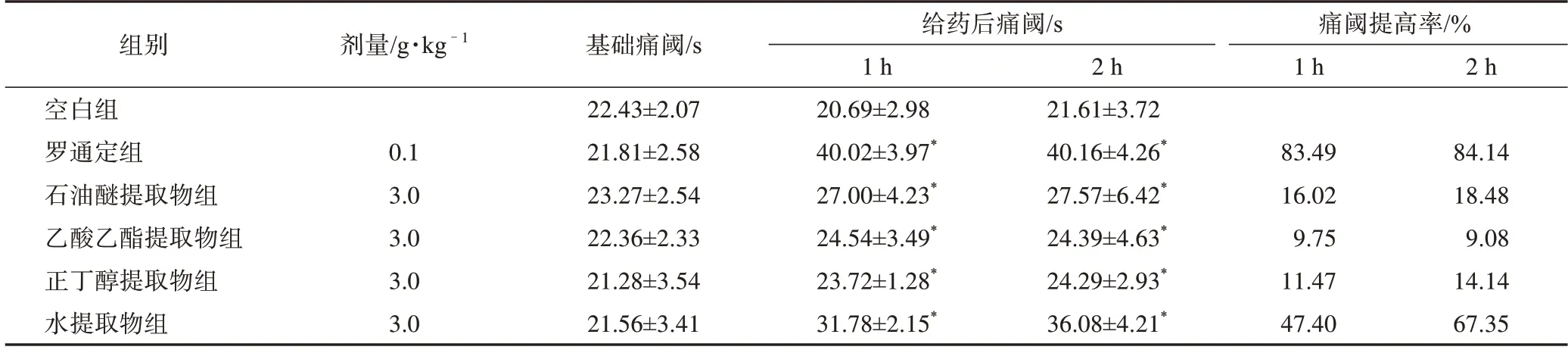
表3 金線吊烏龜不同提取部位對小鼠的痛閾提高率(, n=10)
3.2 金線吊烏龜不同提取物的抗氧化活性
3.2.1 DPPH 自由基清除結果 各提取部位對DPPH 自由基的清除率測定結果及IC50見圖1、表4。在實驗質量濃度范圍內,金線吊烏龜各提取部位對DPPH 自由基均有不同程度的清除作用,呈現量效關系,清除能力大小依次為乙酸乙酯提取物>正丁醇提取物>石油醚提取物>水提取物。當質量濃度為0.4 mg·mL-1時,乙酸乙酯提取物對DPPH自由基的清除率高達93.78%,且乙酸乙酯提取物清除作用的IC50值最低,為(0.084±0.008)mg·mL-1,表明乙酸乙酯提取物對DPPH自由基的清除能力最強,且與其他3個提取部位之間差異有統計學意義(P<0.05)。
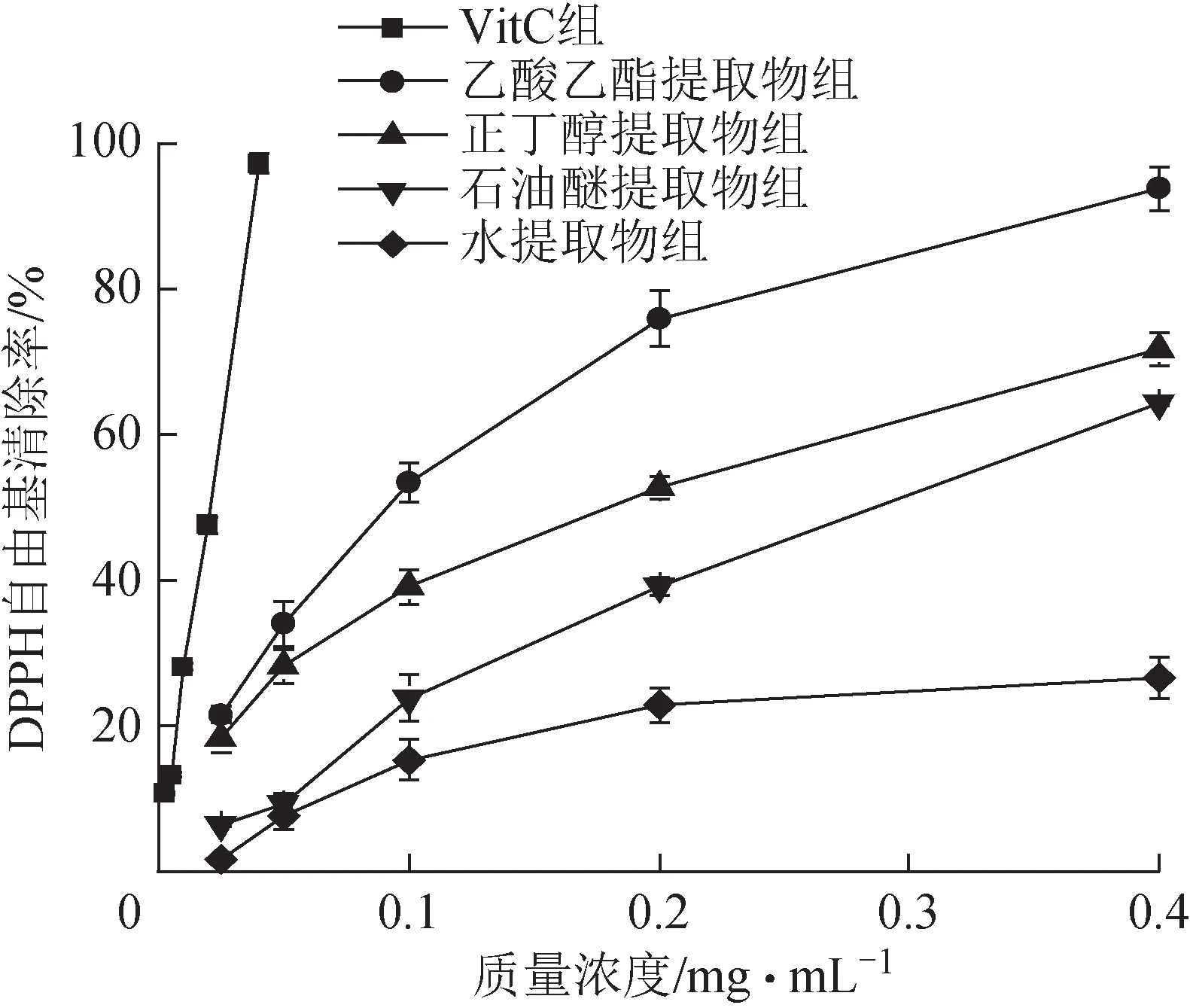
圖1 金線吊烏龜不同提取部位對DPPH自由基的清除能力(, n=3)
3.2.2 ABTS 自由基清除結果 各提取部位對ABTS 自由基的清除率測定結果及IC50見圖2、表4。在實驗質量濃度范圍內,金線吊烏龜各提取部位對ABTS 自由基均有不同程度的清除作用,呈一定的量效關系,清除能力大小依次為乙酸乙酯提取物>正丁醇提取物>石油醚提取物>水提取物。乙酸乙酯提取物清除作用的IC50最低,為(0.063±0.005)mg·mL-1,表明金線吊烏龜的乙酸乙酯提取物對ABTS 自由基的清除能力最強,與其他3 個提取部位之間差異有統計學意義(P<0.05)。
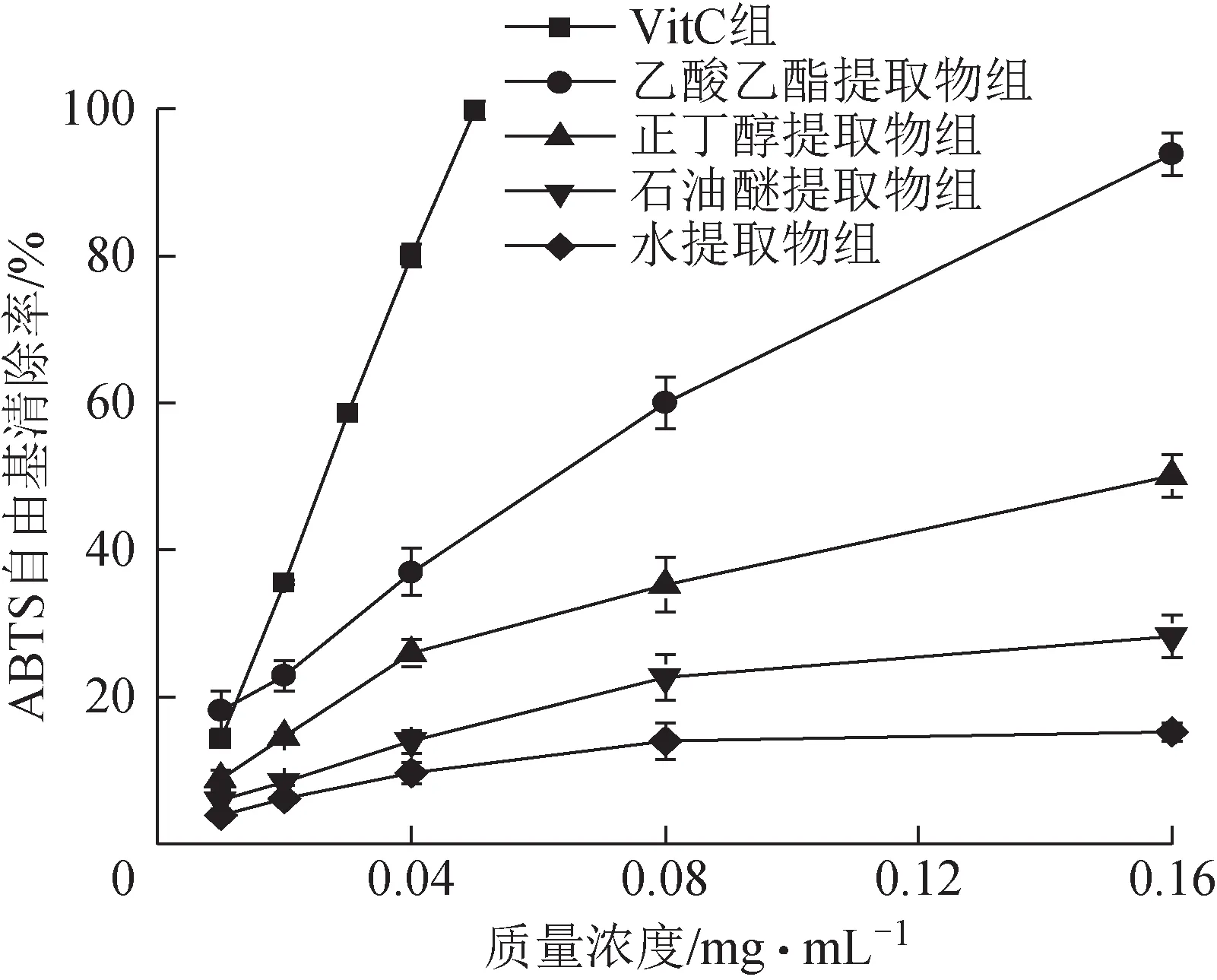
圖2 金線吊烏龜不同提取部位對ABTS自由基的清除能力(, n=3)
表4 金線吊烏龜不同提取部位抗氧化活性的IC50(, n=3)mg·mL-1
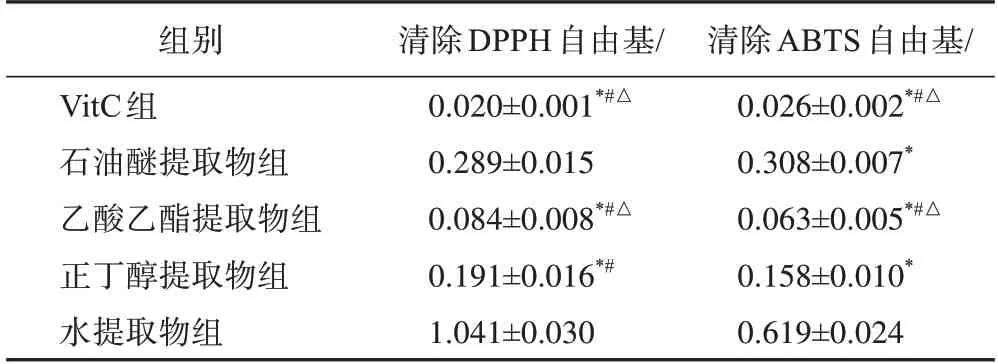
表4 金線吊烏龜不同提取部位抗氧化活性的IC50(, n=3)mg·mL-1
注:與水提取物比較,*P<0.05;與石油醚提取物比較,#P<0.05;與正丁醇提取物比較,△P<0.05。
3.3 金線吊烏龜不同提取物的抑制亞硝化活性
3.3.1 亞硝酸鹽清除結果 各提取部位對亞硝酸鹽的清除率測定結果及IC50見圖3、表5。在實驗質量濃度范圍內,金線吊烏龜各提取部位對亞硝酸鹽均具有不同程度的清除作用,有較好的量效關系,清除能力大小依次為水提取物>乙酸乙酯提取物>正丁醇提取物>石油醚提取物。當水提取物質量濃度為20 mg·mL-1時對亞硝酸鹽的清除率達到97.39%,且水提取物清除作用的IC50值最低(4.35±0.15)mg·mL-1,表明水提取物對亞硝酸鹽的清除能力最強,與其他3個提取部位之間的差異有統計學意義(P<0.05)。
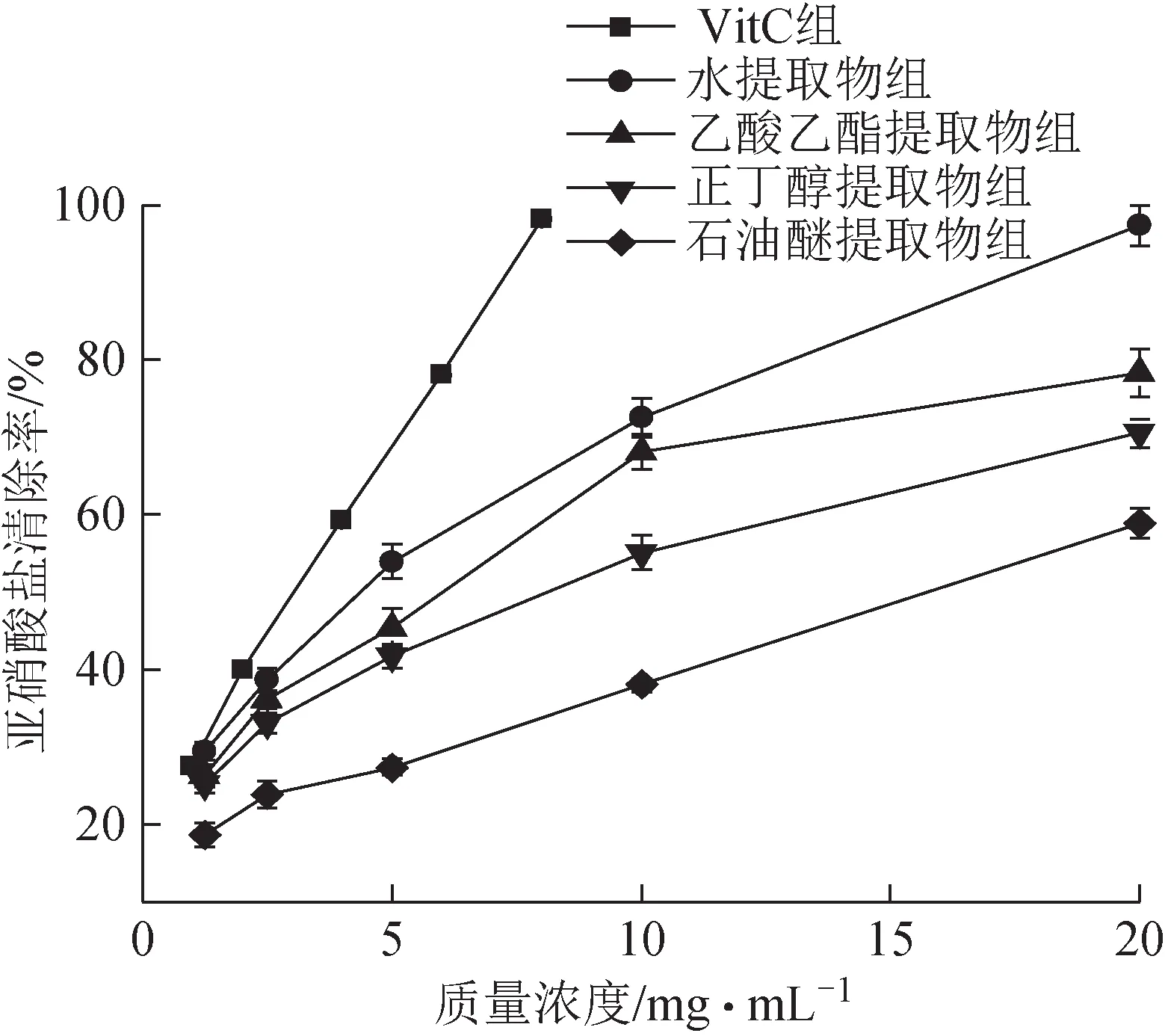
圖3 金線吊烏龜各提取部位對亞硝酸鹽的清除能力(, n=3)
3.3.2 亞硝胺合成的阻斷結果 各提取部位對亞硝胺合成的阻斷率測定結果及IC50見表5、圖4。在實驗質量濃度范圍內,金線吊烏龜各提取部位對亞硝胺的合成均有一定的阻斷作用,阻斷能力隨質量濃度的增加而增強,阻斷率大小依次為水提取物>乙酸乙酯提取物>正丁醇提取物>石油醚提取物。且水提取物阻斷作用的IC50值最低,為(11.08±0.27)mg·mL-1,表明水提取物對亞硝胺合成的阻斷能力最強,與其他3 個提取部位之間差異有統計學意義(P<0.05)。此外,隨著質量濃度的升高,水提取物阻斷亞硝胺的能力會優于同等質量濃度的陽性對照VitC。
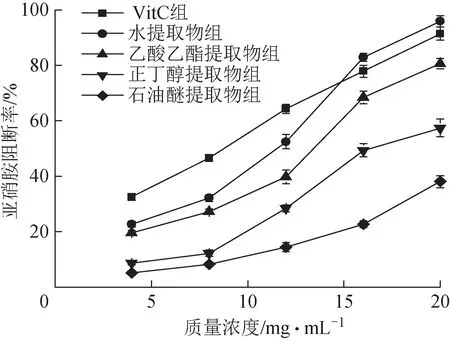
圖4 金線吊烏龜不同提取部位對亞硝胺合成的阻斷能力(, n=3)
表5 金線吊烏龜各提取部位抑制亞硝化活性的IC50(, n=3)mg·mL-1

表5 金線吊烏龜各提取部位抑制亞硝化活性的IC50(, n=3)mg·mL-1
注:與石油醚提取物比較,*P<0.05;與正丁醇提取物比較,#P<0.05;與乙酸乙酯提取物比較,△P<0.05。
4 結論與討論
研究表明,人體內環境穩態被打破是導致各種癌癥的危險因素,如炎癥是諸多癌癥的發病基礎,自由基增多使活性氧的濃度增加,在癌癥的發展中同樣起促進作用。此外,長期攝入N-亞硝基化合物及自身代謝產生的內源性N-亞硝基化合物是食管癌、肝癌和鼻咽癌高發的重要因素。因此,癌癥與炎癥、自由基及N-亞硝基化合物這三者之間存在一定關聯性[9-10]。目前,對于金線吊烏龜的研究多以化學成分研究為主,對其藥效學報道較少,故本研究開展了基于抗炎、鎮痛、抗氧化和抑制亞硝化3 種藥效的金線吊烏龜不同提取部位的篩選研究,旨在對各提取部位進行精準、系統分析,從而明確各極性部位的藥理活性,并為其藥效物質的分離純化提供實驗基礎。
疼痛作為生命的第五大體征,其產生的主要原因是組織損傷引起的炎癥[11]。吲哚美辛、布洛芬和雙氯芬酸鈉等非甾體類藥物,抗炎、鎮痛的同時也存在影響血小板聚集和消化道損傷等嚴重不良反應,延緩患者康復且增加醫護人員的負擔[12-13]。因此,在天然藥物中尋找和開發強效、低廉且不良反應少的新型抗炎鎮痛藥已成為新的研究趨勢。本研究通過二甲苯致小鼠耳廓腫脹反應制備急性炎癥模型,考察藥物抗炎活性;采用醋酸扭體法考察藥物外周鎮痛活性,熱板法考察藥物中樞鎮痛活性。結果表明,金線吊烏龜4 個提取部位均有不同程度的抗炎、鎮痛活性,其中水提取物的作用效果最顯著,說明金線吊烏龜抗炎、鎮痛活性物質富集于極性較大的水提取物,這可能與其富含多種生物堿類活性成分有關。文獻報道多種生物堿類成分在相關疾病的抗炎、鎮痛治療中發揮較好的療效[14],如羅昱瀾等[15]用千金藤屬植物廣西地不容中分離得到的總堿進行抗炎、鎮痛評價,效果顯著,因此有望從金線吊烏龜大極性部位甚至總生物堿中探索出新型、高效的抗炎鎮痛藥。
自由基化學性質活潑,在機體內部通過氧化反應使細胞膜和遺傳物質產生應激性損傷,引起機體老化,進而增加各種退行性疾病的風險[16],清除、抑制自由基已成為臨床常見輔助治療手段[17]。綜合DPPH 法和ABTS 法2 種評價體系的測定結果,金線吊烏龜4 個提取部位均具有良好的抗氧化活性,且中等極性的乙酸乙酯提取物和較大極性的正丁醇提取物抗氧化活性較好,可能與這2 個部位富含黃酮等較大極性的化學成分有關。文獻[18]報道植物總黃酮具有良好的抗氧化活性。此外,吳冬青等[19]發現,金線吊烏龜總黃酮清除DPPH 自由基活性顯著且穩定性好,因此可針對金線吊烏龜的乙酸乙酯和正丁醇提取部位甚至總黃酮進行更深入的研究,進行抗氧化活性成分的靶向分離。
病因學分析表明,消化道癌癥發病風險增加與N-亞硝基化合物的合成有直接關系[20]。亞硝酸鹽作為N-亞硝基化合物的前體化合物,廣泛存在于腌制食品中,攝入體內后在人體胃酸環境可與胺類發生亞硝胺反應,形成N-亞硝基化合物,進而引發一系列的腫瘤,甚至可以透過胎盤屏障誘導下一代患癌[21]。因此,清除體內亞硝酸鹽和阻斷亞硝胺合成反應,是預防和控制相關癌癥的有效途徑。通過模擬人體胃內環境,綜合評價金線吊烏龜的抑制亞硝化活性,結果表明,4 個提取部位均具有一定的抑制亞硝化活性,其中水提取物的抑制亞硝化活性最強,可能與水提取物富集極性較大的生物堿類活性物質有關,文獻報道千金藤屬植物塊根、莖葉和種子中提取的多種生物堿,具有抗癌細胞生長和抗骨肉瘤等多種臨床藥理活性[4,22],提示可以從金線吊烏龜水提取物中探索有助于癌癥病因性預防的生物堿類成分。
綜上所述,金線吊烏龜具有一定的抗炎、鎮痛、抗氧化和抑制亞硝化活性,后續重點對其大、中極性提取部位開展系統的化學成分、構效關系及作用機制研究,將有助于闡明金線吊烏龜藥用科學內涵,為這一藥用資源的綜合開發利用提供理論基礎。

