澳大利亞衛生技術評估及決策轉化的分析和借鑒
張 秋 劉藹霞
衛生技術評估(health technology assessment, HTA)是一種對于衛生技術的性質、效用和結果進行系統性評估的方法。隨著我國老齡化趨勢的加重和疾病譜的改變,社會對健康的剛性需求逐漸增加[1]。《2019年我國衛生健康事業發展統計公報》顯示,我國醫療衛生總費用逐年攀升,國內生產總值(GDP)比重增長6.6%,個人衛生費用負擔依然很重。《2021年國家醫療質量安全改進目標》中也提出要持續提升醫療質量安全管理科學化和精細化水平,保障醫療安全,把為人民群眾提供安全、優質的醫療服務作為衛生健康工作的核心任務。所以隨著醫療新技術和新藥不斷出現,醫療資源的合理優化配置和利用成為未來新醫改的關鍵。
由于醫療領域科學決策的需求,HTA在我國的重要性日益凸顯[2]。我國于20世紀80年代引入HTA。2009—2016年我國衛生部和英國國家衛生與服務優化研究院開展多項HTA建設合作。為了更好地發揮HTA的決策作用,2018年舉辦了首屆中國衛生技術評估大會并設立國家藥物與衛生技術綜合評估中心。2019年我國進一步提出采用HTA科學開展藥品臨床綜合評價。經過多年的發展,HTA呈現出快速發展趨勢,但我國在HTA的評估流程設計及政策轉化方面仍存在不足,有待進一步的優化。
澳大利亞是最早運用HTA制定醫療衛生領域決策的典型國家之一,尤其是在藥品準入審核方面[3]。澳大利亞充分利用HTA進行決策,憑借干預措施,以確保納稅人的資金,實現以相對最少的醫療衛生成本獲得相對最大的健康狀況改善結果。在澳大利亞,運用HTA研究成果來通過上市決策的公共和私人資助計劃包括:藥物福利計劃(pharmaceutical benefits scheme, PBS)、國家免疫計劃(national immunization program, NIP)、醫療保險福利計劃(the medicare benefits schedule, MBS)、假肢列表和國家血液協議,這些計劃目錄的增加均通過HTA來實現。
目前,澳大利亞聯邦層面最權威的兩個獨立評估機構為藥物福利咨詢委員會(Pharmaceutical Benefits Advisory Committee, PBAC)和醫療服務咨詢委員會(Medical Services Advisory Committee, MSAC)。PBAC是世界上第一個法定的專門開展藥品報銷目錄評價和遴選的國家機構。因而研究澳大利亞HTA體系及機制,對我國現階段正趨于逐步完善的HTA機制有一定的參考意義和價值。
1 澳大利亞HTA體系
1.1 澳大利亞HTA流程介紹
治療用品管理局(the Therapeutic Goods Adminis- tration, TGA)、MSAC、PBAC和假肢清單咨詢委員會(the Prostheses List Advisory Committee, PLAC)分別執行HTA程序,向澳大利亞政府衛生部提供咨詢意見。HTA流程對于支持補貼醫療技術的可持續管理至關重要。澳大利亞政府通過多樣化的衛生資金安排,如最典型的公共衛生補貼——PBS和MBS,以及私人醫療保險中的假肢名單,為與健康有關的產品和服務的成本價格提供補貼,資助澳大利亞人獲得必要的醫療服務和技術。澳大利亞政府通過明確細化的HTA實施流程以及切實的研究成果來鞏固利益相關者對HTA決策的信心。
在澳大利亞,各HTA機構主要通過如下兩種方式來參與政府HTA決策:第1種方式:衛生技術通過澳大利亞治療用品注冊處(Australian Register of Therapeutic Goods, ARTG)批準上市前,在市場監管下評估其安全性和有效性。通過評估來確保衛生技術的安全及使用效果,并使用適當的質量控制辦法進行生產。第2種方式:評估衛生技術的相對安全性、臨床效果和成本-效益,基于此決定是否通過MBS、PBS和NIP分別為醫療服務(有或沒有設備)、程序和診斷技術、藥品和疫苗提供公共資金;是否在私人醫療保險中通過假肢列表補償假肢裝置;以及是否對衛生保健干預措施進行后市場監督,通告還處在上市批準階段的衛生技術的上市決定或那些被證明不安全或使用效果不如預期的衛生技術的償付情況。澳大利亞現行的HTA批準上市和補償流程如圖1。
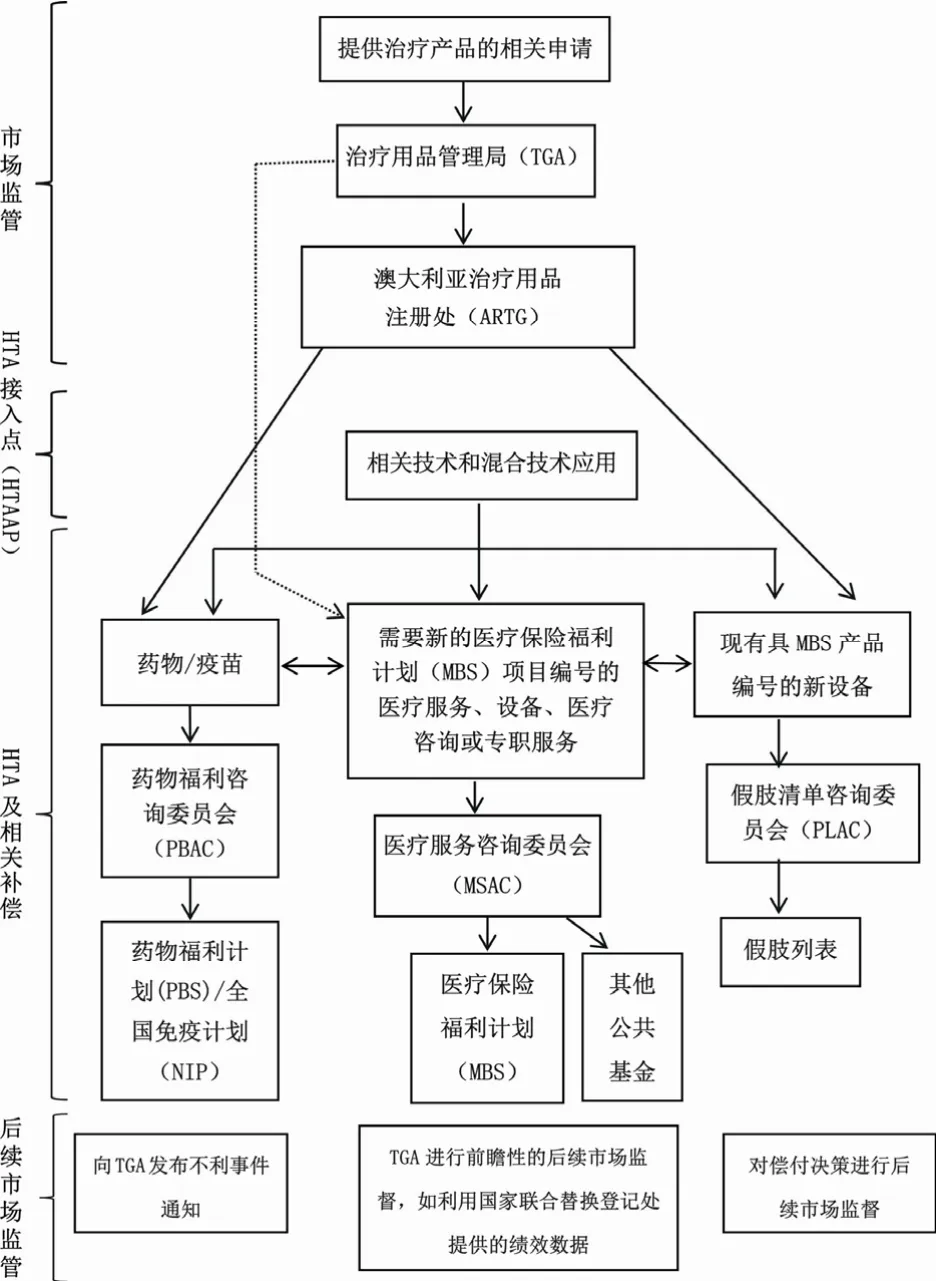
圖1 澳大利亞現行HTA批準上市和補償流程[4]
澳大利亞HTA流程大概分為3部分:第一部分是市場監管,表示衛生技術的相關申請必須提交給TGA,以便批準進入ARTG。第2部分是HTA及其補償流程,圖中顯示了各種評估途徑。對于藥物或疫苗,可以向PBAC申請,如果成功,新項目將被納入PBS或NIP;對于需要新的MBS項目編號的醫療服務或設備,需要向MSAC提出申請,如果成功,新服務將包含在MBS中;對于需要新的MBS項目編號的醫療咨詢或專職服務,需要向MBS質量框架提出申請,如果成功,新服務將包含在MBS中;對于現有具有MBS產品編號的新設備,需要向假肢名單咨詢委員會(Prostheses List Advisory Committee, PLAC)提出申請,如果成功將在假肢列表中列出。圖中的HTA接入點(HTA assess point, HTAAP)管理相關技術和混合技術應用,這些技術需要由多個委員會考慮決定。第3部分后續市場監督,新的衛生技術上市后,TGA可能會收到一些不利事件,此時TGA便發揮其后續市場監管的作用。例如利用國家聯合替換登記處提供的績效數據,以及通過MBS質量框架對償付決策進行后續監督。
1.2 澳大利亞HTA重要機構PBAC
TGA、MSAC、PBAC和PLAC分別執行HTA程序,向澳大利亞政府衛生部提供咨詢意見。每個機構功能獨立,可響應不同的政策需求,相互間聯系緊密。
成立于1953年的PBAC是世界上第一個依法成立的專門開展藥品報銷目錄評價和遴選的國家機構[5]。本文將重點對澳大利亞的PBAC進行介紹。
PBAC是由澳大利亞政府設立的獨立專家機構。其委員會由21名獨立專家組成,包括醫生、衛生專業人員、衛生經濟學家和消費者代表,他們被要求簽署并遵循嚴格的利益沖突聲明條款。PBAC下設藥物利用小組委員會(Drug Utilization Sub Committee, DUSC)、經濟小組委員會(Economics Sub Committee, ESC),協助分析和提供不同領域的建議。
PBAC的主要作用是推薦在PBS上市的新藥。PBAC每年舉行3次會議,除非PBAC提出積極的建議,否則PBS目錄不能列出新藥。在推薦目錄藥物時,PBAC會考慮澳大利亞注冊使用該藥物的醫療條件及臨床有效性、安全性和成本-效益與其他治療的比較。
PBAC的評審流程主要分為4個步驟:第1步,向TGA提交申請;第2步,PBAC評審材料交DUSC和ESC審核;第3步,PBAC提出建議;第4步,價格談判;第5步,衛生部決定是否列入PBS目錄及談判價格確定。具體流程見圖2。
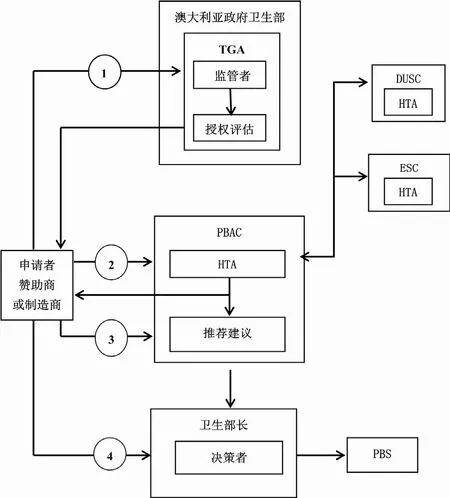
圖2 澳大利亞PBAC評審流程[6]
2 澳大利亞HTA成果的政策轉化
澳大利亞強調利用HTA對PBS、NIP及MBS做出相關決策。三者的實施不僅有效遏制全民醫療費用的不合理增加,而且進一步完善了澳大利亞的醫療衛生體系。
2.1 PBS
PBS于1948年設立,為退休人員提供免費藥品,并為社區群眾免費提供139種“救命和預防疾病”藥品。據澳大利亞衛生部最新發布的《衛生部2019—2020年年度報告》數據顯示,多于160萬澳大利亞 人可使用免費或打折PBS藥物。同時,政府將補貼大部分醫療條件下的藥品費用。
PBS的藥品目錄每季度出版一次。政府對PBS藥品目錄中每種藥物的價格進行管理。隨著需求的增加和新藥的加入,PBS的整體成本會增加。當一個藥品的預算超過一定的數額時需要國會參與討論。政府通過制定若干戰略確保PBS仍然為社區提供負擔得起的必要藥品,并幫助維持制藥企業的正常運營。在PBS目錄以外的處方藥市場份額非常小,因此盡管目錄中的藥品價格會被PBS管制,制藥企業仍愿意努力將其生產和銷售的藥品列入PBS目錄[7]。
2.2 MBS
作為澳大利亞政府補貼的醫療保險服務的清單,MBS為所有澳大利亞居民和某些類別的澳大利亞游客提供獲得醫療和醫院服務的機會。公共服務部管理醫療保險福利的支付。
MSAC的評估重點是在診斷技術、醫療服務或設備的安全性、有效性和經濟性上,被通過的MSAC報告最終會以MBS的形式公布出來,MBS對HTA的應用正是通過MSAC來實現。
2.3 NIP
免疫接種是有史以來最成功、最具成本-效益的健康干預措施之一[8]。NIP由澳大利亞聯邦和州及地區政府于1997年設立。NIP是一項包括各級政府(澳大利亞、州、領地)、醫療保健提供者、管理人員和研究人員的合作方案。2018年澳大利亞發布了《2019—2024國家免疫戰略》,旨在擴大和改進國家的免疫規劃,最大限度地提高各年齡段公民的免疫覆蓋率以預防疾病。
目前的預防接種規劃包括一份按年齡組別和/或醫療風險劃分的推薦疫苗表,根據年齡組別和風險向澳大利亞人士免費提供。根據NIP獲得免費疫苗的資格與享受醫療保險福利的資格有關。澳大利亞實施全民醫保制度。據經合組織數據顯示,2019年澳大利亞政府/社會健康保險總保健覆蓋率估值達100%,私人醫療保險覆蓋率達53.6%。
由于澳大利亞規定所有申請加入PBS目錄的藥品或加入NIP的疫苗都必須經由PBAC評審,因此藥品在ARTG注冊成功之后需要通過PBAC的評審才能最終進入PBS目錄。
澳大利亞目前正在推行COVID-19免疫接種計劃,每個澳大利亞人都將獲得接種COVID-19疫苗的資格。但在疫苗提供給澳大利亞人之前,必須得到監管和澳大利亞所有疫苗、藥品和其他醫療用品管理局(TGA)的批準。COVID-19疫苗的供應批準須遵守嚴格的條件,例如阿斯利康的臨時批準有效期為兩年,期間要求阿斯利康繼續向TGA提供有關正在進行的臨床試驗和上市后評估的長期有效性和安全性信息。所有注冊疫苗均由TGA密切監測及負責應對任何安全問題。澳大利亞國內目前有阿斯利康和輝瑞的COVID-19疫苗獲準使用:輝瑞疫苗主要用于16歲及以上人群,阿斯利康用于18歲及以上人群。截至2021年3月29日數據,已有541 761澳大利亞人接種了COVID-19疫苗。
3 借鑒
3.1 設置職能明確的HTA機構
設置職能明確的HTA機構利于評估成果高效率完成政策轉化。澳大利亞的HTA機構是由多層次構成的,其中聯邦層面最為有名的兩個機構即PBAC和MSAC,均為國家級評估機構,負責對合作的大學、專業機構、私人顧問和衛生權威機構部署HTA的具體研究工作。此外,澳大利亞的多數醫院還會通過設立治療委員會開展HTA工作。
在我國,HTA體系由高校、研究所以及一些非附屬醫院等構成,相較于澳大利亞HTA的研究機構的設置,我國缺乏職能明確的調控機制和管理機構,這使各HTA研究機構相互之間協調起來十分困難。因此我國HTA機構的設置尚待完善,隨著這幾年HTA在國內被更多地應用,需要有更多專業的、權威的機構建立起來,形成我國的HTA網絡。
3.2 加強我國HTA的決策透明性、規范性
澳大利亞的PBAC成員的結構組成利于提高消費者和臨床醫生等主要利益相關方的接觸水平,從而為PBAC的決策過程提供信息。同時,PBAC和MSAC僅提供評估報告和相關的建議,并不最終決定藥物或醫療設備是否進入相關國家福利計劃中,擁有最終決定權的是衛生部。評估機構獨立于政府衛生部門是十分正確的做法,一方面政府對HTA機構進行監督,另一方面,一定程度上減少甚至杜絕了各利益相關方為了自身利益最大化而將實際價值并不高的藥品或醫療設備、技術、服務等推向市場,導致資源的不合理配置。過程和結果的透明性和規范性的提高將增加公眾對國家衛生體系的信心。
我國不斷強調醫療保險的循證決策,國家基本藥物工作委員會負責基本藥物目錄審核[9],同時HTA輔助醫保目錄的準入決策。但HTA的人員構成、部門協調、工作流程缺乏系統化和規范化。目前,我國基本藥物審核仍以官方機構專家掌握主要決策,主觀性較強,透明性較差[8]。其導致公眾對于醫保目錄準入和HTA的概念并不了解。我國應積極創新醫保藥物準入模式,不斷加強HTA的公平性、全面性,立足本國國情,廣泛動員醫學專業人員、經濟學專家及患者代表等社會群體的參與。
3.3 完善我國HTA方面的政策法規
HTA是澳大利亞藥物定價的基本準則[10]。澳大利亞PBAC的職責是依法為衛生部提供有關藥物的效果和經濟效益方面的建議和咨詢。1993年以后,澳大利亞相關法規規定,一份完整的申報產品的藥物經濟學分析報告是申請人在提交產品列入藥物福利計劃報銷目錄的申請時所必備的。藥物經濟學報告中需要提供該藥與同類藥相比的優勢及證據并給出具體數據,只有當該種藥品的療效、安全性和成本-效果方面與同類藥相比有更優異的表現時才會被納入PBS目錄中得到國家補貼。在澳大利亞,藥品的HTA在法律的保障下快速發展。
對照我國,HTA研究成果能成功轉化為政策的主要原因是政策需要,大多數的HTA工作以政府的項目委托方式展開,對HTA引入決策過程始終缺乏制度安排,這種零散的作業方式顯然無法滿足科學決策的要求。其中,HTA強調藥物經濟性。HTA的藥物經濟性證據在2017年中國基本醫保藥品準入談判工作時被首次引入,HTA的應用提升了藥品談判的相對公平性。近年來,國家層面進一步關注到了HTA應用的經濟價值和臨床價值,如降低醫療衛生成本,輔助醫保政策設立;提高藥品療效、安全性及經濟性的臨床價值等。2018年,國家發布關于基本藥物制度的意見中提出對基本藥物目錄定期評估、動態調整,優先調入有效性和安全性證據明確、成本-效益比顯著的藥品品種[11]。我國部分社會機構發布HTA相關的行業性規范指南,中國藥學會發布了2020年版《中國藥物經濟學評價指南》,但由于制定主體缺乏官方性,指南執行力度較弱[12]。我國需要借鑒澳大利亞這方面的成功經驗,將HTA納入到相關法規中,規范質量控制標準。

