伊犁河谷不同藜麥品種對鹽脅迫的生理響應及耐鹽評價
崔宏亮, 宋曉曉, 姚慶, 安萬剛, 邢寶, 秦培友*
(1.新疆伊犁州農業科學研究所,新疆 伊寧 835000;2.新疆伊寧市園林管理中心,新疆 伊寧 835000;3.中國農業科學院作物科學研究所,北京 100081)
土壤鹽漬化是制約農業生產的主要因素之一[1]。伊犁河谷作為新疆重要的糧食生產基地,可利用耕地面積29.8萬hm2,其中鹽漬化土地1.96萬hm2。選育耐鹽作物及耐鹽品種是應對土壤鹽漬化最直接有效的途徑,但可種植的耐鹽作物品種少。藜麥(Chenopodium quinoa Willd.)原產于南美洲安第斯山區,屬莧科藜屬一年生自花授粉植物[2],具有耐鹽、耐寒、耐旱、耐貧瘠等特性。Prado等[3]研究發現,藜麥耐鹽性強,是應對土壤鹽漬化的理想作物。新疆自2014年開始引種,伊犁是最先引種的地區。長期理論研究發現,鹽脅迫對植物的傷害主要表現為滲透脅迫、離子毒害、營養失衡和氧化破壞[4]。當植物遭受鹽脅迫時,可通過改變滲透勢、啟動抗氧化酶促系統等途徑在一定程度上緩解鹽脅迫所造成的損傷。耐鹽性不同的植物自身調節能力不同,相關指標變化各異。目前對藜麥在鹽脅迫下生理響應及機理研究尚不多,本試驗首次以伊犁地區種植藜麥品種為材料,以蒸餾水為對照,設置了8個NaCl濃度梯度,分析了不同NaCl濃度下藜麥種子的萌發、幼苗生長及生理指標,研究藜麥種子及幼苗在鹽脅迫下的生理響應,并選育耐鹽品種,對緩解當地鹽脅迫對藜麥生長發育的不良影響、改良鹽漬化條件下農業生產具有一定的理論指導和現實意義,使藜麥在伊犁地區更好地引種和適種。
1 材料與方法
1.1 供試材料
供試藜麥品種為 NXSG56、NXSG85、HP9、GY3、QA13-9,千粒重分別為 3.54 、3.61、3.85、3.25、3.42 g,來源于中國農業科學院作物科學研究所。
1.2 試驗設計
1.2.1 種子萌發試驗 試驗于2019年6—7月在伊犁州農業科學研究所實驗室進行。從供試藜麥品種中分別挑選無病蟲害、籽粒飽滿且大小接近的種子,用75%酒精消毒60 s后,用蒸餾水反復沖洗8~10次后將種子置于墊有雙層濾紙的培養皿中 ,分 別 用 50、100、150、200、250、300、350、400 mmol·L-1NaCl溶液處理,以蒸餾水為對照(CK),每皿均勻放入50粒種子,加入8 mL處理液,每個濃度重復3次。將所用培養皿置于溫度25℃、12 h光照/12 h黑暗、相對濕度80%的光照培養箱中培養7 d,每天統計種子萌發情況。
1.2.2 幼苗生長期試驗 試驗于2019年8—10月在伊犁州農業科學研究所進行。從供試藜麥品種中分別選取無病蟲害、籽粒飽滿且大小接近的種子,用75%乙醇消毒60 s后用蒸餾水反復沖洗8~10次后風干,播于裝有相同質量蛭石和珍珠巖(體積比1∶1)混合基質的花盆中,花盆口徑28 cm、高10 cm,每盆播40粒種子,正常田間管理,待幼苗4片真葉時選擇長勢一致的幼苗按10株·盆-1均勻定苗。定苗后7 d,以蒸餾水為對照(CK),分別向各花盆中加入等量 50、100、150、200、250、300、350、400 mmol·L-1NaCl溶液進行脅迫處理,每個處理重復5次,處理后第5、10、15天分別隨機取樣,每次每個處理取3株幼苗,測定相關生長及生理指標。
1.3 常規指標測定方法
1.3.1 種子發芽指標測定 根據以下公式計算種子各發芽指標[5]。

1.3.2 生長指標測定 胚根長度在種子處理第7天用游標卡尺測量,每處理取5株,取平均值。根長抑制率用以下公式計算。

NaCl處理幼苗第5、10、15天,取植物全株,洗凈并用濾紙吸干表面水分,在分析天平上稱量地上部分鮮重、地下部分鮮重,然后將鮮樣放入105℃烤箱殺青15 min后在70℃下烘干至恒重,用分析天平稱量地上部分鮮重、地下部分干重,重復測定3次。
1.3.3 生理指標測定 NaCl處理幼苗第5、10、15天,分別取樣測定葉片相對電導率,葉片葉綠素、可溶性糖、脯氨酸含量;幼苗處理第15天,取樣測定葉片纖維素、丙二醛(malondialdehyde,MDA)、葉片Na+、K+含量及超氧化物歧化酶(superoxide dismutase,SOD)活性。采取電導儀法[6]測定葉片相對電導率,采用乙醇提取法[6]測定葉綠素含量,采用蒽酮比色法[6]測定可溶性糖含量,采用水合茚三酮法[6]測定脯氨酸含量,采用比色法[6]測定纖維素含量,采用硫代巴比妥酸法[6]測定MDA含量,采用氮藍四唑法[6]測定SOD活性,采用火焰光度法[7]測定葉片Na+、K+含量。每個指標重復測定3次。
1.4 數據處理
采用Microsoft Excel 2010和SAS 8.1軟件進行數據統計分析及差異性檢驗。
2 結果與分析
2.1 NaCl脅迫對不同品種藜麥種子萌發的影響
發芽率是衡量種子質量的重要指標。由表1可知,NaCl濃度對不同品種藜麥種子萌發的影響不同。隨著NaCl濃度升高,5種藜麥種子的發芽率及發芽勢均呈先升高后下降的趨勢。當NaCl濃度為100 mmol·L-1時,各藜麥品種種子發芽率和發芽勢均達到最大;當NaCl濃度為300 mmol·L-1時,各品種種子發芽率及發芽勢急劇下降;除QA13-9種子發芽勢在NaCl濃度為350 mmol·L-1時最低外,其余各品種發芽率及發芽勢均在NaCl濃度為 400 mmol·L-1時最低。其中NXSG85在NaCl濃度為400 mmol·L-1時相對于對照發芽率及發芽勢降幅最小,NXSG56次之,QA13-9降幅最大。
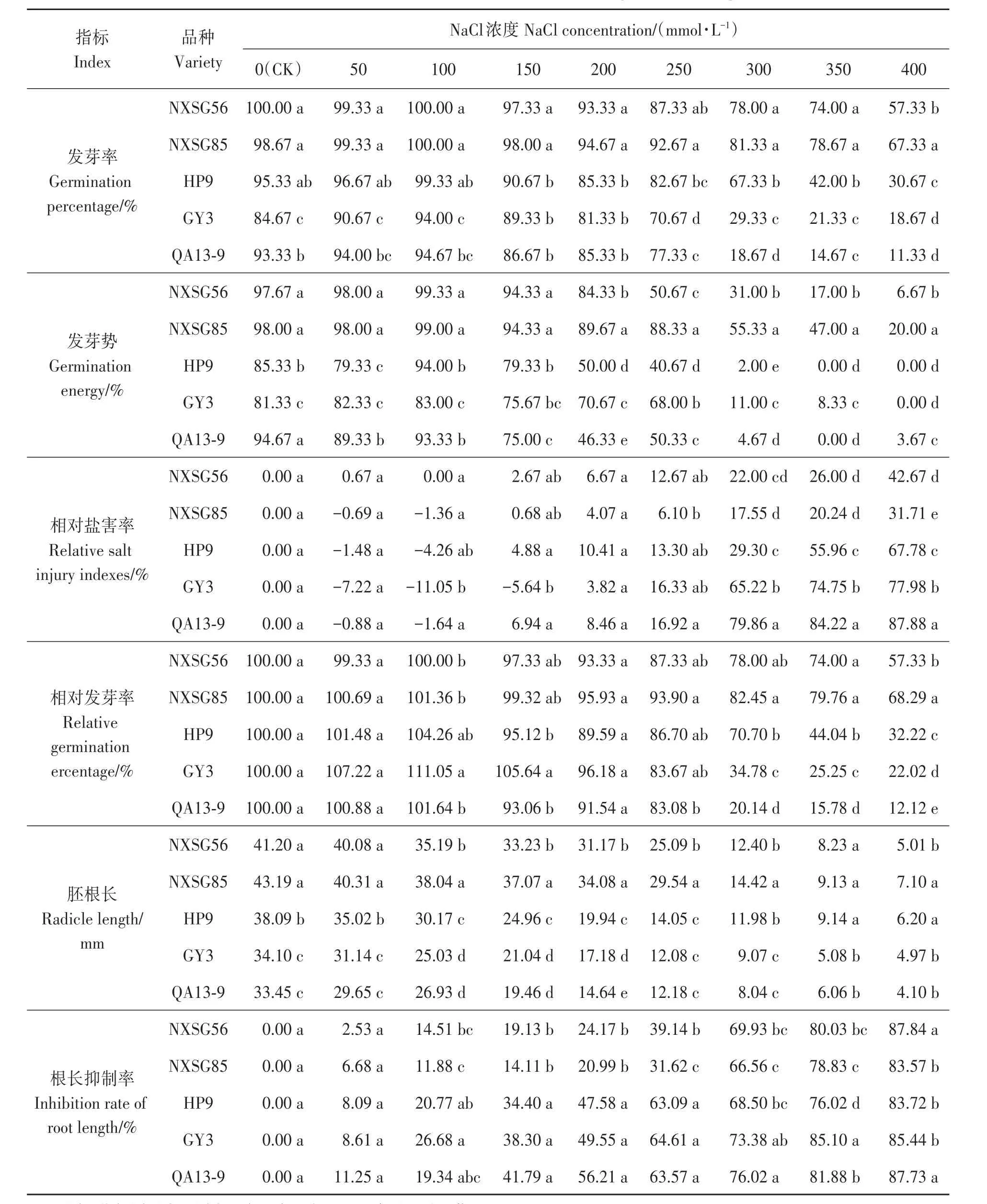
表1 不同濃度NaCl處理對藜麥種子萌發的影響Table 1 Effect of different concentration of NaCl on seed germination of quinoa
隨NaCl濃度升高,除NXSG56外,其余各藜麥品種種子相對發芽率均先上升后下降,各品種種子相對發芽率均在NaCl濃度為100 mmol·L-1時最大,GY3、QA13-9在 NaCl濃度為 300 mmol·L-1時相對發芽率急劇下降,且二者在NaCl濃度400 mmol·L-1時相對發芽率均顯著低于其他品種。
隨NaCl濃度升高,除NXSG56外,其余各藜麥品種種子相對鹽害率先下降后上升,NaCl濃度100 mmol·L-1時各品種種子相對鹽害率最小,NaCl濃度400 mmol·L-1時,各品種種子相對鹽害率均達最大值,且彼此之間差異顯著,QA13-9相對鹽害率顯著高于其他品種,GY3次之;NXSG85相對鹽害率顯著低于其他各品種。
種子胚根長隨NaCl濃度升高均呈下降趨勢,同一NaCl濃度下,各品種間胚根長存在差別。NaCl濃度為200 mmol·L-1時,各品種種子胚根長差異顯著,NXSG85的胚根長顯著大于其他品種,GY3、QA13-9的胚根長始終顯著小于其他品種。隨濃度升高NaCl對各品種根長抑制率上升,低濃度(50 mmol·L-1)對各品種的根長抑制率差異不顯著,當NaCl濃度大于100 mmol·L-1時,對各品種根長有不同程度抑制作用,對NXSG85的根長抑制率始終最低。
2.2 NaCl脅迫對不同藜麥品種幼苗生長的影響
由表2可知,隨NaCl濃度上升各品種幼苗地上部分鮮重均呈下降趨勢;第5天時,隨NaCl濃度上升,NXSG56、GY3品種地上部分干重先上升后下降,其余品種均呈下降趨勢,其他取樣時間均呈下降趨勢;隨NaCl濃度上升,地下部分干重、地下部分鮮重基本均先上升后下降,各品種地下部分干重、地下部分鮮重分別在NaCl濃度250、200 mmol·L-1時達最大值,NXSG85 地下部分干重、地下部分鮮重始終大于其余各品種,QA13-9地下部分干重始終小于其余各品種。NaCl脅迫抑制地上部分鮮重和干物質積累,低濃度NaCl脅迫可促進地下部分鮮重增加及干物質積累。

表2 NaCl脅迫對不同藜麥品種幼苗生長的影響Table 2 Effect of NaCl on biomasses of quinoa seedlings 續表Continued

表2 NaCl脅迫對不同藜麥品種幼苗生長的影響Table 2 Effect of NaCl on biomasses of quinoa seedlings
2.3 NaCl脅迫對不同藜麥品種幼苗葉片相對電導率的影響
由圖1可知,隨NaCl脅迫時間延長,同一藜麥品種幼苗葉片相對電導率呈上升趨勢。隨著NaCl濃度升高,各品種藜麥幼苗葉片相對電導率基本均呈上升趨勢。同一NaCl濃度脅迫下,不同品種間幼苗葉片相對電導率存在差異,NaCl脅迫第5天,不同NaCl濃度下QA13-9幼苗葉片相對電導率顯著高于其余品種,NXSG85葉片相對電導率最小且顯著低于其余各品種;NaCl脅迫第10天,不同NaCl濃度下NXSG85幼苗葉片相對電導率始終高于其余品種;NaCl脅迫第15天,QA13-9葉片相對電導率始終最小且顯著低于其余各品種。
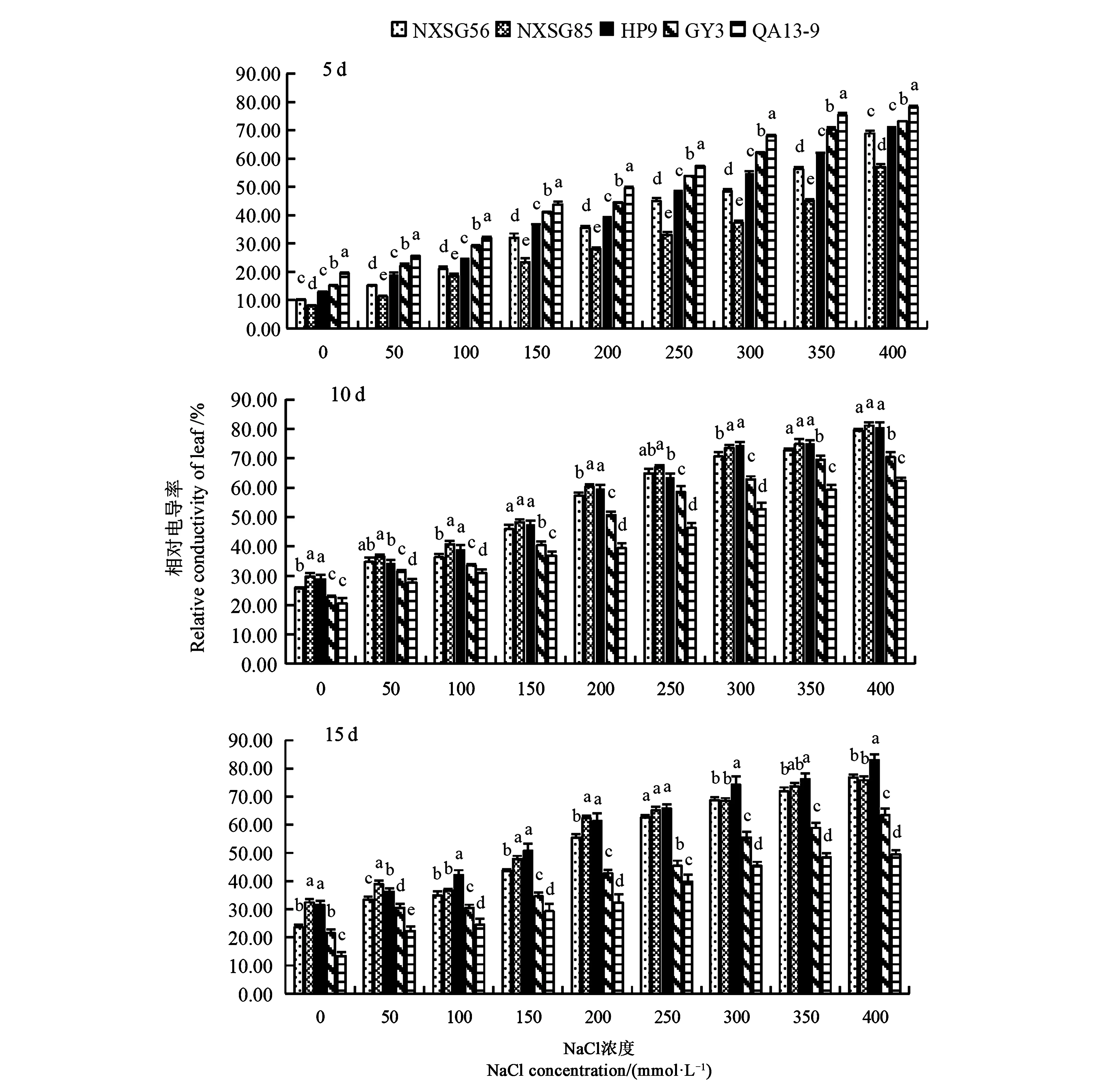
圖1 NaCl脅迫對不同藜麥品種幼苗葉片相對電導率的影響Fig.1 Effects of NaCl on relative conductance of quinoa seedlings
2.4 NaCl脅迫對不同藜麥品種幼苗葉片生理指標的影響
2.4.1 NaCl脅迫對不同藜麥品種幼苗葉片葉綠素含量的影響 由圖2可知,隨NaCl脅迫時間延長,同一藜麥品種幼苗葉片葉綠素含量呈上升趨勢。隨著NaCl濃度升高,各品種藜麥幼苗葉片葉綠素含量基本均呈先上升后下降趨勢,NaCl脅迫第5天各品種幼苗葉片葉綠素含量在NaCl濃度200 mmol·L-1時達最大;NaCl脅迫第10、15天各品種幼苗葉片葉綠素含量在NaCl濃度150 mmol·L-1時達最大,說明低濃度NaCl可促進幼苗葉片葉綠素合成,高濃度NaCl抑制幼苗葉片葉綠素合成。同一NaCl濃度脅迫下,不同品種間幼苗葉片葉綠素含量存在差異,各品種間幼苗葉片葉綠素含量在NaCl濃度為400 mmol·L-1時存在顯著差異,在NaCl脅迫第10、15天,NXSG85幼苗葉片葉綠素含量始終顯著大于其余各品種,QA13-9幼苗葉片葉綠素含量始終小于其余各品種,且在NaCl濃度大于100 mmol·L-1時顯著小于其余各品種。
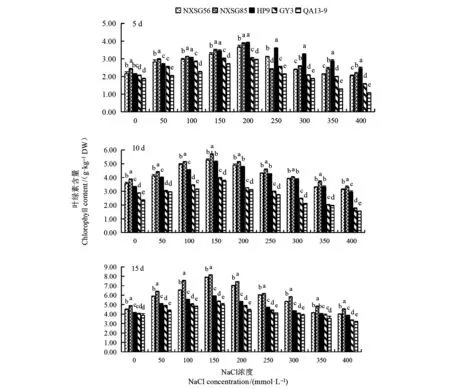
圖2 NaCl脅迫對不同藜麥品種幼苗葉片葉綠素含量的影響Fig.2 Effects of NaCl stress on chlorophyll contents of quinoa seedlings
2.4.2 NaCl脅迫對不同藜麥品種幼苗葉片纖維素含量的影響 由圖3可知,各品種藜麥幼苗葉片纖維素含量隨NaCl濃度升高基本呈下降趨勢。同一NaCl濃度下,各品種幼苗葉片纖維素含量存在差異,當 NaCl濃度低于 250 mmol·L-1時,NXSG85幼苗葉片纖維素含量始終顯著高于其余各品種,HP9含量次之;當NaCl濃度為250~350 mmol·L-1時,HP9品種幼苗纖維素含量最高,但在濃度250 mmol·L-1時與NXSG85差異不顯著;在 NaCl濃度為 400 mmol·L-1時,NXSG85 品種幼苗葉片纖維素含量最高且顯著高于其余各品種;在各NaCl濃度下,QA13-9品種幼苗葉片纖維素含量基本始終低于其余各品種。
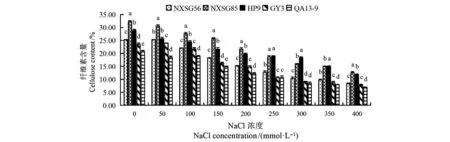
圖3 NaCl脅迫對不同藜麥品種幼苗葉片纖維素含量的影響Fig.3 Effects of NaCl stress on cellulose contents of quinoa seedlings
2.5 NaCl脅迫對不同藜麥品種幼苗葉片滲透調節物質含量的影響
2.5.1 NaCl脅迫對不同藜麥品種幼苗葉片可溶性糖含量的影響 由圖4可知,隨NaCl脅迫時間延長,同一藜麥品種幼苗葉片可溶性糖含量先下降后上升。NaCl脅迫初期,隨NaCl濃度升高同一藜麥品種幼苗葉片可溶性糖含量基本呈先上升后下降趨勢,在NaCl濃度200 mmol·L-1時達最大;在NaCl脅迫第10、15天,隨著NaCl濃度升高同一藜麥品種幼苗葉片可溶性糖含量呈上升趨勢。同一NaCl濃度下,不同品種間幼苗葉片可溶性糖含量存在差異,NaCl脅迫初期,當NaCl濃度低于200 mmol·L-1時,NXSG85品種幼苗可溶性糖含量始終最高,當NaCl濃度升高至200 mmol·L-1時,隨其濃度上升,HP9幼苗葉片可溶性糖含量始終最高;NaCl脅迫第10天,NXSG85葉片可溶性糖含量始終大于其余各品種;NaCl脅迫第15天,HP9葉片可溶性糖含量始終顯著大于其余各品種。在整個脅迫期,QA13-9幼苗葉片可溶性糖含量基本始終顯著小于其余各品種。

圖4 NaCl脅迫對不同藜麥品種幼苗葉片可溶性糖含量的影響Fig.4 Effects of NaCl stress on soluble sugar contents of quinoa seedlings
2.5.2 NaCl脅迫對不同藜麥品種幼苗葉片脯氨酸含量的影響 由圖5可知,隨NaCl脅迫時間延長,同一藜麥品種幼苗葉片脯氨酸含量呈上升趨勢。在NaCl脅迫初期,隨著NaCl濃度升高同一藜麥品種幼苗葉片脯氨酸含量均呈上升趨勢,隨NaCl脅迫時間延長,同一藜麥品種幼苗葉片脯氨酸含量呈上升趨勢。在NaCl脅迫初期,當NaCl濃度≤250 mmol·L-1時,QA13-9幼苗葉片脯氨酸含量顯著高于其余各品種,隨著NaCl濃度持續升高,GY3幼苗葉片脯氨酸含量急劇上升且顯著高于其余各品種;在NaCl脅迫第10、15天,NXSG85幼苗葉片脯氨酸含量始終高于其余各品種。
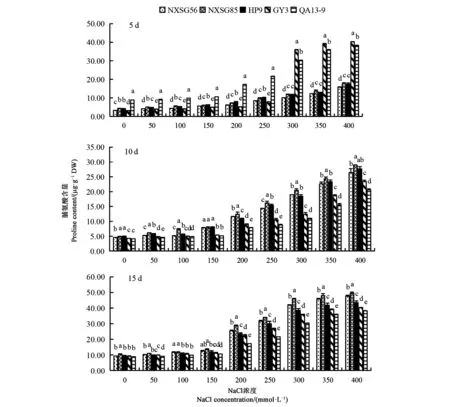
圖5 NaCl脅迫對不同藜麥品種幼苗葉片脯氨酸含量的影響Fig.5 Effects of NaCl stress on proline contents of quinoa seedlings
2.5.3 NaCl脅迫對不同藜麥品種幼苗葉片Na+、K+含量的影響 由表3可知,隨NaCl濃度升高,各品種幼苗葉片Na+含量均上升,GY3增幅最小,QA13-9增幅最大。同一NaCl濃度下,各品種間幼苗葉片Na+含量存在差異,NXSG85葉片Na+含量始終顯著高于其余各品種。隨NaCl濃度升高,各品種幼苗葉片K+含量呈下降趨勢,NXSG56降幅最小,GY3降幅最大。同一NaCl濃度下,各品種間幼苗葉片K+含量存在差異,當NaCl濃度為50~150 mmol·L-1時,GY3品種幼苗葉片K+含量最高,其余濃度下,NXSG85葉片K+含量始終顯著大于其余各品種。分析K+/Na+可知,隨NaCl濃度升高,各品種幼苗葉片K+/Na+呈下降趨勢,QA13-9降幅最小,GY3降幅最大。各品種間幼苗葉片K+/Na+存在差異,低NaCl濃度下,GY3品種幼苗葉片中K+/Na+最大且顯著大于其余各品種,當NaCl濃度≥100 mmol·L-1時,QA13-9幼苗葉片 K+/Na+顯著小于其余品種。
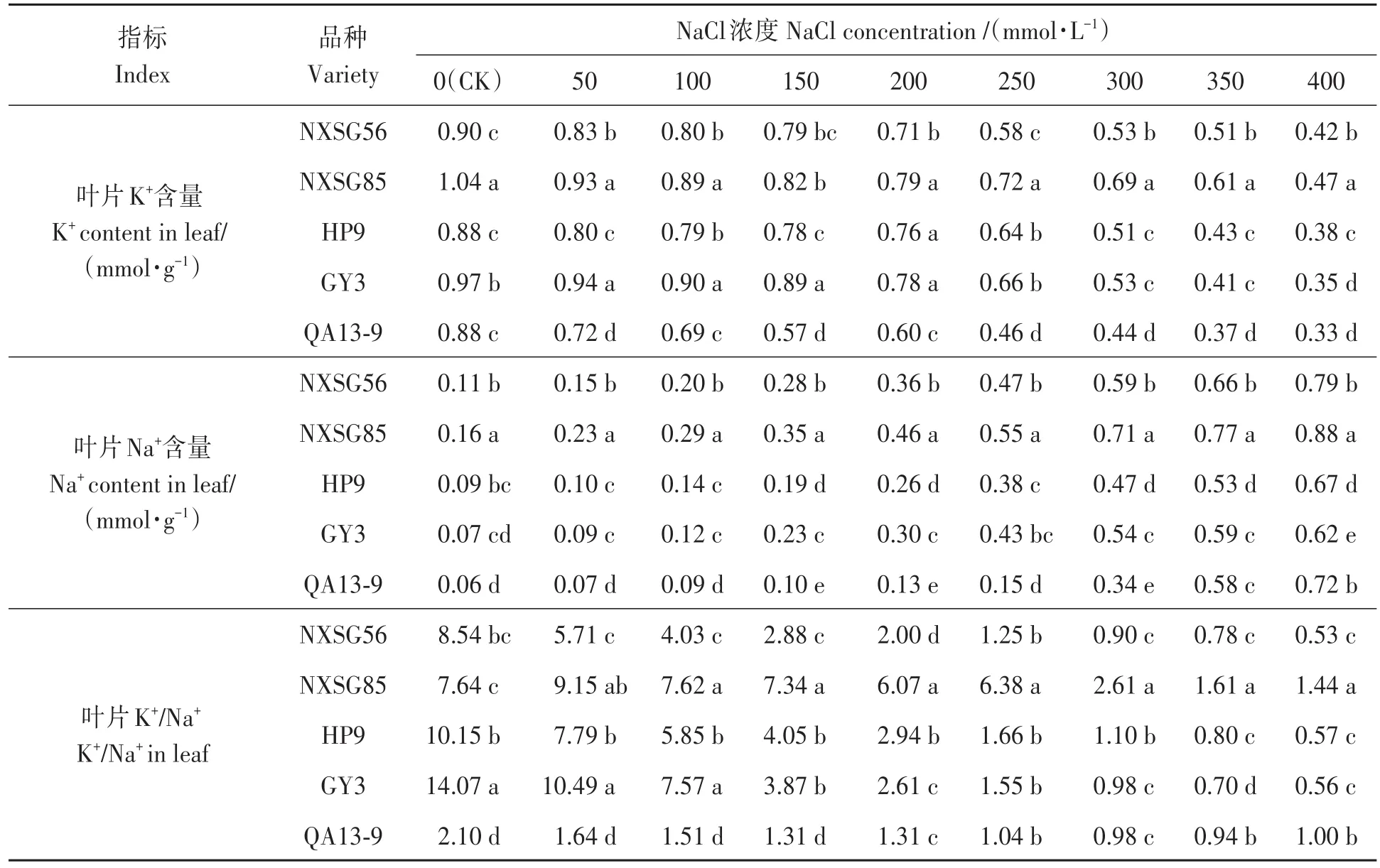
表3 NaCl脅迫對不同藜麥品種幼苗葉片K+、Na+含量及K+/Na+的影響Table 3 Effect of NaCl on K+,Na+contents and K+/Na+of quinoa seedlings
2.6 NaCl脅迫對不同藜麥品種幼苗葉片活性物質的影響
2.6.1 NaCl脅迫對不同藜麥品種幼苗葉片MDA含量的影響 MDA是膜脂過氧化的終產物,其含量反映細胞膜脂過氧化程度[8]。由圖6可知,NaCl脅迫下,各品種葉片MDA含量均高于CK。隨著NaCl濃度的升高,NXSG56品種藜麥幼苗葉片MDA含量呈先上升后下降趨勢,且在NaCl濃度300 mmol·L-1時達最大值;其余各品種幼苗葉片MDA含量均呈持續上升趨勢。NXSG85的增幅最小,QA13-9增幅最大,說明NaCl脅迫下QA13-9幼苗膜脂損傷更為嚴重。在同一NaCl濃度下,NXSG85幼苗葉片MDA含量始終低于其余各品種。
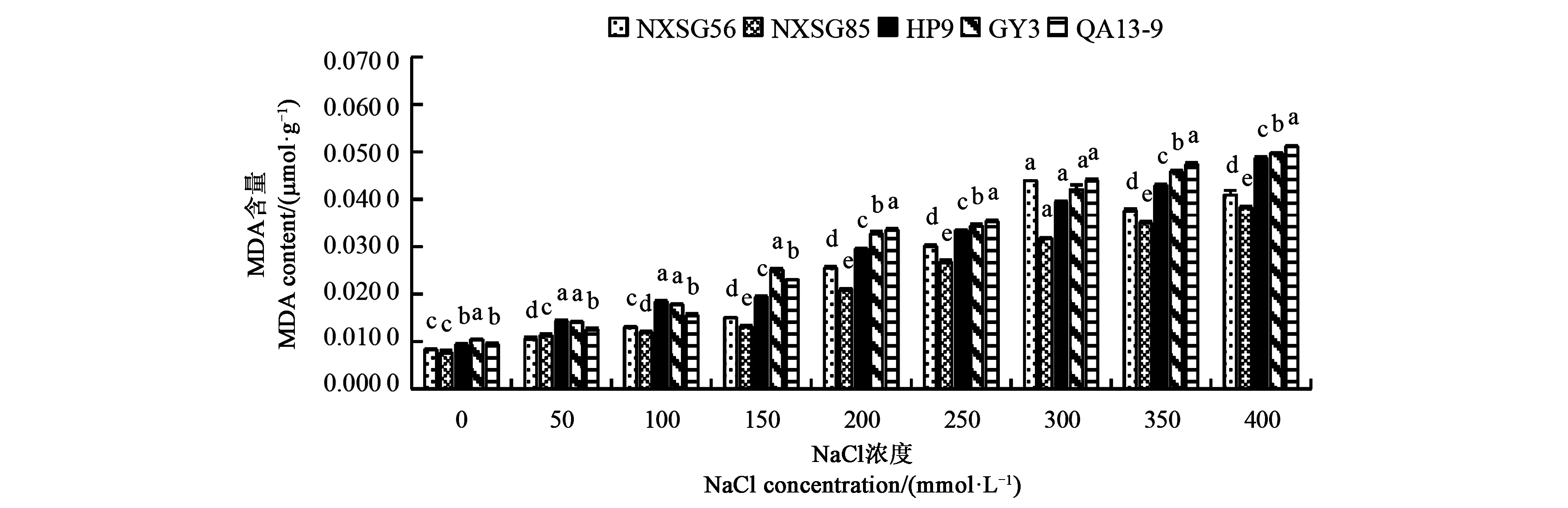
圖6 NaCl脅迫對不同藜麥品種幼苗葉片MDA含量的影響Fig.6 Effects of NaCl stress on MDA contents of quinoa seedlings
2.6.2 NaCl脅迫對不同藜麥品種幼苗葉片SOD活性的影響 植物受到脅迫時體內細胞代謝紊亂,自身啟動抗氧化酶促系統,以維持正常生理功能[9]。由圖7可知,隨著NaCl濃度升高,各品種藜麥幼苗葉片SOD活性均呈先上升后下降趨勢,且在NaCl濃度300 mmol·L-1時達最大值。同一NaCl濃度下,各品種幼苗葉片SOD活性差異顯著,NXSG85幼苗葉片SOD活性始終顯著高于其余各品種,QA13-9幼苗葉片SOD活性始終顯著低于其余各品種。
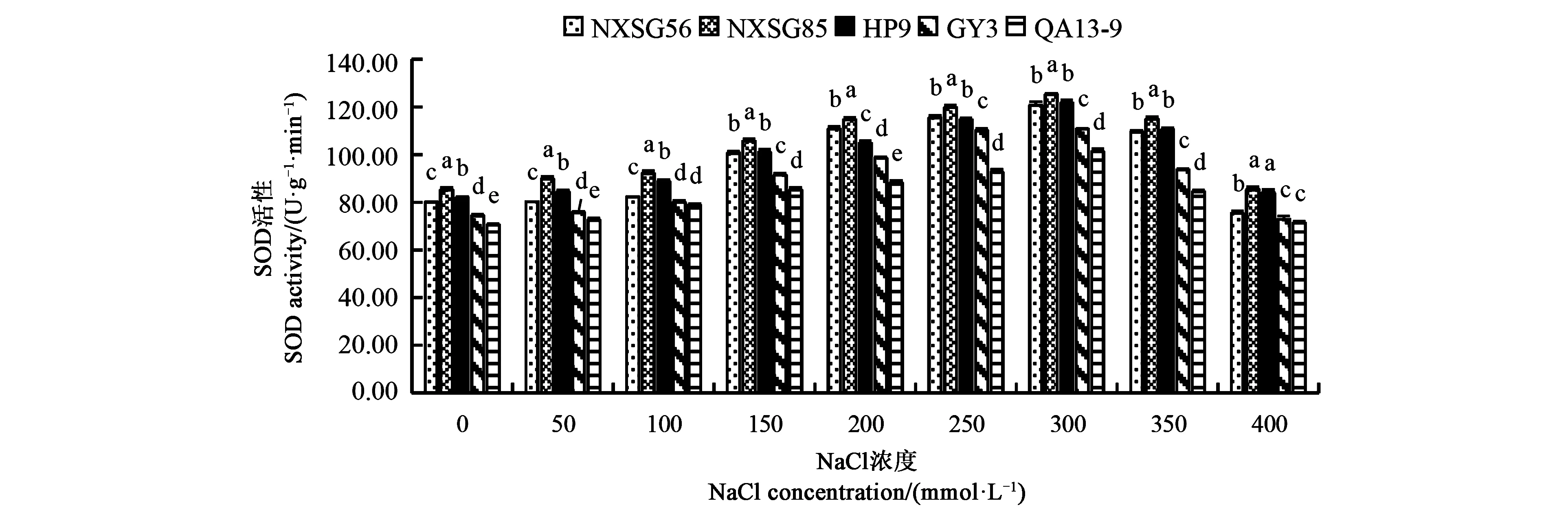
圖7 NaCl脅迫對不同藜麥品種幼苗葉片SOD活性的影響Fig.7 Effects of NaCl stress on the activities of SOD of quinoa seedlings
3 討論
3.1 NaCl脅迫與藜麥種子萌發及幼苗生長
種子萌發及幼苗早期階段是植物種群能否在鹽漬條件下建植成功的關鍵時期[10]。NaCl濃度直接影響種子萌發質量,表現為降低種子發芽率、發芽勢,延遲初始萌發時間等[11-12]。本研究表明,低濃度NaCl可促進藜麥種子萌發,而高濃度抑制萌發,當 NaCl濃度為100 mmol·L-1時,各藜麥品種種子發芽率達最大值,這與楊發榮等[13]的研究結果一致。
形態變化是植物遭受逆境脅迫時最直接的反映。本研究發現隨NaCl濃度上升各藜麥品種幼苗地上部分鮮重、干重均持續下降,地下部分鮮重、干重呈先上升后下降的趨勢。NaCl脅迫抑制地上部分鮮重和干物質積累,低濃度NaCl脅迫可促進地下部分鮮重增加及干物質積累。這可能是藜麥幼苗對低濃度NaCl脅迫的一種應激反應,通過促進根系生長以增強根系吸水能力,以抵抗高鹽濃度引起的滲透脅迫[14],但生理機制尚需進一步研究。
3.2 NaCl脅迫與藜麥幼苗葉片相對電導率
相對電導率反應細胞膜的受害程度,其值越大表明植物生物膜系統受害程度越大。本研究發現,隨NaCl脅迫時間延長及濃度升高各品種幼苗葉片相對電導率基本均持續上升。可能是高NaCl濃度下,植物自身調節無法維持膜系統穩定性,細胞質膜遭到破壞,透性增加,外界物質進入細胞內導致細胞內電導率升高,這與馬琳[15]的研究結果一致。
3.3 NaCl脅迫與藜麥幼苗葉片生理指標
葉綠素含量是反映光合強度的重要指標,一定程度上可以用來衡量植物抗逆性[16]。本試驗中各品種幼苗葉片葉綠素含量隨NaCl濃度升高均先上升后下降,與劉曉青[17]的研究結果一致。可能是低濃度NaCl促進葉綠素合成,增強植物光合作用以減輕鹽脅迫對植株的傷害,而高NaCl濃度下葉綠體結構遭到破壞,導致葉綠素含量下降,也可能是葉綠素酶活性提高導致葉綠素降解[18],具體機制有待進一步研究。
3.4 NaCl脅迫與藜麥幼苗滲透調節物質
滲透調節物質在植物對抗逆境過程中起重要作用[19]。劉雅輝等[20]研究發現,在NaCl脅迫下,棉花葉片脯氨酸含量持續上升,與本研究結果一致,說明藜麥幼苗通過提高自身脯氨酸含量增加細胞吸水能力以抵御鹽脅迫損傷。但本研究發現,隨NaCl濃度升高各品種幼苗葉片可溶性糖含量先上升后下降。可能是低鹽濃度時植物可通過增加可溶性糖含量提高滲透勢,但當NaCl濃度達到一定值時,細胞膜結構受損,細胞內可溶性糖外滲,導致可溶性糖含量下降。無機鹽離子是植物細胞滲透調節重要物質,鹽脅迫后Na+進入植物體內大量積累引起植物體內離子穩態失衡而產生Na+毒害效應[21],本研究發現,隨NaCl濃度升高幼苗葉片Na+含量持續上升,K+含量、K+/Na+持續下降,與劉自剛等[22]對白菜葉片的研究結果一致。
3.5 NaCl脅迫與藜麥幼苗活性物質
MDA是膜脂過氧化的終產物,其含量反映細胞膜脂過氧化程度,一定程度上可代表植物對逆境響應的強弱[23]。本研究表明,在NaCl脅迫下各品種葉片MDA含量均高于CK。隨NaCl濃度升高NXSG56品種幼苗葉片MDA含量先上升后下降,原因有待于進一步探討。其余品種葉片MDA含量均持續上升,與朱紅霞等[24]的研究結果一致,可能是隨著NaCl濃度升高,抗氧化酶系統清除活性氧的能力逐步降低,導致MDA積累增多,進一步傷害膜系統。同一NaCl濃度下,NXSG85幼苗葉片MDA含量始終低于其余各品種,說明該品種在NaCl脅迫下清除活性氧的能力較其他品種強,對逆境的抗性較強。
SOD作為消除活性氧的關鍵酶,是植物體內重要的酶促防御系統。本研究發現,隨NaCl濃度升高,各品種藜麥幼苗葉片SOD活性均先上升后下降,與周麗等[25]的研究結果一致,在NaCl濃度300 mmol·L-1時SOD活性最大。原因可能是脅迫初期,植物啟動自身防御系統,通過提高SOD活性以清除體內的自由基;當NaCl濃度持續升高,植物體內自由基大量積累,蛋白質合成受阻,酶活性降低。NXSG85幼苗葉片SOD活性始終顯著高于其余各品種,一定程度上反映出該品種抗性較其他品種強。

