電磁刺激療法預防卒中吞咽障礙吸入性肺炎的研究進展
鄉靖楠,賈杰,劉翠鮮
卒中相關性肺炎(stroke associated pneumonia,SAP)是卒中后致死的重要危險因素之一[1-2],而吞咽障礙是SAP的主要原因之一,可使SAP風險增加10倍以上[3]。預防卒中吞咽障礙吸入性肺炎對改善卒中患者的結局意義重大。隨著技術的發展,一些新型的物理療法,如電刺激、磁刺激等,也逐漸應用于吞咽障礙的治療中。本文總結目前針對卒中吞咽障礙吸入性肺炎發生機制、治療靶點、電刺激和磁刺激療法的相關研究,以期為新型治療技術的臨床推廣提供支持。
1 卒中吞咽障礙吸入性肺炎的機制與治療靶點
1.1 吸入性肺炎 吸入性肺炎與自身免疫力下降、吞咽障礙嚴重程度相關。目前卒中誘導的免疫抑制理論被廣泛關注,Hannawi等[4]認為卒中后機體會減少外周淋巴細胞以及限制自身反應性T淋巴細胞攻擊中樞神經系統的抗原,從而導致免疫功能下降。在此基礎上若并發吞咽障礙,約60%的患者會出現誤吸,37%誤吸的患者會發生吸入性肺炎,誤吸使卒中患者發生肺炎的危險性增加6.95倍[5-6]。
卒中可導致吞咽器官與組織運動不充分、氣道保護機制協調性降低,患者在吞咽過程的咽期常出現舌骨與喉上抬前移速度減慢或幅度減小、會厭翻轉不充分、聲帶閉合不全、咳嗽反射減弱、氣道清除異物能力下降,因此易發生誤吸,相應的也增加了肺炎的風險[5]。
1.2 干預靶點 吞咽神經肌肉支配通路(大腦皮質-延髓吞咽中樞-周圍神經-相關肌群)任何一個環節被破環均可導致氣道保護機制的紊亂:①咽期雖然屬于吞咽的非隨意期,但肌群的收縮也與吞咽運動皮質區激活相關。卒中后大腦皮質與延髓間的聯系被切斷,會導致吞咽啟動延遲,無法在食團到達咽部時啟動氣道保護機制。②吞咽中樞模式發生器位于延髓,因此延髓卒中后一般吞咽障礙較明顯,可出現吞咽啟動延遲,喉上抬不足、聲帶麻痹等情況。③周圍腦神經受損,尤其是迷走神經損傷會出現會厭翻轉不完全、喉上抬力量不足與關閉不全的表現[7]。由此可見,大腦皮質、延髓、外周神經和肌肉都可能作為卒中吞咽障礙吸入性肺炎的干預靶點。
2 電磁刺激療法的臨床應用
2.1 外周肌群刺激
2.1.1 外周電刺激 與磁刺激相比,電刺激療法在卒中吞咽障礙吸入性肺炎相關的臨床應用中更廣泛,主要有表面神經肌肉電刺激(neuromuscular electrical stimulation,NMES)和咽腔電刺激(pharyngeal electrical stimulation,PES),其作用原理為加強吞咽肌群收縮,增大舌骨與喉部運動,通過重復誘發吞咽動作提高吞咽與呼吸的協調性,從而改善氣道的保護機制。
目前以吸入性肺炎為主要結局指標的相關研究較少,更多的是以誤吸的改善為結局指標。Hamada等[8]對53例急性卒中后吞咽障礙患者的住院時長、出院前功能狀態以及肺炎發生率進行了回顧性分析,其中18例接受NMES聯合常規吞咽功能訓練的患者中僅有2例(11.1%)發生肺部感染,發生率顯著低于未接受NMES治療的患者(42.9%,15/35)。Zhang等[9]納入了卒中亞急性期吞咽障礙的患者,進行每日30 min,每周5 d,持續6周的NMES聯合常規訓練,結果顯示聯合訓練組肺炎發生率顯著低于常規訓練組(7.4%vs. 21.4%)。此外,聯合訓練組27例患者治療前有濕啰音(提示食物殘留附著于聲帶)者為25例,治療后下降為6例(P<0.001)。
臨床應用NMES的治療強度尚未有一致性標準,有的學者采用引起肌肉收縮的運動性刺激,有的學者采用達到感覺閾值以上的感覺性刺激。Sproson等[10]招募了30例卒中亞急性期吞咽障礙患者,對實驗組進行了持續4周的運動性NMES結合吞咽動作訓練治療,實驗組治療后食物與液體的滲透-誤吸量表(penetration aspiration scale,PAS)評分均低于對照組,表明誤吸發生減少。Oh等[11]對卒中亞急性期患者進行感覺性NMES治療,比較刺激作用于舌骨上肌群與舌骨下肌群2個不同部位的治療效果,結果顯示2組的PAS均較治療前顯著下降,組間比較顯示舌骨上肌群刺激組治療后PAS評分更低(2.07±1.64分vs.3.13±1.97分,P<0.05)。Rofes等[12]則探究了運動刺激與感覺刺激2種不同刺激強度對卒中慢性期吞咽障礙患者的療效。經過連續10 d,每日1 h的治療后,不同刺激強度治療的患者均較治療前滲漏誤吸次數減少、喉前庭關閉與舌骨垂直移動的反應顯著提高。該研究還證明NMES運動刺激可提高患者的舌骨水平前移反應,減少咽部食物殘留,提高食管上括約肌開放反應,后兩者的改善可降低吞咽后因食物殘留、反流導致的誤吸風險。Gallas等[13]對11例卒中慢性期吞咽障礙患者進行NMES結合少量進食訓練,吞咽造影顯示NMES可降低PAS,減少咽部殘留,但喉閉合時間未有明顯改善,刺激咽部皮層的運動誘發電位(motor evoked potentials,MEP)亦無顯著變化,推測可能原因為該研究采用的高強度、短時的刺激模式并不是針對卒中慢性期的最佳方案。
相較于NMES,PES利用帶電極的腔內導管深入至咽部進行刺激,更適用于氣管切開的吞咽障礙和較嚴重的吞咽障礙患者[14]。由于氣管切開改變了正常吞咽時氣道內壓力高于大氣壓的情況,導致食團更易掉入氣管,且患者不能通過用力咳嗽來清除滲漏誤吸,據報道,43%~83%的氣管切開患者存在誤吸[15]。Jayasekeran等[16]通過前驅研究認為PES每日1次,每次刺激10 min,連續治療3 d為較佳干預方案,之后在急性卒中患者中進行了驗證,顯示PES干預組PAS>3分的患者比例顯著低于假刺激組。Fraser等[17]使用5 Hz的PES,以患者最大耐受強度的75%對16例急性卒中后吞咽障礙的患者進行10 min治療,治療后患者PAS評分的降低具有統計學意義,且吞咽啟動反應和咽部皮質的興奮性均得到了顯著提高,誤吸的改善與吞咽皮質興奮性的增加呈正相關性。Suntrup等[18]對重癥監護病房中成功脫離呼吸機但伴有嚴重吞咽障礙的卒中患者進行連續3 d的PES治療,PES組治療結束后72 h內成功拔管率顯著高于假刺激組(75%vs. 20%)。Dziewas等[19]進行了1項多中心、前瞻性、單盲、安慰劑平行隨機對照試驗,也取得了與Suntrup的研究相似的結論。不過Bath等[20]進行的納入162例卒中吞咽障礙患者的多中心隨機對照試驗,主要結局指標為PAS,次要結局指標為吞咽障礙的嚴重程度、功能狀況、生活質量和不良事件的發生率,結果顯示,與假刺激組相比,PES治療對上述指標均未達到有統計學意義的改善,研究者認為可能是該研究中納入患者的吞咽障礙程度較輕,患者功能的自愈掩蓋了PES的療效。
2.1.2 外周磁刺激 近年來國內外開始探索重復外周磁刺激(repetitive peripheral magnetic stimulation,rPMS)用于治療吞咽障礙的安全性和可行性。Momosaki等[21]在2015年嘗試對8例雙側卒中的吞咽障礙患者聯合應用rPMS和一般吞咽康復訓練,rPMS作用于舌骨上肌群,每次治療10 min,每日2次,持續6 d,初步驗證了rPMS治療吞咽障礙、減少誤吸的可行性和有效性,但該試驗并未設置對照組。馬明等[22]在Momosaki的研究基礎上對60例卒中亞急性期吞咽障礙患者聯合rPMS與常規吞咽功能訓練,并將干預時間延長為4周。治療后實驗組與對照組的PAS均較治療前明顯改善,且實驗組顯著優于對照組。Momosaki等[23]還招募了10位健康志愿者,探究不同頻率(20 Hz和30 Hz)的rPMS對吞咽相關運動皮層興奮性的影響,結果顯示這2種頻率刺激均可使皮質產生的MEP振幅顯著增加,且效應可一直維持到刺激后30 min,2組間的MEP差異無統計學意義。張云等[24]對比了rPMS與NMES治療卒中后咽期吞咽障礙的療效,結果顯示rPMS組的PAS改善程度顯著優于NMES組(治療后2.56±0.66分vs. 3.25±1.12分),提示rPMS可能對感覺通路輸入、吞咽肌群運動與協調有更大的激活效應。
2.2 吞咽皮質區刺激 無創大腦調控新技術實現了臨床對卒中等大腦神經系統損傷的直接、安全干預,主要方法有重復經顱磁刺激(repeated transcranial magnetic stimu lation,rTMS)和經顱直流電刺激(transcranial direct current stimulation,tDCS)。1項meta分析顯示這2種調控技術均可以改善卒中患者的吞咽障礙預后和嚴重程度評分(dysphagia prognosis and severity scale,DOSS)、標準吞咽功能評價(standardized swallowing assessment,SSA)、PAS等指標,且在改善功能障礙和減少誤吸發生上,rTMS優于tDCS[25]。
功能MRI的研究已證實大腦皮質存在多個吞咽功能區,目前臨床上多選擇下頜舌骨肌皮質代表區作為刺激部位[26]。下頜舌骨肌屬于舌骨上肌群,可幫助舌骨上抬,增強該肌肉的力量有利于加速吞咽啟動,減少誤吸與吸入性肺炎的發生。Park等[27]研究高頻rTMS對卒中后吞咽障礙患者下頜舌骨肌皮質的影響,將患者分為雙側皮層刺激組、患側皮層刺激組和偽刺激組,連續治療2周,結果顯示雙側刺激組的PAS改善最顯著。Zhong等[28]探討了高頻rTMS刺激卒中吞咽障礙患者健側半球、患側半球和小腦3個部位的療效。治療后,3組治療的PAS均顯著優于對照組,提示刺激上述3個部位對吞咽障礙均有積極作用。華何柳等[29]在治療期間的上午將tDCS陽極電極置于卒中后吞咽障礙患者的患側半球,下午將陽極電極換到健側半球,每次治療20 min,每周5 d,持續4周,治療后實驗組的飲水誤吸、攝食誤吸和總誤吸率均低于對照組,差異有統計學意義。
另外,刺激咽部皮質區的研究也在進行,有學者指出咽部運動感覺皮層興奮性提高表現出的效應可減少誤吸和咽部殘留[30]。這一點也在Fraser等[17]的研究結論中得到印證。Park等[31]將高頻rTMS置于卒中亞急性期患者健側咽部運動皮層,每天治療10 min,干預2周后發現實驗組PAS明顯降低,且這種效果在治療結束2周后仍然存在。試驗組誤吸與食物殘留發生率由66.7%降至33.3%,而對照組無明顯變化。Lim等[32]對比了健側半球咽部運動皮層低頻rTMS和NMES治療卒中亞急性期患者的效果。每次治療20 min,每周5 d,連續2周。治療結束后rTMS和NMES組的PAS均顯著低于對照組,2組間差異無統計學意義。李小霞等[33]對腦干卒中后吞咽障礙患者給予tDCS陽極交替刺激雙側大腦半球口咽部皮層感覺區,每次治療20 min,每日2次,治療3周后,實驗組在吞咽造影下觀察的誤吸情況和PAS較治療前及對照組均明顯改善。
2.3 迷走神經刺激 除外周肌群與大腦皮層刺激以外,研究者還開始嘗試將電、磁刺激放置于吞咽外周神經的解剖定位點上。迷走神經中的喉下和喉返神經運動纖維支配氣道關閉,喉上神經負責會厭及氣道內組織黏膜的感覺,在正常氣道保護調控中發揮著重要作用。有研究者嘗試使用rTMS刺激迷走神經來使腦干卒中患者的吞咽功能恢復,結果顯示,與基線相比,實驗組治療后環咽肌的MEP振幅顯著增加,潛伏期顯著縮短,PAS平均降低了1.2分,而假刺激組的所有結局指標均無顯著變化[34]。阮麗英等[35]聯合rTMS刺激迷走神經和間歇性管飼治療卒中后吞咽障礙,每次刺激10 min,每日1次,每周5 d,共治療4周。期間實驗組吸入性肺炎的發生率為5.1%,對照組為35.9%,差異具有統計學意義。Yuan等[36]報告了1例采用迷走神經電刺激治療延髓背外側梗死后重度吞咽障礙的案例。該患者治療前不能安全吞咽任何食物,誤吸與咽部殘留嚴重。對其進行每次20 min,每日2次,每周5 d的迷走神經電刺激,治療3周后患者能夠安全進食高稠食物,6周后能夠攝入更稀的液體與固體食物,咽部殘留情況與喉抬升顯著改善。
3 總結與展望
目前多數研究證實電、磁刺激可改善卒中吞咽障礙患者的誤吸,從而預防吸入性肺炎的發生。電、磁療法作用部位廣泛,從肌群到中樞皮層再到周圍神經刺激的每一步探索,體現了吞咽康復領域的研究者們針對神經感覺運動通路治療的設計逐漸完整化,形成了“外周+中樞”的閉環康復模式[37](圖1)。電、磁刺激療法表現出不同優勢:磁刺激對神經激活力度更強、定位更精準、能夠作用到更深層部位;電刺激相對便攜、價格低廉,臨床應用范圍更廣泛。
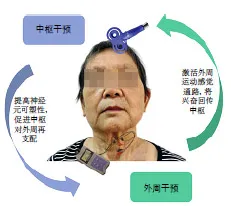
圖1 以“中樞磁刺激+外周電刺激”為例的吞咽康復閉環模型
在電、磁療法預防卒中吞咽障礙吸入性肺炎的主題上,目前將肺炎作為觀測指標的研究仍然較少,期待未來能有更多納入包括肺炎相關生化指標、呼吸功能指標、影像學量化指標等作為評價方法的研究來進一步揭示潛在機制。隨著越來越多外周+中樞聯合干預研究的出現,下一步研究方向或將集中在探尋聯合干預的方式、干預的順序、治療強度、頻率、持續時間、間隔期等多種因素之間更佳的搭配方案。
【點睛】電刺激和磁刺激作為新興的卒中后吞咽障礙相關吸入性肺炎的治療措施,在臨床中不論單獨應用還是互相聯合,以及與其他康復措施聯合治療均顯示出了積極的效果,值得進一步探索其機制和更優化的方案。

