分泌型磷蛋白24 與維持性血液透析患者心臟瓣膜鈣化及心血管事件的相關性研究
王雪榮,許雯婷,包 婷,李新玉,劉桂凌,袁 亮,王德光
血液透析是終末期腎臟病患者常用的腎臟替代治療方式。據統計,中國維持性血液透析(maintenance hemodialysis, MHD)患者已近70萬,心血管疾病是MHD患者常見的死亡原因[1]。MHD患者常出現鈣磷代謝紊亂,腎性繼發性甲狀旁腺功能亢進(secondary hyperparathyroidism,SHPT)發病率高,心臟瓣膜鈣化(cardiac valve calcificatio, CVC)和血管鈣化的發生率增加,增加心血管事件(cardiovascular events,CVE)的發生率[2]。研究[3]發現,心臟單個瓣膜鈣化增加患者因心血管疾病所致死亡風險和全因死亡風險,兩個瓣膜鈣化患者心血管疾病所致死亡和全因病死率顯著增加。雖然心血管鈣化影響患者預后,但心血管鈣化的具體機制尚不完全明確。
分泌型磷蛋白24(secreted phosphoprotein 24, SPP24)是主要由肝細胞分泌的蛋白質,與胎球蛋白A具有同源性[4]。胎球蛋白A對血管鈣化具有保護作用, 但無SPP24與心血管鈣化的相關性研究。因此,該研究探討SPP24與MHD患者CVC、CVE的相關性,為進一步干預心血管鈣化、改善患者預后提供干預靶點。
1 材料與方法
1.1 研究對象選取2020—2021年在安徽醫科大學第二附屬醫院住院的MHD患者,共88例。該研究已通過安徽醫科大學第二附屬醫院倫理委員會批準(倫理編號:YJ-YX2017-004)。納入標準:① 患者年齡≥18歲;② 透析齡≥3月;③尿素清除指數(KT/V) ≥1.2。排除標準:① 既往有嚴重的風濕性心臟瓣膜病、其他先天性心臟瓣膜疾病患者;② 4周內出現急性心肌梗死患者;③ 既往存在肝癌、肝性腦病患者。
1.2 研究方法
1.2.1一般資料 收集患者的臨床資料如姓名、年齡、性別、身高、吸煙史、飲酒史、糖尿病史和高血壓疾病史、透析齡、近1月服藥史資料。收集患者體質指數(body mass index,BMI)資料。患者近1月服藥史包括是否使用磷結合劑、擬鈣劑、維生素D受體拮抗劑(vitamin D receptor, VDR)等。
1.2.2實驗室相關指標 患者均需行血常規檢查,并完善肝功能、腎功能、血糖、血脂、血鈣、血磷、全段甲狀旁腺激素(intact parathyroid hormone,iPTH)檢查。
1.2.3CVC的評估與分組 所有患者均在安徽醫科大學第二附屬醫院做心臟超聲檢查,評估患者CVC情況。根據心臟彩超結果分為CVC組和無CVC組。CVC分為單個瓣膜鈣化如二尖瓣鈣化、主動脈瓣鈣化,部分患者同時存在2個瓣膜鈣化如主動脈瓣和二尖瓣聯合瓣膜鈣化。
1.2.4SPP24指標檢測 采集患者透析前血液5 ml,采用EDTA抗凝管,以3000 r/min離心5 min,分裝后-80 ℃冰箱留存,以備SPP24指標的測量。SPP24試劑盒購于美國mni.mAbs公司(貨號:OM542174),使用酶聯免疫吸附法(enzyme linked immunosorbent assay,ELISA)測量。樣品采用1 ∶10比例稀釋,測量所得數值乘以10,即為標本的濃度。

2 結果
2.1 臨床資料分析共納入88例維持性血液透析患者,其中男性50 例,女性38例。CVC患者47例,其中主動脈瓣和二尖瓣聯合瓣膜鈣化患者22例。與無CVC組相比,CVC組患者年齡較大(P=0.001),血磷水平升高(P=0.001),差異有統計學意義。見表1。

表1 CVC組和無CVC組患者臨床資料
2.2 各組SPP24水平與無CVC組相比,CVC組患者血SPP24水平降低(P=0.040),差異有統計學意義。與無鈣化和單個CVC組相比,二尖瓣和主動脈瓣聯合瓣膜鈣化患者水平降低(P=0.003)。
使用Spearman方法進行相關性分析,CVC和血SPP24水平變化存在負相關(r=-0.220,P=0.040); 聯合CVC與血SPP24水平也存在負相關(r=-0.318,P=0.003)。
2.3 CVC影響因素分析所有患者均行心臟彩超評估CVC情況,根據評估結果分為CVC組和非CVC組,首先進行CVC單因素Logistic回歸分析,單因素分析中P<0.2的自變量如年齡、透析齡、高血壓、血紅蛋白、血磷、全段甲狀旁腺激素、堿性磷酸酶、SPP24納入多因素分析中。多因素logistic回歸分析提示,年齡增加(Odds Ratio,OR=1.055,P=0.045)、高血磷(OR=8.234,P=0.008)是CVC的危險因素,高SPP24水平(OR=-0.997,P=0.038)是CVC的保護因素。

表2 維持性血液透析患者CVC的影響因素單因素分析

表3 維持性血液透析患者CVC多因素分析
2.4 維持性血液透析患者二尖瓣和主動脈瓣聯合瓣膜鈣化的影響因素本研究中22例患者存在二尖瓣和主動脈瓣聯合瓣膜鈣化。針對聯合瓣膜鈣化的患者進行影響因素分析。首先,對聯合瓣膜鈣化患者進行單因素logistic分析,單因素分析中P<0.2的自變量如年齡、透析齡、高血壓、血紅蛋白、血磷、堿性磷酸酶、SPP24納入多因素分析中。多因素分析發現,年齡增加(OR=1.086,P=0.028)、長透析齡(OR=1.250,P=0.029)、高磷血癥(OR=7.393,P=0.015)均是心臟聯合瓣膜鈣化的危險因素,高SPP24水平(OR=0.964,P=0.025)是心臟聯合瓣膜鈣化的保護因素。

表4 維持性血液透析患者聯合CVC的影響因素分析
2.5 CVE的影響因素88例患者進行2~14月隨訪,24例患者出現心腦血管事件。使用COX模型探討心腦血管事件的影響因素,單因素分析中P<0.2自變量如透析齡、血磷、CVC、SPP24水平納入多因素分析中。多因素分析發現,CVC( hazard ratio,HR=4.156,P=0.034)增加心腦血管事件的發生風險,高SPP24水平(HR=0.976,P=0.038)減少CVE的發生風險。見表5。

表5 維持性血液透析患者CVE影響因素分析
使用COX模型探討二尖瓣和主動脈瓣聯合CVC對CVE的影響。首先,單因素分析中P<0.2的自變量如透析齡、血磷、聯合CVC、SPP24水平納入多因素分析中。多因素COX分析發現,聯合CVC(HR=3.071,P=0.023)增加CVE的發生風險,高SPP24水平(HR=0.996,P=0.030)減少CVE的發生風險。見表6。
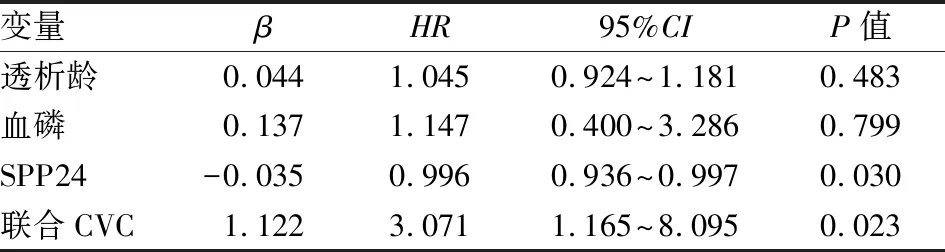
表6 聯合CVC對維持性血液透析患者CVE影響分析
3 討論
該研究發現,MHD患者CVC組SPP24水平顯著降低,多因素分析發現高SPP24水平是CVC的保護因素。對患者進行隨訪分析發現CVC是CVE的危險因素,高SPP24水平是CVE的保護因素。
CVC的發病機制目前尚不完全明確。SPP24主要在肝臟表達,在骨及軟骨細胞中也有表達。既往研究[5]發現,SPP24參與骨關節炎的發生、發展。國外研究[6]發現,SPP24通過拮抗骨形態發生蛋白-2(bone morphogenetic protein 2,BMP-2)的作用,抑制胰腺癌進展。SPP24與MHD患者CVC的相關性未見報道。該研究發現SPP24是CVC保護因素,可能機制包括如下幾個方面:① SPP24主要來源于肝臟,是胎球蛋白A-礦物質復合體(fetuin-mineral complex, FMC)的重要組成部分。FMC包含磷酸鈣晶體,與SPP24、基質Gla蛋白結合形成初級和次級鈣蛋白顆粒,鈣蛋白顆粒在體內儲存高濃度磷酸鈣晶體,阻止血管及軟組織鈣化[7-8]。② 既往研究[9-11]證實,SPP24能與BMP-2結合,從而抑制BMP-2介導的成骨作用。BMP-2能促進平滑肌細胞向成骨細胞轉分化,促進血管鈣化發生;BMP-2也能促進間充質細胞向成骨細胞轉分化,造成CVC[12-14]。推測SPP24可能抑制BMP-2的上述作用,從而對CVC起保護作用。③ SPP24與胎球蛋白A、基質Gla蛋白、磷酸鈣形成復合體,高磷血癥的發生率可能降低,從而延緩CKD患者CVD的發生發進展。
鈣磷代謝紊亂是MHD患者常見的并發癥,安徽省鈣磷水平達標率低,防治形勢嚴峻[15]。該研究表明,高磷血癥是CVC的危險因素,未發現血鈣、iPTH水平和CVC的相關性;考慮與部分患者使用非含鈣磷結合劑,血鈣水平控制尚可相關,納入的MHD患者多伴有難治性腎性繼發性甲旁亢,雖使用活性維生素D3、擬鈣劑等藥物治療,但是藥物治療后PTH控制不理想,所以CVC組和無CVC組患者iPTH無顯著差異。
臨床研究[3]表明,伴有CVC的CKD患者全因死亡風險和心血管疾病所致死亡風險顯著增加。該隨訪研究提示,CVC是CVE的危險因素;高SPP24水平是CVE的保護因素,推測高SPP24水平可延緩患者CVC;SPP24與胎球蛋白A具有同源性,胎球蛋白A對血管鈣化有保護作用[5],因此推測SPP24對血管鈣化可能有保護作用,從而對CVE也有保護作用。在下一步工作中,課題組將通過動物實驗和細胞實驗進行SPP24影響心血管鈣化的機制研究,為有效防治心血管鈣化提供干預和治療靶點。
該研究表明,SPP24水平與血磷水平呈負相關(結果未展示),提示高磷可能抑制SPP24的表達,因此,應積極糾正鈣磷代謝紊亂,提升SPP24的水平,從而抑制心血管鈣化。
該研究顯示傳統危險因素如高血壓、糖尿病與CVC無相關性,可能與本研究納入糖尿病患者所占比例低,高血壓患者血壓控制達標率尚可有關。
綜上所述,高磷血癥、高齡均是CVC患者的危險因素,高SPP24水平是CVC的保護因素。CVC增加CVE發生風險,高SPP24水平減少CVE發生風險。

