甲氧明在缺血性腦卒中伴冠心病患者全身麻醉神經介入手術中的應用
劉 帆, 周東旭
血管內神經介入手術是治療缺血性腦卒中主要方法之一,常在全身麻醉下進行[1-3]。 缺血性腦卒中患者多為老年人,常患有高血壓、高脂血癥、冠心病、糖尿病等多種疾病,機體儲備和心腦血管自我調節功能下降,對麻醉耐受力低,術中輕微的血流動力學波動就易導致心腦血管血流灌注不足,進而增加圍手術期心腦血管意外發生率[4]。 血管活性藥物常用于維持神經介入手術患者血流動力學平穩。一線血管活性藥物多巴胺的藥理作用呈劑量依賴性,小劑量激活外周多巴胺受體,擴張心、腦、腎及腸系膜血管,中等劑量激動心臟β1受體,可提高心率(HR)、加強心肌收縮力;大劑量作用外周α 受體,增加外周血管阻力,升高血壓[5]。多巴胺β1 受體激動作用可增加心肌缺血風險,大劑量應用常引起患者心律失常發生。 一項多中心研究表明,多巴胺應用患者心房顫動(房顫)發生率為20.5%[6]。 甲氧明是α1激動劑,可激動外周血管α1受體,產生收縮作用,升高血壓,增加心腦灌注[7]。 近年甲氧明越來越多地應用于老年患者全身麻醉誘導及術中低血壓預防和治療,同時也廣泛應用于椎管內麻醉低血壓治療、無痛胃腸鏡、腹腔腫瘤熱灌注及顱腦損傷手術患者[8]。 Sun 等[9]研究發現,大劑量應用甲氧明可增加高血壓和心動過緩發生率,且會增加老年患者術后認知功能障礙發生率。 有研究表明,圍術期應用不同血管活性藥物對患者腦組織氧飽和度(SctO2)影響不同[10]。 本研究探討甲氧明和多巴胺對缺血性腦卒中伴冠心病患者的作用,為此類患者臨床應用血管活性藥物提供參考。
1 材料與方法
1.1 一般資料
選擇2019 年至2020 年擬在全身麻醉下擇期行介入手術治療的缺血性腦卒中伴冠心病患者80 例,年齡40~75 歲, 男女不限, 美國麻醉醫師協會(ASA)分級Ⅱ~Ⅲ級。 按數字表法隨機分為甲氧明組(A 組)和多巴胺組(B 組),每組40 例。納入標準:根據病史、體檢、頭顱CT、MR、腦血管造影確診為缺血性腦卒中且血管狹窄程度>75%,有冠心病史。排除標準:腦出血、動靜脈畸形、顱內動脈瘤、心功能Ⅲ級;術前心律失常、嚴重肝腎功能異常、認知功能障礙、精神疾病。 本研究經醫院倫理委員會批準,所有患者均簽署手術知情同意書。
1.2 麻醉方法
術前常規訪視患者, 完善影像學和血液學檢查。 所有患者均禁食6~8 h,禁飲水2 h。 清醒進入手術室后建立兩路外周靜脈通道, 常規監測心電圖、HR、血氧飽和度(SpO2)、無創動脈血壓,Fore-Sight 腦部血氧飽和度監護儀(美國CAS 醫療系統公司)監測SctO2,ICON 無創心輸出量測量儀(德國Osypka公司) 監測心肺功能,VistaTM腦電雙頻指數監護儀(美國Aspect 醫療系統公司)持續監測鎮靜深度;給予復方氯化鈉溶液10 mL/kg 補充生理需要量,后給予咪達唑侖0.05 mg/kg、依托咪酯0.2 mg/kg、舒芬太尼0.3 μg/kg、羅庫溴銨0.6 mg/kg 誘導,可視喉鏡下氣管插管, 妥善固定后接麻醉機控制呼吸,調整呼吸參數潮氣量6~8 mL/kg,呼吸頻率12 次/min,吸呼比1∶2,維持呼吸末二氧化碳分壓為30~35 mmHg(1 mmHg=0.133 kPa);瑞芬太尼(0.2 μg·kg-1·min-1)復合七氟烷(體積分數為0.5%~3%)維持麻醉,調整七氟烷用量使腦電雙頻指數(BIS)維持在40~60;兩組患者于麻醉誘導完成后(T1)至支架植入時(T7)分別持續靜脈泵注射甲氧明(0.5~3 μg/kg-1·min-1)、多巴胺(0.5~10 μg/kg-1·min-1),使血壓波動幅度不超過基礎值20%;支架植入成功后停止泵注,使血壓緩慢下降,防止腦血管再通后缺血-再灌注損傷。 手術結束后停止所有麻醉維持藥物。 待患者清醒,自主呼吸恢復、肌力和咳嗽反射恢復、潮氣量正常后拔出氣管導管。
1.3 觀察指標
觀察并記錄兩組患者麻醉誘導前(T0)、麻醉誘導完成后(T1)、氣管插管即刻(T2)、氣管插管后5 min(T3)、手術開始時(T4)、手術開始10 min(T5)、球囊置入時(T6)、支架植入時(T7)、手術結束時(T8)的SctO2、平均動脈壓(MAP)、HR、心輸出量(CO)、心臟搏出量(SV)、 系統血管阻力(SVR)、每搏變異(SVV)、收縮力指數(ICON)、射血前期(PEP)時間、收縮時間比(STR)變化以及術中不良反應發生情況。
1.4 統計學方法
采用SPSS 21.0 軟件進行統計學分析。 計數資料用χ2檢驗,計量資料用t 檢驗,組內不同時點用重復測量方差分析。 P<0.05 為差異有統計學意義。
2 結果
兩組間年齡、 性別、 基礎疾病及體重量指數(BMI)差異均無統計學意義(P>0.05),見表1。兩組間患者T0~T8 時點SctO2、MAP 差異均無統計學意義(P>0.05);B 組T3~T7 時點HR 高于A 組,差異有統計學意義(P<0.05), T2~T7 時點CO 略高于A 組,差異無統計學意義(P>0.05),見圖1。 B 組T2~T7 時點SV 略高于A 組, 差異無統計學意義(P>0.05); 兩組間不同時點SVV 差異均無統計學意義(P>0.05);兩組間T1 時點SVR 均低于T0 時點,且T2~T6 時點A 組SVR 高于B 組,差異有統計學意義(P<0.05);兩組間T1 時點ICON 值較T0時點減少,PEP 時間、STR 較T0 時點增高, 差異均無統計學意義(P>0.05),T2~T8 時點ICON、PEP 時間、STR 差異均無統計學意義(P>0.05),見圖2。 A組心律失常和心肌缺血發生率低于B 組,差異有統計學意義(P<0.05),見表2。

表1 兩組患者一般情況比較

圖1 兩組不同時點SctO2、MAP、HR、CO 比較
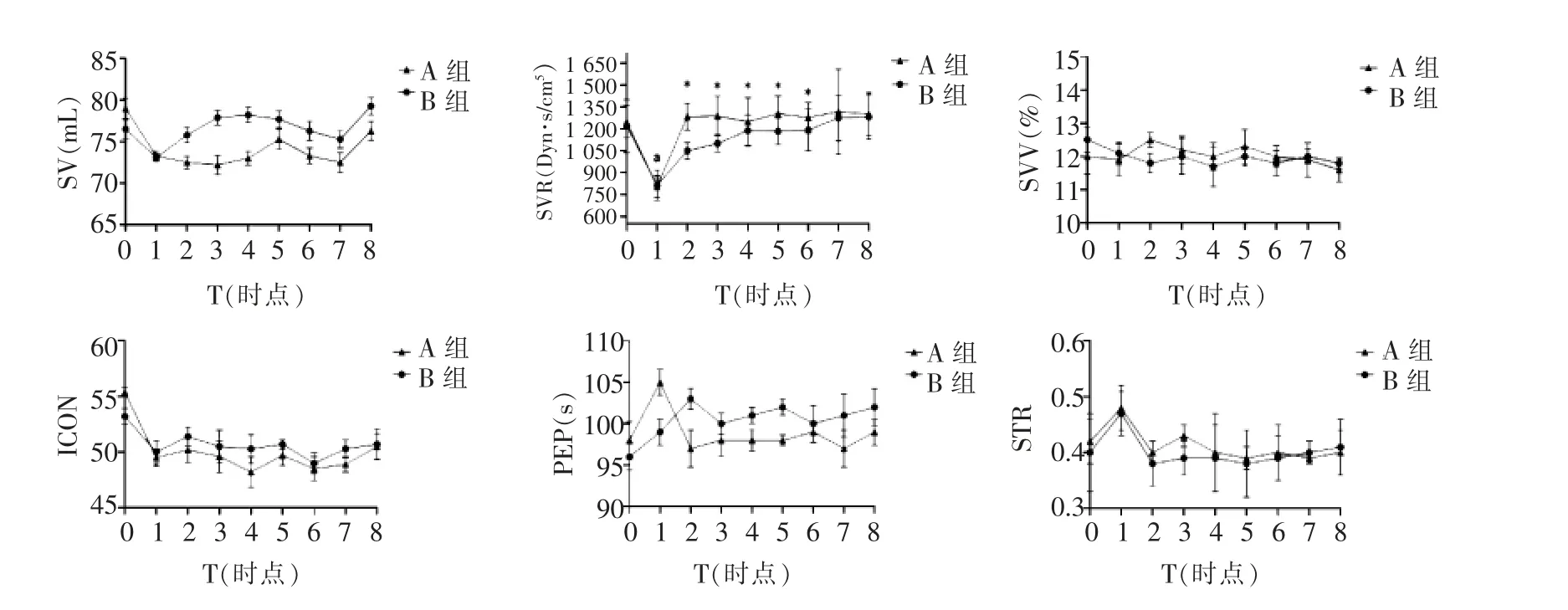
圖2 兩組不同時點SV、SVR、SVV、ICON、PEP 時間、STR 比較

表2 兩組不良反應發生率比較
3 討論
缺血性腦卒中主要由腦血管動脈粥樣硬化、心源性血栓栓塞、腦血管閉塞等引起,常導致患者腦血流障礙、腦組織缺血缺氧性壞死。 腦卒中常發病于老年患者且此類患者常伴發有高血壓、 糖尿病、冠狀動脈粥樣硬化等多種基礎疾病。 全身麻醉藥物應用不僅會抑制心腦血管, 降低心腦血管供血供氧,而且圍術期氣管插管和拔管等操作刺激會增加應激反應,血流動力學劇烈波動會增加心腦血管事件發生率。 因此神經介入手術中不僅要通過血管活性藥物維持患者心腦血管灌注, 而且要加強監測,指導圍術期管理。SctO2是目前臨床上常用的腦灌注監測指標之一, 有利于及時發現腦部缺血缺氧,調整用藥,改善患者預后[11]。 無創心功能檢測儀是利用電子心力測量法,通過頸部和胸部心電傳感器對患者血流量、血流阻力、心肌收縮力及患者液體量進行連續測量,可連續反映心功能變化,對臨床救治具有良好指導意義[12-13]。 因此,本研究采用Fore-Sight 腦部血氧飽和度監護儀和ICON 無創心輸出量測量儀監測患者心腦灌注。
郭小瑋等[14]研究表明,甲氧明能維持老年胃腸疾病患者圍術期SctO2和血流動力學平穩, 不增加心腦血管并發癥發生率。 本研究結果與其一致。 大腦局部SctO2可用腦血流量和腦代謝比值表示,反映大腦氧合狀態,臨床上常用于間接反映腦血流量變化。 本研究中兩組患者均接受相同的麻醉手術方式,可認為腦代謝情況相對恒定,此時SctO2變化主要與腦血流量相關; 兩組SctO2差異無統計學意義提示患者腦血流平穩,這可能與兩種藥物維持患者MAP 水平有關。全身麻醉藥物可減少患者外周血管阻力,使左心收縮功能減低,左心SV 降低,一定程度減少全身血流和組織灌注[15-16]。 因而本研究中兩組患者T1 時點MAP、SVR、ICON 均低于T0 時點,PEP 時間、STR 較T0 時點增高。 劉中光等[17]研究表明,神經介入手術患者支架植入成功后停止輸注多巴胺,血壓短時間回降,不會產生持續高血壓而增加缺血-再灌注損傷風險。 本研究中兩組患者MAP水平差異無統計學意義,且支架植入后停止輸注兩種血管活性藥物,血壓均在短時間內下降,也未產生腦血管再通后缺血-再灌注損傷。 張樹峰等[18]研究表明, 缺血性腦血管病伴冠心病患者介入手術治療中應用多巴胺,心肌缺血、心律失常等心臟并發癥發生率更高。本研究結果與其一致。這是由于中等劑量多巴胺可激動心臟β1受體,增加心肌氧耗量, 而甲氧明在增加外周血管阻力的同時反射性降低HR,不僅增加冠狀動脈灌注,而且不增加心肌氧耗,能更好地保護心肌,改善心肌缺血缺氧現象[19-20]。
綜上所述,缺血性腦卒中伴冠心病患者全身麻醉下行神經介入手術時靜脈泵注射甲氧明和多巴胺,均能維持患者SctO2和血流動力學平穩,但甲氧明能增加外周血管阻力,提高冠狀動脈血流,降低HR,減少心臟做功,降低心臟并發癥發生,對冠心病患者更有利。

