經顱多普勒超聲在VA-ECMO患者腦血流動力學評估中的觀察性研究*
呂盛秋,呂 宇,黃京菊,覃 濤,楊 耿,楊葉桂,盧俊宇**
(1.廣西醫科大學第二附屬醫院重癥醫學科,廣西南寧 530007;2.廣西醫科大學第二臨床醫學院,廣西南寧 530007)
經顱多普勒超聲(Transcranial Doppler Ultrasound,TCD)是一項重要的無創腦監測技術,近年來在各類重癥神經損傷患者中已進行了大量研究并被廣泛應用,包括重型顱腦創傷、膿毒性腦病、心肺復蘇后缺血缺氧性腦病等[1-4]。而接受體外膜肺氧合(Extracorporeal Membrane Oxygenation,ECMO)支持治療的患者亦存在發生各類急性腦損傷的高危風險[5],特別是接受動脈靜脈體外膜肺氧合(Venoarterial Extracorporeal Membrane Oxygenation,VA-ECMO)治療的患者,因心臟泵血功能下降導致機體血流動力學紊亂,往往表現為平均動脈壓(Mean Arterial Pressure,MAP)下降、脈壓差(Pulse Pressure,PP)變小,進而導致腦灌注不足。利用TCD在VA-ECMO治療的患者中進行相關腦血流動力學評估,有助于早期發現該類患者是否發生腦損傷及其病理生理學變化,便于病情判斷。本研究擬通過TCD監測VA-ECMO患者腦血流動力學,分析腦血流參數變化與患者脈壓、ECMO流量的關系,為指導臨床治療提供依據。
1 對象與方法
1.1 研究對象
2020年11月至2022年1月廣西醫科大學第二附屬醫院收治的行VA-ECMO支持治療的成人患者(年齡>18歲),共16例。本研究為前瞻性觀察研究,經患方知情同意并經廣西醫科大學第二附屬醫院倫理委員會批準。
1.2 方法
1.2.1 臨床治療
所有納入患者均采用股靜脈和股動脈置管方式放置ECMO導管;在ECMO轉機后,對患者常規進行鎮靜鎮痛、呼吸機輔助通氣(保護性通氣策略),通過調節呼吸機和ECMO氣流使血氣二氧化碳分壓(PaCO2)維持在35-45 mmHg;當紅細胞壓積<30%時輸注紅細胞,血小板計數小于100×103/mm3時輸注血小板;通過使用肝素維持活化凝血時間(ACT)目標在180-220 s;同時盡量維持MAP在70-80 mmHg[6],若此時PP≤10 mmHg,予降低后負荷處理使MAP進一步降低至60-75 mmHg[7],并維持ECMO流量在4.0 L/min以上。
1.2.2 觀察指標
(1)基礎數據。根據轉機后脈壓差是否大于10 mmHg將納入觀察的VA-ECMO患者分為兩組,A組PP>10 mmHg,B組PP≤10 mmHg。記錄兩組VA-ECMO治療患者的一般資料特征,急性生理和慢性健康狀況評估(APACHE Ⅱ)評分、全面無反應性量表(FOUR)評分、血管活性藥物評分(VIS)、ECMO治療時間、ICU住院時間、出院時腦功能表現分級(Cerebral Performance Category,CPC),其中CPC 1-2級為神經功能預后良好,CPC 3-5級為預后不良。若住院期間顱腦CT證實存在腦梗死、腦出血、腦水腫、缺血缺氧性腦病或有癲癇癥狀發作,則認為患者ECMO治療期間出現神經系統并發癥并記錄。
(2)血流動力學管理指標。記錄兩組患者行TCD檢查時的MAP、PP、ECMO血流速度、患者尿量。
(3)相關生物標志物。記錄患者上ECMO 24 h內的紅細胞壓積、ACT、降鈣素原(Procalcitonin,PCT)。
(4)TCD監測。使用TCD(以色列瑞邁德有限公司,Digi-Lite,2.0 MHz探頭)在患者ECMO轉機后24 h內獲取相關腦血流參數,包括雙側大腦中動脈(Middle Cerebral Arterys,MCA)血流頻譜形態、收縮期血流速度(Vs)、舒張期血流速度(Vd)、平均血流速度(Vm)、阻力指數(RI)、搏動指數(PI),并計算腦血流指數(Cerebral Blood Flow Index,CBFi,CBFi=10 MAP/1.47PI)。
(5)統計學方法。采用SPSS 25.0軟件對數據進行統計學處理。正態分布的計量資料以均數±標準差表示,組間比較采用t檢驗;非正態分布的計量資料以四分位數間距表示,組間比較采用Mann-Whitney U檢驗。計數資料用例數(%)表示,組間比較采用卡方檢驗。P<0.05認為差異有統計學意義。
2 結果與分析
2.1 一般臨床資料與實驗室結果
共納入16例VA-ECMO支持治療患者,其中男性10例,女性6例。上ECMO的原因有急性心肌梗死6例(37.5%)、心臟術后低心排綜合征4例(25%)、暴發性心肌炎2例(12.5%)、心肌病3例(18.75%)及肺栓塞1例(6.25%)。其中,順利撤除ECMO的患者A組8例(80%),B組2例(33.33%),差異無統計學意義(P>0.05)。出院時表現為CPC 1-2級的患者A組4例(44%),B組1例(20%),差異無統計學意義(P>0.05);16例患者中有2例因家屬放棄治療無法確定其神經功能結局。12例患者在ECMO期間或ECMO撤機后完成了CT檢查,其中6例CT有陽性發現,A組和B組各3例。A、B兩組MAP及ECMO流量差異均有顯著意義,B組MAP低于A組[(59.44±15.54)mmHg vs (77.93±8.68) mmHg,P=0.008],B組ECMO流量高于A組[(4.29±0.88)L/min vs (3.37±0.74) L/min,P=0.041](表1)。
2.2 TCD腦血流動力學監測結果
兩組患者腦血流動力學結果如表2所示,相較于PP>10 mmHg組(A組),PP≤10 mmHg組(B組)患者MCA的Vs、Vm有所下降,但差異無統計學意義,兩組患者兩側MCA的CBFi差異亦無統計學意義。B組患者右側MCA的PI值[0.32(0.14,0.48)]較A組[0.68(0.33,0.82)]明顯下降(P=0.039),右側MCA的RI值[0.26(0.12,0.37)]較A組[0.47(0.27,0.52)]也明顯下降(P=0.039),二者差異均有統計學意義。
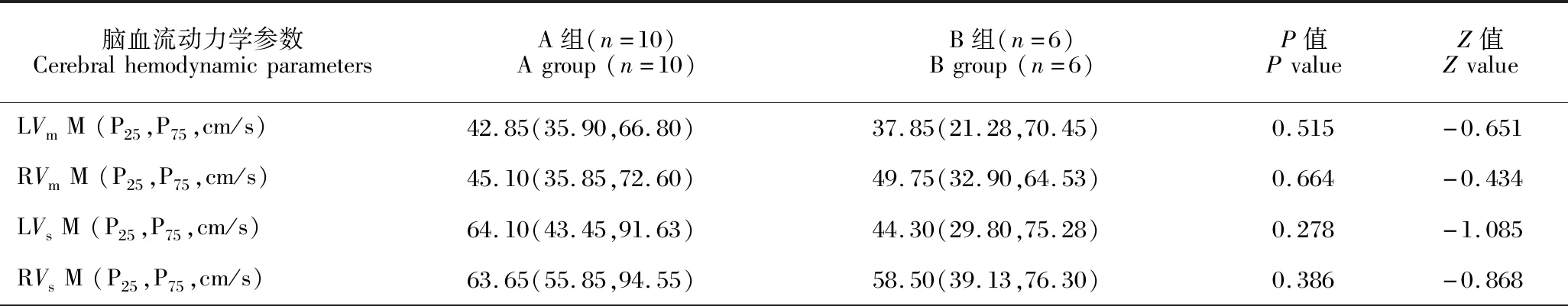
表2 不同脈壓差患者TCD腦血流參數Table 2 TCD cerebral blood flow parameters of patients with different pulse pressure differences
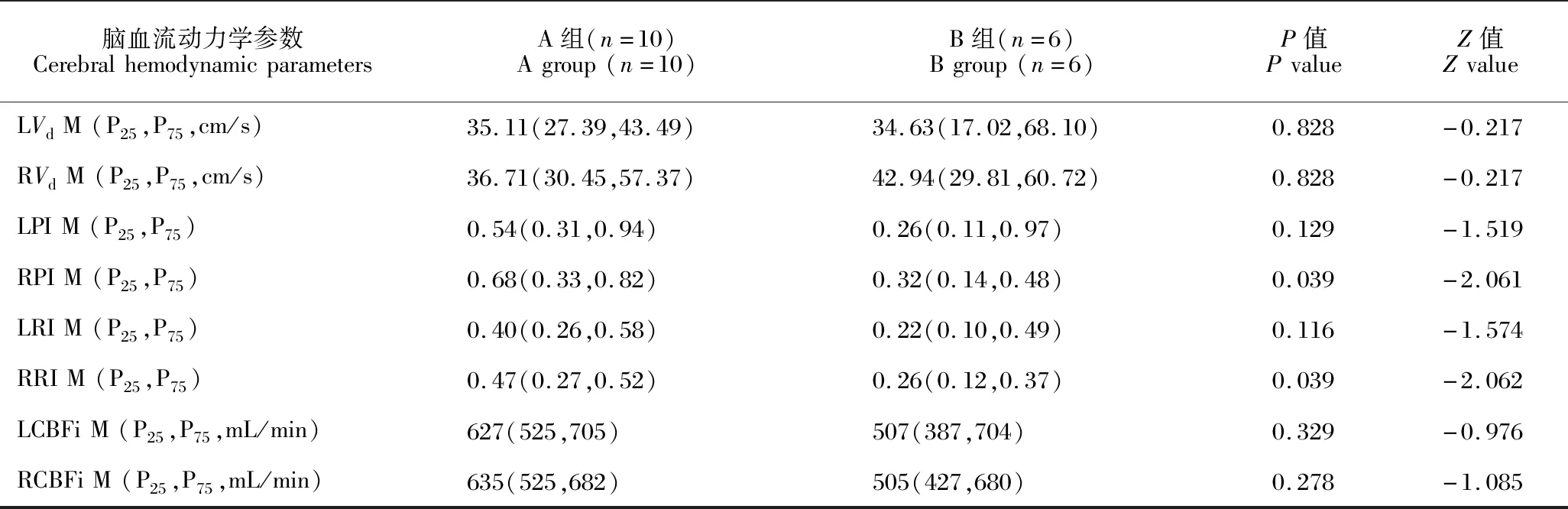
續表Continued table
3 討論
危重患者的血流動力學紊亂會導致包括大腦在內的器官灌注不足。有研究報道VA-ECMO輔助治療期間患者神經系統并發癥的發生率為15%,主要有腦死亡、腦梗死、腦出血和癲癇四大類[8]。大腦作為人體的生命中樞,保證腦灌注是診療過程的重中之重,臨床上判斷機體器官灌注常用的指標有神志、尿量、乳酸,但是在危重患者中鎮靜鎮痛藥物的使用、急性腎損傷所致無尿等使上述項目判斷受到限制,腦灌注及腦功能的評估則需要更客觀、可視的檢測手段輔助判斷。TCD具有無創、安全、操作簡單、可重復監測的優點,大量研究證實了TCD在腦灌注、腦血管調節能力以及是否發生腦血管痙攣、顱內高壓、腦死亡等腦損傷方面有預判作用[3,9-11]。而ECMO是一種需要精細管理且費用昂貴的支持治療手段,在治療的過程中更需要實時動態評估各重要器官的灌注,特別是評估大腦中樞的灌注是否充足,有無發生嚴重腦損傷。利用TCD可直觀了解ECMO患者的腦血流變化并判斷腦灌注情況。有學者認為VA-ECMO期間腦血流減少和非搏動性血流可能在腦損傷的發病機制中起作用[12],因此本研究的主要對象為接受VA-ECMO治療的患者,觀察分析其出現脈壓大于10 mmHg以及脈壓下降甚至平流時的腦血流參數特點。
影響腦血流的首要因素是血壓,而在VA-ECMO時ECMO流量也是重要影響因素。脈壓差小于10 mmHg時可認為心肌頓抑、心臟泵功能衰竭,可能反映了左室擴張的發生[7,13]。本研究發現,當脈壓差明顯小于10 mmHg時,MCA血流頻譜形態也和外周動脈血流壓力波形一樣表現為平流或者趨向平流[圖1(a)],MCA血流下降,其中Vs、Vm下降,同時右側MCA的PI值也明顯下降,這與Kavi等[14]的研究一致,此時低PI受心功能影響,不應誤認為是腦血管擴張或腦血流停滯。當心肌頓抑或心臟驟停時,腦灌注只能依靠提高ECMO流量來維持[15],當患者血流形態為非搏動血流時,其腦血流形態與正常生理狀態及心泵功能尚存的其他疾病狀態均不同,此時多少血流量能保證腦灌注,又該使用何種腦血流指標判斷病情及預后仍未明確,這也是筆者開展此研究的原因。在一項兒童VA-ECMO的研究中發現,PI的增高可能提示患兒存在急性神經損傷[16]。本研究中有6例患者顱腦CT發現存在腦出血或腦梗死,但其PI普遍偏低或正常,僅有1例PI高于正常,但本研究例數較少,無法證實PI與腦血管事件的相關性,能否使用PI預判成人VA-ECMO患者發生急性神經系統并發癥仍待進一步研究。另外還發現1例急性心肌梗死導致心臟驟停后行VA-ECMO治療的患者的脈壓差低于10 mmHg時ECMO流量為4.7 L/min,此時大腦中動脈Vs、PI值均較低[圖1(a)],但該患者仍獲得良好神經功能結局,原因可能是充足的ECMO流量維持了大腦平均腦血流速度,使血氧輸送得以保證,而隨著心功能的好轉,PI逐漸恢復至正常生理水平[圖1(b)]。下一步可能需要進一步分析這類患者PI的動態變化與預后的相關性。
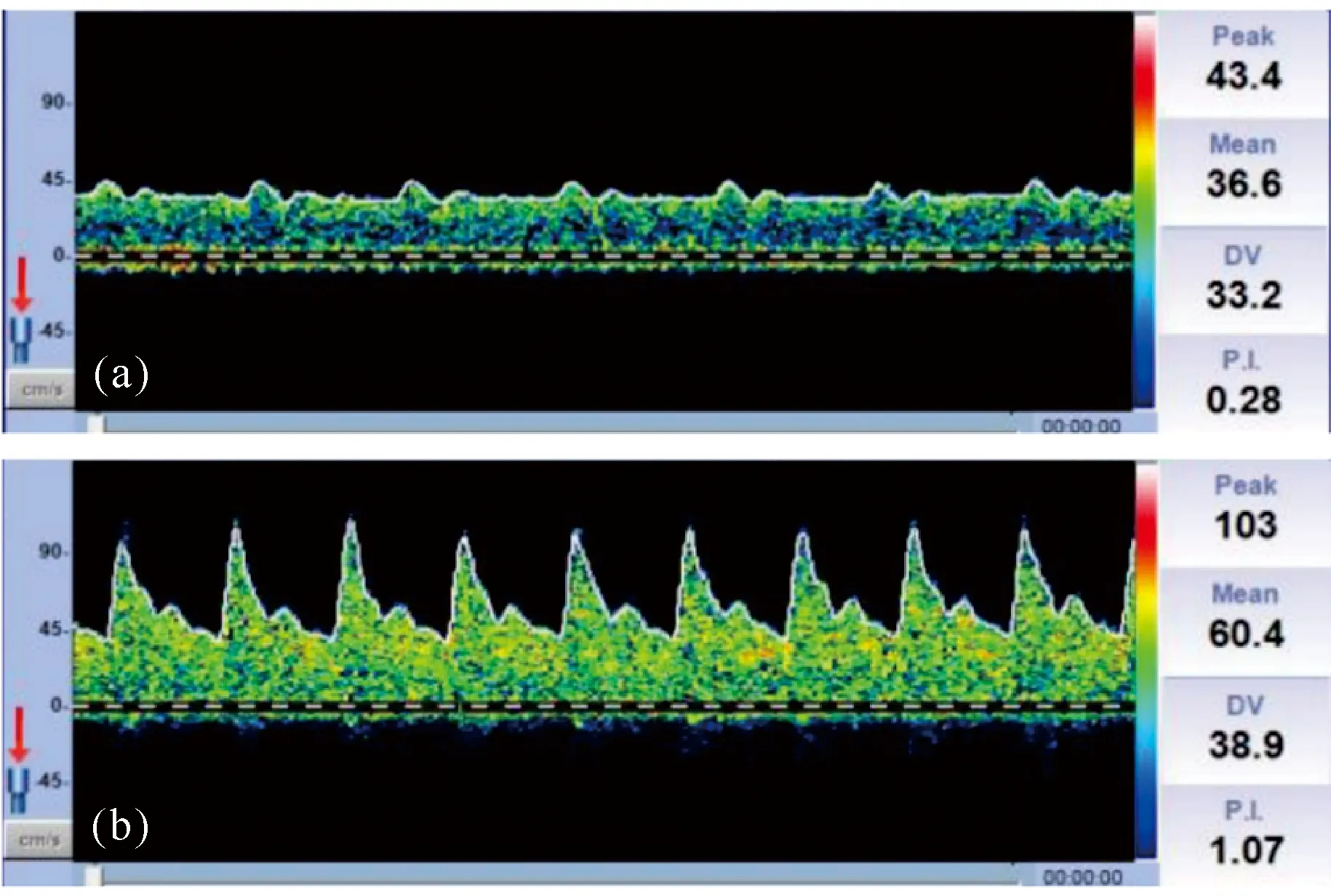
圖1 急性心肌梗死患者行VA-ECMO治療時其腦血流變化情況Fig.1 Changes of cerebral blood flow in patients with acute myocardial infarction treated with VA-ECMO
VA-ECMO治療心功能衰竭病人時往往會面臨左心超載的問題,較高的流量及壓力可加重心臟后負荷,而較低的壓力可能又無法保證患者腦血流灌注,因此MAP往往需要控制在相對較低但又能保證器官基本灌注的水平,通過優化ECMO流量、血管活性藥物和液體療法改善左室擴張。但如何尋找VA-ECMO最佳MAP仍懸而未決。有研究通過回顧性分析尋找最佳灌注壓,發現VA-ECMO患者的MAP低于70 mmHg時無一存活[6],但該研究并未觀察及收集患者腦血流的情況,無法了解當時的腦灌注。在本研究中,脈壓差≤10 mmHg的7例VA-ECMO患者均面臨左心超載的問題,均給予了降低后負荷的處理,同時提高了ECMO血流。筆者動態觀察了1例患者從非搏動血流到恢復搏動血流時的腦血流(圖2),為減輕左室超載使用了硝酸甘油,患者MAP曾低至55 mmHg,但其ECMO流量基本維持在4 L/min以上,停用鎮靜鎮痛后該患者蘇醒,且其腦電圖、腦局部組織氧飽和度均未見明顯異常。說明利用TCD動態監測ECMO患者腦血流或許可指導調整最佳MAP及ECMO流量,但仍需設計合理的大樣本臨床對照研究進一步證實。
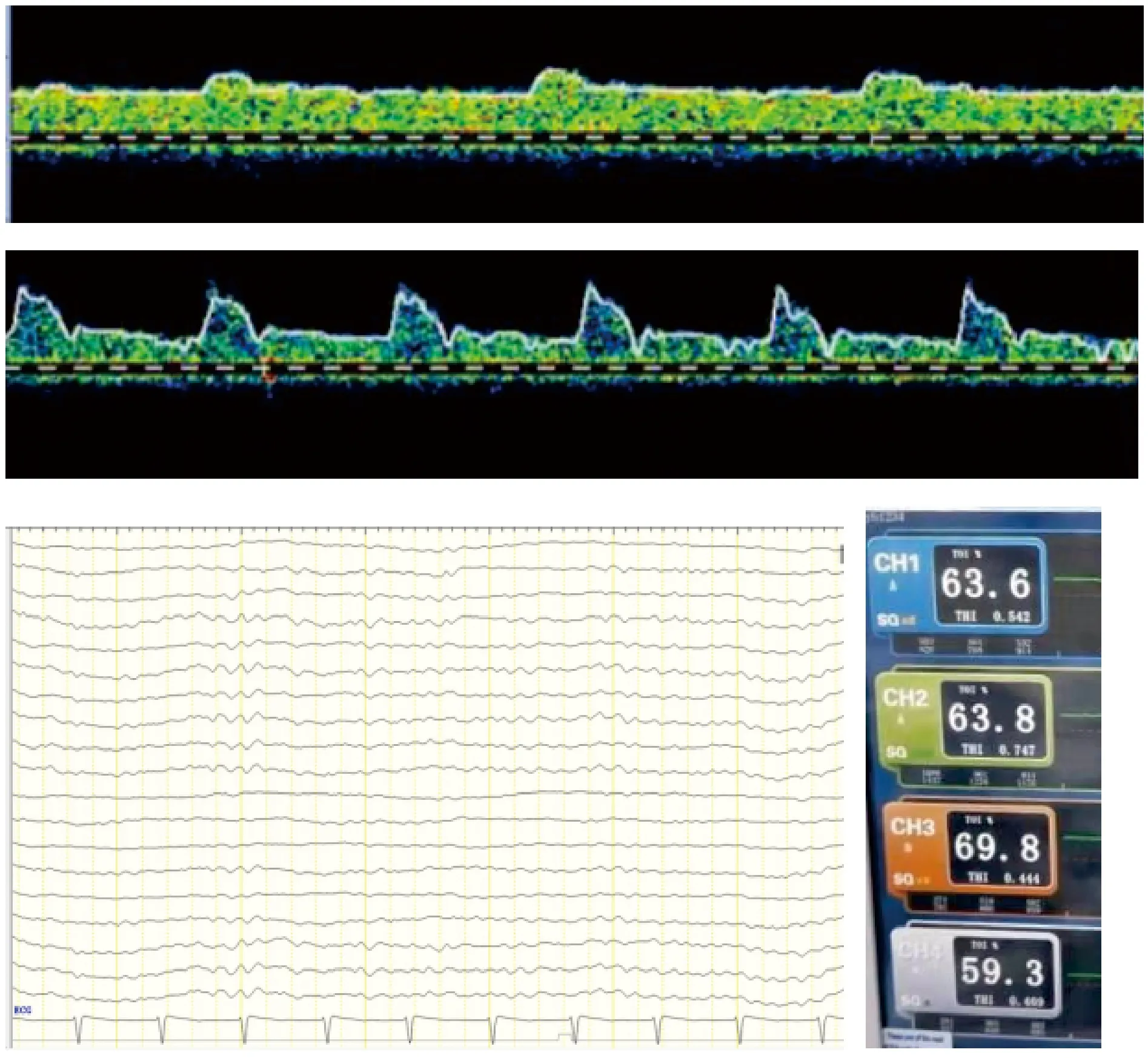
圖2 心臟術后低心排綜合征患者的MCA血流頻譜及其腦電圖、局部組織氧飽和度Fig.2 MCA blood flow spectrum,EEG and local tissue oxygen saturation in patients with low cardiac drainage after cardiac surgery
本研究存在局限性。首先,未能對患者ECMO上機前進行顱腦CT檢查,無法確定其腦血管病變是否發生于ECMO治療前,部分患者因為病情不穩定無法完成CT檢查。其次,由于家屬自動放棄等原因,未能追蹤到這類患者的神經功能結局。最后,因為研究的樣本量較小,結果可能會受影響,且研究僅納入了VA-ECMO患者,不能反映其他人群情況,而VV-ECMO患者也可能存在腦血流動力學異常,未來還需要進一步驗證。
4 結論
在VA-ECMO治療的過程中利用TCD監測該類患者的腦血流動力學具有可行性,TCD在ECMO患者腦功能評估中具有重要指導意義。但利用TCD在早期發現患者神經系統并發癥的證據仍不充分,今后將繼續開展該方向的臨床研究。

