兩種腔鏡入路治療較大體積腎上腺腫瘤的療效分析
徐秀民,左澤平,龔 強,宇洪濤,王月生,謝友弟,朱金海,錢俊杰,王一行,周 軍,吳 俊,李 瑋,楊 超
(1.銅陵市人民醫院泌尿外科,安徽 銅陵,244000;2.安徽醫科大學第二附屬醫院泌尿外科)
腹腔鏡手術治療腎上腺腫瘤始于上個世紀九十年代,具有手術切口小、術中副損傷少、出血量少、術后康復快等優勢,已成為目前微創治療腎上腺腫瘤的首選方式[1-3]。臨床行腹腔鏡腎上腺腫瘤切除術時,較小的腫瘤多經后腹腔鏡三層面或單層面入路切除;體積較大的腫瘤,需根據腫瘤位置、性質、毗鄰情況及術者手術偏好等采取不同的入路[4-5]。本文通過回顧分析48例腹腔鏡下兩種不同入路治療直徑>5 cm的腎上腺腫瘤患者的臨床資料,探討其臨床療效及安全性。
1 資料與方法
1.1 臨床資料 選取2017年1月至2021年8月收治的48例腎上腺腫瘤直徑≥5 cm的患者。入選標準:(1)腎上腺原發腫瘤;(2)腎上腺CT檢查示瘤體直徑≥5 cm;(3)影像學檢查無鄰近臟器侵犯或遠處轉移。排除標準:(1)患有嚴重基礎疾病無法耐受手術;(2)有腹部或腹膜后手術史;(3)瘤體巨大,不適合腔鏡手術。術前患者均行腎上腺CT平掃+增強確診,同時完善腎上腺相關內分泌檢查:促腎上腺皮質激素、血皮質醇、腎素、血管緊張素Ⅰ、血管緊張素Ⅱ、立臥位血醛固酮、兒茶酚胺、電解質等,腫瘤性質經影像學及腎上腺內分泌檢查初步明確。48例患者按手術入路分為兩組,腹膜后組(n=24)與經腹腔組(n=24),其中男16例,女32例,22~75歲,平均(51.08±10.99)歲。腫瘤位于左側25例,右側23例,瘤體直徑平均(6.51±1.22)cm。兩組患者性別、年齡、腫瘤直徑、腫瘤位置及BMI差異無統計學意義(P>0.05),具有可比性,見表1。
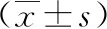
表1 兩組患者臨床資料的比較
1.2 手術方法 經腹膜后組:全身麻醉后留置導尿管,患者取健側臥位,腰部墊高,抬高腰橋;腋后線12肋下切開皮膚約1.5 cm至皮下脂肪層,血管鉗鈍性撐開肌層至腰背筋膜下,手指伸入腹膜后間隙鈍性分離,推開腹膜;自制手套氣囊置入腹膜后腔,充氣500 mL,持續約2 min后退出,在手指引導下,于腋前線11肋緣下穿刺5 mm或12 mm Trocar,腋中線髂嵴上約1.5 cm處穿刺12 mm Trocar作為腔鏡通道,腋后線12肋下穿刺12 mm Trocar后用7號絲線縫合密閉切口并固定;連接氣腹管,壓力維持在12~14 mmHg,置入30°腹腔鏡,觀察后腹腔有無副損傷,超聲刀清理腹膜后脂肪靠背側打開Gerota筋膜(圖1);以腰大肌作為解剖標志,沿腎上腺3個相對無血管層面分別游離背側、腹側、腎上極,充分暴露腫瘤,沿瘤體包膜表面用超聲刀進行游離,尋及中央靜脈后用Hem-o-lok雙重夾閉離斷,完整切除腫瘤;術中游離腹側面時注意避免損傷腹膜,左側操作時注意避免損傷胰尾、脾臟及胸膜;右側操作時注意避免損傷下腔靜脈、十二指腸降段,適當延長手術切口取出標本[6]。再次檢查手術區域無明顯出血后,取出標本,于腔鏡通道留置引流管并固定,逐層縫合關閉手術切口。經腹腔組:全身麻醉后留置導尿管,患者取60°~70°健側臥位,Veress針穿刺臍部建立氣腹。左側采用3枚Trocar,取左側腹直肌旁平臍水平處切開皮膚約1.5 cm,穿刺12 mm Trocar作為腔鏡通道,連接氣腹管,壓力維持在12~14 mmHg,置入觀察鏡,觀察腹腔臟器有無副損傷;直視下分別于左鎖骨中線髂前上棘內上方約3 cm處、左肋緣下腹直肌外緣穿刺12 mm或5 mm Trocar;腫瘤位于右側時,Trocar位置與左側相反,多數情況下需于劍突下增加一個5 mm Trocar作為輔助通道,持針器鉗夾側腹膜向上挑起肝臟,充分暴露手術視野。超聲刀打開結腸旁溝,左側離斷脾結腸韌帶,右側離斷肝結腸韌帶,將結腸向內下側游離(圖2)。沿瘤體包膜分離腎上腺周圍組織,尋及中央靜脈用Hem-o-lok雙重夾閉離斷,完整切除腫瘤;術中左側操作時注意避免損傷胰尾及脾臟,右側注意避免損傷十二指腸及腔靜脈,腫瘤靠近腎門時注意避免損傷腎蒂血管,根據瘤體大小適當延長手術切口取出,留置腹腔引流管并固定,退出腔鏡及Trocar,逐層縫合關閉手術切口。

圖1 清理腹膜外脂肪后超聲刀靠背側縱行打開Gerota筋膜顯露腰大肌
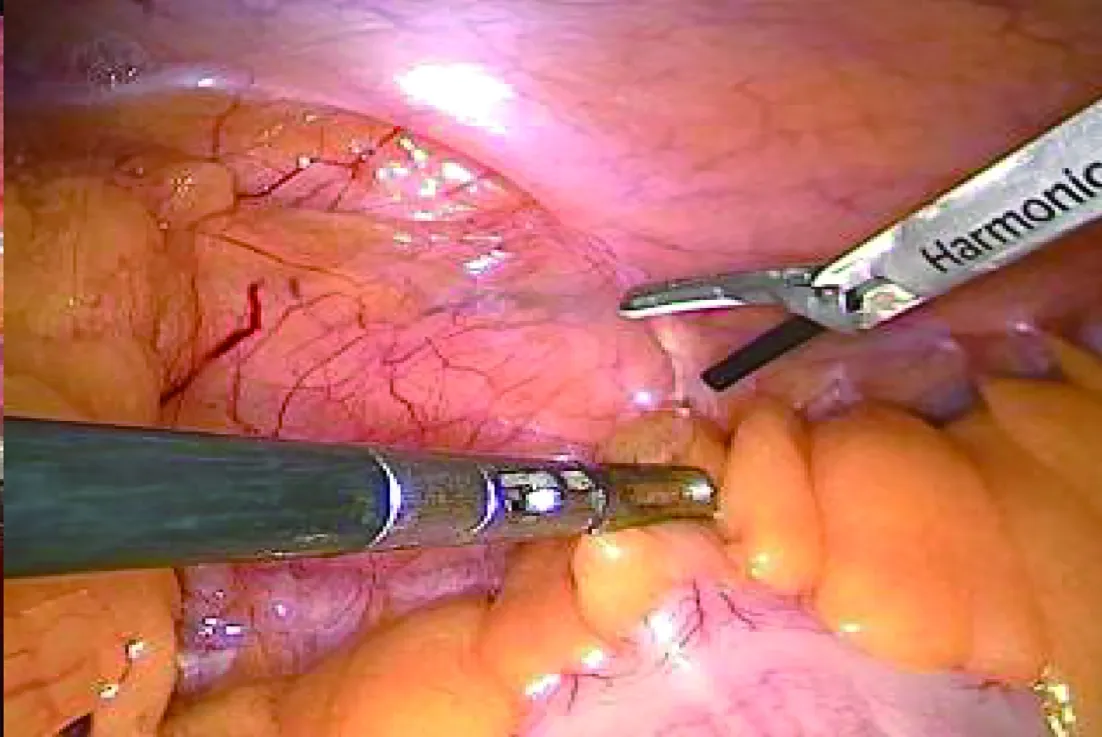
圖2 超聲刀打開結腸旁溝,將結腸游離后向內下側牽拉
1.3 觀察指標 觀察兩組手術時間、術中出血量、術中皮下氣腫例數、術中瘤體破裂例數、術后引流管保留時間、術后首次腸道通氣時間、術后住院時間。
2 結 果
2.1 臨床療效 患者均順利完成腔鏡腎上腺腫瘤切除術,術中無鄰近臟器副損傷、輸血病例及中轉開腹,術后無繼發大出血、感染、腎上腺危象、腫瘤復發等并發癥發生。兩組術中出血量、術后住院時間差異無統計學意義(P>0.05)。引流管基本于術后2~4 d內拔除,兩組引流管放置時間差異無統計學意義(P>0.05)。腹膜后組術中出現瘤體包膜破裂6例(4例髓質脂肪瘤,2例腎上腺囊腫),經腹腔組術中出現瘤體包膜破裂1例,兩組差異有統計學意義(P<0.05)。腹膜后組出現5例皮下氣腫,高于經腹腔組(P<0.05)。總體手術時間長于經腹腔組(P<0.05),在體型肥胖、瘤體較大的患者中,手術時間明顯延長。后腹腔組通氣時間早于經腹腔組(P<0.05)。見表2。
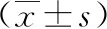
表2 兩組患者圍手術期觀察指標的比較
2.2 隨訪及預后 術后1~3個月復查促腎上腺皮質激素、血皮質醇、腎素、血管緊張素Ⅰ、血管緊張素Ⅱ、立臥位血醛固酮、兒茶酚胺、電解質未見明顯異常,預后良好。
3 討 論
腎上腺解剖位置深,周圍毗鄰重要的大血管及臟器,具有血供豐富、組織包膜脆弱等特點,術中游離過程中容易發生損傷出血導致嚴重并發癥。雖然傳統開放手術存在手術視野顯露困難、創面大、出血多、康復慢、術后并發癥多等不利因素,但對于巨大腎上腺腫瘤或有鄰近器官累及的患者,開放手術仍是重要的手術方式[7]。隨著腹腔鏡醫療設備的更新換代、3D腹腔鏡及超高清腹腔鏡系統的臨床應用,超高清成像系統可將手術區域放大數倍,增加了視野清晰度,避免了術中不必要的副損傷,縮短了手術時間。近年,隨著腹腔鏡技術的進展及臨床實際應用水平的提高,在復雜性泌尿系疾病中的應用也取得了較大的成功[8-10]。兩種腹腔鏡入路有各自的優勢與不足。腹膜后組術中瘤體破裂例數多于經腹腔組,經后腹腔相較經腹腔入路操作空間小,對于較大的腫瘤,操作空間有限,部分腫瘤在分離過程中受到擠壓可能導致包膜破裂,在腫瘤質地較脆(如髓質脂肪瘤、腎上腺囊腫)的患者中更容易發生。經腹腔入路術中解剖標志清晰,手術視野層次清晰,腫瘤顯露較容易,手術出血更容易控制,同時可獲得理想的操作空間進行充分分離,避免腫瘤在游離過程中破裂導致種植性轉移。腹膜后組皮下氣腫例數多于經腹腔組,考慮可能因部分患者腋后線12肋下的Trocar深層組織縫合不嚴密、氣體經軟組織間隙曼延所致,嚴重時氣腫可曼延至頸胸部,術中監測血CO2分壓明顯升高,一般不影響術中操作及患者生命體征,患者多于術后第1天恢復正常。腹膜后組手術時間長于經腹腔組,后腹腔入路操作空間較小,絕大多數需常規清理腹膜外脂肪,對于體型較肥胖的患者,清理脂肪時間明顯延長。瘤體較大及靠近腎門血管時,分離可能導致瘤體包膜破裂、周圍血管損傷、腹膜穿孔,造成瘤體表面滲血、視野模糊、操作空間受限,一定程度上增加了手術難度[11]。經腹腔入路操作空間大,手術視野層次清晰,解剖標志清楚,可獲得理想的操作空間進行充分游離,手術出血更容易控制,可較早顯露鄰近臟器處理中央靜脈,對于雙側病變者亦可同期處理[12-13]。腹膜后組術后首次通氣時間早于經腹腔組,經腹腔入路術中對腸道的游離、牽拉導致術后胃腸道功能恢復慢,術后首次通氣時間延長[14]。經腹膜后入路因腹膜對腹腔消化道臟器的遮擋,術中避免了對腸道分離、牽拉的操作,對術后腸道功能恢復基本無影響,但缺點是經腹膜后操作空間有限,較經腹腔操作空間小,游離暴露較大瘤體時較為困難[7,15]。
根據我們的臨床經驗,不論選擇何種腔鏡手術入路,術中均應解剖層次清晰,避免發生不必要的副損傷;一般腫瘤與正常腎上腺組織交界處較脆弱,切勿用力牽拉撕扯,游離出部分正常腎上腺組織后可用Hem-o-lok夾閉離斷,以保留正常腎上腺組織(圖3)。此外,游離腫瘤過程中盡量不要直接鉗夾腫瘤或包膜,適當提起腫瘤周圍的脂肪組織,沿腫瘤包膜與脂肪之間的間隙細致分離,避免暴力牽拉,以免瘤體破裂出血增加操作難度[16]。對于術前高度懷疑嗜鉻細胞瘤、瘤體巨大(直徑>10 cm)的患者,建議采用經腹入路,一方面可更好地獲得操作空間,另一方面可較早控制腫瘤血供、縮短手術時間。分離腫瘤時更應小心謹慎,避免過度擠壓瘤體釋放兒茶酚胺引起術中血壓波動造成嚴重并發癥。在惡性腫瘤根治方面,經腹腔入路較腹膜后入路同樣具有操作空間大、早期控制瘤體血供的優勢,一定程度上避免了腫瘤擠壓破裂種植轉移及血行轉移的風險。當腫瘤位置較低、靠近腎門血管時,需充分顯露腫瘤周圍的重要血管及臟器(圖4),避免因術中解剖層次不清導致重要血管、鄰近臟器損傷[17]。得益于近年來腔鏡醫療器械、技術水平的發展,在腰腹聯合入路、機器人輔助腔鏡手術治療巨大腎上腺腫瘤方面也取得較大的成功[18-20]。
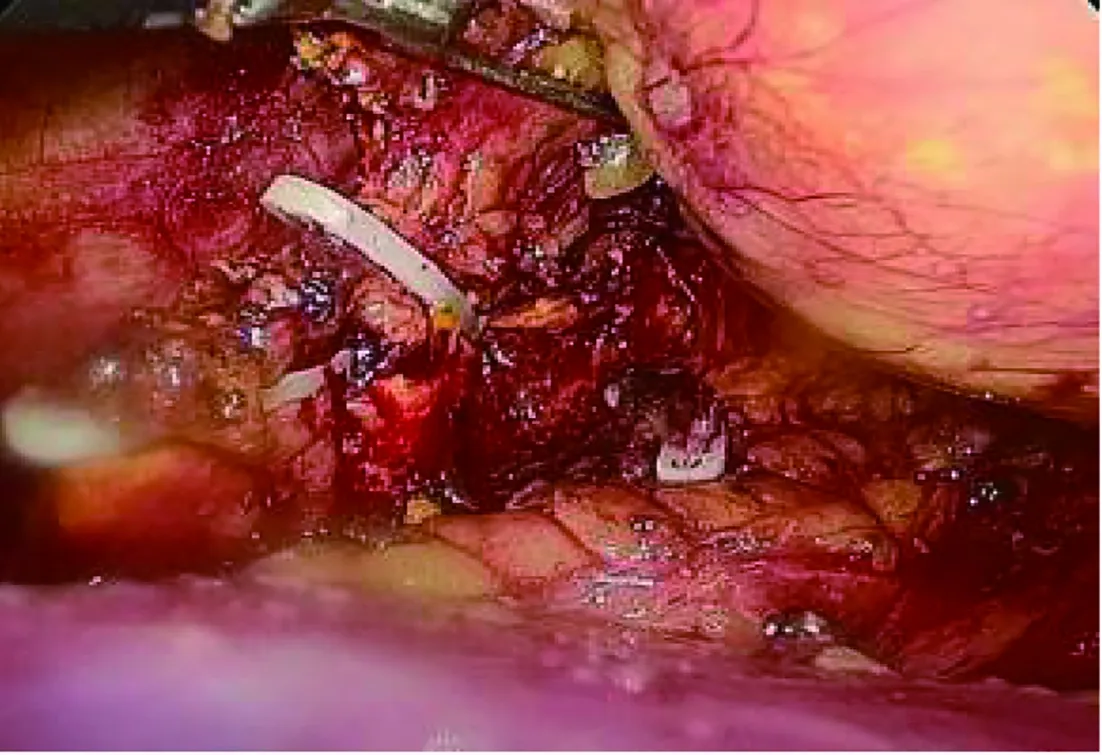
圖3 游離正常腎上腺組織后用Hem-o-lok夾閉離斷,保留部分正常腎上腺組織
綜上,經后腹腔與經腹腔入路切除較大體積腎上腺腫瘤均是可選擇的入路,實際工作中術者應根據患者的個體特征、醫院設備條件及術前影像學檢查綜合評估[21]。同時術前應明確腫瘤性質、大小及鄰近臟器、血管的關系,在臨床實踐中積累經驗,提高手術技能,以期取得最佳的臨床療效。

