醒腦解郁方對卒中后抑郁模型大鼠海馬神經元形態及凋亡的影響
王豆,李濤,馮亞倫,楊一帆,毛美玲,閆詠梅
1.陜西中醫藥大學附屬醫院,陜西 咸陽 712000;2.陜西中醫藥大學,陜西 咸陽 712046
卒中后抑郁(post-stroke depression,PSD)是卒中后常見的神經精神并發癥,表現為除卒中以外的情緒低落、興趣下降、思維悲觀等抑郁癥狀,伴有相應軀體癥狀的綜合征。Meta分析表明,三分之一卒中幸存者出現PSD。PSD是功能恢復不良、生活質量不佳和康復結果不理想的主要因素。PSD涉及心理因素、遺傳易感性、單胺類遞質缺乏、神經營養因子不足、下丘腦-垂體-腎上腺軸失調、神經炎癥、突觸可塑性損傷、神經元凋亡等。陜西省名中醫閆詠梅教授團隊創制的醒腦解郁方臨床治療PSD療效顯著。本研究觀察醒腦解郁方對PSD模型大鼠海馬組織病理形態和凋亡相關蛋白Bax、Bcl-2表達的影響,從海馬神經元凋亡方面探討醒腦解郁方防治PSD的作用機制,為其臨床應用提供依據。
1 實驗材料
1.1 動物
SPF級雄性SD大鼠72只,成都達碩動物實驗公司提供,動物許可證號SCXK(川)2020-030,體質量(200±20)g,飼養于陜西中醫藥大學中心實驗室動物房,自由攝食飲水,適應性喂養1周。
1.2 藥物及制備
醒腦解郁方(石菖蒲12 g,遠志12 g,丹參30 g,柴胡12 g,合歡皮15 g,姜黃10 g,巴戟天10 g),飲片購自陜西中醫藥大學附屬醫院中藥房。所有飲片混勻,加10倍量蒸餾水常規煎煮2次,每次30 min,混合2次煎液,濃縮至原藥材濃度為1.05、2.1 g/mL,置于4℃冰箱保存備用。鹽酸氟西汀膠囊,20 mg/粒,禮來蘇州制藥有限公司,批號7723A,用蒸餾水配制成濃度為0.208 mg/mL溶液。
1.3 主要試劑與儀器
多聚甲醛固定液(武漢塞維爾生物科技有限公司,批號G1101),DAB顯色液(北京中杉金橋生物試劑公司,批號K182720A),中性樹膠(西安灝洋,批號LWG-15),HE染色試劑盒(北京索萊寶科技有限公司,批號G1120),Nissl染色試劑盒(北京索萊寶科技有限公司,批號G1432),RIPA裂解液、蛋白酶抑制劑、磷酸酶抑制劑、BCA蛋白定量檢測試劑盒、5×SDS-PAGE蛋白上樣緩沖液、SDS-PAGE凝膠試劑盒、超敏ECL化學發光液(武漢博士德生物工程有限公司,批號分別為14F27C02、14D28C78、14G02A83、14G30C40、14G22C12、14G29C38、14G10A97),PVDF膜(美國Epizyme,批號280679876),Bcl-2抗體(江蘇親科生物研究中心有限公司,批號BF9103),Bax抗體、β-actin抗體、抗兔二抗、抗鼠二抗(武漢博士德生物工程有限公司,批號分別為BM3964、BM0627、MF094、MF093)。TC-120S型組織脫水機(上海寰熙醫療器械),TB-718E型組織包埋機(湖北泰維科技),RM2235型石蠟切片機(德國Leica公司),DP73型光學顯微鏡(日本Olympus公司),JXFSTPRP-64型全自動樣品快速研磨儀(上海凈信實業發展有限公司),Micro 17R型冷凍離心機(美國Thermo Fisher公司),PowerPac Basic凝膠電泳系統、GelDoc XR+型凝膠成像系統(美國Bio-Rad公司)。
2 實驗方法
2.1 分組、造模及給藥
采用大腦中動脈栓塞(MCAO)聯合慢性不可預知溫和刺激(CUMS)制備PSD大鼠模型。72只大鼠隨機分為假手術組、卒中組、PSD組、氟西汀組和醒腦解郁方低、高劑量組,每組12只。除假手術組外,其余各組采用線栓法制備MCAO模型,大鼠術前禁食禁水12 h,10%水合氯醛腹腔注射麻醉,沿頸部正中縱向切開皮膚及淺筋膜,鈍性分離后,充分暴露并分離頸總動脈、頸外動脈、頸內動脈及迷走神經,結扎近心端頸總動脈、頸外動脈,于頸內動脈近心端穿線備用,將栓線從頸總動脈分叉處插入頸內動脈,深度約18~22 mm,60 min后撤掉栓線,結扎頸內動脈近心端。假手術組僅暴露并分離頸總動脈、頸外動脈、頸內動脈及迷走神經,不插入栓線。術后連續3 d肌肉注射青霉素(4萬U/只)預防感染。術后24 h采用Longa 5分法對大鼠進行神經功能評定,取評分1~3分大鼠進行后續實驗。卒中造模成功后次日,除假手術組、卒中組外,其余各組采用改良CUMS法制備抑郁模型,包括禁食禁水、濕籠、夾尾、強迫游泳、電擊、晝夜顛倒、晃籠,每日給予大鼠1種刺激,7種刺激隨機進行,相鄰2 d刺激不同,連續21 d,造模期間每種刺激共使用3次;同時,氟西汀組予鹽酸氟西汀2.08 mg/kg灌胃;醒腦解郁方低、高劑量組分別予10.5、21 g/kg醒腦解郁方藥液灌胃(相當于60 kg成人劑量的1、2倍),假手術組、卒中組和PSD組予0.9%氯化鈉溶液灌胃,灌胃體積3 mL/只,連續21 d。
2.2 取材
末次給藥結束后,各組隨機取6只大鼠水合氯醛腹腔注射麻醉,斷頭取全腦,冰盤上分離海馬組織,置于4%多聚甲醛中,4℃固定,用于HE染色和Nissl染色。剩余大鼠麻醉后用150 mL生理鹽水進行心臟灌注,迅速取腦,于冰盤上快速分離海馬組織,置于-80℃冰箱凍存,用于Western blot檢測。
2.3 一般狀況觀察
每日觀察并記錄大鼠精神狀態、自主活動、毛色、進食、飲水、糞便情況。
2.4 神經功能缺損評分
給藥結束后即刻,按照Longa 5分法對大鼠進行神經功能缺損評分。0分,無神經缺損;1分,肢體癱瘓側前爪舒展不完全;2分,行走時向肢體癱瘓側轉圈;3分,行走時向肢體偏癱側傾斜;4分,喪失自發行走能力,存在意識喪失現象。
2.5 海馬組織病理觀察
取4%多聚甲醛固定的海馬組織,經脫水、透明、常規石蠟包埋,切片,行HE、Nissl染色,顯微鏡下觀察海馬組織形態變化。
2.6 Western blot檢測
取100 mg海馬測組織,按1∶10加入裂解液(含蛋白酶抑制劑、磷酸酶抑制劑),冰上裂解30 min,超聲勻漿,12000 r/min離心10 min,取上清液,采用BCA法檢測蛋白濃度。加入5×蛋白上樣緩沖液,100℃煮5 min。按30 μg蛋白/孔道上樣,SDS-PAGE分離蛋白,轉移至PVDF膜,加5%脫脂牛奶,室溫封閉1 h。TBST洗膜,加入Bcl-2一抗(1∶1000)、Bax一抗(1∶1000)、β-actin一抗(1∶2000),4℃孵育過夜,TBST洗膜3次,每次15 min,滴加二抗(1∶5000),室溫搖床孵育1 h,TBST洗膜3次,每次10 min。超敏ECL試劑曝光,凝膠成像系統觀察并拍照。利用Image J 2.0軟件分析蛋白條帶灰度值,以β-actin為內參,計算目的蛋白相對表達量。
3 統計學方法

4 結果
4.1 醒腦解郁方對模型大鼠一般狀況的影響
卒中組大鼠精神萎靡,活動尚可,形體較瘦弱,毛色少光澤,毛量減少,飲食與糞便尚可;PSD組大鼠精神萎靡,活動性差,形體消瘦,毛色枯黃,毛量減少,飲食減少,糞便量較少、偶有稀溏;氟西汀組及醒腦解郁方低、高劑量組大鼠精神狀態尚可,活動量增加,毛色有光澤,毛量增多,飲食增多,糞便正常。
4.2 醒腦解郁方對模型大鼠神經功能缺損評分的影響
與假手術組比較,卒中組和PSD組大鼠神經功能缺損評分明顯升高(<0.01);與PSD組比較,氟西汀組及醒腦解郁方低、高劑量組大鼠神經功能缺損評分明顯降低(<0.05)。見圖1。
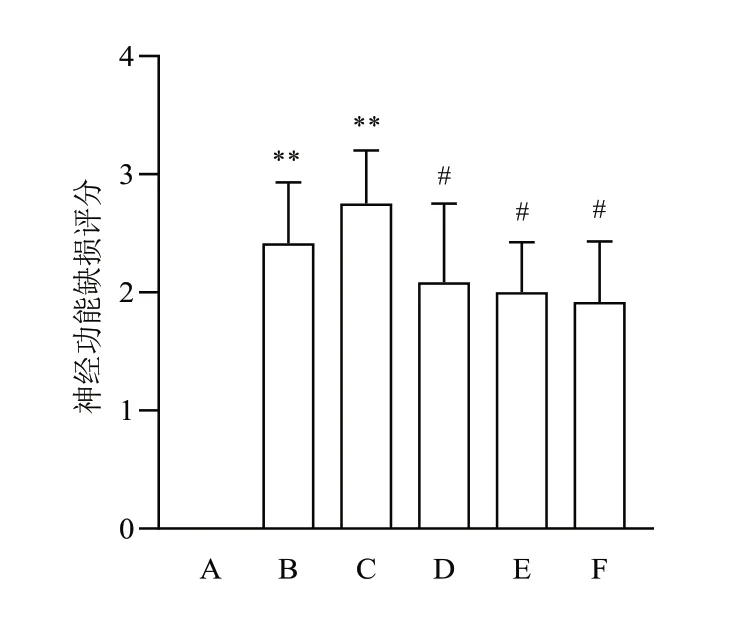
圖1 各組大鼠神經功能缺損評分比較(±s,每組12只)
4.3 醒腦解郁方對模型大鼠海馬組織病理形態的影響
假手術組大鼠海馬組織神經細胞形態完整、排列密集,胞漿染色均勻,核仁清晰,細胞間隙無水腫,尼氏體豐富,未見明顯壞死、炎性細胞浸潤等病理改變;卒中組和PSD組大鼠海馬組織可見部分細胞結構模糊、排列紊亂、數量減少,胞核固縮,尼氏體數量減少,壞死灶邊緣有炎性細胞浸潤;氟西汀組及醒腦解郁方低、高劑量組大鼠海馬組織神經細胞結構較完整,細胞數量較多,排列較為緊密、整齊,尼氏體較豐富。見圖2、圖3。
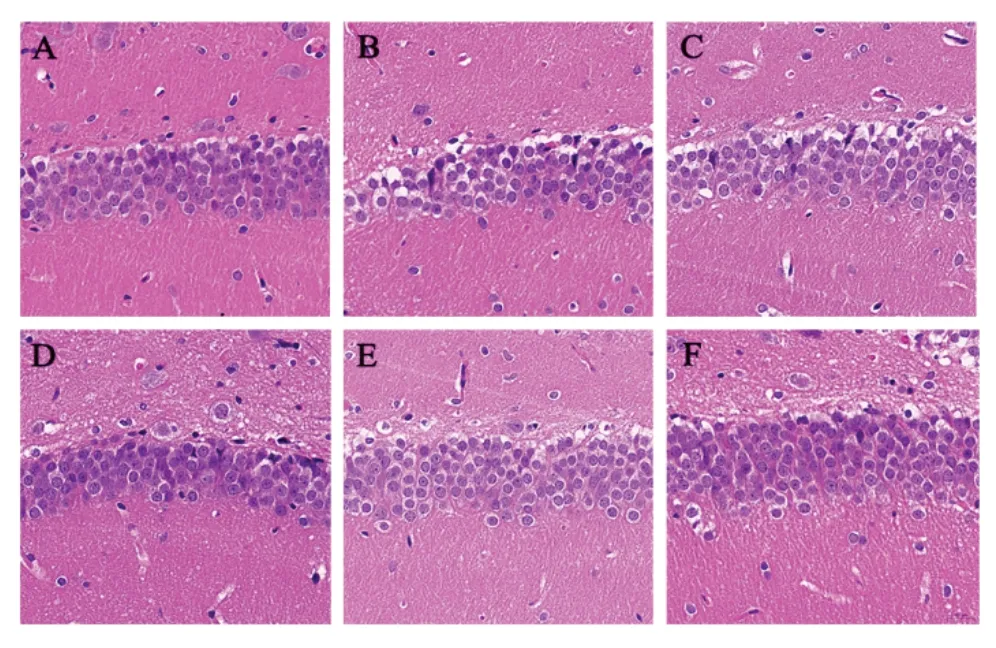
圖2 各組大鼠海馬組織形態(HE染色,×400)
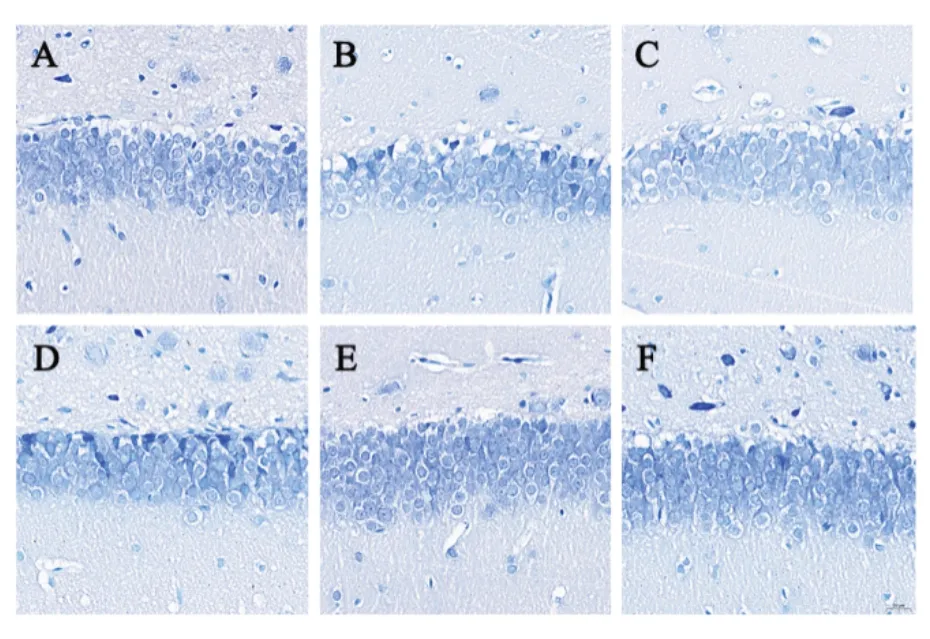
圖3 各組大鼠海馬組織形態(Nissl染色,×400)
4.4 醒腦解郁方對模型大鼠海馬組織Bax、Bcl-2蛋白表達及Bcl-2/Bax比值的影響
與假手術組比較,卒中組和PSD組大鼠海馬組織Bax蛋白表達明顯升高(<0.01),Bcl-2蛋白表達及Bcl-2/Bax比值明顯降低(<0.01);與PSD組比較,氟西汀組及醒腦解郁方低、高劑量組大鼠海馬組織Bax蛋白表達明顯降低(<0.01),Bcl-2蛋白表達及Bcl-2/Bax比值明顯升高(<0.01)。見圖4、表1。
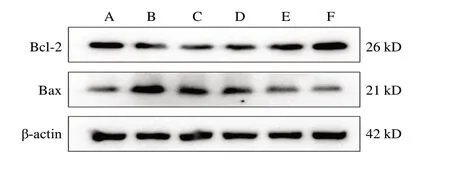
圖4 各組大鼠海馬組織Bax、Bcl-2蛋白免疫印跡

表1 各組大鼠海馬組織Bax、Bcl-2蛋白表達及Bcl-2/Bax比值比較(±s)
5 討論
根據PSD癥狀,可歸屬于中醫學“中風”“郁證”范疇。依據發病次序,為“中風后郁證”,但多從“郁證”論治。西醫學認為PSD是抑郁的一種特殊類型。《CCMD-3中國精神障礙分類與診斷標準(第二版)》將其歸入“腦血管病所致精神障礙”。此外,PSD的臨床表現具有復雜性、多樣性,除具備卒中本身的神經功能損傷癥狀外,還有核心和非核心癥狀之分。其中核心癥狀為抑郁、興趣減退、易疲勞,嚴重者有自殺傾向。非核心癥狀以體質量下降、睡眠障礙、不明原因疼痛、食欲減退或亢進、性欲減退等生理癥狀為主,可伴有注意力下降、緊張不安、焦慮、運動性激越、自責、自罪等。
PSD發生的機制和學說主要包括遺傳機制、社會心理學說、生物學機制等。PSD的遺傳機制與個人、家族史、基因等有關。社會心理學說即生物-心理-社會模式,卒中后患者日常生活質量下降,疾病負擔沉重,家庭及社會環境改變,致患者心理應激障礙,心理平衡失調,導致PSD發生。PSD作為一種器質性情感障礙,其神經生物學基礎主要是5-羥色胺、去甲腎上腺素及多巴胺等單胺類遞質失衡,神經營養因子不足,下丘腦-垂體-腎上腺軸功能異常,機體腸道菌群紊亂,中樞神經系統炎癥因子水平升高,海馬、杏仁核、額葉皮質等部位神經突觸可塑性損傷,細胞自噬與凋亡等。其中神經細胞凋亡在PSD的發病過程中存在持續作用,被認為與PSD等并發癥的發生發展關系密切。
細胞凋亡是一種程序性的細胞死亡,生理情況下有益于機體代謝,病理狀態下則造成組織損傷。卒中后缺血、缺氧導致腦內自由基、谷氨酸、炎癥因子等異常增多,產生細胞毒性作用,進而損傷神經元及突觸可塑性,誘導神經細胞凋亡,影響卒中恢復或導致抑郁等合并癥。線粒體凋亡途徑是細胞凋亡的關鍵環節,Bcl-2蛋白是重要的抗凋亡蛋白,Bax是主要的促凋亡蛋白。Bcl-2/Bax比值可直接反映細胞凋亡狀態,Bcl-2/Bax比值降低提示促進凋亡,升高則細胞凋亡被抑制。已有研究顯示,抑制凋亡可明顯改善神經功能,改善抑郁癥狀。臨床研究顯示,PSD患者血清Bax、Caspase-3等凋亡因子表達顯著升高,藥物逆轉凋亡蛋白表達后,抑郁癥狀明顯改善。動物實驗發現,PSD模型大鼠海馬組織Bax蛋白表達升高,Bcl-2蛋白表達下降。部分抗抑郁藥物可調節海馬組織Bax、Bcl-2蛋白表達,改善PSD大鼠抑郁狀態,可能與促進腦源性神經營養因子(BDNF)表達有關。課題組前期動物實驗發現,醒腦解郁方可通過BDNF/ERK/CREB通路和降低促炎因子表達改善PSD模型大鼠抑郁狀態,發揮明顯抗抑郁作用。因此,本研究進一步探討醒腦解郁方對PSD模型大鼠海馬組織凋亡相關蛋白表達的影響。結果表明,醒腦解郁方可通過上調海馬組織抗凋亡蛋白Bcl-2表達,下調促凋亡蛋白Bax表達,升高Bcl-2/Bax比值,發揮抗PSD作用。
PSD與海馬區神經元萎縮密切相關。影像學研究發現,重度抑郁患者大腦海馬體積有不同程度縮小,突觸數量亦有所減少。動物模型可見海馬超微結構改變,包括海馬樹突萎縮、神經元增殖減少。慢性應激誘導的抑郁動物模型還可觀察到海馬區神經元、膠質細胞均出現萎縮和缺失現象,且上述改變在應用抗抑郁藥物后可逆轉。相較于單純中風患者,PSD患者日常生活質量明顯下降,尤其在認知、情感、肢體功能及社會功能等領域。中風后神經元損傷或凋亡是PSD不良預后的重要原因。減輕神經元損傷,保護神經元存活,促進神經元修復和再生可能是預防和治療PSD的重要手段。當神經元受損時,尼氏體發生溶解和消失。本實驗發現,PSD模型大鼠海馬神經元數量減少、排列紊亂,胞核皺縮、溶解、碎裂,胞漿濃縮,細胞間隙變大,尼氏體數量減少;醒腦解郁方治療后,大鼠海馬組織神經細胞結構較完整,細胞數量較多,形態呈圓形或橢圓形,排列較為緊密、整齊,尼氏體較豐富,表明醒腦解郁方可減輕和修復神經元損傷。
PSD臨床治療以抗抑郁藥物為主,雖具有不同程度療效,然而存在肝腎毒性、撤藥綜合征,增加心腦血管疾病風險等,限制臨床應用。閆詠梅教授將PSD的核心病機概括為痰瘀交阻、氣郁不暢、正氣虧虛,創制醒腦解郁方,臨床應用數十年,療效顯著。醒腦解郁方由石菖蒲、遠志、丹參、柴胡、合歡皮、姜黃和巴戟天組成。藥理研究表明,石菖蒲超臨界萃取物可改善大鼠抑郁樣行為,其主要成分β-細辛醚可通過調節神經元存活發揮抗抑郁作用;遠志活性部位YZ-50可抑制神經細胞損傷和凋亡,發揮抗抑郁作用;丹參酮可保護腦缺血引起的神經元損傷及凋亡;柴胡皂苷A可通過促進海馬區BDNF表達,減少神經細胞凋亡,發揮抗抑郁作用。
綜上,醒腦解郁方可通過改善海馬神經元形態,促進海馬組織抗凋亡蛋白Bcl-2表達,抑制促凋亡蛋白Bax表達,增加Bcl-2/Bax比值,發揮抗PSD作用。

