一步法制備烯丙基糖苷研究
劉文清
(河北科技大學化學與制藥工程學院,河北石家莊 050018)
烯丙基是一位“多才多藝”的明星官能團,其結構中的雙鍵,可發生多種化學反應:如環氧化、雙羥基化、環加成、巰烯點擊化學等(如圖1所示)。眾所周知,復雜多糖的結構改造往往始于其基本組成砌塊如單糖或二糖的化學修飾,而其中還原端烯丙基化是合成多種新型糖綴合物的重要步驟[1-2]。因此,烯丙基糖苷在糖化學合成中扮演著重要角色[3-4]。
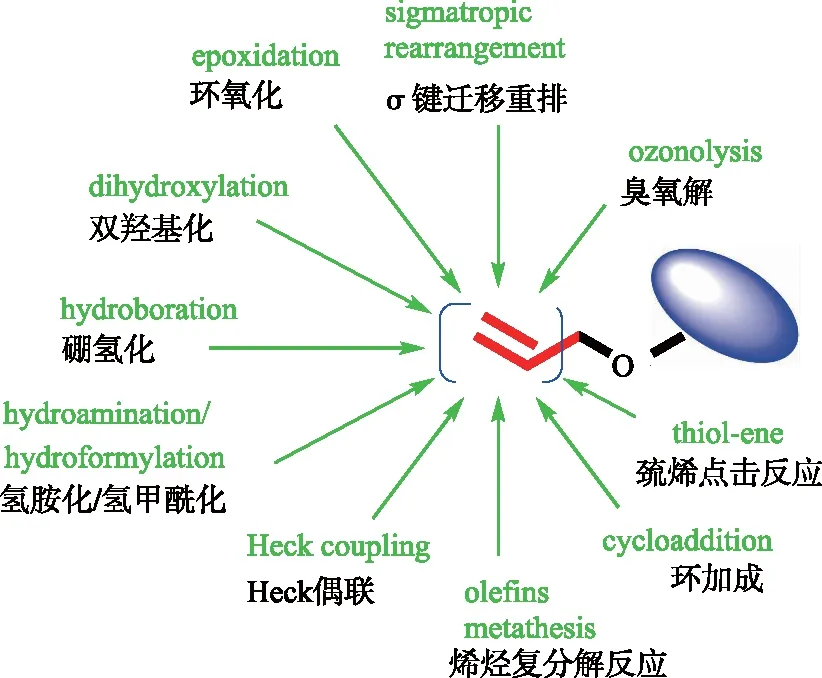
圖1 烯丙基在化學合成中的多樣性
文獻報道的烯丙基糖苷的合成方法按反應機理的不同分為2大類(如圖2所示),第1大類方法是通過氧鎓離子發生端位碳上親核加成的糖基化反應,有3種合成方式。其一,是未被保護的糖在酸催化下直接與醇反應生成相應的糖苷,即Fischer糖基化反應。通常情況下,反應以醇為溶劑,加熱回流,一般得到吡喃糖苷、呋喃糖苷以及少量開環產物的混合物。常用的酸催化劑有CF3SO3H,CF3COOH或H+型磺酸樹脂等質子酸[5-9],也有使用BF3·Et2O等路易酸的報道[10]。這種方法的缺點是,反應常局限于低沸點的醇,并且反應受端基效應的影響,主要生成α-吡喃糖苷[11-13]。其二,是被保護基保護的鹵代糖,其端基的溴或氯在重金屬鹽(Ag2CO3或HgO)作用下活化,與醇反應生成相應的糖苷,即Koenigs-Knorr糖基化。該方法通過C-2酯基的鄰基參與效應,可選擇性得到1,2-trans-糖苷,尤其是獲取Fischer反應難以得到的β吡喃糖苷[14]。但這種方法的不足之處在于,反應步驟較長,總收率只有44%~65%[15]。其三,是全酰基保護的糖,其端位乙酸酯在路易斯酸(如BF3·Et2O,TMSOTf或FeCl3)作用下活化,通過C-2相鄰酯基的參與,與醇反應生成1,2-trans-糖苷[16-17],即Helferich糖基化反應。該方法一般適用于結構簡單的糖,反應收率較高[18-20]。第2大類方法是端基O-發生親核取代的烷基化反應,以不加保護基的糖為起始原料,烯丙基溴為烷基化試劑,在NaH堿性條件下,可得到β異構體為主的烯丙基糖苷[21]。該方法條件溫和,操作簡便,路線相對較短。但反應使用高沸點溶劑,導致后處理純化困難,常需增加一步乙酰化來提純產物,給操作帶來不便。
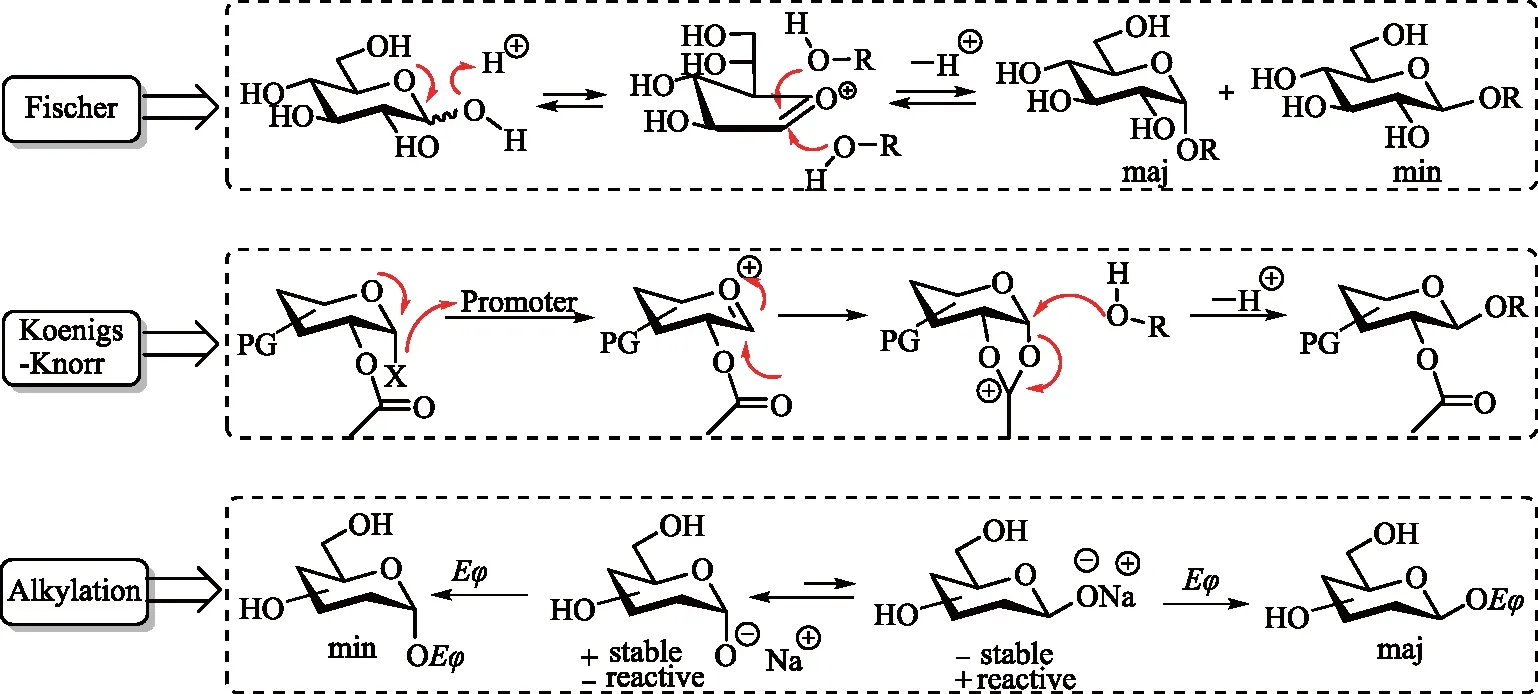
圖2 烯丙基糖苷的合成機理
為了解決烯丙基糖苷現有合成方法步驟較長、后處理困難等問題,可以從2方面入手進行研究。一方面,采用更加有優勢的端基O-烷基化的合成方法,根據端位半縮醛羥基的pKa值小于其他羥基pKa值,從而在堿作用下可以選擇性地得到目標化合物;另一方面,考慮到糖易溶于水的特性,摒棄高沸點的有機溶劑,而選擇水為反應溶劑,從而提高溶解度,促進反應高效進行,并且簡化后處理純化過程。
本研究設計以不加保護基團的糖為起始物,以水為溶劑,在堿性條件下,以烯丙基溴為烷基化試劑,經一步反應得到烯丙基糖苷目標化合物。常見的不加保護基的單糖或二糖,商品廉價易得,水為反應溶劑更加綠色環保,盡管反應為非均相體系,但通過增大攪拌速度,可促進反應進行。在堿性環境中,反應主要生成以動力學控制的β異構體產物。該合成方法基于糖端位O-烷基化的反應機制,從反應選擇性、溶解度和后處理純化等方面綜合考慮,通過一步法實現路線短、反應高效、后處理簡單的目標,反應如圖3所示。
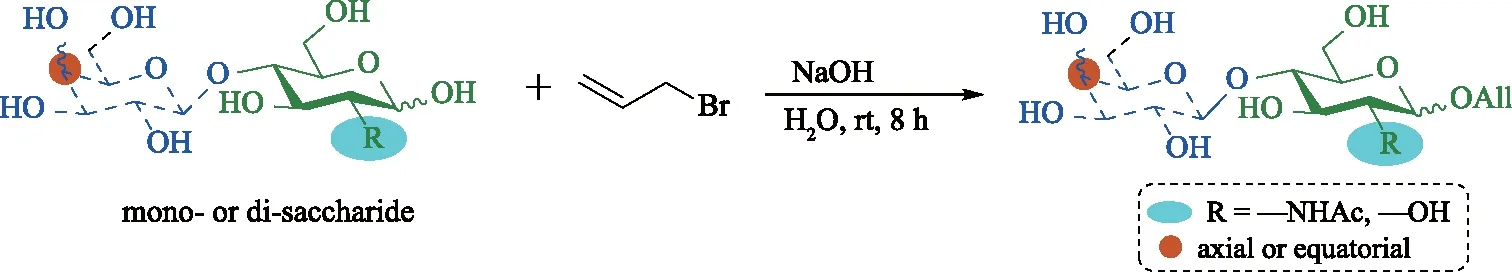
圖3 烷基化反應合成烯丙基糖苷
1 實驗部分
1.1 主要儀器與試劑
341型旋光儀(美國珀金埃爾默公司提供),Bruker AV-400型核磁共振儀(瑞士布魯克公司提供),MicrOTOF-Q高分辨質譜儀(瑞士布魯克公司提供)。
烯丙基溴、D-葡萄糖、D-半乳糖、D-乳糖、D-纖維二糖、N-乙酰基D-葡萄糖胺,均購自阿拉丁試劑有限公司;其他試劑由天津市永大化學試劑有限公司提供。
1.2 實驗方法
在烯丙基糖苷的制備過程中,按照投料量為n(糖)∶n(烯丙基溴)∶n(NaOH) = 1∶2∶1.25反應,以水為反應溶劑,糖的濃度為0.18 mol/L。首先將烯丙基溴加入到一定量糖的水溶液中,再緩慢滴加NaOH溶液(c=1.1 mol/L),0.5 h滴畢,室溫反應約8 h。采用TLC(展開劑V(乙酸乙酯)∶V(甲醇)=7∶3)監測反應進程。反應液用有機溶劑(乙酸乙酯或正己烷)萃取除去過量的烯丙基溴,水相減壓濃縮后干燥,經重結晶(醇類溶劑)或柱層析純化(洗脫劑V(乙酸乙酯)∶V(甲醇)=8∶2~5∶5)得到目標化合物。
1.2.1 烯丙基β-D-吡喃葡萄糖苷的制備

1.2.2 烯丙基β-D-吡喃半乳糖苷的制備

1.2.3 烯丙基2-乙酰氨基-2-脫氧-β-D-吡喃葡萄糖苷的制備

1.2.4 烯丙基β-D-吡喃葡萄糖基-(1→4)-β-D-吡喃葡萄糖苷的制備

1.2.5 烯丙基β-D-吡喃半乳糖基-(1→4)-β-D-吡喃葡萄糖苷的制備

2 結果與討論
2.1 堿的種類選擇
以纖維二糖的烯丙基化反應考查了堿的種類對反應的影響,如表1所示。選取Cs2CO3,Bu4NOH,LiOH,KOH和NaOH 5種堿,以反應收率和2種異構體的比例來分析實驗結果。
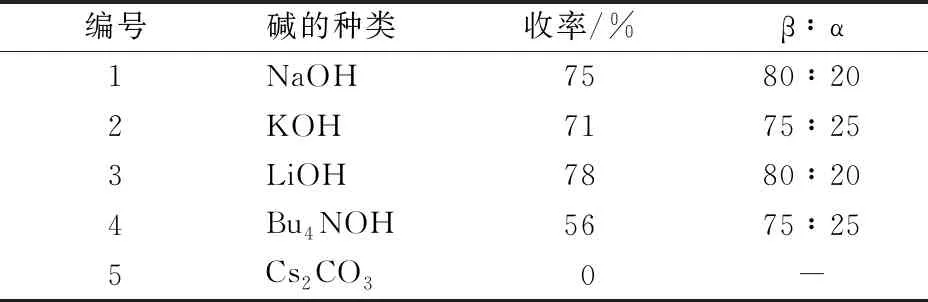
表1 堿的種類對反應收率的影響
由表1實驗結果可知,加入Cs2CO3反應不發生;以LiOH為堿的反應收率最高,β異構體的比例也最大;反應中加入NaOH的收率略低于LiOH,而β∶α的比例與之相當。
通常,在端位烷基化反應中,主要得到反應活性更高的平伏鍵異構體產物(β吡喃糖)。SCHMIDT課題組的ZHU等[22]報道指出Na+對于反應的立體選擇性至關重要,這歸因于Na+可與端位烷氧負離子發生螯合作用,從而有助于促進其β異構體的形成。相反,若反應中加入冠醚,則螯合作用消失,此時反應更傾向于生成穩定性更高的α異構體產物。這一現象在VAUZEILLES等[21]和LUBINEAU等[23]均有報道。
因此,從反應成本、產物收率及選擇性角度綜合考慮,最終選擇NaOH為該反應的堿。
2.2 堿的用量選擇
以纖維二糖的烯丙基化反應來考查NaOH的用量影響,選取1.05,1.25,1.50,3.00 mmol這4種投料量,以反應收率來分析實驗結果,見表2。
由表2可知,NaOH用量在1.05 mmol時,反應的起始原料較多,反應時間較長,反應進行不完全;當使用量增大到3.00 mmol時,反應原料基本消失,但反應產生了更多的副產物。因此,選擇在NaOH用量為1.25 mmol時進行反應,收率較高。

表2 堿的用量對反應收率的影響
在優化堿的用量實驗中,同步通過TLC觀察反應時間對反應結果的影響。結果顯示,隨著反應時間延長,反應進行程度越大,但超過8 h,副產物逐漸增多,因此,最終確定反應時間為8 h。
2.3 后處理優化
由于反應是在水相中進行,產物又溶于水,為尋找高效簡便的后處理方式,嘗試以下3種方法(見表3)。

表3 反應的后處理方法優化
3 結 語
以探索更加高效簡便的烯丙基糖苷合成方法為研究目標,通過分析糖端位O-烷基化的反應機理,從反應的區域選擇性、溶解度和后處理純化等方面進行方法設計和條件優化。反應的區域選擇性方面:根據端位半縮醛羥基的pKa值小于其他羥基pKa值,采用氫氧化鈉這一廉價易得的堿,選擇性得到以β異構體為主的端位烯丙基糖苷。溶解度方面:考慮糖易溶于水的特性,選擇水為反應溶劑更加綠色環保,提高溶解度,促進反應高效進行。后處理純化方面:使用低毒的乙酸乙酯萃取過量的烯丙基溴,再經減壓濃縮、干燥后,經重結晶或柱層析純化,操作簡單易行。通過反應條件優化,確定了n(糖)∶n(烯丙基溴)∶n(氫氧化鈉)=1∶2∶1.25,室溫反應8 h,合成了5種烯丙基糖苷目標化合物,反應收率在72%~90%,實現了一步法快速高效制備烯丙基糖苷的目標(見表4)。

表4 烯丙基糖苷反應結果
完成了水相中一步法制備烯丙基糖苷的研究工作,相較于傳統的Fisher或Koenigs-Knorr等糖基化反應,該方法條件溫和,操作簡便,高效快捷,為進一步構建結構復雜的糖綴合物提供了一種新的合成思路。未來還需要針對該方法的后處理過程開展深入研究,重點優化重結晶等適合工業化的分離提純方式,不斷提升其工業應用價值。

