CD47單抗與CD38單抗對輸血前檢查的影響對比分析
王曉寧,劉 冰,王 恒,張冬霞,盧偉偉*
(1.吉林大學第一醫院 輸血科,吉林 長春130021;2.吉林省腫瘤醫院 輸血科)
CD47是一種廣泛表達的跨膜糖蛋白,也稱為整聯蛋白相關蛋白(IAP),分子量52kDa[1]。該蛋白具有免疫球蛋白可變的N端結構域、5個跨膜結構域和一個短的C端胞內尾,胞內尾部有四種可變不同剪接異構體,從而形成4個亞型。CD47亞型2主要在造血細胞、血管內皮細胞和上皮細胞中表達,1亞型在角質形成細胞中表達,3和4亞型在神經元細胞、腸黏膜細胞和睪丸細胞中均有表達[2]。CD47在體內多種正常細胞和組織上表達,包括紅細胞和血小板。2012年,Willingham等發現CD47在實體腫瘤細胞上過表達,在卵巢癌、乳腺癌、結腸癌、膀胱癌、膠質母細胞瘤、肝細胞癌和前列腺腫瘤細胞中的表達均顯著高于正常細胞[3]。CD47與血液腫瘤關系更為密切,在急性髓系白血病、非霍奇金淋巴瘤和急性淋巴細胞白血病中檢測到CD47的高表達[4]。但是應用此類藥物后,會對患者輸血檢驗產生一定的影響,包括抗篩陽性、直抗陽性等。分析用藥后對患者輸血前的影響,可以加快輸血檢驗時間,提高輸血效率。
1 材料與方法
1.1 樣本來源應用藥物TJ011133前后的患者標本10例。
1.2 試劑與儀器單克隆抗-A、抗-B、抗-D及反定型用試劑紅細胞(長春博德),抗球蛋白檢測卡、Rh血型抗原檢測卡及低離子鹽溶液(長春博迅),抗人球蛋白試劑(上海血液生物),抗體篩查細胞(長春博迅),凝聚胺試劑盒(珠海貝索),pH7.4磷酸鹽PBS緩沖液,二硫蘇糖醇(DTT),血型血清學離心機(日本久保田,型號KA2200),卡式離心機(長春博研,型號TD-A)。
1.3 給藥方法劑量遞增研究將采用改良的“3+3”方案,直至確定MTD或RP2D。TJ011133暫定每周給藥1次,每28天為1個治療周期。Ⅰ期劑量遞增階段預設五個遞增劑量水平,分別為:1 mg/kg、3 mg/kg、10 mg/kg、20 mg/kg和30 mg/kg,每周給藥1次。治療每28天為1個治療周期,首次給藥起28天為DLT觀察期。
1.4 方法
1.4.1樣本采集 采集被檢對象靜脈血,加入含EDTA或枸櫞酸鈉抗凝劑的試管中。將采集的標本配制成0.5%-0.8%紅細胞生理鹽水懸液。將Rh血型抗原檢測卡(單克隆抗體)做標記,將待檢者0.5%-0.8%紅細胞懸液分別加入第1- 6支微管中(第1-5支微管分別含有IgM單克隆抗-D、抗-C、抗-c、抗-E、抗-e抗體,第6支微管為中性膠做陰性對照),每管50 μl。使用專用離心機離心5 min,900 rpm 2 min,1500 rpm 3 min,取出,根據試劑說明書,判定結果。
1.4.2血漿鑒定及抗體篩查 ABO血型、直接抗人球試驗、Rh血型、抗體篩查,參照第18版《AABB技術手冊》[5]進行檢測。
2 結果
2.1 血型應用CD47前后血型結果對比,見表1。
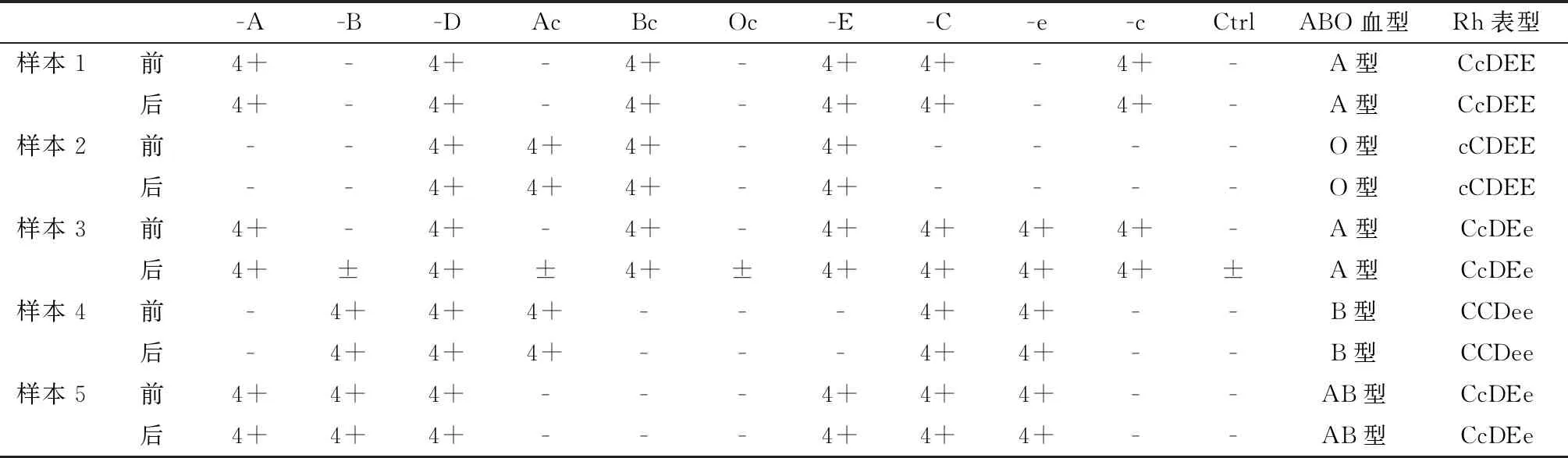
表1 應用CD47前后ABO血型和Rh五分型結果對比
2.2 抗篩及直抗應用CD47前后抗篩結果對比,檢測用藥前患者自身、直抗、鹽水抗篩、凝聚胺抗篩、經典抗人球抗篩、微柱凝膠抗篩均呈陰性結果,無不規則抗體產生,患者用藥后復查,直抗、自身一般呈“2+”,四種方法檢測的抗篩均呈強陽性結果。結果見表2。

表2 應用CD47抗篩前后抗篩結果對比
2.3 交叉配血應用CD47后普通交叉配血出現明顯困難,應用廠家提供的中和試劑(中和試劑:高特異性中和試劑通過與血漿中的TJ011133藥物結合,阻止藥物與紅細胞結合帶來的輸血前實驗干擾)和ImmucorAHG(anti-IgG)兩種方法去除CD47的用藥對配血、直抗、自身的干擾,應用效果見表3。
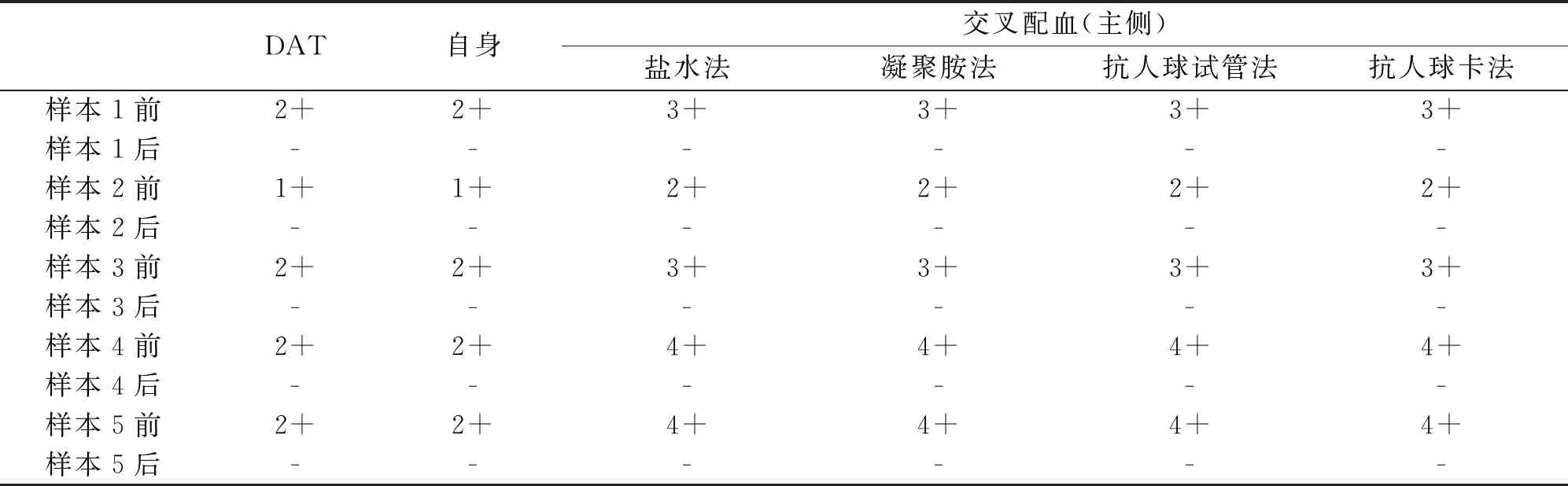
表3 去干擾處理前后結果對比
2.4 應用CD47(TJ011133)與CD38(達雷妥尤單抗Daratumumab,DARA)效果對比通過對比CD47和CD38的輸血后效果,發現CD47明顯強于CD38,CD38一般不對血型造成影響,CD47對反定型造成影響。CD38僅對抗人球法造成影響[6],CD47對所有方法均造成影響[7]。見表4。

表4 CD47與CD38單抗效果比較
3 討論
CD47作為新一代腫瘤免疫治療的靶點可以引起先天性和適應性免疫應答的作用機制,這已經反復在臨床試驗上得到證實[8-9]。近年來,CD47單克隆抗體的臨床研究在美國迅速開展。截至2021年8月28日,在臨床試驗中登記了CD47靶向治療的46項臨床試驗。這些臨床試驗中研究了不同類型的癌癥患者,包括29項實體瘤試驗和14項血液系統惡性腫瘤試驗和3項混合試驗[10]。在我國,抗CD47治療方面也取得了很大進展。根據NMPA的信息,至少有17種CD47靶向藥物已被批準用于臨床研究,占全球CD47靶向藥物的一半以上。本次實驗是針對應用TJ011133的患者,TJ011133(lemzoparlimab)是一種高度差異化的紅細胞保護CD47抗體,具有獨特的表位。它具有很強的抗腫瘤活性,并盡量減少與正常紅細胞的結合,從而減少某些CD47單抗可能引起的HA[11]。
本次試驗的五名患者,均為曾經有過輸血史的患者,為避免患者在用藥前產生不規則抗體或其他藥物性抗體,均使用4種方法測定了抗篩、DAT和患者自身。均為陰性,確定患者未產生同種抗體、自身抗體及干擾配血結果的藥物性抗體。其中有一例患者對ABO血型和Rh五分型均造成了一定的影響,且影響不明顯(凝集強度為±),其他患者均未對血型檢測造成影響,這與應用CD38單抗的患者用藥后基本一致[12]。應用CD47后,配血、抗篩均發生凝集,且凝集強度強,可以證明CD47是一個高親和力抗體,不同于CD38抗體的去除方式[13],DTT無法去除CD47抗體的干擾,這是由于CD47是Rh抗原膜復合物的組成部分,大部分與底層細胞骨架相連[14],因此應用DTT無法去除CD47的干擾,應用ImmucorAHG和中和試劑則可以有效去除干擾,完成配血工作。
隨著CD47臨床藥物研究的開展,包括IBI188、SRF231等的應用,這種因藥物導致的干擾將越來越多的在臨床出現[15]。積極配合臨床,在用藥前完善基礎檢驗,積累更多的患者信息,將對用藥后的去干擾提供更多的判斷依據。

