成組生物毒性測試在污染場地土壤生態毒性評價中的應用*
高金玲 汪 貞 古 文 范德玲 梁夢園 劉濟寧 張 志
(1.黑龍江大學現代農業與生態環境學院,黑龍江 哈爾濱 150080;2.生態環境部南京環境科學研究所,江蘇 南京 210042)
《土壤污染防治行動計劃》明確提出,對于土壤污染要“分類別、分用途、分階段治理”。現階段,我國污染土壤的分類以保護人體健康與保障農產品質量安全為出發點,通過化學分析手段測定污染物賦存量,與篩選值進行比較來確定分類。盡管我國已建立了土壤污染檢測的化學分析方法體系,但是化學分析難以對土壤中的所有污染物進行全面測定,現有土壤環境質量標準中有限的污染物限量標準難以滿足風險評估需求。此外,化學分析不能客觀反映多污染物組分的協同作用,具有很大的局限性。未來有必要基于生態風險建立篩選值,為污染土壤的安全利用增加一道防線。
土壤生態毒性測試是通過外源污染物對受試生物(植物、動物、微生物)在分子、細胞、器官、個體、種群及群落等不同生命層次上的脅迫效應來評估土壤的污染程度的方法[1]。該方法可以比較全面地反映土壤污染的程度和影響,對化學分析方法能起到很好的補充作用。《土壤質量 土壤和土壤材料生態毒理特性的生物測試方法選擇與評估指南》(ISO 17616:2019)建立了系統的土壤生態毒性診斷技術,采用污染土壤樣品測定蚯蚓等9種陸生生物和土壤微生物的急慢性毒性,以評估污染物對土壤棲息地功能的影響;采用污染土壤浸提液測定發光菌等6種水生生物的毒性,以評估污染物對土壤滯留功能的影響;基于毒性終點的毒性效應分別制訂了毒性判別標準,并規定至少一項試驗結果為陽性時,表明土壤有毒[2]6。總體看來,ISO 17616:2019實現了土壤毒性有無的定性判斷。判斷污染場地土壤生物毒性程度,確定基于生態風險的篩選值,建立毒性高低與篩選值之間的對應關系,可以為更精細的場地修復與利用提供依據。因此,需要基于生態毒性測試建立毒性分級系統。目前針對土壤毒性分級系統的研究相對缺乏,少量研究報道了成組毒性測試綜合指數(TBI)法[3]1943。此外,毒性單位分級評價法[4]是一種廣泛應用于水[5-6]和沉積物[7-8]毒性評價的方法,算法與原理簡單,但應用于土壤毒性評價鮮有報道。
應用ISO 17616:2019方法時,需開展13項毒性測試,測試成本高、周期長,為了提高試驗經濟性,有必要探討使用更有限的生物組合開展測試[9]。本研究基于ISO 17616:2019,篩選了4種代表性受試生物,對《土壤污染防治行動計劃》中涉及的3個行業的7個污染場地土壤開展了成組生物毒性測試,參考毒性單位分級評價法建立了毒性分類標準,對成組生物毒性測試的結果進行了定量評估,并與TBI法的結果進行比較,以期為成組生物毒性測試在污染場地土壤生態毒性評價方面的推廣應用提供參考。
1 材料與方法
1.1 儀器與試劑
主要儀器:人工氣候箱(RXZ-600)、水質參數分析儀(美國哈希,HQ 40d)、總有機碳(TOC)分析儀(德國耶拿,Multi N/C 3100)、分光光度計(日本SHIMADZU,UV-2450)、天平(美國METTLER TOLEDO,MS105DU)、酶標儀(美國MD Electronics,spectraMax iD3)。
主要試驗材料:人工土壤(配置方法參考文獻[10])、Elendt M7培養基(固體,配置方法參考文獻[11])、ASTM培養基(液體,配置方法參考文獻[12])、活性炭(分析純,200目)、氯化鈉(分析純)、氯化鈣(分析純)。
1.2 土壤樣品來源與理化指標的測定
2020年8—11月,采集了江蘇昆山(JSKS)、山西孝義(SXXY)、山西陽泉(SXYQ)、廣東韶關(GDSG)、廣東廣州(GDGZ)、山西太原(SXTY1、SXTY2)共6個城市的7個污染場地土壤樣品,樣品編號、來源以及涉及的行業信息見表1。土壤含水率測定參考《土壤 干物質和水分的測定 重量法》(HJ 613—2011);pH測定參考《土壤 pH值的測定 電位法》(HJ 962—2018);電導率測定參考《土壤 電導率的測定 電極法》(HJ 802—2016);TOC測定參考《土壤 有機碳的測定 燃燒氧化-非分散紅外法》(HJ 695—2014);陽離子交換量測定參考《土壤 陽離子交換量的測定 三氯化六氨合鈷浸提-分光光度法》(HJ 889—2017)。
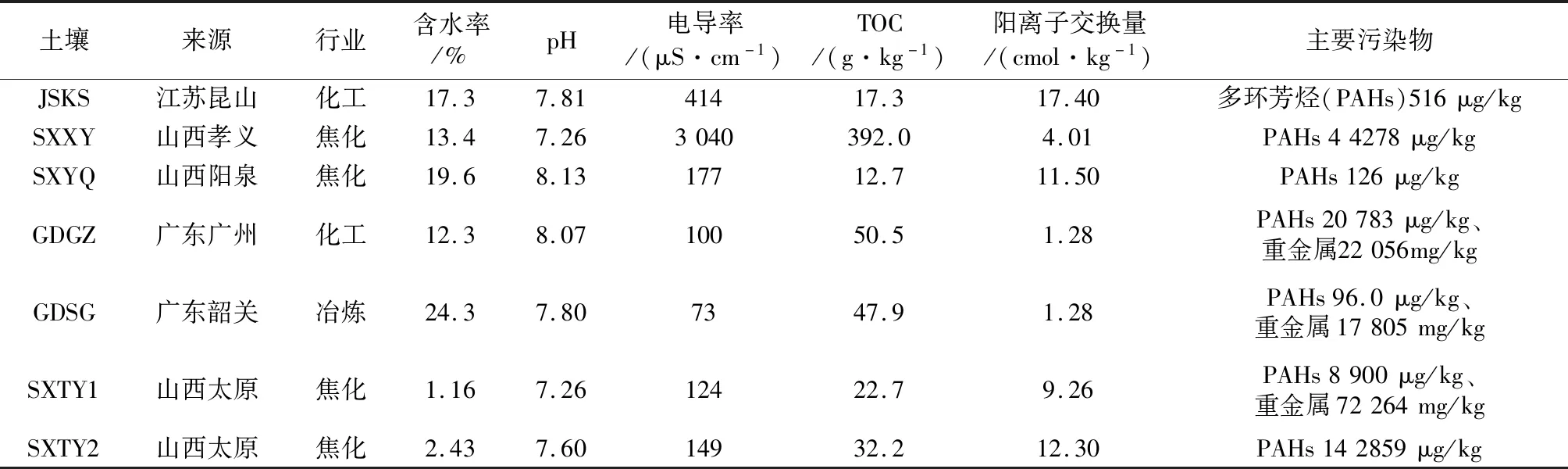
表1 污染場地土壤樣品來源與理化指標Table 1 Source and physicochemical indicators of contaminated sites soil samples
1.3 供試生物及飼養
發光菌為費氏弧菌(Vibriofischeri)凍干粉,購買自北京金達清創環境科技有限公司。
大型溞(Daphniamagna)由實驗室馴養,在Elendt M7培養基,溫度(20±1) ℃,光照強度1 000~1 500 lx,光暗比16 h∶8 h,以小球藻(ChlorellavulgarisBeij.)濃縮液喂食條件下培養。
白符跳(Folsomiacandida)由實驗室馴養,在底部鋪有0.5 cm厚石膏/活性炭混合基質的培養皿中培養,培養溫度為(20±1) ℃,光照強度400~800 lx,光暗比為12 h∶12 h,以市售酵母粉喂食。試驗采用同步化的白符跳(9~12 d)作為受試生物。
玉米種子購自江蘇省農業科學院。
1.4 土壤浸提液的制備方法
稱取過2 mm尼龍篩的污染場地土壤樣品,加入0.001 mol/L CaCl2溶液,土水比為1 g∶10 mL,振蕩提取24 h。提取后的溶液過0.45 μm有機濾膜得到土壤浸提液,置于4 ℃保存。
1.5 成組生物毒性試驗
發光菌急性毒性試驗:每瓶費氏弧菌凍干粉加入3 mL菌體復蘇液,混勻制成菌懸液。土壤浸提液用30.0 g/L的NaCl溶液稀釋成不同濃度,各取1 mL分別加入0.1 mL滲透壓調節液,搖勻,加入到96孔酶標板,每孔200 μL,每個樣品設置3個平行。向已加入空白對照樣品和試驗樣品的酶標板中添加復蘇好的菌懸液,每孔10 μL,室溫下放置,15 min后用酶標儀測定混合液的發光強度。空白對照組為30.0 g/L 的NaCl溶液。
大型溞急性活動抑制試驗:添加ASTM培養基將土壤浸提液稀釋成不同濃度試驗溶液,每種試驗溶液加入5只溞齡<24 h的幼溞,每個濃度設4個平行,觀察并記錄24、48 h大型溞的活動情況。試驗期間不喂食。空白對照組為ASTM培養基。
大型溞繁殖毒性試驗:在大型溞急性活動抑制試驗的基礎上開展大型溞繁殖毒性試驗。添加ASTM培養基將土壤浸提液稀釋成不同濃度試驗溶液,每個試驗溶液加入1只溞齡<24 h的幼溞,每個濃度設10個平行,觀察21 d內繁殖的幼溞數量。試驗期間,每3天更換試驗溶液,每天以小球藻濃縮液喂食,繁殖的幼溞及時計數并移出試驗容器。空白對照組為ASTM培養基。
白符跳急性毒性試驗:將污染場地土壤樣品與人工土壤混合成不同質量分數,稱取30 g放入培養皿中,加水至飽和持水量的50%,老化48 h,同時設置人工土壤作為空白對照組。每個培養皿引入10只9~12 d的白符跳。7 d后觀察,記錄死亡數并計算死亡率。空白對照組和試驗組各設置4個平行。急性毒性試驗期間不喂食。
白符跳繁殖毒性試驗:在白符跳急性毒性試驗基礎上設置5個質量分數的混合土壤,第21天記錄成蟲的存活數,并將成蟲移走等待卵孵化。第28天記錄幼蟲數量。試驗期間,每周以酵母粉喂食。空白對照組為人工土壤。
玉米種子發芽與根伸長試驗:將污染場地土壤樣品與人工土壤混合成5個不同質量分數,每個質量分數設置3個平行,稱取100 g放入結晶皿中,加入去離子水使含水率為70%±5%,每個結晶皿均勻放入10顆玉米種子。20 ℃黑暗條件下培養,當空白對照組(人工土壤)的根長≥20 mm時,結束試驗,測量每顆種子的根長。
1.6 數據統計與分析
半數抑制濃度(IC50)、半數致死濃度(LC50)以及半數效應濃度(EC50)的計算采用修正版斯皮爾曼-卡伯法,無可觀察效應濃度(NOEC)的計算參照文獻[13]。劑量—效應曲線采用Origin 8.1中的Logistic函數擬合。
1.7 毒性單位分級評價法
參考文獻[4]將IC50、LC50、EC50、NOEC轉化為毒性單位。
如受試生物的效應分數未達到50%,毒性單位按照下式計算:
TU=RE×10 000/50
(1)
式中:TU為毒性單位;RE為100%污染場地土壤或其浸提液對受試生物的抑制率或致死率,%。
每項試驗單獨計算TU,所有試驗的TU平均值作為最終TU。根據最終TU將土壤毒性劃分為5個等級(見表2)。
1.8 TBI法
參考文獻[3]和[14],計算TBI和判別系數(C)。
基于TBI的毒性標準見表3。

表2 基于毒性單位的土壤毒性分級標準Table 2 Toxicity classification for soils based on TU

表3 基于TBI的土壤毒性分級標準Table 3 Toxicity classification for soils based on TBI
2 結果與討論
2.1 成組生物毒性測試結果
2.1.1 發光菌急性毒性試驗
7個污染場地土壤的浸提液發光菌急性毒性試驗結果如圖1所示。質量分數10%(即稀釋為原土壤浸提液的10%,其余類推)、20%、40%、80%、100%的GDSG土壤浸提液均具有發光抑制效應,發光抑制率為11.9%~63.5%。SXXY、SXYQ、JSKS、GDGZ、SXTY1以及SXTY2低濃度組都表現出生物毒性興奮效應,高濃度組(質量分數超過80%)才表現出明顯的發光抑制效應,其中質量分數100%組的發光抑制率均超過90%。
2.1.2 大型溞急性活動抑制與繁殖毒性試驗
SXXY、SXYQ、JSKS、GDGZ及SXTY1所有試驗組均未顯示出活動抑制效應。GDSG、SXTY2土壤浸提液大型溞急性活動抑制試驗結果如圖2(a)所示。GDSG土壤浸提液對大型溞的活動抑制率存在明顯的劑量—效應關系;SXTY2土壤浸提液低濃度組未顯示出活動抑制效應,質量分數100%組的活動抑制率約為60%。
GDGZ、SXTY1所有濃度組的繁殖抑制效應并不突出,繁殖抑制率分別為4.29%~11.5%和4.17%~9.72%;GDSG、SXXY、JSKS、SXYQ以及SXTY2土壤浸提液對大型溞的繁殖抑制率存在明顯的劑量—效應關系(見圖2(b))。由于GDSG土壤浸提液質量分數10%組對大型溞有急性致死效應,繁殖試驗的最高質量分數為8%,其繁殖抑制率為42.2%。SXXY、JSKS、SXYQ以及SXTY2土壤浸提液質量分數100%組的抑制率分別為58.3%、47.3%、46.9%和20.6%。
2.1.3 白符跳急性毒性與繁殖毒性試驗
白符跳急性毒性如圖3(a)所示,GDSG、SXTY2以及GDGZ對白符跳的存活抑制率與濃度存在明顯的劑量—效應關系,質量分數100%組的存活抑制率分別為56.7%、66.7%以及36.7%。SXXY、SXYQ、JSKS和SXTY1表現出較低的毒性效應,質量分數100%組的存活抑制率分別為6.7%、3.3%、3.3%和10.0%。
白符跳繁殖毒性測試結果如圖3(b)所示,SXTY2、SXTY1、GDSG、GDGZ以及SXXY對白符跳的繁殖抑制率與濃度存在明顯的劑量—效應關系,質量分數100%組的繁殖抑制率分別為81.0%、60.2%、60.7%、61.7%以及26.3%。SXYQ以及JSKS未表現出明顯的毒性效應,質量分數100%組的繁殖抑制率分別為0.9%和2.0%。
2.1.4 玉米種子發芽與根伸長抑制試驗
7種污染場地土壤均未對玉米種子發芽產生抑制效應,但對根伸長產生了不同程度的抑制效應,結果如圖4所示。玉米種子的根生長抑制率與SXTY1土壤存在明顯的劑量—效應關系,質量分數100%組的根長抑制率為52.9%。SXXY、SXYQ、GDGZ、GDSG質量分數100%組的根長抑制率分別為22.9%、12.9%、26.4%、18.5%,與空白對照組有顯著性差異(P<0.05)。JSKS和SXTY2未表現出明顯的毒性效應,質量分數100%組的根長抑制率分別為5.40%和9.67%。
不存在對所有污染物都敏感的生物毒性測試方法,單一測試難以準確評價污染土壤對生態系統的危害,生物組合測試具有更高的敏感性和生態相關性,能更全面地解釋毒性效應和毒性機制[15]。高靈敏度的單一測試是成組生物毒性測試方法的關鍵[16]5-6,[17]。本研究基于ISO 17616:2019,又兼顧了土壤浸提液和土壤,并參照美國環境保護署提出的廢水綜合生物毒性測試至少需3種生物進行測試[18]的要求,選擇發光菌、大型溞、白符跳以及玉米種子開展綜合毒性測試。有研究表明,發光菌(以費氏弧菌為例)對于大多數環境污染物的響應有足夠的靈敏性[16]7。大型溞廣泛應用于水質監測和水生生物毒理研究,對水環境中多種有毒化學物質敏感性強[19]。與蚯蚓相比,跳蟲對土壤污染物更加敏感[20-21]。玉米是世界三大糧食作物之一,具有重要的經濟價值以及地區生態學價值。因此,本研究選擇的4個受試生物為對污染物響應敏感的生物或者具有重要的生態學價值的生物。多營養級的成組生物毒性測試能有效評估樣品的毒性[16]9,本研究選擇的4種生物包含分解者、水生生態系統消費者、陸生生態系統消費者、陸生生態系統生產者。需要說明的是,不同場地土壤浸提液的營養元素存在差異,這種差異會對藻類的生長與生理指標產生影響,干擾藻類生長抑制試驗的結果[2]7,因此,未選擇藻類開展生物組合測試。
從本研究的7個污染場地土壤測試結果來看,不同物種的急慢性毒性效應有差異,證實了對代表不同營養水平的生物體進行成組生物毒性測試的必要性[14]16。其中發光菌的敏感性最高,對7個污染場地土壤浸提液均有響應。大型溞對兩個污染場地土壤浸提液有急性毒性響應,對5個污染場地土壤浸提液有繁殖毒性響應。白符跳對3個污染場地土壤有急性毒性響應,對5個污染場地土壤有繁殖毒性響應。因此,基于大型溞和白符跳的試驗結果,繁殖毒性敏感性高于急性毒性,符合繁殖終點一般比存活更敏感[22-23]的結論。玉米種子的敏感性較差。
2.2 基于ISO 17616:2019毒性標準的毒性評價
匯總2.1節的質量分數100%組的生物毒性數據,結果見表4。ISO 17616:2019列出了發光菌、溞類急性毒性,白符跳繁殖毒性以及植物種子生長抑制參考標準,抑制率限值分別為20%、20%、50%和30%;此外,還根據網紋溞(Ceriodaphniadubia)繁殖毒性抑制率限值為30%,赤子愛勝蚓(Eiseniafetida)等初級消費者急性毒性抑制率限值為20%,分別作為大型溞繁殖毒性和白符跳急性毒性參考標準。按照1項試驗結果毒性超標即判斷為有毒的原則,7個污染場地土壤毒性綜合判斷均有毒。
2.3 基于毒性單位分級評價法的毒性評價
根據2.1節的生物毒性數據,采用1.7節所述的方法計算各污染場地土壤或其浸提液的效應濃度,結果見表5。
根據1.7節所述的毒性單位分級評價法,計算各樣品以不同受試生物開展的毒性試驗的毒性單位,并評估毒性,結果見表6。結果表明,7個污染場地土壤的滯留功能,GDSG為高毒,SXTY1和GDGZ為低毒,其余均為中毒;7個污染場地土壤的棲息地功能,GDGZ、GDSG、SXTY1、SXTY2為中毒,SXXY為低毒,JSKS和SXYQ為無毒。
2.4 基于TBI法的毒性評價
根據2.1節的生物毒性數據,采用1.8節所述的方法計算各污染場地的TBI并評價毒性,結果見表7。
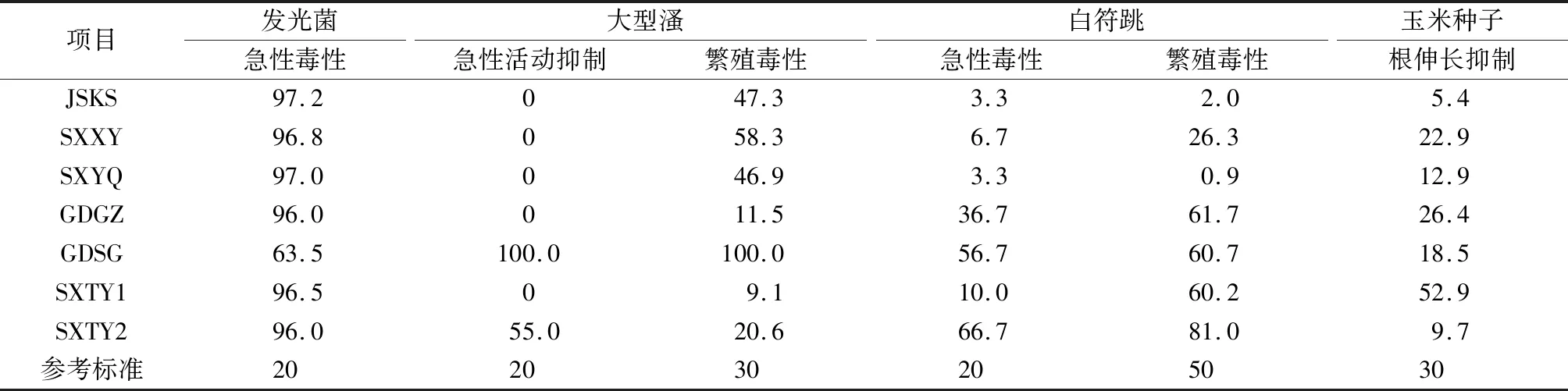
表4 污染場地土壤或浸提液質量分數100%組的抑制率Table 4 Inhibition rate of 100% treatment groups of contaminated sites soils or leachates %
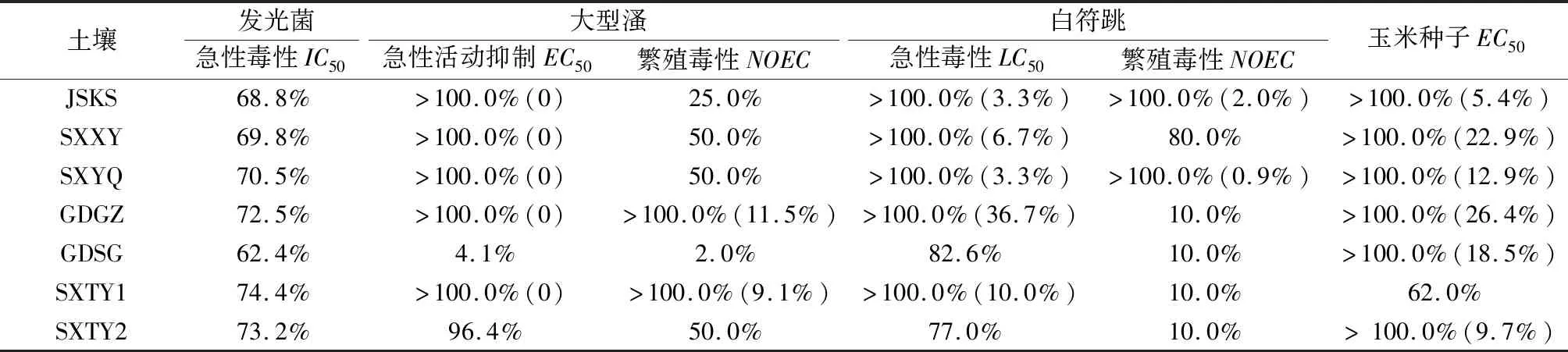
表5 污染場地土壤或浸提液的效應濃度1)Table 5 Effect concentration by contaminated sites soils or leachates
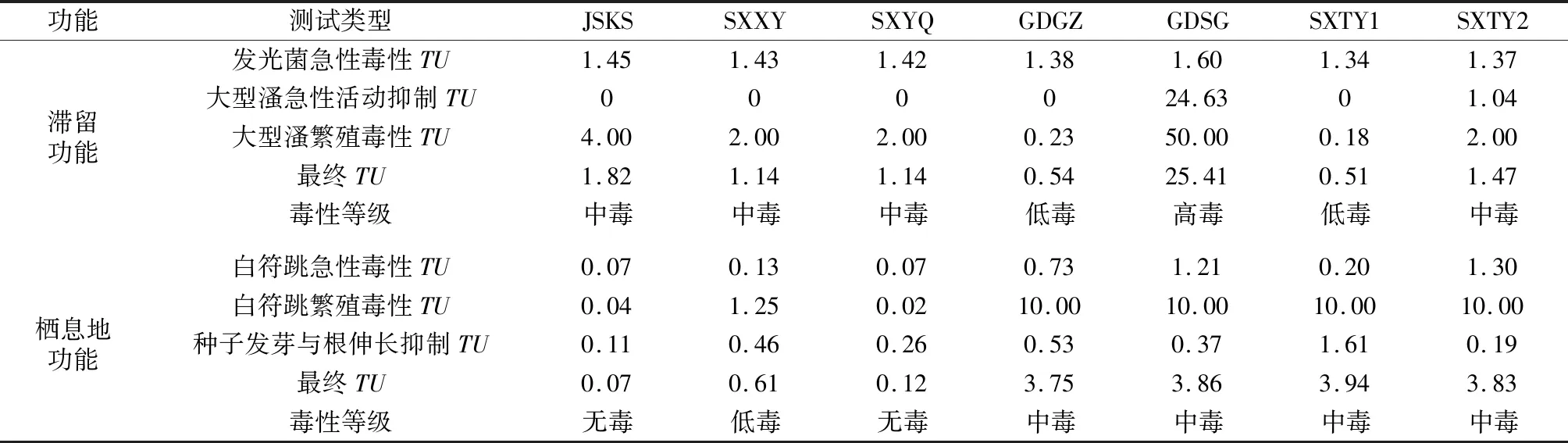
表6 污染場地土壤或浸提液的毒性單位與生態毒性評估Table 6 Toxic unit and ecotoxicity assessment for contaminated sites soils or leachates
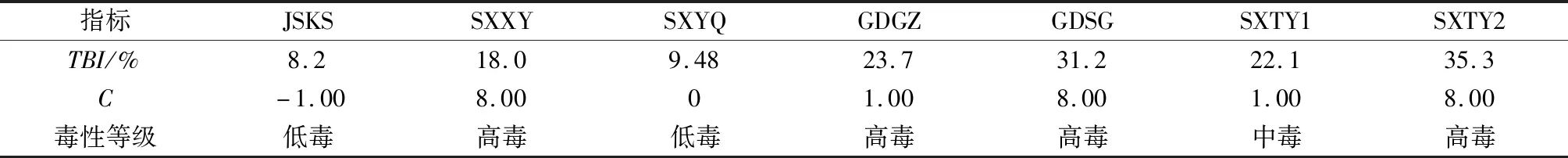
表7 污染場地土壤TBI與生態毒性評估Table 7 TBI and ecotoxicity assessment for contaminated sites soils

表8 ISO 17616:2019毒性標準、毒性單位分級評價法與TBI法的比較Table 8 Comparison of toxicity standard from ISO 17616:2019,toxicity unit classification system method and TBI method
表7結果表明,JSKS、SXYQ為低毒,SXTY1為中毒,SXXY、GDGZ、GDSG、SXTY2為高毒。
通過毒性標準將成組毒性測試所得的多個毒性數據整合成易于理解的單一值,有助于土壤環境管理進行有關的決策[14]2。總體看來,本研究采用的3種方法都實現了成組生物毒性測試結果的整合。毒性單位分級評價法、TBI法的評價結果均指示7個污染場地土壤有毒,與ISO 17616:2019毒性標準的評估結果一致,但毒性單位分級評價法與TBI法判定的毒性程度存在差異。
表8對3種方法的算法難易程度、結果區分度、客觀性以及結果可比性進行了分析。基于ISO 17616:2019毒性標準的毒性評價方法簡單,只需要100%污染場地土壤或其浸提液的抑制率或死亡率,與標準限值比較即可得出結果。但由于發光菌的敏感性較強,基于ISO 17616:2019毒性標準的毒性評價結果全部為有毒。因此,該方法的結果易受敏感物種的影響,且不能進一步區分不同土壤的毒性高低,結果區分度低。基于毒性單位分級評價法的毒性評價算法簡單,實現了滯留功能和棲息地功能的分別評價,有助于聚焦土壤受損功能。土壤健康狀況主要用于評估土壤作為一個重要的生命系統發揮作用的能力[3]1937,聚焦土壤受損功能有助于后續的修復與利用。另外,該方法有統一的算法和毒性標準,可以實現不同研究結果、不同場地之間的比較。基于TBI法的毒性評估實現了土壤毒性的整體評價,但計算相對復雜,且該方法需要基質系數和嚴重度系數,需要使用者主觀定值,尤其是嚴重度系數,需要根據測試項目指定。不同項目的成組生物測試由于嚴重度系數的差異,TBI法結果可能難以比較。
綜上所述,毒性單位分級評價法能夠聚焦土壤的受損功能,且算法與毒性標準可以統一,更具有推廣應用價值。
3 結 論
(1) 采用發光菌、大型溞、白符跳以及玉米種子4種受試生物構建了成組生物毒性測試系統,對3個行業的7個污染場地土壤開展了成組生物毒性測試。4種生物的急慢性毒性效應有差異,發光菌的敏感性最高,大型溞和白符跳的繁殖毒性敏感性高于急性毒性,玉米種子的敏感性較差。
(2) 采用ISO 17616:2019毒性標準、毒性單位分級評價法與TBI法評估了7個污染場地土壤的毒性。毒性單位分級評價法、TBI法的整體結果為污染場地土壤均有毒,與ISO 17616:2019毒性標準的評估結果一致,但毒性單位分級評價法與TBI法判定的毒性程度存在差異。
(3) 與ISO 17616:2019毒性標準、TBI法相比,毒性單位分級評價法算法簡單,能夠聚焦土壤受損功能,算法與毒性標準可以統一,更具有推廣應用價值。

