不同分級進展期胃癌新輔助化療效果的DCE-MRI定量參數對比分析
童華潔
龍巖人民醫院放射科,福建省龍巖市 364000
胃癌是起源于胃黏膜上皮的惡性腫瘤,也是消化道最常見的惡性腫瘤,多數胃癌患者早期無明顯癥狀,到確診時已進入中晚期,錯過了最佳治療時期,影響患者后續治療及預后效果。相關研究表明,部分胃癌患者在術前進行新輔助化療(NAC)能有效提高手術根治率、降低局部復發風險,有助于延長患者生存時間[1]。但對NAC治療響應較差的患者卻可能產生其他不良反應,延誤手術時機,導致患者預后較差。目前臨床上僅能通過術后的病理學檢查判斷胃癌治療效果,因此,找到一種能在術前準確預測NAC療效的方式在胃癌患者的治療中變得尤為重要。定量動態增強磁共振成像(DCE-MRI)是一種通過藥代動力學模型計算血流相關參數,反映腫瘤血流動力學信息的成像方式,在鼻腔鼻竇癌、前列腺癌等惡性腫瘤的診斷中效能良好[2-3],但關于其在進展期胃癌NAC療效中的診斷價值目前尚不明確,故本文回顧性分析了我院68例進展期胃癌患者的臨床資料,旨在探究DCE-MRI的定量參數在進展期胃癌NAC效果中的價值。現研究取得一定成果,報道如下。
1 資料與方法
1.1 一般資料 回顧性分析我院2019年1月—2021年10月收治的68例進展期胃癌患者臨床資料,根據術后病理學檢測結果將患者分為TRG1組(n=9)、TRG2組(n=13)、TRG3組(n=15)、TRG4組(n=17)、TRG5組(n=14),將TRG1組、TRG2組、TRG3組納入有效組(37例),將TRG4組、TRG5組納入無效組(31例)。納入標準:(1)經病理學診斷后確診為胃癌患者[4-5];(2)處于胃癌進展期;(3)均接收DCE-MRI檢查,并于檢查1周后接受NAC,并于NAC后30d內進行胃癌手術。排除標準:(1)臨床資料不完整;(2)腫瘤直徑<1cm;(3)DCE-MRI圖像偽影嚴重,影響評估。有效組中男31例,女6例;年齡48~73歲,平均年齡(55.92±10.24)歲;腫瘤部位:食管胃連接部及胃底16例、胃體8例、胃竇9例、彌漫4例;組織學類型:腺癌34例、黏液腺癌1例、印戒細胞癌2例。無效組中男26例,女5例;年齡49~72歲,平均年齡(56.12±11.23)歲;腫瘤部位:食管胃連接部及胃底17例、胃體5例、胃竇7例、彌漫2例;組織學類型:腺癌29例、黏液腺癌1例、印戒細胞癌1例。
1.2 方法 DCE-MRI:采用GE公司的3.0T 磁共振掃描儀(Discovery 750)進行檢查,檢查前囑患者禁食4~6h,檢查前20min注射鹽酸山莨菪堿10mg減少患者食管蠕動。檢查:囑患者取仰臥位,足先進,定量DCE掃描使用LAVA序列。先進行T1原始值圖采集,將病變最大層面作為中心,掃描參數:重復時間(TR)/回波時間(TE):2.6ms/1.2ms,翻轉角:3°、6°、9°、12°,層厚4.0mm,層間距0mm,矩陣224×224,視野(FOV):40cm×40cm,激發次數(NEX):1.0,掃描時間:6s,掃描層數:44層。之后進行增強掃描,掃描開始后持續靜脈注射對比劑釓噴酸葡胺0.2ml/kg,流速2.5ml/s,之后相同速率注入20ml生理鹽水,掃描參數同上,翻轉角15°,6s/期,每隔5~10s掃描3期,共掃描42期。所有患者檢查后均采用奧沙利鉑+替吉奧進行NAC,共持續治療4個周期后評估療效。
1.3 評估標準 所有患者均于術后進行病理學檢測,根據Mandard標準進行腫瘤退縮分級(TRG)[6],具體如下:TRG1:腫瘤完全退縮;TRG2:大部分瘤床纖維化,僅有單個或小灶癌細胞殘留;TRG3:纖維化區域大于腫瘤殘留區域;TRG4:纖維化區域小于腫瘤細胞殘留區域;TRG5:腫瘤無退縮。
1.4 觀察指標 使用磁共振掃描儀自帶軟件處理DCE-MRI圖像,進行量化分析,先配準并載入圖像,選擇腹主動脈作為輸入動脈,并于病灶最大層面勾畫感興趣區(ROI),避開明顯壞死、出血等區域,計算動脈輸入函數(AIF),得出藥代動力學量化參數容量轉移常數(Ktrans)、速率常數(Kep)、血管外細胞外間隙容積比(Ve)
1.5 統計學方法 采用統計學軟件SPSS22.0行數據單因素分析,計數資料以百分率表示,采用χ2檢驗,計量資料以均數±標準差表示,兩組比較采用t檢驗,以P<0.05提示差異有統計學意義。
2 結果
2.1 5組患者DCE-MRI定量參數比較 TRG1組、TRG2組、TRG3組Ktrans、Kep、Ve值均明顯高于TRG4組、TRG5組(P<0.05)。見表1。
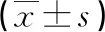
表15組患者DCE-MRI定量參數比較
2.2 兩組患者NAC前DCE-MRI定量參數比較 有效組患者Ktrans、Kep、Ve值均明顯高于無效組(P<0.05)。見表2。
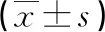
表2兩組患者NAC前DCE-MRI定量參數比較
2.3 預測效能分析 DCE-MRI定量參數Ktrans、Kep、Ve值對進展期胃癌患者NAC療效預測的截斷值分別為0.16/min、0.74/min、0.26,其ROC曲線AUG分別為0.975、0.793、0.869。見圖1、表3。

圖1Ktrans、Kep、Ve值預測進展期胃癌患者NAC療效的ROC曲線

表3ROC曲線參數
3 討論
DCE-MRI是一種無創評估腫瘤血管改變情況的影像學檢查方法,其參數可反映病灶組織血管的生理學和解剖學特點,常被用于抗腫瘤療效的評估中。DCE-MRI定量參數中的Ktrans值主要反映血容量、血流量以及在腫瘤組織間隙及血漿中藥物的交換能力,同時也是最具代表性的血管通透標志物,其數值越大,血管通透性越強。本文結果顯示,有效組的Ktrans值明顯高于無效組,且Ktrans值預測進展期胃癌患者NAC療效ROC曲線顯示其AUG為0.975,這說明高血管通透性及血流灌注可使NAC藥物更好的滲透進入腫瘤組織中,有助于消滅腫瘤細胞。這與劉曉冬等[7]的研究結果一致,提示Ktrans值可反映進展期胃癌患者NAC不同療效間的血流灌注差異,可為NAC治療效果評估提供重要參考。
DCE-MRI定量參數中的Kep值通常與組織血管通透性及血管表面積有關,主要反映對比劑擴散后回到血管內的速度,其數值越大表明血管通透性越強。本文結果顯示,有效組的Kep值明顯高于無效組,且Kep值預測進展期胃癌患者NAC療效ROC曲線顯示其AUG為0.793,這與焦學瑩等[8]在評估DCE-MRI定量參數預測肺癌化療療效時的研究結果一致,這可能是因為,在進行化療后患者受栓塞劑阻塞及化療藥物的殺傷作用導致病灶區域血流灌注及血流通透性降低[9-10],從而使Kep值減小,不利于NAC取得良好療效,提示Kep值可作為癌癥患者化療效果評估的重要指標。
DCE-MRI定量參數中的Ve值為單位體素中血管外細胞外間隙的容積,其數值越大表明單位體素中血管外細胞間隙越大,與細胞密度及微血管密度相關。本文結果顯示,有效組的Ve值明顯高于無效組,且Ve值預測進展期胃癌患者NAC療效ROC曲線顯示其AUG為0.869。這可能是因為當Ve值較高時表示患者腫瘤組織間存在較大的血管外細胞間隙,能使NAC藥物更容易進入到腫瘤組織中,有效消滅腫瘤細胞。但也有相關文獻得出不同結果[11-12],推測Ve值在不同腫瘤中可能存在不同結果。
但本次研究仍有不足之處,如樣本量過少,得出實驗結果可能存在偏差;醫師在勾畫ROI區域時可能存在一定誤差,影響后續研究結果,在往后勾畫ROI區域時應多參考超聲圖像,盡量做到精確勾畫。
綜上所述,DCE-MRI定量參數能有效評估進展期胃癌患者術前NAC療效,為患者選擇化療方案提供重要依據。

