聚乙烯醇-細菌纖維素復合可吸收生物屏障膜的制備及理化性能研究
趙正宜,肖劍虹,劉重遠,鄒多宏,2
引導性骨再生(guided bone regeneration, GBR)技術已經成為牙槽骨缺損修復與再生的常規及有效的治療方案。目前臨床常應用的屏障膜為可吸收生物膜,存在機械強度弱,容易穿孔并破裂等缺點[1]。聚乙烯醇(polyvinyl alcohol, PVA)是一種由聚醋酸乙烯酯水解而成的,無色、無毒、無腐蝕性、可降解的水溶性有機高分子聚合物。PVA所表現出來的性能在生產、生活中具有相當廣泛的應用,例如造紙、紡織品、粘合劑、涂料、薄膜以及藥物輸送等[2-4]。細菌纖維素(bacterial cellulose, BC)是一種天然纖維素,由醋酸桿菌、固氮菌、根瘤菌及假單胞菌等細菌產生[5]。BC不同于植物纖維素,其具有獨特的結構特性,如高化學純度、高楊氏模量、高吸水能力以及超細的網狀纖維狀結構,在醫用敷料、組織工程及納米合成功能材料等領域具有廣泛的應用前景[6-7]。該研究主要采用溶液共混的方法將PVA與BC共混,制備PVA-BC可吸收生物屏障膜,并對其物理性能和生物相容性進行研究,探索其作為新型骨組織工程生物屏障膜的可行性,為將來臨床應用提供一種選擇。
1 材料與方法
1.1 實驗材料PVA 1 750±50(上海國藥集團化學試劑有限公司),BC(生化級,阿拉丁生化科技股份有限公司,上海),鼠胚胎成纖維細胞(NIH/3T3細胞,中國科學院細胞庫)。
1.2 試劑和儀器DMEM、胰酶消化液(美國Hyclone 公司);胎牛血清(美國Gibco 公司);CCK-8試劑盒(日本株式會社同仁化學研究所);力學萬能實驗機(5565A,美國英斯特朗公司);CO2孵箱(美國Thermo 公司);掃描電鏡(Supra40,德國蔡司公司);X 射線衍射儀(X′Pert3 Powder,荷蘭帕納科公司);傅里葉變換紅外光譜儀(Nicolet 8700,美國熱電尼高力儀器公司);酶標儀(美國Bio-tek 公司)。
1.3 薄膜制備首先配制1 g/L PVA溶液,稱取PVA固體加入去離子水中,放入磁子,在90 ℃下攪拌3 h獲得透明PVA溶液。將BC以不同含量加入到PVA溶液中,分別制備PVA∶BC質量分數比為10 ∶3、10 ∶5、10 ∶7、10 ∶9的溶液,攪拌2 h形成均勻的PVA/BC二元共混液,置于真空箱內多次去除氣泡,然后將混合液倒入培養皿中,置于恒溫加熱臺等待24 h干燥成膜,見圖1。

圖1 PVA-BC復合膜的合成方案及形貌
1.4 力學測試薄膜拉伸實驗使用萬能力學試驗機(Instron 5565,美國) 進行測試,使用500 N重力傳感器,速度為0.01 mm/s。條形樣品(50 mm×3 mm) 在室溫條件下進行拉伸。每組樣品重復測試6次。取抗拉強度最大的復合膜組,重新制備待測樣品后浸泡于去離子水中1 h,同樣的方法測量濕態樣品抗拉強度,最后繪制出相應的應力-應變曲線和斷裂應力值圖。
1.5 樣品表征選取抗拉強度最大的復合膜組和純PVA膜組樣品,力學測試后收集斷裂截面,經過制樣、噴金等步驟,用掃描電鏡觀察兩組截面的微觀結構。采用X射線衍射分析儀掃描檢測PVA、BC和PVA-BC薄膜,掃描速度為0.2°/min,在5°~55°(2θ)范圍內進行分析。分別將PVA、BC和PVA-BC薄膜樣品在傅里葉變換紅外光譜儀上進行各成分分析,采集波長范圍為500~4 000 cm-1。
1.6 細胞相容性實驗采用CCK-8法測定薄膜對細胞增殖能力和活力的影響。取抗拉強度最大的復合膜組和純PVA膜組,兩組分別作為實驗組和陰性實驗組,按照國際標準組織(ISO/EN 10993-12)[8]規定提取浸提液。將滅菌后的上述兩組樣品分別浸泡于含10%胎牛血清和1%青霉素/鏈霉素的DMEM培養基中,樣品與培養基的比例為1 g/10 ml,24 h后獲得浸提液。使用96孔板,NIH/3T3細胞播種,細胞密度為每孔1×104個,空白對照組細胞僅用培養基培養,陰性實驗組和實驗組細胞貼壁后分別更換為每孔100 μl的純PVA膜和抗拉強度最大的復合膜浸提液,每組每個時間點5個復孔,在37 ℃、5%CO2培養箱中培養。在第1、4、7天,配置含10% CCK-8的DMEM,每孔加100 μl,37 ℃、5%CO2培養 2 h。用酶標儀在 450 nm 處讀取吸光度(optical density, OD)值。
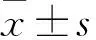
2 結果
2.1 各組膜抗拉強度的比較圖2為各組薄膜樣品應力-應變曲線及斷裂應力值。在一定范圍內,隨著BC含量的增加,PVA-BC復合膜的抗拉強度也增加,當PVA與BC的質量分數比為10 ∶7時,復合膜的抗拉強度達到最大(155.5±14.7) MPa,顯著高于純PVA薄膜(56.0±6.7) MPa。隨后繼續增加BC的含量,抗拉強度開始下降,各組差異有統計學意義(F=67.239,P<0.001);兩兩比較顯示,純PVA膜組與10 ∶3、10 ∶5、10 ∶7、10 ∶9 PVA-BC組組間差異均有統計學意義(P<0.05),10 ∶7 PVA-BC組與10 ∶3、10 ∶5、10 ∶9 PVA-BC組組間差異均有統計學意義(P<0.05),即當PVA與BC質量分數比為10 ∶7時,復合膜的抗拉強度最大。考慮到GBR膜實際使用為體內濕態環境,取干態抗拉強度最大的10 ∶7 PVA-BC膜組進行濕態下的力學測試。圖2C、2D顯示濕態下的復合膜強度達到(13.8±1.2) MPa。

圖2 PVA-BC復合膜的抗拉強度測試A:各組樣品的典型拉伸應力-應變曲線;B:各組樣品的斷裂應力值;與PVA組比較:#P<0.05;與10 ∶7組比較:*P<0.05;C:PVA-BC復合膜的典型拉伸應力-應變曲線干濕態對比;D:PVA-BC復合膜的斷裂應力值干濕態對比
2.2 試件表征純PVA薄膜和PVA-BC復合膜的橫斷面電鏡下觀察結果顯示,PVA薄膜的斷面光滑致密,幾乎無孔(圖3A、3B),共混膜PVA-BC的橫斷面形貌略粗糙于純PVA膜,厚度約為30 μm,BC的加入降低了材料的延展性,形成強韌的薄膜。結果表明,PVA薄膜加入BC后韌性和拉伸強度均有提高,未觀察到團聚和宏觀上的分離情況,表明薄膜中PVA和BC分散良好(圖3C、3D)。XRD結果顯示混合薄膜顯示出多個衍射峰,分別為PVA的特征峰19°和BC的3個特征峰14°、16°和22°。圖3F顯示復合膜在3 410 cm-1處有1個寬闊的吸收峰,在 2 939 cm-1、1 424 cm-1、1 142 cm-1、1 093 cm-1和851 cm-1均存在吸收峰,表明復合膜與PVA結晶度相關。復合膜在3 400 cm-1、2 920 cm-1、1 643 cm-1及1 064 cm-1附近有明顯吸收峰,表明所得產物具有纖維素的特征峰(圖3E)。

圖3 PVA-BC復合膜的微觀結構和成分分析A、B:純PVA薄膜截面;C、D:PVA-BC復合膜截面;E:PVA-BC復合膜的X射線衍射結果;F:PVA-BC復合膜的傅里葉變換紅外光譜結果
2.3 細胞相容性實驗結果CCK-8法檢測結果顯示,在共培養的第1、4、7天的相同時間點進行檢測,NIH/3T3細胞在空白對照組、陰性實驗組和實驗組都保持了較高的增殖水平,相同時間點各組OD值差異均無統計學意義(P>0.05) ,見表1。說明PVA-BC薄膜具有良好的生物相容性。

表1 各組材料與NIH/3T3細胞共培養不同時間后的OD值比較
3 討論
GBR技術中的屏障膜將快速增長的軟組織與緩慢生長的骨組織分離開,以達到屏障的作用,最終達到牙槽骨組織的修復與再生的效果。目前使用的GBR膜可分為可吸收膜和不可吸收膜,不可吸收膜雖然具有更加穩定的機械性能以提供穩定的骨修復環境,但卻需要二次手術取出,另外也存在術后暴露的問題,從而增加了患者的二次創傷及骨增量失敗的風險[9];可吸收膜由天然或合成材料制成,植骨術后一定時間(2周至幾個月不等)完成吸收,無需二次手術取出,在一定時間內有效阻止了軟組織進入骨修復區域,從而促進了新骨形成。但可吸收生物屏障膜存在機械強度不足的問題,這樣不利于牙槽骨修復的效果,特別針對大面積骨缺損的修復重建(高度/寬度>5 mm)。
因此,本研究將PVA溶液和BC溶液以不同比例混合攪拌制備PVA-BC薄膜,旨在制備出新型可代謝高機械性能GBR膜。PVA本身具有高親水性和優異的力學性能,無毒且溶于水,具有良好的可降解性,是一種生物相容性良好的水凝膠,具有生物醫學應用所需的特性[10]。BC在生物材料領域有著廣泛的應用,其具有生物相容性好、親水性強、機械強度高、比表面積大等優點,已有多項研究[11-12]表明,向聚合物網絡中引入BC可大大提高復合物的機械性能,可充當納米復合材料的增強添加劑[13]。因此,本研究旨在制備一種基于PVA的復合材料,由PVA作為連續相,添加BC作為增強納米材料,BC可通過廣泛形成氫鍵與PVA聚合物基體發生強烈的相互作用,使PVA和BC納米纖維表面形成牢固的界面,形成非常堅固的納米復合材料[14]。完成制備后進行拉伸測試,當PVA與BC質量分數比為10 ∶7時,復合膜抗拉強度達到最大(155.5±14.7) MPa,此外,PVA和BC的高保水性使薄膜具有足夠的柔韌性和濕潤性,取該最強組,測試濕態下抗拉強度為(13.8±1.2) MPa,顯著高于市售Bio-Gide膠原膜1.16 MPa[10]。因此,該復合膜在濕態情況下也具備一定強度。生物相容性實驗表明PVA-BC膜具有良好的生物相容性。
綜上所述,本研究通過溶液共混法制備出PVA-BC復合膜,并探索出最佳機械性能比例,對其結構、成分、形態進行表征,并進行生物相容性檢測。結果表明,這種復合膜具有較高的機械性能,且生物相容性良好,具備成為GBR膜候選材料的潛力。下一步將通過體內大動物實驗進一步明確其在牙槽骨缺損修復與再生中的作用。

