高強度聚焦超聲消融術聯合不同藥物治療子宮腺肌病的臨床療效
董 欣,張亞琴,龐曉卿,秦麗欣,楊 茉,任 鵬,李曉雪
子宮腺肌病(adenomyosis,AM)是指具有生長功能的子宮內膜腺體和間質侵入子宮肌層內,在體內性激素的影響下局限或彌漫性生長的一種婦科良性疾病[1],主要癥狀為子宮增大、進行性痛經及月經量增多等,嚴重者可引起流產及不孕,嚴重影響患者的生活質量[2]。傳統的藥物治療無法根治,容易復發[3],子宮切除術或病灶切除手術創傷較大,影響生育功能[4]。近年來,聚焦超聲消融術(focused ultrasound ablation surgery,FUAS) 作為一種新型的無創技術得到快速發展,其安全性、有效性得到臨床廣泛的認可[5-7],但由于AM 病灶具有散在分布和界限不清的特點,所以單純進行FUAS很難徹底清除病灶,復發的可能性較大。本研究通過探討單純FUAS治療、FUAS聯合左炔諾孕酮宮內緩釋系統(levonorgestrel -releasing in uterine system,LNG-IUS)和FUAS聯合地諾孕素(dienogest,DNG)三種方案治療AM的臨床效果,旨在為制定臨床治療方案提供依據。
1 對象與方法
1.1 對象 選取2018-01至2020-10在我院經MRI檢查明確診斷的AM患者150例進行回顧性分析,均自愿接受FUAS治療且依從性好。據術后應用藥物不同分為:FUAS治療組(A 組)、FUAS治療+ LNG-IUS組(B組)和FUAS治療+DNG組(C組),每組50例。本研究經醫院倫理委員會批準。
1.2 入選和排除標準 入選標準:(1)符合《子宮腺肌病診治中國專家共識》中子宮腺肌病診斷標準,并經MRI確診;(2)有痛經、經期延長、月經量大等明顯臨床癥狀;(3)子宮肌壁單側增厚為主、如前壁型、后壁型或局限性病灶(腺肌瘤);(4)MRI檢查顯示子宮內存在界線不清、信號強度低的病灶,T2加權像可有高信號強度的病灶,子宮內膜-肌層結合帶變寬,>12 mm,且子宮肌壁厚度>30 mm;(5)在1年內局部病灶未接受過射頻、介入等治療;(6)2年內無生育要求者。排除標準:(1)合并陰道炎、盆腔炎、腫瘤等婦科或其他疾病;(2)月經期、哺乳期及孕產婦;(3)心腦血管、肝腎功能、造血功能、神經系統等嚴重功能不全;(4) 既往有結締組織疾病; (5)存在麻醉禁忌證,依從性差,不能配合治療。
1.3 方法 所有患者均進行FUAS治療:采用重慶海扶技術有限公司研制JC-200型高強度聚焦超聲腫瘤治療系統,根據病灶范圍制定消融計劃,治療功率350~400 W,以點輻照方式布點治療病灶靶區。根據病灶和患者的反應來調整輻照參數,直至全部計劃治療區域出現滿意的灰度變化,最后超聲造影評價消融范圍,滿意后結束治療。A組僅接受FUAS治療;B組FUAS術后1周內在超聲引導下放置LNG-IUS;C組FUAS術后3 d開始口服DNG,2 mg/次,1次/d,持續12個月以上。3組均連續觀察12個月。
1.4 觀察指標及療效標準 分別在治療前(T1)及治療后3個月(T2)、6個月(T3)、12個月(T4) 時觀察以下指標:(1)子宮體積、病灶體積,通過磁共振檢查或超聲檢查結果進行測量并計算,子宮體積(cm3)=縱徑×橫徑×前后徑×0.523,病灶體積(cm3)=縱徑×橫徑×前后徑×0.523。(2)病灶消融率,腺肌病灶消融體積(cm3)=縱徑×橫徑×前后徑×0.523;消融率(%)=無造影劑灌注區體積/腺肌病灶體積×100%。(3)腫瘤標志物,采集靜脈血放射免疫法檢測患者血清糖類抗原125(CA125)水平。(4)痛經程度,采用視覺模擬(VSA)評分評價患者的痛經程度,0分為無疼痛;1~3分為輕度疼痛,可接受;4~6分為重度疼痛,勉強接受;7~10分為無法忍受,記錄VAS分值。(5)貧血程度,檢測靜脈血血紅蛋白(HB)的含量,評估貧血程度。(6)不良反應及并發癥:骶尾部損傷、皮膚損傷、腸道損傷、陰道異常子宮出血、環異位、脫環、盆腔炎、頭痛、便秘、惡心、潮熱等。
2 結 果
2.1 一般資料比較 3組患者年齡、子宮體積、病灶體積和消融率差異無統計學意義(P>0.05,表1),具有可比性。3組共完成隨訪142例,A組入選44例,失訪3例,行子宮切除術3例;B組入選48例,失訪1例,行子宮病灶切除手術1例;C組入選47例,失訪2例,未堅持服藥1例。
表1 3組子宮腺肌病患者一般資料比較
2.2 不同時間相關指標比較 與T1比較,3組患者T2-T4時,子宮體積、病灶體積均明顯縮小,CA125水平明顯降低,差異有統計學意義(P<0.05)。與A組比較,B、C組子宮體積、病灶體積T4時均明顯縮小,CA125水平T3、T4時均明顯降低,差異有統計學意義(P<0.05);且C組子宮體積T4時明顯小于B組,CA125水平T3、T4時也明顯低于B組,差異有統計學意義(P<0.05,表2)。
表2 3組子宮腺肌病患者不同時間點子宮體積、病灶體積、CA125水平的情況
2.3 VAS評分與HB數值比較 與T1比較,3組患者T2-T4時VAS評分均明顯降低,HB均明顯升高,差異有統計學意義(P<0.05);與A組比較,B、C兩組VAS評分T4時明顯降低,差異有統計學意義(P<0.05,表3),且C組VAS評分T4時明顯低于B組,差異有統計學意義(P<0.05)。
表3 3組子宮腺肌病患者不同時間點VAS評分與HB的情況
2.4 不良反應 3組均未發生皮膚損傷及腸道損傷等不良反應,未出現同床不適、潮熱、惡心、嘔吐等不適癥狀。3組均發生陰道不規則出血和骶尾骨疼痛,但差異無統計學意義,經對癥處理6個月內消失。見表4。
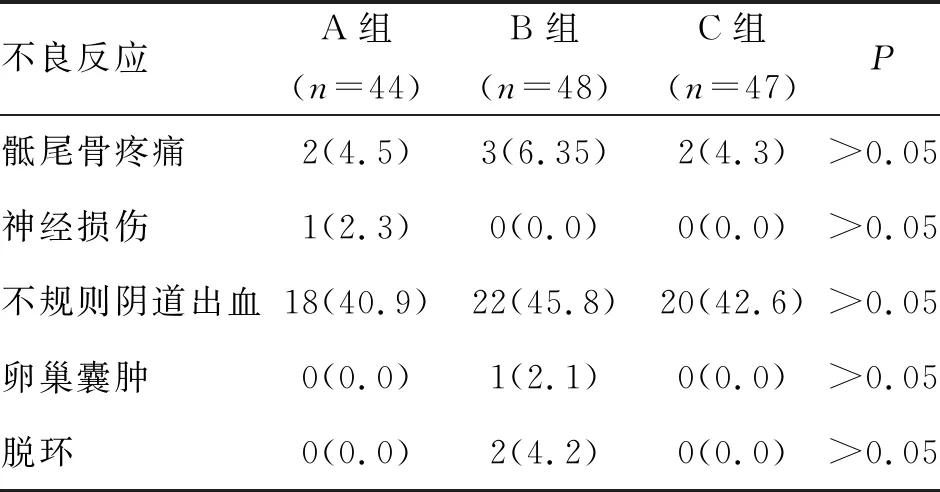
表4 3組子宮腺肌病患者不良反應情況 (n;%)
3 討 論
AM 是一種婦科常見的良性腫瘤,傳統的治療方式主要包括藥物治療或手術治療[8]。藥物治療創傷最小,多以緩解臨床癥狀、滿足患者生育要求和幫助部分患者安全過渡到絕經期,免于子宮切除為目的,但長期服用藥物,用量大,不良反應多,且停藥后易復發[9]。子宮切除術對于有生育需求的育齡期婦女并不適合。有研究發現,FUAS 聯合長期藥物治療在防治AM 復發方面具有一定的臨床效果,但這些治療措施的臨床效果尚缺乏對比性的臨床經驗[10,11]。鑒于此,本研究比較了單純FUAS 治療、FUAS 聯合LNG-IUS 和FUAS 聯合DNG 治療后患者子宮體積、病灶體積、CA125水平的變化,以及患者痛經程度和貧血狀況的變化,探討聯合治療方案對AM的治療效果。
有研究表明,血清CA125水平可反映AM 病灶大小和范圍,對AM 復發的監測具有重要價值,痛經緩解程度與血清CA125下降相關[12,13]。本研究結果表明,所有患者在FUAS 治療后的12個月內,其子宮體積、病灶體積均較治療前顯著縮小,痛經程度和CA125水平明顯降低,而且HB 明顯上升,說明單純FUAS 治療和FUAS聯合治療方案均可以緩解痛經、貧血的臨床癥狀,這也進一步證實了FUAS治療AM 的有效性[3]。本研究還發現,C組治療3個月后,子宮體積、病灶體積、CA125水平、VAS 評分明顯低于A 組,在觀察的12個月內子宮體積持續縮小,且CA125水平持續下降,并維持在正常水平。治療后12個月,B、C兩組子宮體積、病灶體積、CA125水平、VAS 評分明顯小于A 組,說明FUAS 聯合兩種藥物治療在預防復發、緩解痛經方面均優于單純FUAS 治療。分析其原因可能與以下幾點有關:(1)在預防復發方面,LNG-IUS 在宮腔內釋放高濃度的左炔諾孕酮(LNG)能抑制子宮內膜中雌激素受體的合成[14],降低子宮內膜生長速度,從而降低病灶復發率;而DNG 則能同時抑制卵巢的內分泌功能以及子宮內膜細胞的增殖和纖維化的雙重作用來降低子宮內膜的增殖速度,降低復發率,因此其效果更明顯。(2)在緩解痛經方面,AM痛經的發生與異位病灶產生高濃度的前列腺素及炎癥因子,導致的子宮痙攣性收縮有密切關系。宮腔放置LNG-IUS 后,局部釋放的高濃度左炔諾孕酮可使異位的內膜蛻膜化和萎縮[15],還能降低子宮平滑肌對縮宮素的敏感性及興奮性,降低子宮收縮的強度,減輕痛經的程度[14,15]; DNG不但可以通過降低內膜增殖速度,緩解由于纖維組織過度增殖和纖維化、瘢痕形成所引起的疼痛[16],還可通過抗炎和抑制新生血管形成發揮緩解疼痛的作用[17,18],作用更迅速更廣泛。因此,FUAS 聯合DNG治療在緩解痛經和預防復發方面優于單純FUAS 和FUAS 聯合LNG-IUS。另外,由于DNG無蓄積性,對患者機體激素代謝影響較小,安全性較高[19],可以長期服用。但其價格較為昂貴,且部分患者依從性較差,提示臨床制定AM 長期治療方案時,除考慮患者年齡、子宮情況、卵巢儲備功能、生育需求等因素外,還需要考慮患者經濟狀況、依從性等因素,盡量做到個體化和規范化治療[10]。FUAS 聯合LNG-IUS 組僅有2例在術后6個月發生脫環,其原因也與AM 患者在接受FUAS 治療后,子宮體積逐漸縮小有一定的關系。
綜上所述,FUAS治療AM時,聯合用藥方式在防止復發、緩解癥狀方面效果更好,且以聯合DNG藥物治療效果為佳,但不論選擇何種治療方式均應考慮到患者的依從性,以選擇患者易于接受的治療方式為前提。本研究還存在樣本量較小、隨訪時間較短等問題,下一步將針對遠期療效及DNG對肝酶、血脂、血流變和骨密度影響等方面進行前瞻性研究。

