硅酸鈉誘導的馬鈴薯抗黑痣病StWRKY11基因克隆及生物信息學分析
張冬梅,馮亞艷,修志君,楊春芳,杜美娥,李得宙,張笑宇
(1.內蒙古農業大學 園藝與植物保護學院,內蒙古 呼和浩特 010020;2.內蒙古自治區農牧業科學院植物保護研究所,內蒙古 呼和浩特 010031;3.鄂爾多斯生態環境職業學院 生態工程系,內蒙古 鄂爾多斯 017010;4.內蒙古農業大學 農學院,內蒙古 呼和浩特 010019;5.內蒙古農業大學 發展規劃處,內蒙古 呼和浩特 010018)
馬鈴薯黑痣病(RhizoctoniasolaniKühn)是馬鈴薯生產中的主要病害。目前主要使用化學防治,而相比于化學防治,誘導抗病性具有長效、不污染環境的特點,已被廣大學者關注。硅證實是具有誘導植物抗病性的礦質營養元素[1],但其抗性機制沒有定論,尤其對分子抗病機制研究的很少。WRKY轉錄因子作為誘導型調節因子,主要功能是激活或抑制特定基因的轉錄,影響植物體內蛋白質的表達[2]。該轉錄因子的共同特點是具有1~2個WRKY結構域,結構域C端具有1個C2H2或C2HC的鋅指結構[3]。根據結構域數量及鋅指結構的類型將其分為3個組,第1組一般包含2個WRKY域,鋅指結構模式為CX4-5CX22-23HXH;第2組和第3組一般都只包含1個WRKY域,但第3組僅在組成鋅指的氨基酸有變化,為CX7CX22-23HXC[4]。WRKY轉錄因子通過結合核酸序列的靶基因啟動子區域W-box(T)(T)TGAC(C/T)調控相關基因表達[5],其中TGAC是核心,固定不變[6],W-box對WRKY轉錄因子功能的發揮具有不可或缺的作用[7]。W-box主要存在于與植物衰老、逆境脅迫、抵抗病原物等相關的基因區域以及水楊酸等誘導基因的啟動子中[8]。
目前,針對WRKY轉錄因子的研究主要集中在擬南芥、水稻、玉米等已測序的物種上,在馬鈴薯中的研究起步較晚且較少。馬鈴薯中已報道82個WRKY轉錄因子[9],Dellagi等[10]研究StWRKY1基因可受軟腐病誘導表達,該基因可參與馬鈴薯對軟腐病的抗性作用。β-氨基丁酸(BABA)誘導馬鈴薯體內的StWRKY5基因[11-12]和StWRKY8基因[13]上調表達調控對晚疫病菌的抗性。轉錄因子WRKY參與馬鈴薯黑痣病的抗性目前未見相關報道。
有報道,WRKY11基因可參與植物的生物脅迫調控,對擬南芥的研究中,可負調控丁香假單胞菌番茄致病變種(Pseudomonassyringaepv.tomato,Pst)[14]、蠟樣芽孢桿菌(Bacilluscereus)AR156[15]和甜菜線蟲(Betavulgaris)[16]誘導的抗病反應;該基因上調表達可提高煙草對赤星病(Alternariaalternate)的抗性[17]。在水稻[18]、擬南芥[19]、煙草[20]、大豆[21]、毛竹[22]和陸地棉[23]的抗高溫、抗旱、抗鹽、抗衰老過程中,有報道WRKY11基因可以參與植物的生長發育過程,調控植物對外界不良環境的抵抗能力。馬鈴薯StWRKY11基因與抗病性方面的相關研究未見報道。
前期明確了硅酸鈉增強馬鈴薯黑痣病菌抗性[24-25],基于硅酸鈉誘導馬鈴薯黑痣病抗性的轉錄組信息,選取上調表達量高的StWRKY11。本研究克隆StWRKY11基因,并利用生物信息學網站對該基因及編碼的蛋白進行了理化性質、信號肽與跨膜結構、結構域預測、亞細胞定位和基因啟動子區順式作用元件預測等生物信息分析,旨在為研究該基因功能,揭示硅酸鈉增強馬鈴薯黑痣病抗性的分子機制。
1 材料和方法
1.1 材料和試劑
供試植物材料:馬鈴薯大西洋(Atlantic)脫毒組培苗,是內蒙古農業大學園藝與植物保護學院植物病理課題組莖尖剝離,病毒檢測的無毒組培苗。供試病原菌:立枯絲核菌(RhizoctoniasolaniAG-3),是本課題組分離鑒定并對馬鈴薯具有強致病性的病原菌。供試培養基:PSA培養基、LB培養基、MS固體培養基、MS液體培養液。
供試試劑:Plant RNA Extraction Kit試劑盒、PrimeScriptTMⅡ 1st Strand cDNA Synthesis Kit反轉錄試劑盒、pMD-19T克隆載體、大腸桿菌感受態細胞DH5α、2 000 bp DNA Marker均購自寶日醫生物技術(北京)有限公司;Easy Taq DNA Polymerase、dNTPS、10×Easy Taq Buffer和瓊脂糖購自全式金試劑公司;瓊脂糖凝膠DNA回收試劑盒(PD209-02)及質粒小提試劑盒(PD103-02)購自天根生化科技(北京)有限公司;氨芐抗生素購自北京索萊寶科技有限公司;其他化學試劑均購于國內試劑公司。
1.2 試驗方法
1.2.1 試驗設計 將馬鈴薯黑痣病菌置于PSA培養基上28 ℃培養5 d,將培養基和病原菌一起用組織搗碎機搗碎,加水稀釋成濃度為1.0×107個菌絲段/cm3的菌絲懸浮液,作為病原菌接種體。將在MS培養基上培養17~18 d的馬鈴薯大西洋脫毒組培苗,移栽至盛有400 g左右無菌蛭石的直徑18 cm、高20 cm的花盆中,每盆5株,共12盆。每7 d澆1次MS營養液,每次500 mL,培養30 d施硅酸鈉并接菌,即澆入含NaSiO3·9H2O(濃度為3.02 g/L)的MS營養液500 mL,同時將病原菌接種體接種至馬鈴薯幼苗地上莖基部向下約3 cm處,每株接種3 mL,以接菌不施硅酸鈉為對照,于生長季在內蒙古農業大學農場室外培養,處理4 d對馬鈴薯幼苗的地下莖取樣,將樣品用液氮冷凍,置于-80 ℃超低溫冰箱中保存備用。
1.2.2 馬鈴薯StWRKY11基因克隆
1.2.2.1 馬鈴薯地下莖RNA提取及cDNA合成 利用 Plant RNA Extraction Kit試劑盒提取處理4 d的馬鈴薯地下莖總RNA,檢測其完整性、濃度和純度;利用PrimeScriptTMⅡ 1st Strand cDNA Synthesis Kit反轉錄試劑盒將其合成第一鏈cDNA,于-20 ℃保存備用。
1.2.2.2StWRKY11基因擴增 以轉錄組數據中StWRKY11基因ORF序列為模板,利用Primer Premier 5.0設計引物,上游引物:5′-ATGGCTGTAGATTTGTTAAATTATTCG-3′;下游引物:5′-CTAAATCTCTAACCCTAATCGTTCTCC-3′。反應體系為25 μL,包括17.5 μL RNase Free dH2O,1.0 μL cDNA,0.5 μL EasyTaqDNA Polymerase,1.5 μL dNTPs Mix,2.5 μL 10×Easy Taq Buffer,上下游引物各1.0 μL。反應條件為:94 ℃預變性5 min;94 ℃變性30 s,54 ℃退火30 s,72 ℃延伸30 s,35個循環;72 ℃延伸10 min;12 ℃保存。PCR產物經1.0%瓊脂糖凝膠電泳檢測。利用天根瓊脂糖凝膠(DNA)純化試劑盒對目的片段進行回收純化,用Nanodrop檢測其濃度和純度。
1.2.2.3StWRKY11基因克隆載體構建 將PCR膠回收產物連接到pMD19-T克隆載體上,連接反應體系為10 μL,包括4.0 μL膠回收產物DNA,1.0 μL pMD-19T,5.0 μL Solution Ⅰ,反應條件為16 ℃連接1 h。將重組連接產物轉化到DH5α大腸桿菌感受態細胞中,再于37 ℃恒溫培養14 h,在 LB(Amp+) 培養基上篩選陽性克隆菌落,挑取單克隆菌落在LB(Amp+)液體培養基,于37 ℃、180 r/min恒溫搖床振蕩培養12 h。利用1.2.2.2中StWRKY11基因特異性引物將陽性克隆DH5α大腸桿菌菌液進行PCR擴增,PCR產物經1.0%瓊脂糖凝膠電泳檢測,選取具有明顯電泳條帶的陽性克隆菌液送至生工生物工程(上海)股份有限公司測序,結果通過DNAMAN進行序列比對,確定目的基因成功連入克隆載體。利用天根質粒小提試劑盒對測序結果一致性高的菌液進行重組質粒提取,并用Nanodrop檢測其濃度和純度。
1.2.3StWRKY11基因的生物信息學分析 根據已有的StWRKY11基因序列,翻譯獲得該蛋白質的氨基酸序列,利用NCBI數據庫ORF Finder(http://www.ncbi.nlm.nih.gov/projects/gorf/)獲得開放閱讀框并分析;運用ExPASy網站中的ProtParam(http://web.expasy.org/protparam/) 對蛋白質的理化性質進行預測;通過 ExPAsy-ProtScale(http://www.expasy.org/cgi-bin/protscale.pl) 在線分析蛋白質的親水性和疏水性;利用TMHMM Server v.2.0(http://www.cbs.dtu.dk/services/TMHMM/)和SignalP 4.1 Server(http://www.cbs.dtu.dk/services/SignalP/)對蛋白質進行跨膜結構域分析和信號肽分析;利用NetPhos 2.0 Server軟件(http://www.cbs.dtu.dk/services/NetPhos-2.0/)預測蛋白質的磷酸位點;蛋白質的二級結構通過SOPMA(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl?page=npsa_sopma.html)在線進行預測分析;利用Wolf PSORT Ⅱ軟件(https://wolfpsort.hgc.jp/)和Softberry(http://www.softberry.com/berry.phtml?topic=promoter)預測蛋白質亞細胞定位;利用 Phyre(http://www.sbg.bio.ic.ac.uk/phyre2/html) 預測蛋白質的三級結構建模;利用PLACE網站(https://www.dna.affrc.go.jp/PLACE/?action=newplace)對StWRKY11基因啟動子區順式作用元件預測;運用NCBI 的Blast選取與該基因編碼的蛋白質同源性較高且已有研究的其他物種的蛋白質氨基酸序列(表1),運用MEGA 7.0構建系統進化樹。
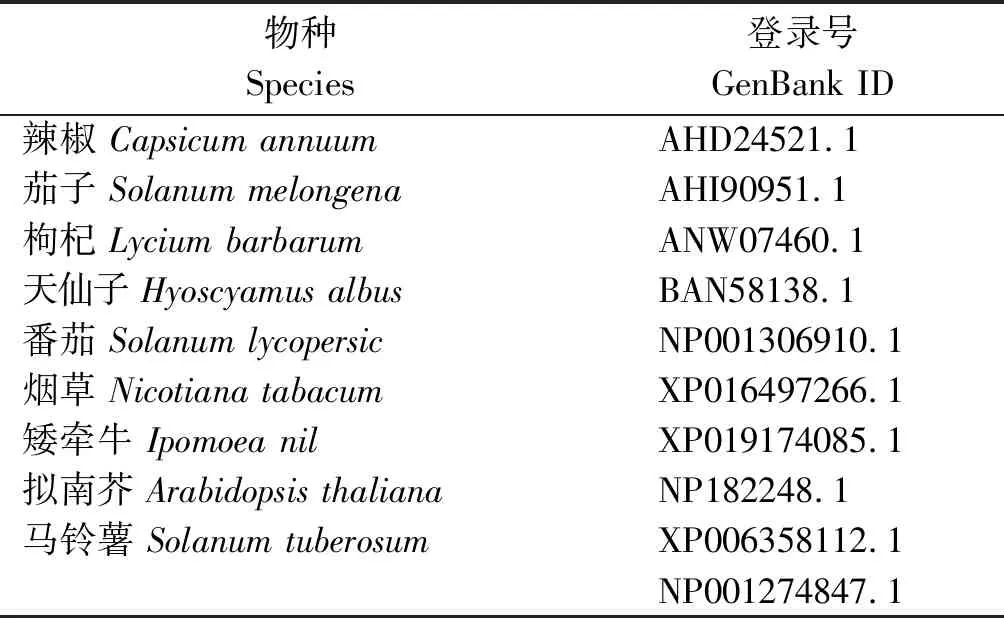
表1 不同物種的WRKY蛋白質氨基酸序列Tab.1 Amino acid sequences of WRKY proteins in different species
2 結果與分析
2.1 馬鈴薯StWRKY11基因的克隆
2.1.1StWRKY11基因擴增檢測結果 提取馬鈴薯地下莖總RNA,并反轉錄得到cDNA,以cDNA為模板,StWRKY11-F和StWRKY11-R為上下游引物,經PCR擴增,利用1.0%瓊脂糖電泳檢測,結果顯示,在1 000 bp處有清晰的電泳條帶(圖1),且周圍沒有雜帶,與預測的StWRKY11基因的大小1 005 bp基本吻合。該基因序列已提交NMDC,登錄號為NMDCN0000N91。

M.DL2000 Marker;1—2.StWRKY11擴增片段。M.DL2000 Marker;1—2.StWRKY11 amplified fragments.
2.1.2StWRKY11基因克隆載體構建StWRKY11基因擴增產物和pMD19-T克隆載體連接,轉化DH5α大腸桿菌后的菌液PCR擴增結果顯示(圖2),在1 000 bp處有清晰的電泳條帶,序列比對的結果顯示,相似度為97.41%,基因的CDS序列長度為1 005 bp,說明StWRKY11基因被成功連接到克隆載體上。
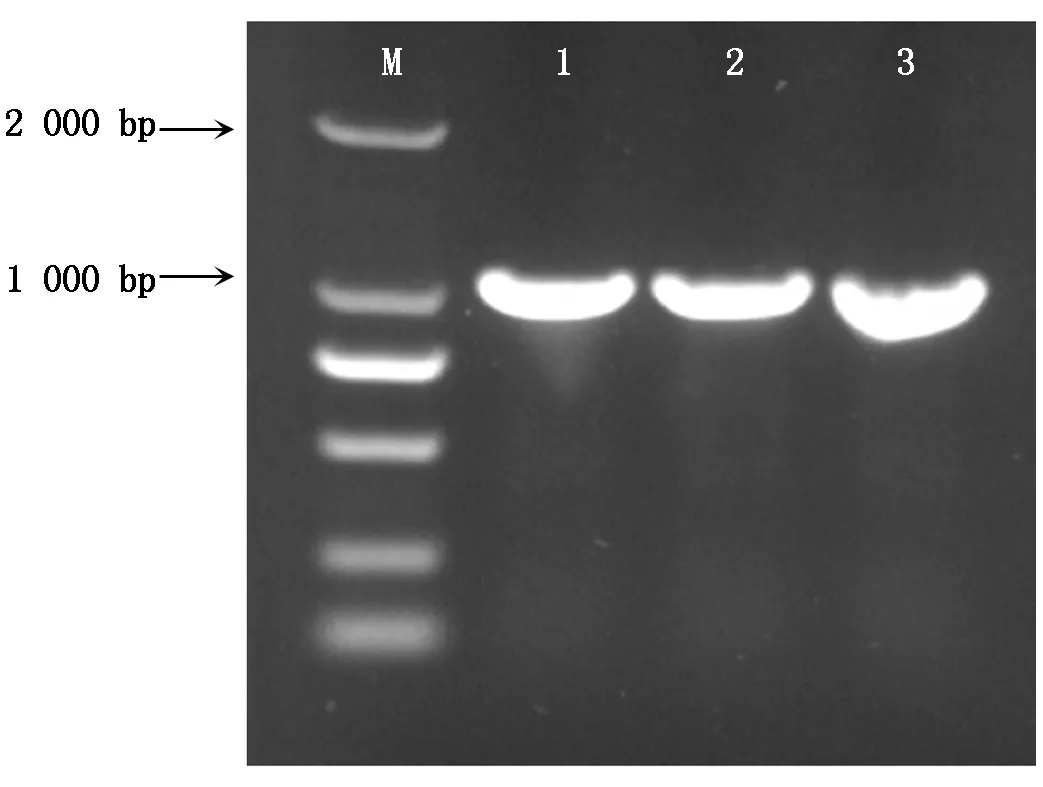
M.DL2000 Marker;1—3.StWRKY11基因克隆擴增片段。M.DL2000 Marker;1—3. StWRKY11 gene clone amplified fragment.
2.2 StWRKY11基因的生物信息學分析
2.2.1StWRKY11基因編碼的蛋白質理化性質及親疏水性分析 通過NCBI數據庫中ORF Finder對StWRKY11基因的開放閱讀框進行分析,結果表明,該基因編碼334個氨基酸,且含有鋅指結構CX5CX23HXH(圖3)。利用ProtParam網站對StWRKY11基因表達蛋白質理化性質進行預測,結果表明,其分子式為 C3013H5023N1005O1260S199,分子質量為81.867 94 ku,理論等電點(pI)為5.09,原子總數為10 500,脂肪族氨基酸指數為29.45,蛋白質的半衰期為10 h,不穩定指數為33.71(小于40),因此將其歸類為穩定蛋白質。

圖3 StWRKY11基因的堿基序列及其表達蛋白質氨基酸序列Fig.3 Sequence of StWRKY11 gene and amino acid sequence of its expressed protein
利用ExPAsy網站中ProtParam和ProtScale,結合分析蛋白質的疏水性和親水性表明,該基因編碼的蛋白質親水性平均值(GRAVY)為 0.746,在多肽鏈上最大值的異亮氨酸(Ile)為4.500,疏水性最強;最小值的精氨酸(Arg)為-4.500,親水性最強,StWRKY11基因編碼的親水性氨基酸小于疏水性氨基酸,推測該蛋白為疏水性穩定蛋白(圖4)。

圖4 StWRKY11基因表達蛋白質親水性/疏水性分析Fig.4 Hydrophilic/hydrophobic analysis of StWRKY11 gene expressed proteins
2.2.2StWRKY11基因表達蛋白質跨膜結構域及信號肽預測 利用TMHMM Server v.2.0網站分析StWRKY11基因表達蛋白質跨膜區分布,結果表明(圖5),該蛋白質沒有跨膜分布,不是一個膜結合蛋白質。通過SignalP 4.1 Server分析蛋白質信號肽,顯示其不含有N端信號肽,該蛋白質無信號肽,為非分泌蛋白質。
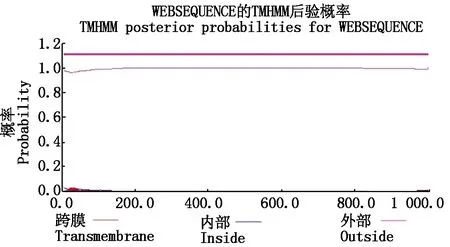
圖5 StWRKY11基因表達蛋白質跨膜區分析Fig.5 Transmembrane region analysis of StWRKY11 gene expression protein
2.2.3StWRKY11基因表達蛋白質磷酸化分析 利用NetPhos 2.0 Server分析StWRKY11基因編碼的蛋白磷酸化位點,結果顯示,共有29個磷酸化位點,其中有3個蘇氨酸(Thr)磷酸化位點分別在第97,127,277位氨基酸上;4個酪氨酸(Tyr)磷酸化位點分別在第55,117,239,244位氨基酸上;22個為絲氨酸(Ser)磷酸化位點,說明該蛋白能夠參與細胞內的生長分化以及信號轉導等多種生命活動。
2.2.4StWRKY11基因表達蛋白質二級結構預測及亞細胞定位分析 利用SOPMA網站對StWRKY11基因編碼的蛋白質二級結構進行分析,結果顯示,該蛋白質二級結構由α-螺旋、無規則卷曲、延伸鏈和β-轉角4種結構形式組成,其中無規則卷曲(Cc)占比最高,達61.68%,無規則卷曲可連接其他二級結構原件;而其他二級結構相對較少,α-螺旋(Hh)占16.77%,延伸鏈(Ee)占13.17%,β-轉角(Tt)占8.38%,這些結構散布于整個蛋白質中(圖6)。利用Wolf PSORT Ⅱ軟件和Softberry網站對該蛋白質亞細胞定位進行推測,其可能定位到細胞核中。
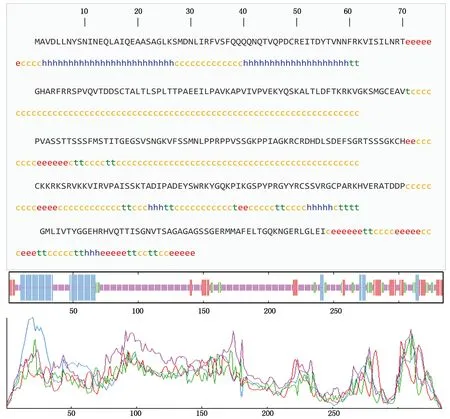
藍色.α螺旋;紅色.延伸鏈;綠色.β-折疊;黃色.無規則卷曲。Blue.α-helix;Red.Extended chain;Green.β-folding;Yellow.Random coiling.
2.2.5StWRKY11基因表達蛋白質三級結構預測 通過Phyre網站對StWRKY11基因編碼的蛋白質三級結構進行分析,結果顯示,該模型未形成多聚體和配體結構,且與擬南芥AtWRKY1基因編碼的蛋白質相似性最高,達55%(圖7)。
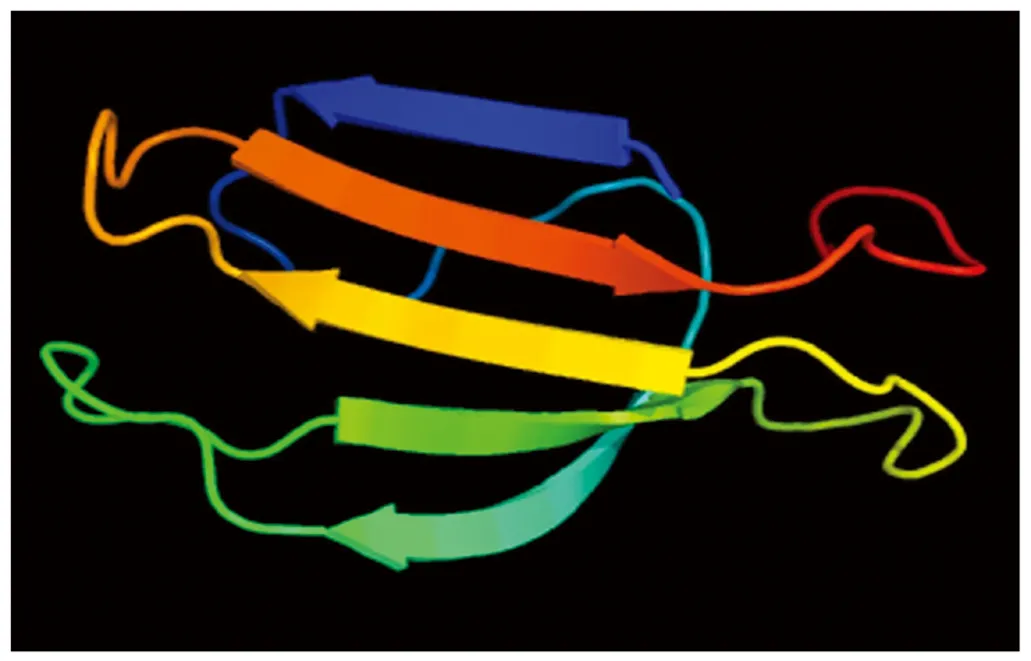
圖7 StWRKY11基因表達蛋白三級結構預測Fig.7 Prediction of tertiary structure of StWRKY11 gene expressed protein
2.2.6StWRKY11基因啟動子區順式作用元件預測 利用網站PLACE分析StWRKY11基因啟動子上游的順式作用元件可見(表2),啟動子上游區域含有轉錄因子固有的核心元件CAAT區(CAAT-box)和TATA區(TATA-box);逆境脅迫相關的順式作用元件,銅響應元件(CURECORECR)、MYB順式元件(MYB2AT)、DNA結合蛋白調控元件(DOFCOREZM)、轉錄激活元件(ARR1)、CGCG區(CGCG-box)和W-區(W-box);植物生長發育相關的順式作用元件,GATA區(GATA-box)、光調控順式元件(GT1CONSENSUS)、ARE調控元件(ARE)、葉肉特異基因表達調控元件(CACTFTPPCA1)、花粉調控元件(GTGANTG10)和脫水順式元件(CBFHV);激素響應相關的作用元件,赤霉素調控元件(PYRIMIDINEBOXOSRAMY1A)、茉莉酸調控元件(ASF1MOTIFCAMV)、脫落酸響應元件(ABRE)。
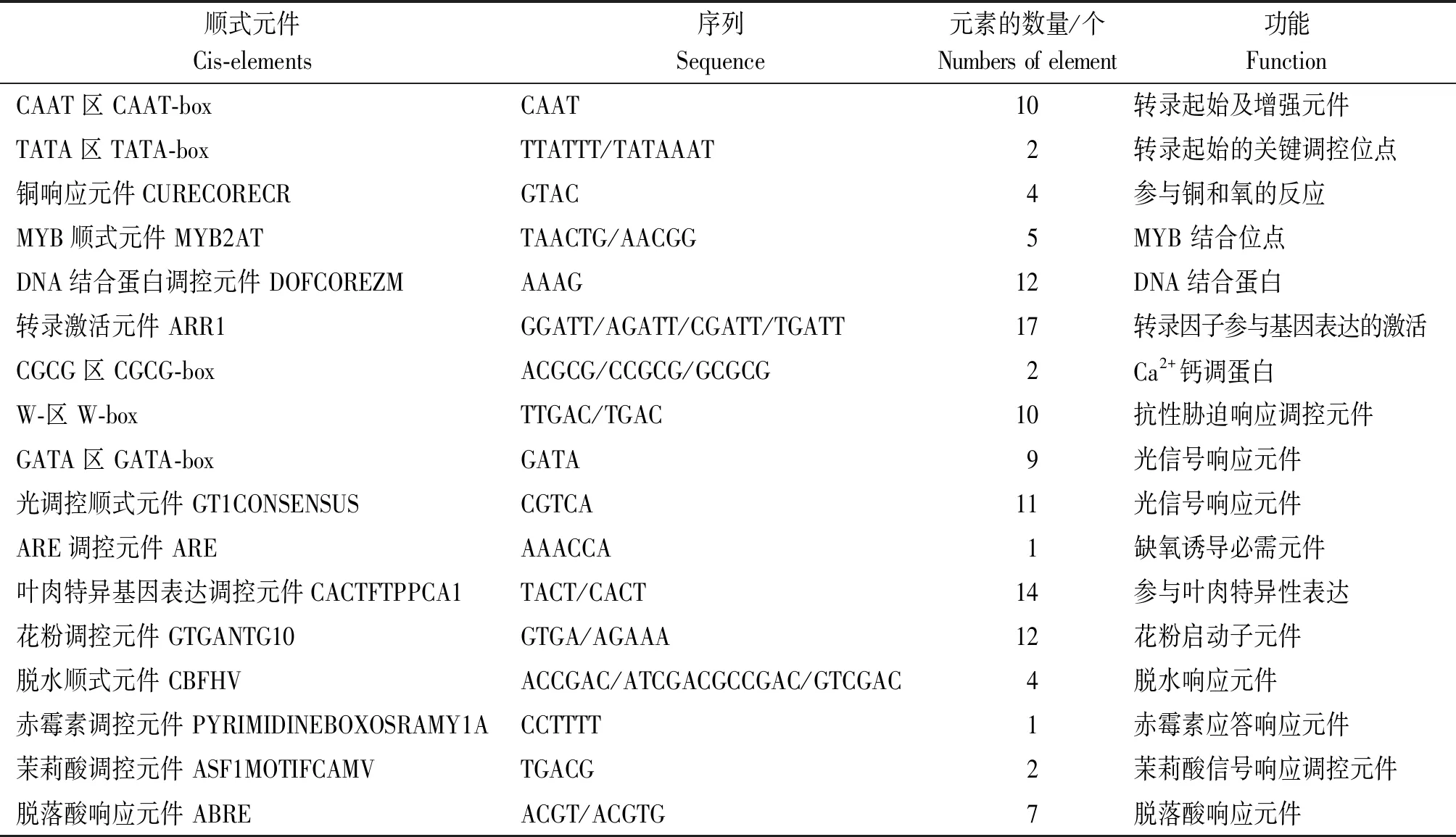
表2 StWRKY11基因啟動子區的順式作用元件分析Tab.2 Analysis of cis-acting elements in the promoter region of StWRKY11 gene
2.2.7 不同物種WRKY序列比對及聚類分析 馬鈴薯StWRKY11基因編碼蛋白質的氨基酸序列和其他物種比較的結果表明(圖8),不同物種中的WRKY蛋白質氨基酸序列均有一段保守的氨基酸序列,即WRKY轉錄因子家族所特有的WRKYGQK序列和鋅指結構。

圖8 StWRKY11基因表達蛋白質與其他物種的WRKY蛋白質氨基酸序列比對Fig.8 The amino acid sequence of StWRKY11 gene expressed protein was compared with that of WRKY protein of other species
通過MEGA7.0軟件構建系統進化樹可見,StWRKY11基因編碼的蛋白質氨基酸序列與馬鈴薯中的StWRKY5親緣關系最近,同源性為95%(圖9)。
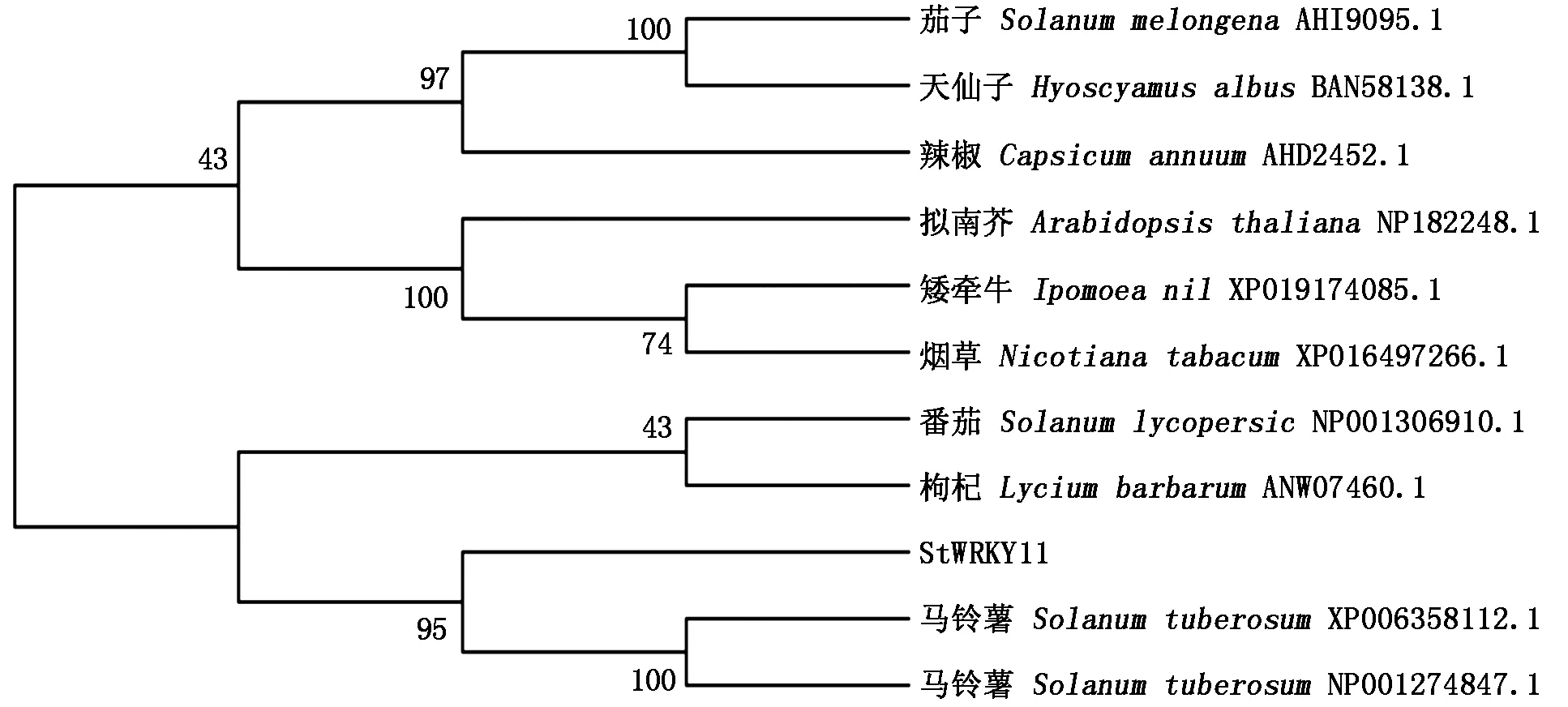
圖9 StWRKY11基因表達蛋白質與其他物種的WRKY蛋白質的系統進化樹Fig.9 The StWRKY11 gene expresses proteins in a phylogenetic tree with WRKY proteins of other species
3 結論與討論
植物在受到衰老、干旱和鹽脅迫后,會激活水楊酸(Salicylic acid,SA)和茉莉酸(Jasmonic acid,JA)的信號轉導途徑[18-19],促進WRKY11基因上調表達,進一步可能通過抑制活性氧(Reactive oxygen species,ROS)的積累或清除過多的ROS及減少膜損傷等方面提高植物耐受性[26]。當植物受到生物脅迫時,通常會啟動茉莉酸和乙烯(ET)的合成途徑,從而激活JA/ET信號轉導途徑,響應抗病轉錄因子WRKY11的表達,進一步激活下游關鍵靶基因(如PR5/Gluc/PRB-1b)[23]和抗病相關基因(NPR1、AOS和LOX2)[27]的表達,從而使植株體自身產生對病原菌的抗性。蠟樣芽孢桿菌AR156侵染擬南芥時,WRKY11基因受JA抑制表達,以此激發植株產生系統誘導抗病性[21],張潔等[28]在2017年研究發現,煙草TT8的WRKY11基因受JA誘導表達,同時也受到ET和SA的共同抑制,負調控煙草對黃瓜花葉病毒(Cucumbermosaicvirus)的抗性。本研究通過分析硅酸鈉增強馬鈴薯黑痣病抗性的轉錄組,篩選到表達量較大基因WRKY11,對該基因進行了克隆,并進一步探討其功能,期望從分子上闡明硅酸鈉誘導馬鈴薯抗黑痣病的機制。
本研究利用克隆技術獲得了馬鈴薯StWRKY11基因的全長序列,并通過在線軟件ORF Finder、ProtParam、TMHMM Server、SignalP 4.1 Server 、NetPhos 2.0 Server、Wolf PSORT Ⅱ、SOPMA和Phyre分析了該基因生物學信息,結果表明,開放閱讀框為1 005 bp,編碼了334個氨基酸,表達蛋白序列中存在結構為WRKYGQK保守結構域,并含有CX5CX23HXH鋅指結構,明確其具有第2類 WRKY的共同結構特征,第2組WRKY蛋白又可以根據鋅指基序中C2之間氨基酸的數量和類型進一步分為5個亞組(Ⅱa、Ⅱb、Ⅱc、Ⅱd 和Ⅱe)[29],StWRKY11基因是馬鈴薯WRKY第2類Ⅱd亞組成員。Ⅱd類WRKY蛋白中保守結構域是可以與鈣調素結合的“C motif”,Ca2+能參與植物抗性信號傳導[30],推測Ⅱd類WRKY轉錄因子可能作為Ca2+受體,通過其“C motif”與鈣調素結合,進而響應抗病反應[31]。
WRKY轉錄因子在參與植物生物學過程中,其活性會受絲裂原活化蛋白激酶(Mitogen-activated protein kinase,MAPK)的調控,MAPK、MAPK激酶(MAPKK)和MAPKK激酶(MAPKKK)構成MAP激酶級聯放大系統,它能通過一系列的磷酸化反應將外界信號逐步放大并傳遞至細胞內,從而引起相應的生理生化活動[32-33],其中磷酸化和去磷酸化都是細胞內信號傳導的重要方式,磷酸化也是一種重要的翻譯后修飾方式[34],磷酸化修飾位點與植物細胞的增殖分化、代謝調節等都有密切聯系[35]。研究報道,MAPK可作為底物和磷酸化激活植物的WRKY基因表達[36-37],由此可知,MAPK可能處于WRKY的上游,其功能會受MAPK激酶的修飾[38]。Kim等[38]研究發現,當施用水楊酸和茉莉酸等外源因子誘導煙草時,會與其細胞膜的受體特異識別并結合,激活植株體內的MAPK信號網絡通路,MAPK可以通過磷酸化或者去磷酸化將信號傳導進入細胞核內,從而激活或抑制WRKY類轉錄因子的活性。本試驗StWRKY11基因編碼的氨基酸,共含有29個磷酸化位點,該基因編碼蛋白質存在多種表達調控方式,能夠參與細胞內的生長分化以及信號轉導等多種生命活動,此結果與前人的研究結果相一致[39]。
馬鈴薯StWRKY11基因表達蛋白的二級結構有4種結構形式:結構元件是α-螺旋、延伸鏈、β-折疊和無規則卷曲,這為實現其功能提供了空間結構及功能元件。亞細胞定位預測中,StWRKY11基因表達蛋白可能定位于細胞核中,這與以往研究報道中WRKY轉錄因子始終定位于細胞核內[40]的結果相吻合。StWRKY11基因表達蛋白不具有跨膜結構,StWRKY11無法通過跨膜結構域固定在細胞膜或細胞器膜上,推測StWRKY11通過核孔復合體進入細胞核中[41],證實了該蛋白定位于細胞核的結果。
Rushton等[42]利用只含W-box轉錄因子結合元件作為啟動子,研究W-box可參與擬南芥對病原體及其他脅迫因子的防衛或脅迫反應,反應程度與W-box的數量及位置有關。本研究中,StWRKY11基因表達蛋白在保守結構域有高度相似性,均含有保守序列(T)TGAC(C/T)(W-box)。推測硅酸鈉增強馬鈴薯黑痣病的抗性可能與保守結構域有關。
StWRKY11基因啟動區順式作用元件預測啟動子區有與抗性脅迫響應相關的順式調控元件,還有與生長發育及赤霉素、脫落酸和茉莉酸等激素響應的順式作用調控元件,該基因可能既參與馬鈴薯對黑痣病菌的抗性也參與生長發育相關途徑,這也可能為解釋硅酸鈉增強馬鈴薯黑痣病的抗性以及增加產量和改善品質的現象提供依據。
馬鈴薯StWRKY11基因與馬鈴薯StWRKY5基因表達蛋白在進化樹上親緣關系最近,同源性為95%,該基因在BABA誘導馬鈴薯提高馬鈴薯晚疫病(Phytophthorainfestans)抗性時表達,表明該基因參與了馬鈴薯的抗病反應[43]。結果顯示,與其他物種的WRKY蛋白同源性較低,這與其他學者的研究一致,即屬內同源性高,屬間同源性相對較低[44]。

