shRNA干擾Keap1對缺氧肝細胞功能的影響
劉 靜
肝纖維化是一個長期的慢性肝損傷過程,其發病機制尚未闡明。氧化應激是指機體或細胞內的氧自由基過度產生和抗氧化功能相對減弱導致兩者之間平衡破壞,繼而引起組織或細胞損傷的一種狀態[1]。氧化應激在肝纖維化中充當重要角色[2]。許多致肝損傷因素都伴不同程度的氧化應激產生,而Kelch樣ECH聯合蛋白1(Keap1)-核因子2相關因子2(Nrf2)信號通路在抵御機體氧化應激過程中起關鍵作用。在氧化應激等狀態下,Nrf2與Keap1解離,使Nrf2轉移入核,啟動下游抗氧化保護性基因的表達,保護機體和細胞免受氧化應激的損傷[3],其中Keap1負性調節Nrf2[4]。本文擬通過構建Keap1 shRNA干擾質粒,探討Keap1下調后對缺氧肝細胞功能的影響,為臨床肝纖維化的防治提供新的靶點。
1 材料與方法
1.1 細胞培養小鼠肝細胞AML12購自上海中科院細胞庫,使用含10%胎牛血清的DMEM-F12培養基,常氧培養在37 ℃、5%CO2和95%空氣飽和濕度培養箱中;缺氧培養在1%O2、5%CO2和94%N2培養箱中。
1.2 質粒載體的構建及轉染由上海吉瑪公司合成4條Keap1 shRNA干擾質粒序列(Plvx/GFP/puro-Keap1-1781、1894、1934、2097)和1條對照shNC序列。將AML12肝細胞接種于6孔板,培養至70%~80%融合度時,用Lipofectamine 2000分別將4條干擾序列及對照序列轉染至AML12肝細胞,36 h后在熒光顯微鏡下觀察綠色熒光蛋白的表達。
1.3 qRT-PCR檢測基因表達轉染36 h提取細胞RNA,逆轉錄成cDNA,并取1 μL cDNA進行PCR反應,反應條件:95 ℃ 30 s、95 ℃ 30 s、60 ℃ 30 s、72 ℃ 30 s,合計40個循環。采用2-ΔΔCt法計算mRNA相對表達量,篩選出干擾效率最高的質粒序列。
1.4 Keap1 shRNA穩轉染細胞株篩選將shRNA干擾效率最高的質粒序列Keap1 shRNA-1781轉染至AML12肝細胞中,加入1.2 μg/mL嘌呤霉素篩選相應的干擾Keap1的穩轉細胞株。
1.5 Western blot檢測Keap1、Nrf2、COL3A1、TGF-β1、VEGF-A、IGF-1蛋白表達將篩選出的穩轉細胞株作為Keap1 shRNA組,與對照組肝細胞缺氧處理不同時間,加入RIPA蛋白裂解液裂解細胞,4 ℃ 12 000g離心10 min,BCA蛋白定量試劑盒進行定量后,取20 μg蛋白進行SDS-PAGE凝膠電泳分離,后轉移至PVDF膜上,5%脫脂牛奶37 ℃封閉1 h,加入相應的抗體4 ℃過夜。加入HRP標記的羊抗兔二抗37 ℃孵育1 h,TBST洗膜3次,每次5 min,ECL顯色。以GAPDH作為對照內參。
1.6 ELISA法測定COL3A1的分泌收集Keap1 shRNA組與對照組肝細胞缺氧培養上清液,根據ELISA試劑盒說明書,測定450 nm波長處的吸光度值,根據標準曲線計算COL3A1濃度。
1.7 WST-1檢測肝細胞活性轉染Keap1 shRNA后的肝細胞與對照組肝細胞培養在96孔板中,缺氧處理0、6、12、24、48 h。參考說明書,每孔加入10 μL WST-1溶液37 ℃培養4 h,用酶標儀測定450 nm處的吸光度值。細胞活力(%)=(A實驗組-A空白組)/(A對照組-A空白組)×100%,空白組為具有WST-1溶液而沒有細胞。
1.8 丙酮酸激酶(PK)活性的測定轉染Keap1 shRNA的肝細胞與對照組肝細胞進行缺氧培養,收集細胞,加入提取液超聲破碎,8 000g4 ℃離心10 min,取上清,置冰上待測。
1.9 ATP含量測定收集缺氧培養后的Keap1 shRNA組與對照組肝細胞,加入酸性提取液,超聲破碎細胞,8 000g4 ℃離心10 min;取上清,再加入等體積的堿性提取液中和,8 000g4 ℃離心10 min,取上清,置冰上待測。
1.10 統計學分析所有數據均用均數±標準差(mean±SD)表示,采用SPSS 13.0軟件進行統計學分析,以P<0.05為差異有統計學意義。
2 結果
2.1 Keap1 shRNA干擾質粒的構建本組以Keap1基因第1781、1894、1934、2097位點為干擾點,將shRNA序列與質粒載體Plvx/GFP/puro連接,構建4種Keap1基因的shRNA質粒載體,基因測序結果證實插入序列正確(表1)。

表1 Keap1基因的4個shRNA靶點序列
2.2 qRT-PCR檢測結果qRT-PCR檢測結果顯示:Keap1 shRNA-1781、1894、1934、2097的相對表達量分別為0.38±0.16、0.42±0.14、0.62±0.18、0.50±0.13,4組重組質粒與對照組相比差異均有統計學意義(P<0.05)。其中Keap1 shRNA-1781差異最顯著,且表達量最低,干擾效果最好(圖1A)。Keap1 shNC組相對表達量為0.88±0.17,與對照組相比差異無統計學意義(P>0.05)。
2.3 Keap1 shRNA穩轉染細胞株建立將Keap1 shRNA-1781轉染至肝細胞36 h后,加入嘌呤霉素,使用熒光顯微鏡觀察細胞熒光,轉染效率超過80%,成功篩選出穩轉細胞株(圖1B)。

圖1 Keap1 shRNA質粒構建篩選:A.qRT-PCR檢測肝細胞中Keap1 shRNA-1781、1894、1934、2097各序列Keap1 mRNA的表達:與對照組相比,*P<0.05,**P<0.01;B.Keap1 shRNA-1781穩轉肝細胞株熒光顯微鏡觀察
2.4 Western blot檢測不同缺氧時間點蛋白表達取轉染Keap1 shRNA后的肝細胞,分別缺氧處理0、6、12、24、48 h,結果顯示缺氧能夠增強Nrf2、COL3A1、TGF-β1、VEGF-A、IGF-1蛋白的表達水平,并且Keap1 shRNA能夠增強Nrf2表達;與Keap1 shNC組相比,Keap1 shRNA組促肝纖維化相關因子COL3A1、TGF-β1、VEGF-A、IGF-1的表達下降,且12 h Keap1 shRNA干擾效果最好(圖2)。

圖2 Keap1 shRNA轉染后缺氧培養0、6、12、24、48 h,Western blot檢測Keap1、Nrf2、COL3A1、TGF-β1、VEGF-A和IGF-1蛋白水平表達:與同一缺氧時間點的shNC組比較,*P<0.05,**P<0.01;與常氧下shNC組相比,#P<0.05,##P<0.01;N.常氧;H.缺氧
2.5 ELISA檢測轉染Keap1 shRNA對缺氧肝細胞COL3A1分泌的影響轉染Keap1 shRNA后,Keap1 shRNA組肝細胞COL3A1的分泌較對照組降低(1.14±0.10vs1.89±0.14)(P=0.002,圖3),并且缺氧能增強肝細胞COL3A1的分泌。

圖3 Keap1 shRNA轉染肝細胞后缺氧處理,通過ELISA測定上清中COL3A1的表達:與缺氧shNC相比,**P<0.01;與常氧shNC組相比,##P<0.01
2.6 WST-1檢測缺氧肝細胞的活性在不同缺氧時間點,與Keap1 shNC組相比,Keap1 shRNA組細胞活性上升(6 h: Keap1 shRNA 1.18±0.16vsKeap1 shNC 0.96±0.13;12 h:Keap1 shRNA 1.05±0.14vsKeap1 shNC 0.77±0.10,P=0.048;24 h: Keap1 shRNA 0.90±0.12vsKeap1 shNC 0.66±0.09,P=0.045;48 h: Keap1 shRNA 0.61±0.08vsKeap1 shNC 0.43±0.06,P=0.032,圖4)。

圖4 Keap1 shRNA轉染肝細胞后,WST-1法檢測缺氧處理不同時間細胞的活性:與同一時間點的shNC組相比,*P<0.05
2.7 缺氧肝細胞能量代謝檢測缺氧導致無氧糖酵解相關酶PK活性和ATP含量下降,而與對照組相比,Keap1 shRNA轉染后的缺氧肝細胞PK活性(Keap1 shRNA 307.30±43.27vsKeap1 shNC 214.23±36.02)(P=0.045)以及ATP含量均提高(Keap1 shRNA 0.45±0.06vsKeap1 shNC 0.31±0.04)(P=0.041,圖5)。
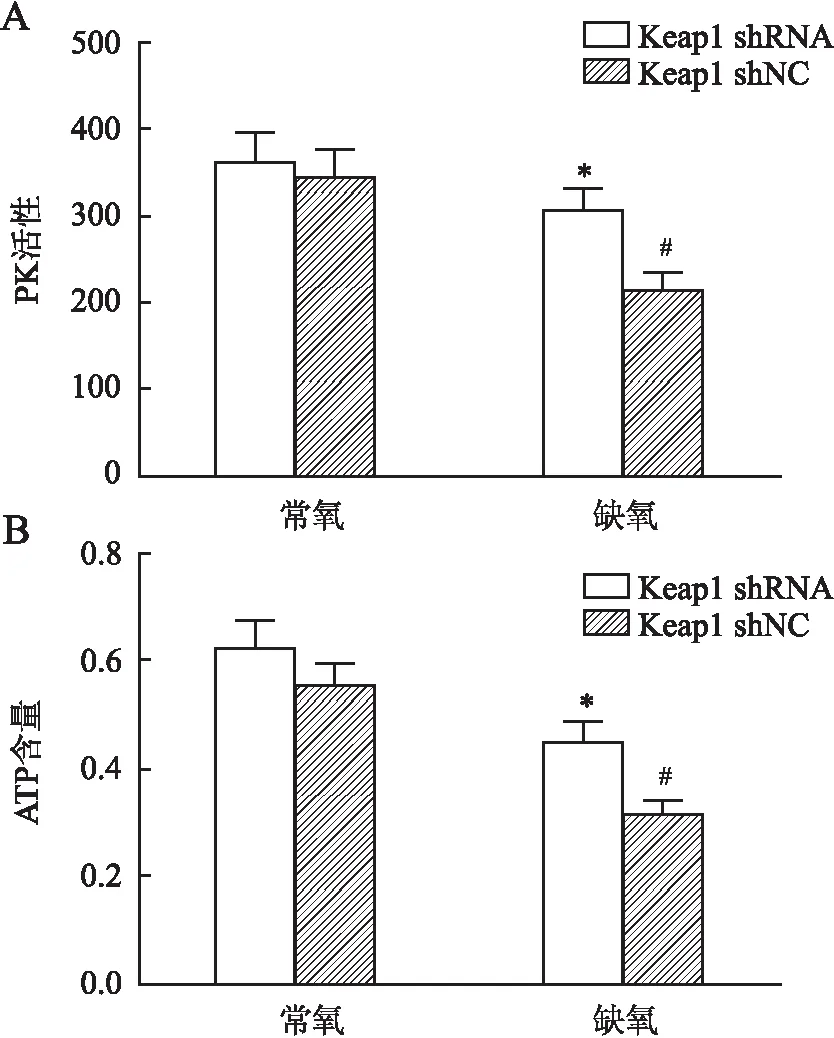
圖5 Keap1 shRNA轉染肝細胞后,缺氧處理PK活性(A)及ATP的含量(B):與缺氧shNC組相比,*P<0.05;與常氧shNC組相比,#P<0.05
3 討論
肝纖維化是一個多種因素引起慢性肝損傷的修復過程。近年,缺氧及缺氧引起的氧化應激與肝纖維化的關系日益受到關注,抑制氧化應激導致的肝損傷已成為防治肝纖維化的新策略。Keap1作為細胞內的氧化應激感受器,抑制Keap1表達可提高細胞對氧化應激損傷的耐受力,有文獻報道Keap1基因敲除的小鼠通過增強Nrf2的表達,使肝臟免于氧化應激損傷[5],因此Keap1基因是應對氧化應激的潛在靶點。
以往對肝纖維化的防治研究主要聚焦于肝星狀細胞,由于其在肝內細胞群體中占比較小,又處于基質包繞的微環境中,藥物吸收困難,故治療效果并不理想;而肝細胞最易受到氧化應激的損傷[6]。因此,本實驗選擇肝細胞作為主要的研究靶點。
RNA干擾(RNA interference, RNAi)已廣泛應用于生物學的各個領域,與siRNA相比,shRNA干擾效果穩定且持久。本實驗根據Keap1基因構建shRNA干擾載體,轉染肝細胞,取得較好的干擾效果,并篩選Keap1 shRNA-1781為最佳干擾序列。
Nrf2作為細胞內重要的轉錄因子,在防治肝纖維化中起重要作用[7]。Xu等[8]報道敲除Nrf2基因的小鼠能夠加重CCl4導致的肝纖維化損傷。另一項研究表明金絲桃苷[9]通過上調Nrf2,增強下游一些抗氧化基因的表達,減輕CCl4導致的肝纖維化損傷。最近研究報道扶正化瘀膠囊通過激活Nrf2-Keap1-Are信號通路實現抗肝纖維化[10],表明Nrf2是肝纖維化治療的潛在靶點[11-13]。本組研究顯示Keap1基因下調后,Nrf2表達上升。
在肝纖維化中以Ⅰ和Ⅲ型膠原為主的細胞外基質過度沉積,是導致肝纖維化發生的重要原因。肝細胞單獨合成膠原的能力雖然是肝星狀細胞的一半,然而在肝內細胞中,肝細胞的數目約是肝星狀細胞的20倍,一旦肝細胞合成膠原的數量有所增加,將會導致大量的膠原合成。據文獻報道,在CCl4誘導的肝纖維化模型中,大部分的膠原都是由肝細胞合成的[14]。同時損傷肝細胞合成的膠原也促進肝星狀細胞的激活,進一步加重肝纖維化。本組結果顯示Keap1 shRNA能較好地抑制缺氧肝細胞Ⅲ型膠原的合成和分泌。TGF-β1、VEGF和IGF-1參與肝纖維化的發生、發展,Keap1 shRNA作用于缺氧肝細胞后,Nrf2表達上調,進而抑制促纖維化因子TGF-β1、VEGF和IGF-1的表達,Oh等[15]的研究顯示Nrf2激活能夠通過抑制TGF-β1來抑制肝纖維化。
缺氧影響細胞的活性,然而轉染Keap1 shRNA后肝細胞對缺氧微環境產生一定的耐受力,使肝細胞活性上升。有研究報道[16]Nrf2缺失或Keap1基因敲除能夠降低肝細胞活性。另外,研究發現Nrf2通過上調糖酵解關鍵基因調控乳腺癌細胞中的代謝重編程。本實驗顯示Keap1下調能夠加強無氧酵解關鍵酶PK的活性,提高缺氧肝細胞的ATP水平,進一步證實干擾Keap1后,可能通過增強Nrf2表達產生抗缺氧效應,從而緩解缺氧肝細胞的能量代謝障礙。然而,與缺氧耐受有關的許多基因都受缺氧誘導因子-1調節,其中包括促紅細胞生成素和無氧糖酵解相關的酶等。Keap1是否通過影響缺氧誘導因子的表達調節缺氧耐受,還有待進一步探討。
總之,本實驗成功構建Keap1 shRNA穩轉染肝細胞株,Keap1下調后能夠降低促纖維化因子的表達,提升缺氧條件下的肝細胞能量代謝。然而,肝纖維化發生機制復雜多樣,本課題組后續將進一步觀察Keap1-Nrf2信號通路在肝纖維化中的調控作用,為預防和治療肝纖維化提供新的思路和途徑。

