球磨法合成高比表面積的α-Al2O3載體在CO氧化偶聯反應中的應用
楊 林,潘振棟,王冬娥,馬懷軍,曲 煒,田志堅*
(1.中國科學院大連化學物理研究所,遼寧 大連 116023;2.中國科學院大學,北京 100049)
乙二醇是重要的有機化工原料,可用于生產潤滑劑、防凍劑、聚酯纖維、聚酯塑料等[1-2]。煤制乙二醇路線符合我國“富煤少油”的能源結構,且已經實現工業化。CO與亞硝酸甲酯(MN)氣相偶聯合成草酸二甲酯(DMO)是煤制乙二醇中的關鍵步驟,可以將無機的C1轉化為有機的C2[3-6]。研究表明,Pd/α-Al2O3是針對CO氧化偶聯合成DMO反應的高效催化劑[7-9]。Yamamoto Y等[7]對比了活性炭、氧化鋁、α-Al2O3、NaY分子篩等載體發現,α-Al2O3做載體時催化劑的催化活性最高,DMO時空收率達到489 g·(L·h)-1。孫國方等[8]研究了以α-Al2O3為載體不同Pd前驅體的影響,發現醋酸鈀為前驅體制備的催化劑催化活性優于其他前驅體,DMO時空收率為798 g·(L·h)-1。侯蕾等[9]在Pd/α-Al2O3催化劑中添加C做助劑,DMO時空收率達813 g·(L·h)-1。Pd/α-Al2O3催化劑的α-Al2O3載體通常是由前驅體經過1 200 ℃以上的高溫焙燒得到,高溫焙燒得到的α-Al2O3比表面積很低,一般小于10 m2·g-1[10]。低比表面積的載體會限制活性組分的分散,進而降低催化劑的催化活性。因此,制備高比表面積的α-Al2O3載體對提高催化劑活性具有重要意義。
機械化學是指通過球磨、研磨、擠壓等機械方法向反應系統中輸入機械能引起的化學變化。機械化學法因其操作簡單、環境友好等特點在材料合成領域具有廣闊的應用前景[11-12]。Tonejc A等[13]在室溫下以γ-AlOOH或Al(OH)3為原料采用球磨法制備得到α-Al2O3,研究表明,輸入機械能可以使α-Al2O3相變在室溫下發生。Amrute A P等[14]通過球磨的方法在室溫下以γ-AlOOH為原料制備比表面積高達140 m2·g-1的納米級α-Al2O3,熱力學計算表明,球磨引起γ-AlOOH表面能變化,從而發生從γ-AlOOH到α-Al2O3的相變,γ-AlOOH中的結構水分子對穩定α-Al2O3納米顆粒起到重要作用。Amrute A P等[15]將制備的α-Al2O3作為載體制得Co基催化劑應用于費托合成反應中,發現催化劑具有極好的催化活性和穩定性。與傳統高溫焙燒法相比,球磨法避免了高溫焙燒,具有節約能源的優點。球磨法為α-Al2O3制備提供了新的路徑,在催化反應中具有廣闊的應用前景。
本文針對CO氧化偶聯反應中催化劑載體比表面積低的問題,采用球磨法制備高比表面積的α-Al2O3載體,通過浸漬法制得Pd/α-Al2O3催化劑。采用XRD、氮氣物理吸附、NH3-TPD、TEM等方法對催化劑進行表征,并在CO氧化偶聯反應中評價催化劑的催化活性。
1 實驗部分
1.1 α-Al2O3載體制備
球磨法:將SB粉(德國Sasol公司)在120 ℃干燥12 h,取2.2 g 干燥后的SB粉和10顆直徑2 cm的瑪瑙磨球放入500 mL瑪瑙球磨罐中,在球磨機設定功率為35 Hz 條件下球磨20 h,得到產物命名為Al2O3-B(B代表ball-milling)。
焙燒法:將同樣的SB粉在1 200 ℃焙燒6 h,得到產物命名為Al2O3-C(C代表calcination)。
1.2 Pd/α-Al2O3催化劑制備
催化劑的制備采用浸漬法。將球磨法與焙燒法制備的Al2O3-B和Al2O3-C粉末壓片造粒,得到(20~40)目的顆粒。將Al2O3-B和Al2O3-C載體顆粒按鈀質量分數1%浸漬于醋酸鈀的丙酮溶液中,在室溫下干燥和400 ℃氫氣氣氛中還原后得到Pd/Al2O3-B和Pd/Al2O3-C催化劑。
1.3 催化劑表征
采用Empyrean-100 X 射線衍射儀分析樣品的物相,樣品的平均晶粒尺寸根據謝樂公式計算得到,計算采用強度最高的衍射峰即位于43.1° 的衍射峰;采用美國麥克儀器公司的ASAP2040介孔微孔氣體物理吸附儀表征樣品的比表面積及孔結構,樣品在350 ℃抽真空預處理 6 h,隨后在液氮溫度下進行氮氣物理吸附實驗;采用美國麥克儀器公司的AutoChem II 2920化學吸附儀進行NH3程序升溫脫附實驗和氫氣脈沖吸附實驗,分別表征樣品的酸性和金屬分散度;采用JEM-2100電子顯微鏡獲得樣品的透射電子顯微照片,表征樣品中的金屬顆粒尺寸。
1.4 催化劑評價
在固定床反應器上進行催化劑的CO氧化偶聯合成DMO的催化活性評價實驗。將(20~40)目的催化劑2 mL裝填到反應器中,反應在常壓、溫度為125 ℃條件下進行,原料氣(體積分數:16%CO、24%MN和60%N2)以12 000 h-1空速通入反應器。反應達到穩定狀態后,開始收集產物。從反應器出口到產物收集罐入口保溫在90 ℃,收集罐罐體保持在室溫,以使主產物DMO(熔點54 ℃)冷凝在罐內實現產物分離。其他未冷凝產物包括碳酸二甲酯、甲醇、甲酸甲酯在-15 ℃的冷阱中冷凝為液體收集。反應的原料氣和尾氣在裝有FID和TCD檢測器的美國Agilent公司的7890A型氣相色譜儀上分析。
CO轉化率XCO使用公式(1)計算:
(1)
式中,[N2]in和[N2]out表示原料氣和尾氣中的N2含量;[CO]in和[CO]out表示原料氣和尾氣中的CO含量。
DMO選擇性SDMO使用公式(2)計算:
(2)
式中,nDMO表示收集的DMO物質的量,XCO表示CO轉化率,Fco表示反應器入口CO物質的量流量,t表示反應時間。
DMO時空收率STY使用公式(3)計算:
(3)
式中,mDMO表示收集的DMO質量,g;Vcat表示催化劑的體積,L;t表示反應時間,h。
2 結果與討論
2.1 載體的表征
對Al2O3-B和Al2O3-C載體進行XRD表征,結果如圖1所示。
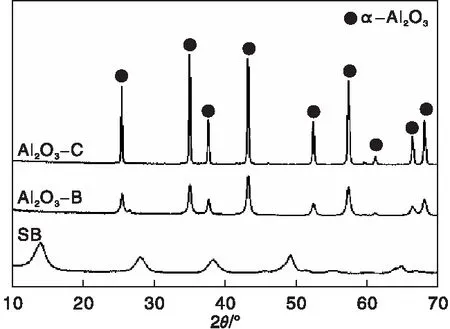
圖1 Al2O3載體的XRD圖Figure 1 XRD patterns of Al2O3 supports
由圖1可以看出,經過球磨或焙燒,原料SB粉的衍射峰消失,Al2O3-B和Al2O3-C載體在2θ=25.5°、35.0°、37.6°、43.1°、52.4°、57.3°、66.4°和68.0°的衍射峰與α-Al2O3的標準衍射峰(JCPDS 01-075-0782)一致,說明Al2O3-B和Al2O3-C載體均是α-Al2O3晶相。與焙燒法制備的Al2O3-C載體相比,球磨法制備的Al2O3-B載體衍射峰強度較低且發生寬化。根據謝樂公式計算,Al2O3-B和Al2O3-C載體的平均晶粒尺寸分別是20.3 nm和50.0 nm,說明球磨法可以獲得平均晶粒尺寸更小的α-Al2O3載體。球磨法得到的Al2O3-B載體的XRD衍射圖中在2θ=26.5°出現一個弱衍射峰,歸屬于石英(JCPDS 01-079-1906),可能來自球磨過程中瑪瑙材質的磨球、球磨罐。
采用氮氣物理吸附的方法對Al2O3-B以及Al2O3-C載體的織構性質進行表征,結果如表1 所示。
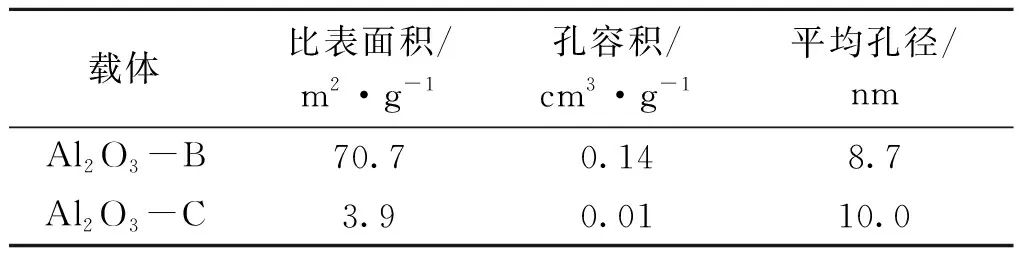
表1 Al2O3載體的織構性質
一般方法制備的α-Al2O3載體比表面積小于10 m2·g-1。由表1可以看出,采用傳統焙燒法獲得的Al2O3-C載體比表面積為3.9 m2·g-1、孔容積為0.01 cm3·g-1;采用球磨法制備的Al2O3-B載體比表面積為70.7 m2·g-1,孔容積為0.14 cm3·g-1,遠高于Al2O3-C載體。這是因為在高溫焙燒過程中氧化鋁發生燒結,孔道坍塌,比表面積下降明顯;而球磨過程在室溫下進行,有利于保持孔結構、獲得高比表面積的α-Al2O3載體。高比表面積的α-Al2O3載體有利于獲得活性組分均勻分散、催化活性高的催化劑。
Al2O3-B和Al2O3-C載體的酸性采用NH3-TPD進行表征,結果見圖2。圖2中位于180 ℃和500 ℃的NH3脫附峰分別歸屬于樣品中的弱酸位和中強酸位[16]。Al2O3-C載體中幾乎沒有酸性位,Al2O3-B載體中的弱酸位和中強酸位明顯多于Al2O3-C載體。這是因為原料SB粉中含有大量的羥基,在高溫焙燒過程中發生表面燒結、羥基脫水縮合生成Al2O3-C載體,因此Al2O3-C載體比表面積低,表面幾乎沒有酸性。在機械球磨過程中,原料SB粉發生相變的同時保留了較大的比表面積,生成的Al2O3-B載體表面可能富含羥基,使表面具有一定酸性。CO氧化偶聯反應中反應物MN在酸性位上會分解為甲氧基和NO[17],若反應體系中甲氧基濃度過高,容易生成副產物碳酸二甲酯,導致催化劑選擇性降低,因此載體的酸性可能影響催化劑的選擇性。
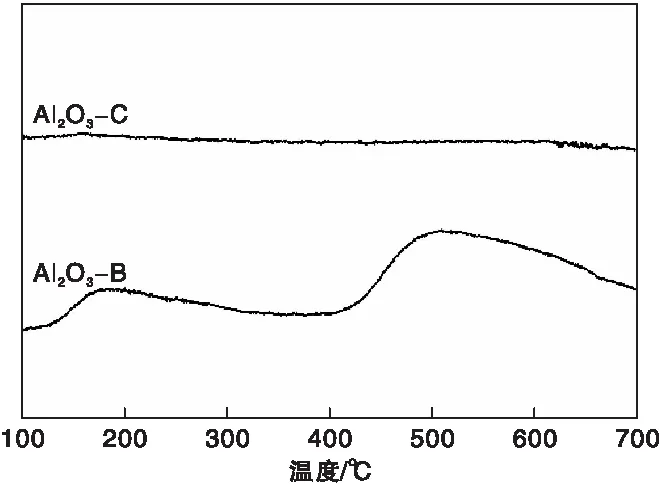
圖2 Al2O3載體的NH3-TPD譜圖Figure 2 NH3-TPD spectra of Al2O3 supports
2.2 催化劑的表征
為了考察催化劑上Pd顆粒的分布情況,采用TEM和H2化學吸附方法對催化劑進行表征,結果見圖3和表2。由圖3可以看出,Pd/Al2O3-C催化劑上低襯度的Al2O3-C載體燒結成大塊,Pd顆粒尺寸分布從2 nm到83 nm,極不均勻地負載在Al2O3-C載體上,因此未進行粒徑統計計算平均粒徑。表2中H2化學吸附的結果表明,Pd/Al2O3-C催化劑中鈀顆粒分散度為2.0%、平均粒徑為56.5 nm,說明鈀顆粒發生嚴重團聚。由圖3還可以看出,襯度較小的(20~50) nm顆粒和高襯度的黑點分別對應Al2O3-B載體和鈀顆粒,說明Pd/Al2O3-B催化劑上鈀顆粒尺寸均勻分布于納米級的Al2O3-B載體上。從TEM照片中統計平均粒徑為4.73 nm。H2化學吸附的結果中,Pd/Al2O3-B催化劑中鈀顆粒的分散度為24.1%、平均粒徑是4.6 nm,與TEM表征結果相吻合。結合載體的氮氣物理吸附表征結果可知,Al2O3-C載體的比表面積僅3.9 m2·g-1,而球磨法制備的Al2O3-B載體的比表面積是其18倍。Al2O3-B載體的高比表面積更有利于活性組分鈀的分散,獲得具有更多活性中心的催化劑,進而提高催化活性。

圖3 Pd/Al2O3-C和Pd/Al2O3-B催化劑的TEM照片Figure 3 TEM images of Pd/Al2O3-C and Pd/Al2O3-B catalysts

表2 Pd/Al2O3-C和Pd/Al2O3-B催化劑上鈀顆粒分散度和粒徑
2.3 催化劑性能
對Pd/Al2O3-C和Pd/Al2O3-B催化劑在CO氧化偶聯生成DMO反應的催化性能進行評價,結果如圖4所示。由圖4可以看出,Pd/Al2O3-C催化劑上,CO轉化率17.1%,DMO選擇性99.2%,時空收率1 378 g·(L·h)-1。而Pd/Al2O3-B催化劑上,CO轉化率顯著提高到27.8%,時空收率達到2 175 g·(L·h)-1;但選擇性略有下降,為93.8%,這是因為生成了副產物碳酸二甲酯。由圖4還可以看出,100 h的穩定性評價測試結果表明,Pd/Al2O3-B催化劑具有很好的穩定性。
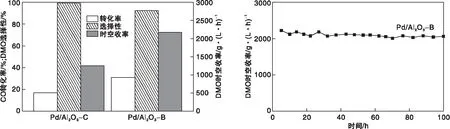
圖4 Pd/Al2O3-C和Pd/Al2O3-B催化劑在CO氧化偶聯反應中的催化活性與Pd/Al2O3-B催化劑的穩定性Figure 4 Catalytic performance of Pd/Al2O3-C and Pd/Al2O3-B in CO oxidative coupling reaction and durability performance of Pd/Al2O3-B catalyst
Pd/Al2O3-B催化劑中鈀顆粒分散度高,相同負載量情況下具有更多的活性中心,因此CO轉化率較高。NH3-TPD表征結果說明,Al2O3-B載體的酸中心數量較多,Pd/Al2O3-B催化劑中DMO選擇性略低與此有關。合成DMO反應中,CO與MN的化學計量比為1∶1,而合成碳酸二甲酯(DMC)的反應中CO與MN的化學計量比為1∶2。根據CO氧化偶聯的反應機理[18],MN在催化劑表面會形成CH3O*中間體,CO*與CH3O*發生連續插入反應生成的COCOOCH3*中間體,再與CH3O*反應生成DMO。若反應體系中CH3O*過多可能直接與COOCH3*中間體反應生成碳酸二甲酯(DMC),從而導致選擇性降低。與Pd/Al2O3-C催化劑相比,Pd/Al2O3-B催化劑雖然選擇性略低,但其參與反應的活性中心多,CO轉化率較高,因此催化劑的時空收率顯著提高。
3 結 論
(1)采用球磨法制備得到α-Al2O3載體,并將此α-Al2O3載體負載活性組分鈀制備的催化劑(Pd/Al2O3-B)應用于CO氧化偶聯合成DMO反應。結果表明,Pd/Al2O3-B催化劑的DMO時空收率達到2 175 g·(L·h)-1,具有很高的催化活性,且在穩定性測試中表現出很高的穩定性。
(2)球磨法為制備α-Al2O3載體提供了新的、低能耗的路徑,可以實現在室溫下制備得到高比表面積的α-Al2O3載體,將此方法制備的α-Al2O3載體應用于CO氧化偶聯反應中具有很高的催化活性。與傳統焙燒法得到的α-Al2O3載體相比,Al2O3-B載體的大比表面積有利于活性組分的分散。Pd/Al2O3-B催化劑中,鈀顆粒尺寸較小,具有更多的活性中心,因此在CO氧化偶聯合成DMO反應中具有出色的催化活性。

