感染性休克患者PCSK9 水平及其對預后評估價值的分析
周 吉 陳 碩 溫旭智
1.江蘇大學附屬宜興人民醫院急診科,江蘇宜興 214200;2.江蘇大學附屬宜興人民醫院腫瘤科,江蘇宜興 214200
膿毒癥是由微生物感染引起的全身性炎癥,具有極高的預后不良率和經濟負擔,其中感染性休克是膿毒血癥最嚴重的并發癥。膿毒癥患者可表現出細胞功能、免疫調節、凝血和代謝紊亂的改變,針對感染性休克的治療,強調干預時間窗短,必須及時控制感染源,恢復血流動力學穩態,因此尋找一種有效的生物標志物在膿毒癥研究中發揮了重要作用。超敏C 反應蛋白(hypersensitive C-reactive protein,hs-CRP)、降鈣素原(procalcitonin,PCT)是評估患者感染程度的經典指標,但在非感染性炎癥情況下可能會升高,缺乏特異性。前蛋白轉化酶枯草溶菌素9(proprotein convertase subtilisin/kexin 9,PCSK9)參與了不同疾病的病理生理學機制,例如動脈粥樣硬化、病毒和細菌感染、癌癥、肥胖癥、糖尿病、阿爾茨海默病、高血壓、關節炎、多發性創傷,表明PCSK9 水平升高與細菌或病毒感染和敗血癥之間存在關聯[1]。研究表明,PCSK9 水平較低的患者感染性休克的結局更好[2],也有研究證實,膿毒癥患者的PCSK9 水平升高,可使內毒素清除率降低和器官衰竭率增加[3],但是國內將PCSK9 用于感染性休克患者預后評估的研究還較少。因此,本研究分析感染性休克患者的PCSK9、CRP、PCT 水平,并探討三者對感染性休克患者預后的預測效能,為臨床上感染性休克患者的預后評估提供參考。
1 資料與方法
1.1 一般資料
回顧性分析2019 年1 月至2022 年3 月江蘇大學附屬宜興人民醫院收治的感染性休克患者135 例,根據1 周內的轉歸情況,將病情穩定、好轉、治愈的患者歸為好轉組(n=77),將出院時意識昏迷、放棄治療、死亡的患者歸為預后不良組(n=58)。納入標準:①有明確的感染灶(血液、尿、腦脊液、傷口、呼吸道分泌物、其他體液等標本培養陽性)同時快速序貫器官衰竭評分≥2分;②體溫>38℃或<36℃;心率>90 次/分或低血壓(收縮壓<90mmHg,1mmHg=0.133kpa,或較基線降低>40mmHg);呼吸頻率>20 次/分或通氣障礙(動脈血 CO2分壓<32mmHg);外周血白細胞計數>12.0×109/L 或<4.0×109/L,或未成熟白細胞比例>10%。③使用足夠液體補液及需要血管活性藥物維持平均動脈壓≥65mmHg,血乳酸>2mmol/L。排除標準:①多發傷伴有活動性臟器出血;②有嚴重的自身免疫性疾病;③惡性腫瘤的終末期患者及使用多種靶向藥物的腫瘤患者;④有慢性感染性疾病,如活動性結核、人類免疫缺陷病毒感染等。其中男68 例,女67 例,年齡23~94 歲,平均(71.20±12.40)歲,健康對照組選擇在江蘇大學附屬宜興人民醫院體檢中心進行定期體檢的健康人135 例,男70 例,女65 例;年齡35~75 歲,平均(55.20±15.15)歲。一般資料比較差異無統計學意義(P>0.05),具有可比性。本研究獲得江蘇大學附屬宜興人民醫院醫學倫理委員會批準(倫理審批號:2019-18),患者均簽署知情同意書。
1.2 方法
離心機購自北京白洋醫療器械有限公司(型號:BY-320C),干式熒光免疫分析儀購自萬孚生物公司(型號:FS-301),全自動生化分析儀購自Mindray邁瑞醫療公司(型號:BC-7500),PCSK9 人酶聯免疫吸附試劑盒購自Abcam 公司(型號:ab209884),hs-CRP 乳膠增強免疫散射比濁法試劑購自深圳邁瑞生物醫療有限公司,PCT 熒光免疫分析試劑購自廣州萬孚生物技術股份有限公司。
使用無抗凝劑的采血管,感染性休克患者在治療前及治療后1d、3d、5d 清晨空腹狀態下,健康體檢組在清晨空腹狀態下,抽取5ml 靜脈血,4000 轉/min離心15min,取血清3ml 儲存于EP 管中,在-80℃冷凍保存備用。采用酶聯免疫吸附法檢測PCSK9,嚴格按試劑盒說明操作,簡易操作如下:24℃解凍患者血液標本;配制洗滌液制備各濃度梯度的PCSK9 標準品;稀釋患者血液樣本加樣于96 孔板每孔100μl,并且加100μl 標準品,25℃恒溫孵育60mmin,結束后洗滌4 次;加入二抗25℃恒溫孵育60min,結束后洗滌4 次;加入顯色劑后避光,溫恒25℃孵育20min;終止反應后在450nm 波長處測定吸光度。采用熒光免疫檢測PCT,按儀器與試劑盒操作說明在干式熒光免疫分析儀上測定。通過全自動生化分析儀,使用乳膠增強免疫散射比濁法檢測hs-CRP 水平。記錄患者在重癥監護病房的住院結局及住院天數。
1.3 統計學方法
采用SPSS 18.0 統計學軟件對數據進行處理分析,符合正態分布的計量資料以均數±標準差()表示,兩組間比較采用獨立樣本t檢驗;計數資料采用例數(百分比)[n(%)]表示,組間比較采用χ2檢驗;采用受試者操作特征(receiver operator characteristic,ROC)曲線分析PCSK9、hs-CRP、PCT的水平,預測感染性休克患者預后的效能。P<0.05為差異有統計學意義。
2 結果
2.1 感染性休克患者與健康體檢組的PCSK9、PCT、hs-CRP 水平比較
治療前,感染性休克組的3 個指標水平均高于健康體檢組,差異有統計學意義(P<0.01),見表1。
表1 感染性休克組與健康體檢組PCSK9、PCT、hs-CRP 水平比較( )

表1 感染性休克組與健康體檢組PCSK9、PCT、hs-CRP 水平比較( )
2.2 預后不良組和好轉組治療各時間點PCSK9、PCT、hs-CRP 水平比較
治療前,預后不良組和好轉組的PCSK9、PCT、hs-CRP 水平比較,差異無統計學意義(P>0.05);治療后1d、3d、5d,預后不良組的PCSK9 水平均明顯高于好轉組,差異均有統計學意義(P<0.01);治療后1d、3d,預后不良組的PCT 水平與好轉組比較,差異均無統計學意義(P>0.05);治療后5d,預后不良組PCT 水平高于好轉組,差異有統計學意義(P<0.01);治療后1d,預后不良組hs-CRP 水平與好轉組比較,差異無統計學意義(P>0.05);治療后3d、5d,預后不良組的hs-CRP 水平明顯高于好轉組,差異有統計學意義(P<0.01),見表2。
表2 預后不良組和好轉組治療各時間點PCSK9、PCT、hs-CRP 水平比較( )
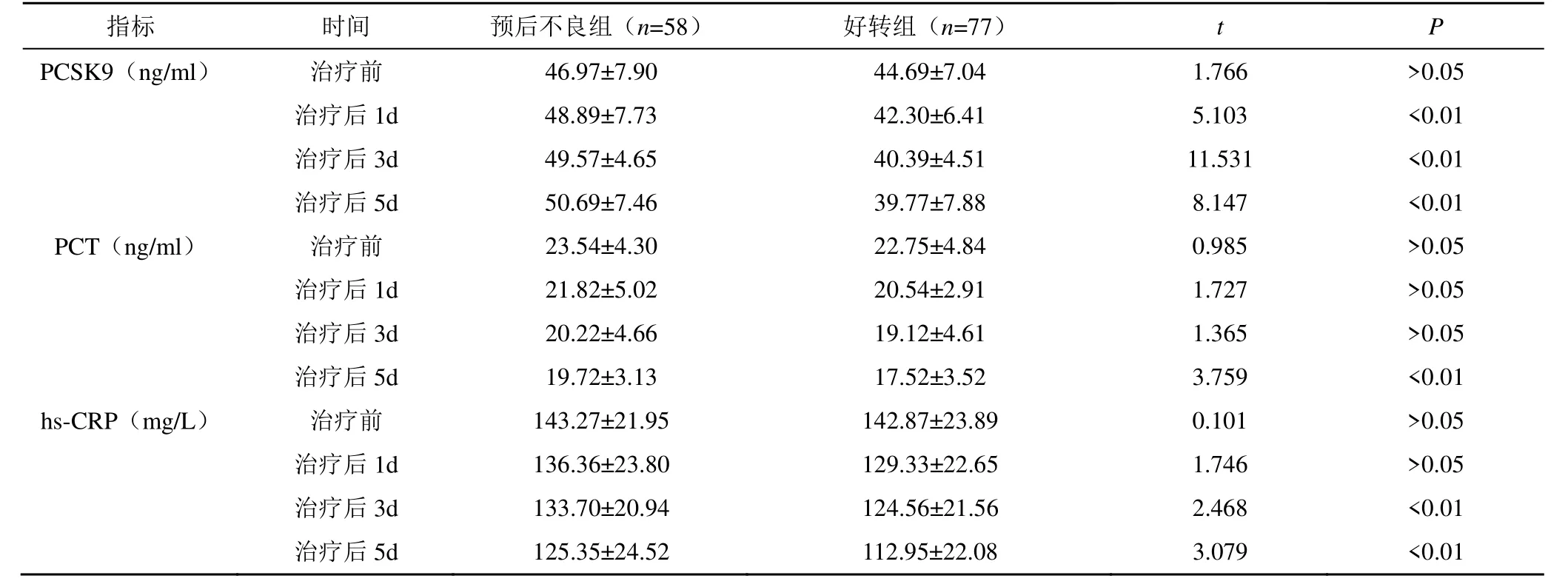
表2 預后不良組和好轉組治療各時間點PCSK9、PCT、hs-CRP 水平比較( )
2.3 PCSK9、PCT、hs-CRP 在預測感染性休克患者預后的ROC 曲線分析
分析治療后5d 的PCSK9、PCT、hs-CRP 水平,計算3 者的預測患者ROC 曲線下面積(area under the curve,AUC),其中PCSK9 的AUC 最大,PCSK9 與hs-CRP 的AUC 比較,差異有統計學意義(Z=3.092,P<0.05)。PCSK9 與 PCT的 AUC 比較,差異有統計學意義(Z=2.291,P<0.05)。PCT 與hs-CRP 的AUC 比較,差異為0.0662,差異無統計學意義(Z=1.014,P>0.05),見圖1、表3。
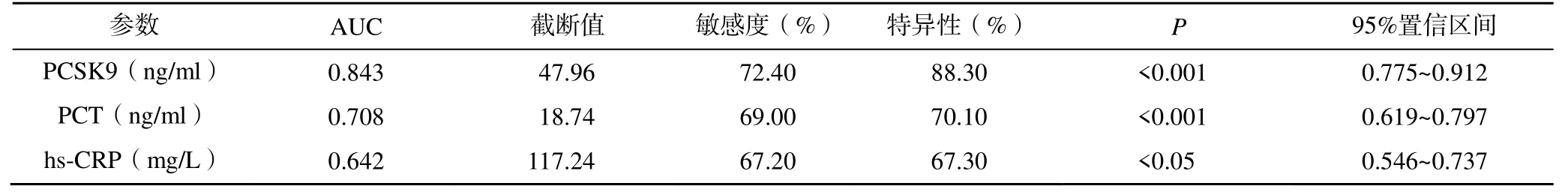
表3 治療后5d PCSK9、PCT、hs-CRP 水平預測感染性休克患者預后效能

圖1 PCSK9、PCT、hs-CRP 水平預測感染性休克患者預后的ROC 曲線分析
3 討論
近年來,感染性休克已然成為重癥醫學科及急診科醫生面臨的最常見和最嚴重的問題,是重癥監護病房中最常見的死亡原因之一,隨著社會老齡化加劇,該疾病的發病率持續上升[4]。感染性休克患者的死亡率為20%~80%[5],感染性損傷可導致患者發生全身性炎癥,進而影響機體多個器官和系統,發生一系列的生理紊亂,目前的治療主要為感染源頭控制、抗生素支持性干預、患者內環境紊亂的糾正[6],特別是早期目標導向治療,發現某些特定炎癥因子作為潛在診斷和判斷其預后的生物標志物,在感染性休克患者的臨床治療方案選擇上至關重要。
PCSK9 是前蛋白轉化酶家族中第9 個成員,人類PCSK9 基因定位于1p32.3,由12 個外顯子組成,全長22kb,編碼692 個氨基酸[7],是由分子量為74 kDa 的可溶性pro-pcsk9 經內質網自催化生成,同時還參與神經細胞凋亡和肝再生,又稱為神經細胞凋亡調節轉化酶-1(neural apoptosis-regulated convertase 1,NARC1)[8],PCSK9 蛋白由信號肽(包括30 個氨基酸)、前結構域(122 個氨基酸)、催化結構域(299 個氨基酸)和富含半胱氨酸、組氨酸的C-端結構域(279 個氨基酸)組成[9],可在肝臟、小腸、腎臟、胰腺表達,肝臟是PCSK9 蛋白發揮作用的主要靶器官[10],也是循環PCSK9 的主要來源。
感染性休克通常是嚴重微生物感染的致命并發癥,可引發不受控的全身性炎癥和器官衰竭,而這些致病微生物細胞壁的致病性脂質部分,如革蘭氏陰性菌的脂多糖、脂磷壁酸、磷脂甘露聚糖[11],這些病原體脂質成分是哺乳動物先天免疫受體Toll樣受體的主要配體,它們在膿毒性炎癥(膿毒性休克或膿毒癥)中發揮重要作用。病原體脂質最初會結合到高密度脂蛋白(high-density lipoprotein,HDL)中,隨后會轉移到低密度脂蛋白(low-density lipoprotein,LDL)或極低密度脂蛋白(very lowdensity lipoprotein,VLDL)中,由肝臟從血液中清除,在肝臟中解毒,最終在膽汁中分泌[12];最近研究發現,PCSK9 會導致脂蛋白受體進行降解,包括低密度脂蛋白受體(low-density lipoprotein receptor,LDLR),極低密度脂蛋白受體(very low-density lipoprotein receptor,VLDLR)和LDLR 相關蛋白1,從而減少肝臟對循環內病原脂蛋白的攝取,病原體脂質的肝臟清除率下降,所以PCSK9 被認為對膿毒癥的發病機制至關重要[13]。在Dwivedi 等[14]的膿毒癥小鼠模型試驗中,通過對PCSK9 基因敲除的小鼠進行肺組織病理學分析以及肺組織的髓過氧化物酶測定,都表明PCSK9 缺乏可以減少全身細菌傳播,使到達肺部的細菌數量下降,中性粒細胞募集減少,全身炎癥反應明顯減輕;Walley 等[15]的一個多中心臨床觀察性隊列研究也發現,有PCSK9 基因的功能喪失感染性休克患者在28d 內的存活率可增加71.7%;Genga 等[16]的一項回顧性觀察研究表明,具有多個功能缺失PCSK9 等位基因的患者1 年死亡或感染相關再入院的風險較低,PCSK9 缺乏可防止全身細菌傳播、器官病理和組織炎癥[17],特別是在肺和肝臟中,而PCSK9 過表達會加劇多器官病理以及早期膿毒癥的高凝狀態和促炎狀態[18],因此PCSK9 可作為一項感染性休克患者預后的生物學標志物。本研究發現,已出現感染性休克的患者在治療前外周血的PCSK9、PCT、hs-CRP 較健康人群明顯升高,差異有統計學意義;比較感染性休克患者預后不良組和好轉組治療前、治療后1d、3d 的PCT 數據,發現兩者差異無統計學意義;治療5d 后兩組的PCT 比較,好轉組PCT 較預后不良組低,差異有統計學意義;對比預后不良組和好轉組的治療前、治療后1d 的hs-CRP,兩者差異無統計學意義,在治療后3d、5d,比較兩組的hs-CRP,好轉組的hs-CRP 水平較預后不良組低,差異有統計學意義;通過患者外周血PCSK9 的數據分析得出,治療前,預后不良組和好轉組比較,差異無統計學意義。治療后1d,對比兩組PCSK9 水平發現預后不良組較高,差異有統計學意義;治療后3d、5d 與預后不良組比較,好轉組的PCSK9 水平明顯出現下降趨勢,差異有統計學意義。本研究數據說明,監測PCSK9 有助于評估感染性休克患者病情,通過ROC 曲線分析可以看出,PCSK9 對比PCT、hs-CRP 的AUC 更大,截斷值、敏感度、特異性均優于PCT 和hs-CRP,說明PCSK9對感染性休克患者的預測效能更高,是一種有效的生物標志物。
綜上所述,感染性休克患者外周血PCSK9 水平明顯上調,動態監測PCSK9 水平有助于評估患者治療后的預后情況,且其預測效能優于PCT、hs-CRP。但本研究也存在一定的局限性,入組的患者人數相對較少,患者疾病分類不夠細化,研究結果可能存在一定的偏倚。同時,PCSK9 是一個感染性休克的潛在治療靶點,未來可開展更大樣本的前瞻性研究,同時將進一步展開PCSK9 抑制劑在感染性休克動物模型中研究。

