微創跗骨竇入路聯合PRP局部注射應用于SandersⅢ型跟骨骨折的臨床效果觀察
高 曦 藍錦福 關 勇 黃朱宋
福建省福州市第二醫院骨科 350007
跟骨骨折作為當前臨床較為常見的一種后足骨折,基于根骨本身解剖結構的復雜性、在后足中的承重功能要求以及周圍軟組織覆蓋較少等原因,導致跟骨骨折治療相對困難。手術治療是當前臨床針對跟骨骨折的共識方案[1]。而在患者手術治療中,多項研究證實跗骨竇入路切口相較于傳統L形切口能更加優秀的恢復跟骨解剖形態,有手術時間短、并發癥發生率相對較低等優勢[2-3],但該項手術對跟骨骨折療效已達上限,患者術后仍不可避免地面臨神經損傷等并發癥威脅[4]。富血小板血漿(PRP)注射是當前臨床在各種肌肉、骨骼疾病治療中廣泛使用的一種治療方案,對促進肌腱、骨骼、組織愈合有良好效果[5]。但當前臨床有關PRP在跟骨骨折中的應用研究較少。基于此,本文以SandersⅢ型跟骨骨折患者為樣本,針對微創跗骨竇入路與PRP局部注射聯合治療的效果進行比較分析。具體如下。
1 資料與方法
1.1 臨床資料 選擇2018年2月—2020年2月我院收治的72例SandersⅢ型跟骨骨折患者作為觀察對象,采用隨機數字表法分為兩組,各36例。觀察組中男16例、女20例,年齡20~65(46.84±9.55)歲,傷后至手術時間(6.13±1.88)d;對照組中男15例、女21例,年齡20~65(45.93±8.96)歲,傷后至手術時間(5.85±1.94)d。兩組患者臨床資料比較差異無統計學意義(P>0.05),具有可比性。本研究獲得醫院倫理委員會批準,且患者及家屬知情同意。納入標準:(1)影像學檢查(X線、CT等)證實為SandersⅢ型跟骨骨折;(2)單側、新鮮、閉合性骨折,無其他部位骨折;(3)無過往下肢手術史、骨折史,能滿足本次隨訪時間要求。排除標準:(1)伴有先天性腳踝關節畸形、嚴重糖尿病且術前血糖水平不穩定者;(2)伴全身性或局部性感染、惡性腫瘤疾病、重度骨質疏松癥。
1.2 治療方法
1.2.1 對照組采用跗骨竇入路手術治療。患者采用腰硬聯合麻醉或全身麻醉,持側臥位,患肢在上。(1)于外踝下0.5~1.0cm位置做微創跗骨竇切口(1.0~2.0cm),切口方向由足部延伸至第四跖骨基底部,沿切口逐層切開皮膚、皮下組織,清理跗骨竇內脂肪、血腫等,明確腓骨長短肌位置。對跟骨外側壁淺面間隙進行銳性分離,將腓腸神經、伴行血管游離后向后牽拉;向前方將距跟骨間韌帶、距跟外側韌帶、跗骨竇韌帶部分切斷,確保跟骰關節充分暴露;向后方將跟腓韌帶部分切斷,確保距下關節面充分暴露。此后將關節面內已經塌陷的內容抬起,直視明確關節面復位效果,使用克氏針臨時固定。(2)于跟骨結節下方2~3cm位置,使用點狀復位鉗完成牽引復位,確認跟骨軸位長度恢復,跟骨內翻畸形恢復;于足跟側外壁使用錘擊法恢復根骨寬度,確保踝關節持跖屈位,能提升跟腱放松效果,緩解跟腱牽拉壓力。使用C型臂X線透視確認根骨長度、寬度、高度、Bohler角度、Gissane角度恢復,確保恢復效果滿意。(3)于跟腱止點位置內側、外側朝向跟骰關節方向,置入6.5mm空心螺釘導針,確保導針深入至關節面下方,完成跟骨軸向固定;于關節面下方外側壁朝向載距突位置置入4.0mm空心螺釘導針,完成關節面固定;使用C型臂X線觀察,確認空心螺釘導針方向、深度符合要求,將空心螺釘擰入并完成固定。(4)使用生理鹽水沖洗后逐層關閉傷口,敷料加壓包扎。術后要求患者保持患肢抬高,完成脫水、消腫、鎮痛等一系列處理措施,術后第2天要求患者進行踝關節屈伸鍛煉。術后第4周X線復查。此后每個月接受1次X線檢查,確認骨折愈合效果。
1.2.2 觀察組同時采用富血小板血漿(PRP)局部注射治療。術前準備、手術方法、術后鍛煉等與對照組相同。但在跟骨關節面恢復、跟骨長度及內翻畸形恢復、相關角度恢復后,抽取患者自體血液100ml,使用兩步離心法完成PRP制作[6];在患者空心螺釘頭部已經到達骨折斷端位置后,于C型臂X線透視下沿螺釘中心將PRP注射至骨折斷端位置,同時注入凝血酶以避免PRP流出。兩組患者均接受術后至少1年隨訪。
1.3 觀察指標 (1)一般手術指標:統計兩組平均手術時間、術中失血量、住院時間、骨折愈合時間、完全負重所需時間及并發癥發生率。(2)足功能評分:使用美國矯形足踝協會制定的后足功能評分量表(Maryland評分)對兩組術后足功能進行評價,Maryland評分量表分值為100分,得分越高即代表患者足功能越好[7]。評估時間為術后3、6、12個月。(3)影像學結果:使用X線測量和統計兩組Bohler角度、Gissane角度,測統時間為術前、術后1年。
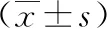
2 結果
2.1 兩組一般手術指標比較 兩組平均手術時間、術中失血量比較,差異無統計學意義(P>0.05);觀察組住院時間、骨折愈合時間、完全負重所需時間短于對照組,差異有統計學意義(P<0.05)。見表1。此外,觀察組并發癥總發生率低于對照組,差異有統計學意義(χ2=4.600,P=0.032<0.05)。見表2。
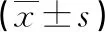
表1 兩組患者手術一般指標比較

表2 兩組患者術后并發癥發生情況比較[n(%)]
2.2 兩組足功能評分比較 術后第3、6、12個月,觀察組Maryland評分高于對照組,差異有統計學意義(P<0.05)。見表3。
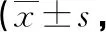
表3 兩組患者手術前后足功能評分比較分)
2.3 兩組影像學結果比較 術前,兩組Bohler角度、Gissane角度比較,差異無統計學意義(P>0.05)。術后1年,兩組Bohler角度高于術前,Gissane角度低于術前,差異有統計學意義(P<0.05);同時兩組Bohler角度、Gissane角度比較,差異無統計學意義(P>0.05)。見表4。
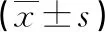
表4 兩組患者手術前后影像學結果比較
3 討論
微創跗骨竇切口入路治療跟骨骨折已經成為當前臨床廣泛使用的一種手術入路選擇,研究證實該項入路在Sanders Ⅱ型~Ⅲ型跟骨骨折患者的治療中具有應力分布均勻、固定穩定性好、手術創傷更小、并發癥發生率更低等多項優勢[8-9]。但基于跟骨骨折病情的復雜性,患者術后仍然面臨骨折延遲愈合、周圍神經損傷等并發癥威脅。對復雜性跟骨骨折患者而言,術后亦常見骨不連等并發癥,對患者康復造成不利影響。另一方面,基于跟骨骨折本身解剖結構與應力特點,患者骨折復位后缺乏有效支撐,單純使用內固定系統并不能為骨折塊與關節面提供長期穩定的有效固定,導致患者骨折后期常見足部僵硬與疼痛等并發癥[10]。因此在微創跗骨竇切口入路治療跟骨骨折的基礎上,仍然應當采取必要措施以保障和提升患者內固定系統支撐的穩定性和持續性,采取有效措施以促使患者骨折快速愈合。
PRP是一種使用離心技術由患者全血中提取得到的血小板血液,其內部血小板濃度是正常水平的5倍左右,同時包含多項能夠促進骨折愈合的生長因子,例如血小板衍生生長因子、胰島素樣生長因子等[11]。研究證實:PRP在局部注射后能夠釋放血小板源生長因子、血管內皮生長因子、轉化生長因子β等多種生長因子,有效促進肌肉軟組織與骨骼疾病的愈合,對加速骨折患者骨折愈合有顯著效果[12]。但此前臨床極少有研究將PRP用于跟骨骨折患者的手術進程中。本文基于PRP的骨折愈合促進效果,選擇Sanders Ⅲ型跟骨骨折患者為研究樣本,在跟骨骨折患者微創跗骨竇入路手術進程中關節復位結束后抽取自體血液完成PRP制備,在空心螺釘到達骨折斷端后選擇注入PRP,同時注入凝血酶以預防PRP流出。如此確保PRP注射后能夠直接作用于患者骨折斷端,充分發揮PRP具備的加速骨折愈合、促進新生骨代謝、縮短骨折修復時間等功效。最終本文結果中觀察組的住院時間、骨折愈合時間、完全負重所需時間短于對照組,并發癥發生率低于對照組,差異有統計學意義(P<0.05)。充分說明PRP在促進骨折愈合方面具有顯著效果。其中觀察組中術后切口相關并發癥發生率為0,說明PRP對促進切口創面愈合亦有積極效果,與其他研究結果[13]相符;術后第3、6、12個月,觀察組Maryland評分高于對照組,差異有統計學意義(P<0.05)。說明PRP聯合微創跗骨竇入路治療跟骨骨折患者,能夠在手術基礎上進一步改善患者術后足功能。相關研究亦證實:PRP能有效提高患者骨折愈合率,為骨組織修復提供充足的生長因子,從而有效提升骨折愈合效果[14]。亦有研究顯示:PRP在肌腱和韌帶損傷修復中亦有優秀的應用效果[15],而微創跗骨竇入路治療SandersⅢ型跟骨骨折患者的手術操作中本身涉及大量肌腱與韌帶切斷操作,使用PRP直接注射到骨折斷端亦有助于患者術后骨折周圍組織的快速恢復,再次為患者術后骨折愈合效果、足功能康復效果提升奠定良好基礎。但需要注意的是,本次研究中存在研究人數較少的局限性,在后續研究中應進一步擴大研究規模并更加深入的分析PRP在不同類型跟骨骨折患者手術治療中的應用效果。
綜上所述,微創跗骨竇入路聯合富血小板血漿局部注射能有效縮短SandersⅢ型跟骨骨折患者的住院時間,促進患者骨折快速愈合的同時對改善術后足功能有顯著作用,對降低患者術后并發癥發生率亦有積極作用,值得深入研究。

