結核病流行背景下胸內結節病與結核病臨床鑒別與處置專家共識
中國防癆協會多學科診療分會 《中國防癆雜志》編輯委員會中華醫學會放射學分會臨床多學科合作工作組
胸內結節病是一種原因不明的,以非干酪樣壞死性上皮樣細胞肉芽腫為病理特征的系統性疾病,而肺結核則是由結核分枝桿菌導致的慢性呼吸道傳染病。兩者病理上均可表現為上皮樣細胞肉芽腫,且在臨床表現、影像學特征等方面具有一定的相似性,給診斷帶來困擾。兩種疾病治療方案截然不同,結節病首選糖皮質激素,而結核病則需進行抗結核治療。如果出現誤診,糖皮質激素的不恰當使用可能會導致結核病惡化,而不必要的抗結核治療則會增加結節病患者藥物不良反應的發生。在結核病高負擔國家和地區,結節病誤診為結核病情況屢見不鮮,需引起關注。據統計,我國約21.0%~40.4%的肺結節病曾被誤診為肺結核[1-2],印度報道結節病誤診結核病的比例也高達30.7%[3]。
我國是結核病高負擔國家,結核病發病例數僅次于印度,居世界第二位。2020年世界衛生組織(World Health Organization,WHO)估算我國結核病發病率為59/10萬[4]。結核分枝桿菌潛伏感染(latent tuberculosis infection,LTBI)為對先前獲得的結核分枝桿菌抗原產生的持久免疫反應狀態,而沒有活動性結核病證據。我國LTBI人口基數龐大,15歲及以上人群潛伏感染率為20.3%,并隨年齡增長呈現增加趨勢[5]。2017年,國家衛生與健康委員會發布了肺結核病診斷標準[6];2019年,中華醫學會呼吸病學分會發布了中國結節病診斷和治療專家共識[7]。但在臨床實際工作中,對兩種疾病鑒別與處置上尚存在一些亟待解決的問題:一是感染因素,包括結核分枝桿菌及非結核分枝桿菌(nontuberculous mycobacteria,NTM)在內,可能與結節病的發病相關[8],雖然迄今為止尚無明確結論,但在臨床工作中,由于缺乏有效的生物學標志物用于兩種疾病的鑒別,給鑒別工作帶來挑戰;二是結核分枝桿菌病原學檢查在鑒別診斷中發揮關鍵作用,但對組織標本中病原學檢查技術的運用尚未形成共識;三是在臨床鑒別過程中,對相關輔助檢查的評價、鑒別診斷流程等方面也需及時更新;四是結節病患者,特別是接受生物制劑、長期糖皮質激素和(或)免疫抑制劑治療的結節病患者,需研究制定LTBI的篩查與管理策略等。為此,中國防癆協會多學科診療分會、《中國防癆雜志》編輯委員會與中華醫學會放射學分會臨床多學科合作工作組聯合組織相關學科專家在充分討論后制定了本共識。
共識形成
中國防癆協會多學科診療分會、《中國防癆雜志》編輯委員會和中華醫學會放射學分會臨床多學科合作工作組聯合成立共識編制指導委員會,確定了共識專家組成員(共計55名)。專家主要來自結核科、呼吸科、影像科、病理科及其他相關學科,在結節病和結核病診療領域經驗豐富,均具有高級職稱資格。指導委員會采用了基于德爾菲法的專家共識編制流程:首先向多學科專家組收集、歸納和形成14個臨床問題,并就臨床問題由專家組投票達成一致。然后,證據組專家結合臨床問題對近20年來國內外發表的相關文獻進行檢索,原始數據來源于PubMed、萬方數據庫和中國知網數據庫。經過篩選,共對304篇文獻進行了系統分析和評價,重點納入了薈萃分析、系統綜述、隨機對照研究、隊列研究、病例系列研究等。在共識編寫過程中,核心撰寫組經過反復征求專家意見,并結合我國診斷和檢測技術應用現狀和實際情況,整合并起草了關于結節病與結核病臨床鑒別和處置的11條推薦意見。最后,使用在線問卷方式,由專家組成員對逐條推薦意見進行評價和賦分,評價內容包括:同意度、重要性、熟悉程度、證據強度、推薦強度等,采取5級,10分評分制。共發出問卷55份,回收有效問卷50份(90.9%)。經統計,各條推薦意見的一致性較高,變異系數均<30%(表1)。

表1 結核病流行背景下胸內結節病與結核病臨床鑒別與處置推薦意見一致性
經過文獻系統評價發現:結核分枝桿菌與結節病發病相關性尚無確定性結論;在結核病流行國家和地區對于結節病與結核病的臨床鑒別與處置仍存在許多不確定性;基于結節病與結核病鑒別的高質量臨床研究證據是不足的,缺乏可靠的新型生物標志物用于結節病和結核病鑒別。因此,本共識中的推薦意見未給出具體的循證醫學證據質量評價和推薦強度分級[9],而是結合當前的研究成果、重要性及技術可及性,對每條推薦意見采取了“應該”“建議”和“可能”表述。經德爾菲法問卷調查,專家對逐條推薦意見的推薦強度表達“同意”和“比較同意”的一致率均>90%。
共識內容
推薦意見1:結節病是一種可累及全身多器官的肉芽腫性疾病,當與結核病鑒別困難時,應積極尋找胸外器官受累證據,提高診斷效率。
90%以上結節病患者有不同程度的肺受累和(或)胸內淋巴結腫大,而胸內結節病患者中約40.6%有胸外受累,最常見部位是胸外淋巴結(23.1%)和皮膚(13.5%)[10],其次為肝或胃腸道、眼、腎、神經系統、心臟、胸膜、肌肉和骨骼受累等(圖1~9)。因此,當胸部病變特征不足以診斷時,應進行詳細的病史采集和仔細的全身體格檢查,努力尋找胸外受累的線索,及時啟動專科檢查。

圖1~9 結節病胸外器官和組織受累表現。圖1~3為結節病皮膚受累表現。圖1可見患者左眉際處多發紅色粟粒大小丘疹,融合成片,約2 cm大小,邊界不清。圖2為結節病凍瘡樣狼瘡,可見患者雙側面頰部紫紅色浸潤性斑塊,表面有鱗屑。圖3可見患者背部多發紫紅色米粒大小丘疹、結節,部分融合,觸之有浸潤感,為典型結節病皮疹表現。圖4~5為同一病例。患者,女,51歲,診斷結節病。圖4為肺CT縱隔窗,顯示右上縱隔氣管旁多組淋巴結腫大,伴斑點樣鈣化,左側胸腔積液,雙腋下多發淋巴結腫大,右胸壁軟組織腫脹。圖5為患者腋前區和肩部皮膚可見多個橢圓形紫紅色結節,質地堅硬;皮膚病變組織活檢,病理提示肉芽腫性變,符合結節病。圖6為胸內結節病患者可見脛前散在大小不等紅色丘疹及斑塊,部分上覆白色鱗屑,斑塊形態不規則,邊界較清楚。圖7~9為眼結節病。圖7為熒光素眼底血管造影,顯示眼結節病患者視網膜血管炎表現。圖8可見眼結節病導致房水混濁,虹膜周邊可見數個灰白色Busacca結節。圖9可見結節病患者右上眼瞼腫脹,瞼結膜炎
結節病所致淺表淋巴結腫大多位于頸、腋窩、腹股溝和滑車上等處,通常無痛、不融合、與周圍組織無粘連。皮膚受累表現包括凍瘡樣狼瘡、結節紅斑、皮下結節、丘疹和斑塊等,其中,凍瘡樣狼瘡為皮膚結節病的特征性表現,表現為耳、頰部、鼻尖、指趾等處對稱出現,浸潤較淺的慢性硬化性丘疹或斑塊。11%~23%的結節病患者伴有眼部病變[11-12],主要表現為肉芽腫性葡萄膜炎(以前和中葡萄膜炎多見,積膿少見)[13-14],角膜炎和結膜炎臨床也較為常見,鞏膜、眼瞼、淚腺、視神經和眶周也可受累,但較少見。2%的結節病有心臟受累,早期無明顯癥狀,隨病情進展可以出現心悸、暈厥、左心衰竭等表現,常規心電圖可作為結節病心臟受累的初篩手段,可發現完全性傳導阻滯,室性或房性心律失常等,結節病易累及肝及胃,而腸道罕見,由于患者臨床表現隱匿或缺少特異性消化道癥狀,常需通過活檢明確診斷。結節病相關胸腔積液出現于1%~3%的結節病患者中,以氣短和乏力為主要表現,由于胸腔積液檢查缺乏特異性,容易與結核性胸膜炎混淆。
肺結核也可以合并肺外結核,常見于血行播散性肺結核、糖尿病合并肺結核,以及其他免疫功能低下患者[15]。肺外結核包括淋巴結結核、結核性漿膜腔積液、骨關節結核、泌尿及生殖系統結核、腸結核和結核性腦膜炎等。肺外淋巴結結核以頸部最為多見,主要位于胸鎖乳突肌外緣及鎖骨上區,呈串珠樣或簇集樣排列,可增大或融合,壞死后形成冷膿腫,易與結節病相鑒別。皮膚結核少見,其中,尋常狼瘡約占皮膚結核的50%~70%,好發于面部,皮損呈片狀,邊界清楚,其內可見紅斑、丘疹和結節,常伴潰瘍壞死和結痂,愈合后易形成瘢痕。結核感染后少數患者可出現結節性紅斑和皮下結節(多見于小腿伸側)、反應性骨關節炎(Poncet綜合征),可能與結核分枝桿菌抗原所介導的超敏反應有關。眼結核包括葡萄膜炎(后葡萄膜炎為主)、脈絡膜結節和結核瘤,以及鞏膜炎和泡性角結膜炎等,結核分枝桿菌檢測常呈陰性。部分眼結核也可能與超敏反應有關,具體機制不詳,此時與結節病鑒別較為困難[16],需結合胸內病變臨床特征綜合評價。
疑診結節病患者應重視血常規、肝腎功能全項、血鈣及尿鈣等檢查。血清血管緊張素轉化酶(serum angiotensin converting enzyme,sACE)升高對于多系統受累結節病的診斷價值優于胸內結節病,但總體上sACE對于結節病診斷的敏感度和特異度不高[7],由于部分繼發性肺結核和粟粒性肺結核也可見顯著升高[17-19],其在兩病鑒別的價值有限。12%的結節病患者肝功能異常,表現為血清堿性磷酸酶和γ-谷氨酰轉肽酶水平升高;7%的結節病患者呈血肌酐升高伴或不伴尿液分析結果異常(如鏡下血尿、無菌性膿尿和蛋白尿)[20];6%的結節病患者血鈣升高,具有發生腎結石風險。以上檢驗指標可作為胸外結節病的篩查線索。結節病相關胸腔積液臨床少見,為滲出液,常規檢查中總有核細胞計數>500個/μl,淋巴細胞百分比>50%,由于部分結節病患者胸腔積液中腺苷脫氨酶也可升高,與結核病鑒別困難[21]。結核菌素皮膚試驗(tuberculin skin test,TST)或γ-干擾素釋放試驗(interferon-gamma release assays,IGRA)對結核病診斷有提示作用,但需要注意的是,由于TST硬結平均直徑≥10 mm或IGRA陽性并不能區分LTBI和活動性結核病,故診斷仍需結合臨床。
影像技術在評價結節病胸外器官受累方面發揮重要作用。心臟磁共振(cardiac magnetic resonance,CMR)對心臟結節病診斷具有價值[20],T2WI或T2-mapping 序列可顯示心肌炎癥、水腫,延時釓增強(late gadolinium enhancement,LGE)序列可顯示為心外膜下、心肌內的壞死、疤痕形成。安裝起搏器的患者可以使用正電子發射計算機體層顯像儀(positron emission tomography and computed tomography,PET/CT)代替CMR來評估心臟受累情況。結節病累及腹部實質器官(包括肝、脾、腎和腹部淋巴結腫大等)推薦磁共振成像(magnetic resonance imaging,MRI)和CT檢查,肝結節病影像表現為肝腫大,可同時伴脾腫大和腹膜后淋巴結腫大。肝實質見彌漫或多發的小結節,增強CT表現為低密度結節,在MRI序列中均顯示低信號。神經系統結節病MRI表現為腦室周圍白質病變、腦膜炎或腦膜腦炎、腦實質病變、顱神經炎和脊髓病,但缺乏特異性[22]。當肝、脾和神經系統受累時需要與血行播散性結核病鑒別。PET/CT在結節病活動性判斷方面具有價值,可以發現更多的器官受累證據,但由于活動性結核病和其他活動性炎癥、惡性腫瘤也會導致病灶的示蹤劑攝取增加,在鑒別診斷上價值受限。
當結節病與結核病鑒別困難時,需兼顧胸內和胸外病變的臨床特點進行綜合判斷,有助于提高鑒別診斷工作效率。獲得組織學證據是必要的,原則上皮疹、皮下結節、淺表腫大淋巴結、眼結膜結節和淚腺腫大等疑似為結節病導致時,均可首先進行活檢。如果這些病變不存在或活檢結果無法診斷,則選擇胸內淋巴結或肺組織活檢。同時推薦對活檢組織、分泌物、胸腔積液、腦脊液和尿液等標本進行常規結核分枝桿菌檢查,以此作為診斷或排除結核病的依據。
推薦意見2:應采用高分辨率CT和增強CT對胸內病變進行系統評價,并結合動態CT隨訪,提出傾向性診斷。
胸部X線攝片對表現典型的結節病和結核病具有診斷價值,并且可用于結節病的分期,但對于不典型病例的鑒別價值有限。高分辨率CT(high resolution CT,HRCT)可清晰顯示肺部病變影像特點,并對結節分布做出準確判斷,推薦用于結節病診斷與鑒別診斷。增強CT(主要為主動脈期和延遲期)有助于觀察胸內淋巴結病變強化特征,辨別有無壞死、融合等。為減少容積效應,更為清晰地顯示淋巴結內部及周圍組織結構改變和微小壞死灶,建議采用增強CT掃描的薄層重建技術。另外,CT可用于指導支氣管鏡對支氣管或肺組織病變的活檢,或經CT引導對肺內病變進行穿刺活檢等。
胸內結節病與肺結核的影像學診斷建議采用分級診斷原則,即基于結節病與結核病兩個極端,采用“確定、可能性大、不確定、可能性小和否定”五等級法對影像表現進行客觀評價。對結節病具有診斷價值的典型征象包括:雙側肺門對稱性淋巴結腫大和(或)伴雙肺中上區多發的淋巴管周分布小結節;對結節病具有排除診斷價值的征象包括:結節呈小葉中心分布為主(小葉中心結節和樹芽征)、空洞性病變伴發氣道播散、胸內淋巴結腫大伴多發壞死或增強CT呈環形強化等,而這些征象群對結核病具有診斷價值。不確定型包括但不限于:(1)肺內結節分布特征判斷困難或出現了混合分布情況等;(2)肺門及縱隔淋巴結不對稱分布或強化特征不典型;(3)出現了結節病與肺結核共有征象[23-33],諸如微結節簇集征、星系征、反暈征、空洞、斑塊/腫塊、實變、淋巴結壞死/強化不均勻、磨玻璃密度影、胸膜受累等;(4)結節病纖維化期與慢性纖維空洞性肺結核鑒別困難時。
需要指出的是,結節病影像學診斷不應基于個別征象做出判斷,而應將CT掃描所顯示胸部病變的征象群及胸外器官受累的影像學特征作為一個整體進行分析,同時,要加強影像學的動態隨訪,觀察病變的演變規律。通過對不典型征象的觀察和經驗積累,并加強與臨床溝通,對診斷“不確定”做出結節病或結核病可能性大和小的傾向性判斷(表2,圖10~21)。需要注意的是,在對不確定征象進行評估的過程中,仍需注意排除其他肺部疾病。

圖10~21 胸內結節病與結核病征象比較。圖10為結節病微結節簇集征,高分辨率CT掃描顯示雙肺中上區多發團片狀微結節簇集影,結節排列紊亂,伴支氣管血管束增粗。圖11為肺結核微結節簇集征,肺CT掃描顯示雙肺中上區多發團片狀微結節簇集,結節排列規則,未見中軸間質異常。左上肺微結節簇集區發生融合和壞死,形成厚壁空洞。圖12~15為結節病(同一病例)。圖12、13高分辨率CT掃描顯示左下肺胸膜下單發不規則實變,矢狀位重建顯示葉間裂胸膜呈結節樣增厚,病變呈非對稱性。圖14為超聲支氣管鏡引導下的經支氣管針吸活檢穿刺組織(縱隔第7組淋巴結)病理檢查為肉芽腫性炎(HE,×100)。組織切片另行抗酸染色和PAS染色均呈陰性,免疫組化CD68(+),符合結節病特征。圖15為左下肺病灶經皮肺穿刺活檢,病理結果為肉芽腫性血管炎,未見干酪性壞死(HE,×100)。圖16為結節病,高分辨率CT掃描顯示雙下肺實變和結節,周圍伴淋巴管周分布的小結節,呈星系征表現(箭)。圖17為結節病,增強CT顯示雙側肺門及縱隔淋巴結腫大,呈對稱性分布,為Ⅰ期結節病典型表現。圖18為結節病,增強CT延遲期顯示右肺門兩枚淋巴結呈環形強化,中心呈低密度,提示壞死(箭),而其余淋巴結未見壞死。圖19為結節病,增強CT延遲期顯示左肺門和隆突下淋巴結中心呈低密度(箭),提示壞死,而其余淋巴結未見壞死。圖20為縱隔淋巴結結核,增強CT顯示血管前間隙、主肺動脈窗和雙側肺門多組淋巴結腫大伴壞死,增強CT均呈典型環形強化特征。圖21為縱隔及肺門淋巴結結核,增強CT顯示雙肺門及縱隔淋巴結腫大,大小不一,右肺門淋巴結融合呈團塊影,未見淋巴結壞死

表2 結節病與結核病影像診斷分級中幾種不確定征象的診斷傾向提示[3,23-32,34-37]
推薦意見3:支氣管鏡檢查應常規用于胸內結節病和菌陰肺結核病鑒別,應重視支氣管黏膜活檢技術的普及和應用。根據病變特點選擇經支氣管鏡肺活檢和淋巴結針吸活檢用于肺組織和縱隔/肺門淋巴結病變診斷。
胸內結節病與結核病鑒別時應進行支氣管鏡檢查。支氣管鏡不但可以直視氣道內病變,還可以通過以下技術取得活檢組織進行病理診斷,包括:支氣管黏膜活檢(endobronchial biopsy,EBB)、經支氣管鏡肺活檢(transbronchial lung biopsy,TBLB)、經支氣管冷凍肺活檢(transbronchial cryobiopsy,TBCB)、胸內結節病支氣管鏡下可觀察到氣管和支氣管的異常表現有[38-40]:(1)黏膜改變。40%~70%的結節病存在氣管和支氣管黏膜異常改變,主要表現包括:黏膜充血、水腫、肥厚和黏膜結節,其中,多發黏膜結節為典型改變,呈黃白色顆粒狀或斑塊狀,散在分布。黏膜彌漫增厚多表現為氣管壁明顯增厚,外觀呈“鋪路石樣”,可延伸至肺葉和肺段支氣管,而黏膜表面多不伴有壞死及潰瘍。(2)管腔狹窄。氣管支氣管因黏膜充血、水腫、肥厚及結節樣增生等而表現為管腔不同程度的狹窄;或因肺門、縱隔淋巴結腫大壓迫,可導致隆突或支氣管嵴增寬,管壁受壓甚至管腔外壓性狹窄。結節病氣道黏膜結節的發生率為12.8%~62.5%,對于黏膜結節經EBB診斷率可達到80.8%,即使無明顯黏膜改變的結節病,EBB活檢陽性率也可達15.3%[41]。因此,應重視EBB在結節病診斷中的普及應用。
經支氣管鏡淋巴結針吸活檢(transbronchial needle aspiration,TBNA)和超聲支氣管鏡引導下的經支氣管針吸活檢(endobronchial ultrasound-guided transbronchial needle aspiration,EBUS-TBNA),也可對刷檢物、支氣管沖洗液(bronchial washing fluid,BWF)及支氣管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)等進行細胞學或病原學檢查。
支氣管結核鏡下活動期可分為Ⅰ型(炎癥浸潤型)、Ⅱ型(潰瘍壞死型)、Ⅲ型(肉芽增殖型)及Ⅳ型(淋巴結瘺型)[42]。炎癥浸潤型表現為支氣管黏膜充血和水腫,病變局部黏膜表面可見灰白色粟粒狀結節,管腔由于黏膜腫脹而有不同程度的狹窄;潰瘍壞死型表現為在充血水腫的基礎上出現潰瘍,表面常有灰白色的干酪樣壞死組織覆蓋;肉芽增殖型可見肉芽組織增生部分阻塞管腔;淋巴結瘺型為縱隔或肺門淋巴結結核破潰入支氣管,瘺口周圍組織充血水腫,局部潰瘍形成。EBB是診斷支氣管結核最可靠的取樣方法,對肉芽腫的檢測敏感度為72.2%~100.0%。支氣管結核的病原學陽性率高達60%~70%[42],懷疑支氣管結核時應收集支氣管管腔內分泌物、壞死組織及BWF等完成結核分枝桿菌涂片、培養或分子生物學檢測。
TBLB診斷肺結節病的陽性率為40%~90%[43]。對于支氣管黏膜正常的疑似結節病,EBB聯合TBLB可提高結節病診斷率;比較而言,TBLB在涂陰肺結核診斷應用中沒有結節病普遍。由于BALF的結核分枝桿菌核酸檢測在菌陰肺結核診斷方面可獲得與傳統TBLB相當的診斷率[44-45],作為替代性技術可避免TBLB活檢造成的氣胸和出血。但當肺內病變需要與結節病鑒別時,TBLB仍不可或缺。
在結核病流行地區,結節病導致的縱隔及肺門淋巴結腫大需重點與淋巴結結核鑒別。TBNA對結節病和結核病的診斷率分別可達42%~76%[46-47]和65%~100%[45]。隨著超聲支氣管鏡的引入,EBUS-TBNA 已成為診斷胸內淋巴結病變的重要手段。EBUS-TBNA對Ⅰ、Ⅱ期結節病的診斷率達87%[20];對淋巴結結核的診斷率達80%~85%[48-49]。
推薦意見4:BALF結核分枝桿菌分子生物學檢測或培養應作為結節病與結核病鑒別的常規手段;BALF中的CD4+/CD8+T細胞比值對兩者鑒別可能具有價值,診斷尚需結合臨床。
1.BALF結核分枝桿菌病原學檢查:胸內結節病主要與涂陰肺結核進行鑒別,該類患者臨床以干咳少痰為主,痰結核分枝桿菌病原學檢查陽性率較低。BALF結核分枝桿菌檢查可以為結核病診斷提供重要的線索和依據。對BALF行GeneXpert MTB/RIF檢查為痰涂片陰性或痰液樣本不足的患者提供了一個可靠的替代方法[50]。國內一項橫斷面研究表明,BALF的GeneXpert MTB/RIF、宏基因組二代測序(metagenomics next-generation sequencing, mNGS)、結核分枝桿菌培養診斷肺結核的敏感度分別為 69.0%、59.9%、59.9%,遠高于BALF涂片法(24.6%)。其中,GeneXpert MTB/RIF敏感度最高,mNGS還可同時檢測NTM和其他致病菌,可以根據診斷需求選擇應用[51]。總之,在結節病與結核病鑒別時,推薦開展BALF結核分枝桿菌分子生物學檢查或培養,優化BALF在兩病鑒別中的應用。
2.BALF細胞學與T細胞亞群分析:BALF有核細胞分類和淋巴細胞亞群對于結節病的診斷及活動性的判斷具有參考價值。肺結節病BALF淋巴細胞百分比一般大于15%,CD4+/CD8+T細胞比值(>3.5)診斷結節病的敏感度為53%,特異度為94%。多項研究表明,肺結核BALF的CD4+/CD8+T細胞比值升高,平均值在 1.23~2.9之間,略低于結節病組[52]。據文獻報道,21%~29%的肺結核患者BALF的CD4+/CD8+T細胞比值大于3.5,但研究均未對入選肺結核患者的臨床表現和影像學類型進行闡述[53-54]。結合上述結果,目前仍認為CD4+/CD8+T細胞比值對于結節病和結核病鑒別具有參考價值,但應盡量避免僅憑CD4+/CD8+T細胞比值診斷或除外結節病,診斷仍需結合臨床。
推薦意見5:病理科醫師對于肉芽腫病變,在病理報告時應詳細描述肉芽腫形態、分布特征及伴隨病變,并提出傾向性意見。
結節病及結核病病理組織學均為肉芽腫病變,均排列緊密,形態類似,但結節病肉芽腫多沿淋巴管間質分布,肉芽腫結節大小較一致,且融而不合,邊界清晰,常伴纖維組織增生,周圍淋巴細胞較少,還可見包涵體(星狀小體、舒曼小體、鈣化小體)等[7]。無論是活檢還是手術樣本,如出現壞死性或松散的肉芽腫及肺泡腔內肉芽腫,以及大量炎癥細胞浸潤、機化性肺炎時,則不支持結節病診斷。結核病肉芽腫可伴或不伴有干酪樣壞死,肉芽腫結節大小不一,常沿氣道分布或隨機分布,結節周圍見較多淋巴細胞浸潤,肺泡腔內可見漿液性或纖維素性滲出[55-56]。外科肺活檢標本中,如僅見到非壞死性肉芽腫,且分布在肺間質內,沒有肺泡腔滲出和壞死性病變,則基本不考慮結核。非常小的活檢標本無法顯示伴隨病變及肉芽腫分布特點。如僅見非壞死性肉芽腫的情況,病理科醫師難以區分增殖性病變為主的結核病和結節病,需結合組織標本的結核分枝桿菌檢測進行綜合評價。
結節病通常為非壞死性肉芽腫,但約20%的結節病可在肉芽腫內出現點灶狀、紅染纖維素樣或凝固性壞死,通常呈小灶性,僅累及部分肉芽腫的中心部分。結節病淋巴結的大體標本中出現較大的融合壞死區域較為罕見,可能與發熱、結節性紅斑和關節痛等伴發癥狀相關,部分的壞死可能與活檢取材有關[57]。壞死性肉芽腫病理診斷結節病應慎重,需滿足以下條件方可診斷:(1)壞死區外病變需符合結節病病理表現;(2)病原菌(包括抗酸染色、組織標本分枝桿菌培養及分子生物學檢測)檢測陰性;(3)臨床表現及胸部CT影像特征應符合結節病的特征。
肉芽腫可見于多種感染和非感染性疾病,其分布、形態及伴隨病變,以及是否合并壞死等組織學特點可為分析病因提供線索。病理科醫師應仔細觀察,對每例患者肉芽腫的組織形態特點進行準確描述并提出傾向性意見(表3,4;圖22~25)。

表3 結節病病理組織學形態特征

表4 結核病病理組織學形態特征

圖22~25 結節病與結核病病理表現比較。圖22為結節病(經支氣管鏡肺組織活檢標本)。病理可見結節病的非壞死性肉芽腫上皮樣細胞排列緊密, 周圍浸潤淋巴細胞較少,病變位于肺間質,肺泡腔內無肉芽腫及炎癥滲出(HE,×20)。圖23為結節病(支氣管鏡內膜活檢標本)。支氣管內膜內見上皮樣細胞肉芽腫結節,中心見少許纖維素樣壞死(箭)(HE,×50)。圖24為肺結核。病變沿氣道分布(箭標記細支氣管炎),肉芽腫大小不等,中心部見干酪樣壞死,周圍見較多淋巴細胞浸潤(HE,×20)。圖25為結核病。肉芽腫內干酪樣壞死,顯微鏡下呈紅染、顆粒狀,周圍見上皮樣組織細胞及多核巨細胞(HE,×100)
推薦意見6:病理報告的肉芽腫病變,建議常規做特殊染色尋找結核分枝桿菌,對需要與結核病鑒別的活檢及手術標本應進行分枝桿菌培養和菌種鑒定。
肉芽腫病變內找到結核分枝桿菌是確診結核病的強有力證據。在我國結核病流行背景下,對病理查見的肉芽腫病變建議常規進行特殊染色(包括但不限于抗酸染色)并報告結果。結核分枝桿菌需在高倍鏡或油鏡下仔細尋找,多在壞死與存活組織交界處,也可在壞死中心或者細胞肉芽腫內查見,有條件可以加做結核分枝桿菌及真菌的熒光染色。病理組織切片抗酸染色技術操作簡便,但陽性率較低,僅達15.5%~29%[58-59]。因此,抗酸染色陰性仍不能排除結核病。另外,由于抗酸染色法難以區分結核分枝桿菌和NTM,應通過對硝基苯甲酸(PNB)選擇性培養基法、MPT64抗原檢測法或核酸擴增實驗完成初步菌種鑒定。
在懷疑結核病時,臨床醫師對獲得的活檢或手術標本應及時送組織培養。組織培養可以檢測出具有生長活性的分枝桿菌,可以通過菌種鑒定鑒別結核分枝桿菌及NTM,并可完成藥物敏感性試驗。結核病病理組織標本中結核分枝桿菌培養的陽性率為30%~73%[58-59],明顯高于抗酸染色。分枝桿菌培養包括固體培養和液體培養兩種方法。液體分枝桿菌培養管(MGIT)方法顯示出比固體培養更高的陽性率[60]。固體培養基方法約4周報告陽性結果,陰性結果通常需要8周;液體培養技術(如全自動快速分枝桿菌培養系統)一般2~3周報陽性結果,陰性結果一般為6周[60]。需要指出的是,分枝桿菌培養耗時較長,難以滿足臨床即時診斷需求,是其主要不足。
在結核病與結節病的組織病理學鑒別中,應綜合評價組織形態學和病原學檢測結果。對具備結核分枝桿菌感染對應的組織形態學表現,同時,組織培養陽性并經菌種鑒定為結核分枝桿菌可確定結核病;具備結核分枝桿菌感染對應的組織形態學表現,但抗酸染色及組織培養陰性,應進一步結合臨床表現及影像學特征,必要時進行組織標本DNA檢測;具備結節病的典型組織形態學表現,同時,組織培養陰性,臨床表現及胸部CT影像特征符合結節病,可做出結節病診斷。如缺乏組織學或病原學證據,或二者不一致,推薦多學科聯合會診(multi-disciplinary team,MDT)。
推薦意見7:結節病與結核病鑒別時,建議將分子生物學技術用于組織學標本結核分枝桿菌檢測,但不能替代分枝桿菌培養作為診斷金標準,陽性結果需結合臨床表現綜合考慮。
近年來,各種結核分枝桿菌分子生物學診斷技術在結核病與結節病的診斷與鑒別診斷中得到應用,如原位雜交、實時熒光定量PCR、線性探針和宏基因組測序技術等。原位雜交技術屬于非擴增探針技術,對組織量要求低,可在組織切片上完成檢測,但敏感度較低[60]。PCR技術具有快速、敏感度和特異度高的優點。其中,GeneXpert MTB/RIF用于快速診斷結核病得到了WHO建議,推薦其作為顯微鏡檢查、培養或組織病理學的替代性診斷,可用于檢測非呼吸道標本(淋巴結和其他組織)[61]。研究表明,EBUS-TBNA活檢標本GeneXpert MTB/RIF診斷結核病的敏感度、特異度、陽性和陰性預測值分別為49.1%、97.9%、92.9%和77.3%[62]。
分子生物學檢測方法提高了結核分枝桿菌DNA檢測陽性率,但同時也增加了診斷困惑。Gupta等[8]通過薈萃分析,對874例證實為結節病的組織學樣本(主要為淋巴結組織)使用PCR法進行核酸擴增并鑒定了不同類型分枝桿菌特異性的核酸序列,發現26.4%(231份標本)結節病樣本呈分枝桿菌陽性,其中,81.0%(187份標本)為結核分枝桿菌DNA檢測陽性。國內報道結節病活檢標本的結核分枝桿菌DNA陽性率為19.2%[63],與之接近。由于傳統的培養技術很難在結節病組織中分離出結核分枝桿菌,二者的關聯性至今仍無定論。有研究推測,一些特異性的、降解不良的分枝桿菌抗原導致了免疫介導的肉芽腫性炎癥,而不是完整的具有活性的分枝桿菌導致結節病[64]。在臨床實踐中,組織學標本結核分枝桿菌DNA陽性與臨床表現不符的情況并不少見,分析存在幾種可能的原因[63-65]:(1)提示為LTBI或結核病亞臨床狀態;(2)陳舊病變殘留結核分枝桿菌死菌或難以降解的抗原片段;(3)因實驗室污染(包括石蠟包埋標本的污染等)造成的假陽性等。因此,對于組織標本結核分枝桿菌DNA陽性并非現癥感染確切依據的情況,應審慎對待。我國為結核高感染國家,結核感染導致的肺內陳舊性病變和淋巴結病變較為多見,自愈后結核分枝桿菌死菌片段殘留在淋巴結或肺組織中可能是造成其DNA陽性的主要原因。鑒于人群的結核高感染環境,應遵循不但要在病變組織中分離培養出活性純系菌株,而且該菌株接種到動物可致病,方可確認致病病原體的科赫法則,強調分枝桿菌培養仍是結核病診斷的金標準。分子生物學檢測技術診斷快速,可以滿足即時診斷需求,在傳統病原學檢查陰性的情況下可以發揮補充證據作用,而不能過度依賴,此與結核病低流行國家和地區情況存在不同。另外,需與結核病鑒別時,應送檢新鮮的活檢或手術組織標本供分子生物學檢測。
最近,有研究針對EBUS-TBNA標本使用結核分枝桿菌RNA恒溫擴增實時熒光檢測(simultaneous amplification and testing method forMycobacteriumtuberculosisRNA,SAT-TB),該技術可以鑒別死菌與活菌,可有效將結節病組織標本中死菌片段造成的PCR假陽性剔除。SAT-TB在區分涂陰肺結核與結節病方面的敏感度、特異度、陽性預測值、陰性預測值和診斷準確率分別為77.8%、100.0%、100.0%、93.1%和94.4%[66]。由于rRNA極易降解,其對標本要求相對較高,該技術尚未推廣應用評價;還有研究通過對測序原始序列中的低質量序列和導管接頭污染進行了去除和過濾,重新制定了NGS測序數據分析標準(深度>10倍和覆蓋率>15%),分別對44例結核病和47例結節病患者的活檢組織標本進行結核分枝桿菌檢測,改良NGS識別結核病的敏感度和特異度分別達到81.8%和95.7%,對快速區分結核病和結節病可能具有價值[67]。
推薦意見8:應采用結核科和呼吸科共同主導的多學科合作模式,開展結節病與結核病鑒別診斷、處置和隨訪工作。
胸內結節病和部分菌陰肺結核診斷都屬排除性診斷。對于經過充分的臨床檢查仍然無法確定診斷的病例需要進行MDT。建議由結核科和呼吸科共同主導,參與學科包括但不限于影像科和病理科,必要時邀請眼科、皮膚科、心血管科、檢驗科等相關學科參與。在多個學科構成的MDT中,各專科醫師既要各司其職,發揮專長,又要與其他專科開展有效的交流與合作,進而達成對于疾病診斷和處理的共識。MDT需要面對的主要問題包括但不限于:(1)臨床表現難以確定結節病或肺結核,需要通過病理進行判定,但病理學表現不典型者;(2)病理學表現符合結節病,但病理組織中結核分枝桿菌或NTM病原學檢查呈陽性者;(3)存在肺內多部位、多形態病變,分別具備結節病和結核病的部分征象特征,臨床診治決策困難者;(4)初診結節病或結核病,在治療過程中出現新的變化,無法用初始診斷解釋的情況;(5)在結節病與結核病鑒別診斷過程中,淋巴增生性疾病、IgG4相關疾病、惡性腫瘤、塵肺及真菌病尚需排除者等。
針對胸內結節病與結核病難以鑒別的情況,需盡可能全面采集臨床信息,并獲得影像學、病理學和病原學的證據后進行綜合評價。對于矛盾性證據,需結合組織標本的結核分枝桿菌培養或對獲得新的組織標本進行重新評價,其中,結核分枝桿菌病原學檢查往往發揮關鍵作用。每次MDT均應確保新發現的證據統一納入綜合證據評價體系中,供多學科專家進行集體決策。胸內結節病與結核病鑒別與處置流程見圖26。
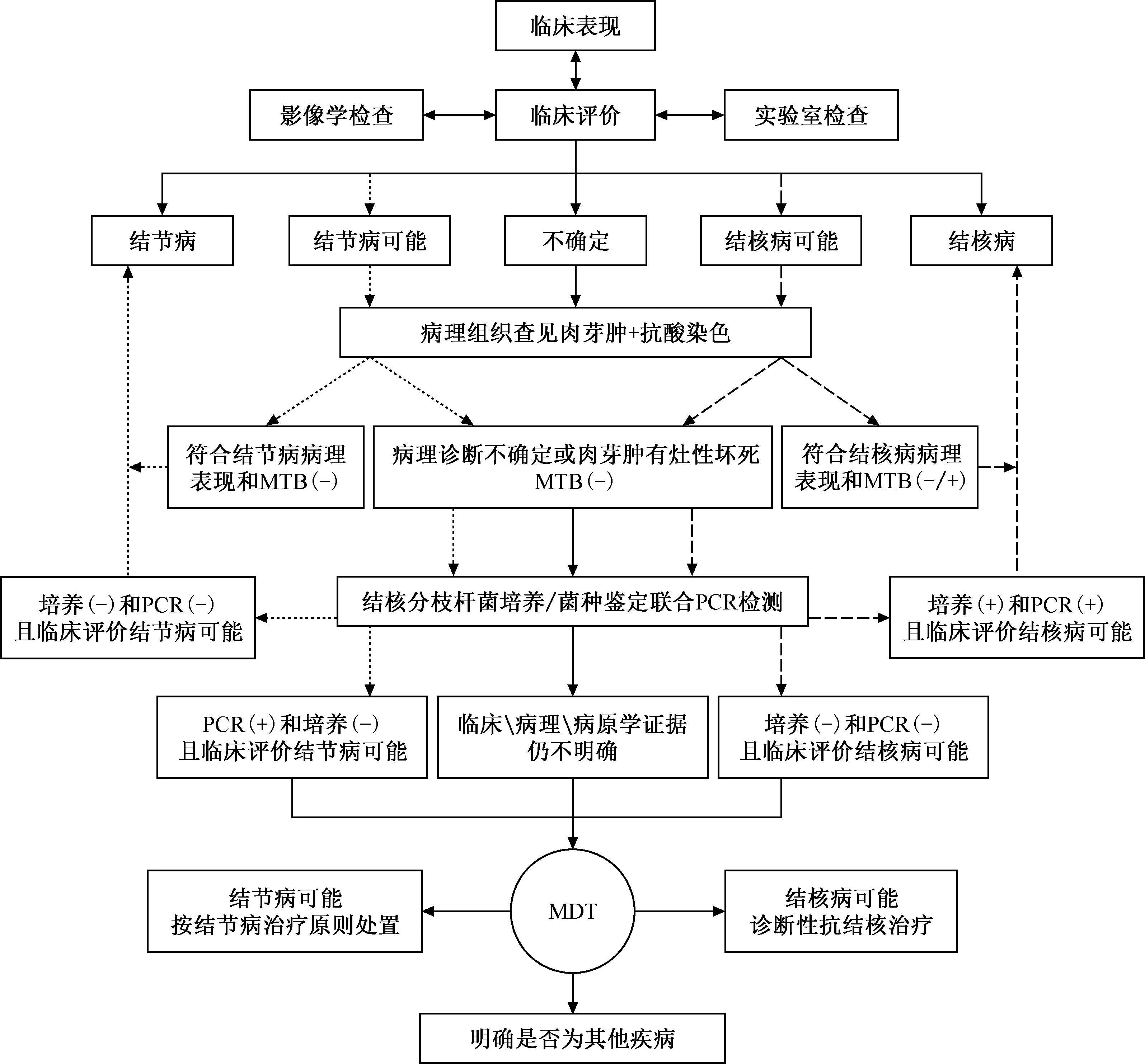
注 MTB:結核分枝桿菌; MDT:多學科聯合會診; 流程圖中,臨床評價的“結節病可能”“不確定”和“結核病可能”分別使用不同箭頭類型代替,代表整個診斷過程均需結合臨床評價做出判斷
推薦意見9:經MDT或完善相關檢查后仍難區分胸內結節病與肺結核時,經權衡利弊和知情同意后,建議選擇診斷性抗結核治療。
經過MDT仍無法對結節病和結核病做出準確判斷或診斷流程無法推進時,在患者知情同意前提下,可采取診斷性治療驗證診斷。實施診斷性治療前需權衡利弊,對于癥狀較輕、病情穩定、無重要臟器受累、無需優先處理結節病前提下,建議優先選擇診斷性抗結核治療。由于不能排除活動性肺結核可能,原則上不推薦采取隨訪觀察或糖皮質激素診斷性治療。
對于診斷困難且滿足以下條件中任意兩條者,建議采取診斷性抗結核治療:(1)IGRA陽性或TST陽性(硬結平均直徑≥10 mm);(2)組織切片抗酸染色和結核分枝桿菌培養陰性,而結核分枝桿菌PCR陽性者;(3)病理提示肉芽腫病變,但根據組織形態不足以確定和排除結核病者等;(4)結節病和結核病影像學診斷分級為“不確定”等。診斷性治療方案采用異煙肼、利福平、吡嗪酰胺和乙胺丁醇聯合治療,在強化期治療階段每月評估癥狀改善,完善痰或BALF結核分枝桿菌病原學檢查,分別在第1和2個月末進行CT檢查(推薦使用低劑量CT),并在第2個月末盡可能通過MDT做出診斷。如病變持續吸收好轉,支持肺結核診斷;如病情持續進展,在排除耐多藥肺結核及其他疾病后,主要考慮結節病診斷時,建議采取糖皮質激素或聯合免疫抑制劑進行治療觀察。
除非存在結節病與結核病共病的可靠證據,原則上不建議同時使用糖皮質激素聯合抗結核藥物進行診斷性治療。主要原因包括:(1)難以評價抗結核治療和激素治療與治療效果的關聯性,造成診斷困惑;(2)長期糖皮質激素治療導致免疫功能低下,增加機會性感染和造成結核播散;(3)雖然結節病在接受免疫抑制治療的過程中具有發生結核病的風險,但患者首診時兩病同時發病的情況較為罕見。
在實施診斷性抗結核治療前,需盡可能排除NTM肺病、真菌病、IgG4相關疾病、淋巴瘤、職業性肺病和惡性腫瘤等疾病。鑒于結核感染與結節病發病的關聯性并未明確,推薦對于采取診斷性治療的患者需開展全周期管理,加強隨訪和遠期效果評價,獲得新的診斷證據后通過MDT及時修正診斷。
推薦意見10:應對結節病患者中的結核發病高風險人群進行LTBI篩查,包括接受腫瘤壞死因子拮抗劑、長期接受糖皮質激素和(或)其他免疫抑制劑治療者,肺結核密切接觸者,HIV感染者,血液透析和器官移植的結節病患者。
腫瘤壞死因子拮抗劑已成為難治性結節病的推薦治療藥物。研究表明,腫瘤壞死因子拮抗劑會導致肉芽腫分解并促進分枝桿菌的繁殖和傳播。據文獻報道,接受腫瘤壞死因子拮抗劑治療的患者發生結核病的相對風險增加高達1.6~25.1倍,具有結核病發病風險的生物制劑主要為英夫利昔單抗和阿達木單抗而非依那西普[68]。2017年,對29項隨機臨床試驗進行的一項薈萃分析顯示,接受腫瘤壞死因子拮抗劑治療患者的結核病罹患率為0.57%[69]。因此,接受腫瘤壞死因子拮抗劑治療的結節病患者是LTBI篩查的重點人群。糖皮質激素也可增加結核病發病風險。英國一項肺結核回顧性病例對照研究顯示,每日使用<15 mg和≥ 15 mg潑尼松(或等效劑量激素)發生結核病風險的校正OR值分別為2.8和7.7,表明糖皮質激素治療劑量與結核病發病風險相關聯,糖皮質激素為增加結核病發病的獨立危險因素[70]。美國胸科協會推薦對接受糖皮質激素治療超過2周且潑尼松15 mg/d(或等效劑量)以上的LTBI者進行預防性治療[71]。
有研究對在結節病隨訪過程中發生結核病的27 例患者進行回顧性調查,發現結節病和結核病的發病間隔平均為(3.5±3)年,74%的患者接受了糖皮質激素或免疫抑制劑治療[72]。法國一項基于585例結節病患者發生嚴重感染的隊列研究表明,14例(2.4%)結節病患者在隨訪期內發生分枝桿菌感染,其中,結核分枝桿菌感染12例,NTM感染2例;另16例(2.7%)發生其他感染(以耶氏肺孢子菌肺炎和隱球菌病為主),進一步分析發現嚴重感染發生與接受≥3種免疫抑制劑治療有關[73]。我國迄今為止尚無結節病患者接受腫瘤壞死因子拮抗劑、糖皮質激素和免疫抑制劑治療過程中發生結核病風險的詳細數據報道。
2018年,WHO發布的Latenttuberculosisinfection:updatedandconsolidatedguidelinesforprogrammaticmanagement[74]提出,肺結核(尤其是涂陽肺結核)的密切接觸者,HIV感染者,接受生物制劑治療、器官移植或血液透析者作為結核發病高風險人群推薦進行LTBI篩查,并推薦對LTBI者進行預防性治療。結節病患者存在上述情況時,也應納入高風險人群管理。鑒于長期接受糖皮質激素和(或)其他免疫抑制劑治療的結節病患者具有結核病發病風險,推薦也將其列為高風險人群。在結核病流行背景下,加強對結節病患者中高風險人群的LTBI篩查與管理符合現代結核病防控策略的要求,對改善結節病患者預后具有潛在的益處。
無癥狀的0或Ⅰ期胸內結節病無需系統性糖皮質激素治療;無癥狀的Ⅱ或Ⅲ期肺結節病,若疾病穩定且僅有輕度肺功能異常,也不主張系統性激素的治療[7]。對于未接受糖皮質激素治療和(或)其他免疫抑制劑治療,且不具備結核感染高風險因素的結節病患者,由于缺乏結核病發病風險的隊列研究證據支持,暫不推薦常規進行LTBI篩查。對于鑒別工作發現的結節病合并IGRA陽性患者,在排除活動性結核病后,建議進行密切隨訪。
推薦意見11:建議對結節病高風險人群中的LTBI者采用異煙肼聯合利福噴丁(利福平)的方案進行預防性抗結核治療。
TST和IGRA為LTBI的主要篩查手段。需要注意的是,由于結節病患者可能存在T細胞無反應性,會出現TST或IGRA假陰性結果,容易導致LTBI漏診[75]。較TST而言,IGRA對結節病期間LTBI篩查可能具有良好的陽性預測價值[76-79],在臨床實踐中可以選擇應用,并積累經驗。對TST和IGRA檢測結果呈陰性的結節病高風險人群,應進行密切隨訪,定期開展痰涂片和影像學復查。
對結節病高風險人群中篩查出的LTBI者推薦預防性治療。由于部分結節病患者在臨床特征上與結核病具有相似性,需借助影像學、組織學和病原學等多重檢測手段排除活動性結核病后方可診斷LTBI。LTBI預防性治療方案包括:單用異煙肼、異煙肼聯合利福平(或利福噴丁)、單用利福平等方案[80-81]。目前,含利福霉素類藥物的治療方案是LTBI預防性抗結核治療的首選療法。研究表明,3個月療程的異煙肼和利福噴丁預防性治療在阻斷發病方面不劣于9個月異煙肼治療,且治療完成率較高,藥物相關肝毒性發生率相對較低[82-83]。考慮到我國的結核病高流行背景及異煙肼高耐藥率[84],建議結節病合并LTBI的高風險人群采用異煙肼和利福噴丁(利福平)聯合治療。建議先接受LTBI預防性治療至少1個月后方可開始或恢復免疫抑制劑或糖皮質激素治療。如條件允許,在完成預防性治療療程后再進行糖皮質激素和(或)免疫抑制劑治療[85]。預防性治療期間應加強患者的系統管理,確保規律服藥,切實達到降低結核病發病風險的目的。
指導委員會成員路希維 劉永煜 成詩明 廖偉華 李敬文
證據組專家成員胡紅玲 張培澤 李智勇 周暉 陳禹 王可 陶傳敏 汪振杰
主要執筆者路希維 曾誼 王凌偉 李智勇 周暉 方芳
共識專家組成員(按姓氏漢語拼音排序)
柴文戍(錦州醫科大學附屬第一醫院呼吸科);曹麗華(大連醫科大學附屬第二醫院呼吸科);曹文利(北京老年病醫院結核科);陳曉紅(福建省福州肺科醫院結核科);陳禹(沈陽市胸科醫院結核科);常建民(北京醫院皮膚科);初乃惠(首都醫科大學附屬北京胸科醫院結核科);車南穎(首都醫科大學附屬北京胸科醫院病理科);鄧國防(深圳市第三人民醫院結核科);丁衛民(首都醫科大學附屬北京胸科醫院內鏡診療中心);段慧萍(太原市第四人民醫院結核科);馮瑞娥(中國醫學科學院北京協和醫院病理科);方芳(北京醫院病理科);高莉(北京大學第一醫院放射科);胡紅玲(武漢市中心醫院呼吸科);金龍(黑龍江省傳染病防治院結核科);梁丹(中山大學中山眼科中心);賴曉宇(廣東省結核病控制中心結核病科);蘭學立(北京大學航天臨床醫學院教育處);李海潮(北京大學第一醫院大內科);李艷霞(大連醫科大學附屬第一醫院呼吸科);李智勇(大連醫科大學附屬第一醫院放射科);李靜(首都醫科大學附屬北京友誼醫院放射科);廖江榮(貴州航天醫院呼吸與危重癥醫學科);梁瑞霞(河南省胸科醫院結核科);林勇(南京市胸科醫院呼吸科);路明(北京大學第三醫院呼吸內科);羅志兵(同濟大學附屬東方醫院呼吸科);馬志明(廣州市胸科醫院呼吸科);逄宇(首都醫科大學附屬北京胸科醫院細菌免疫學研究室);沙巍(同濟大學附屬上海市肺科醫院結核科);施為(中南大學湘雅醫院皮膚科);石志紅(西安交通大學附屬第一醫院呼吸與危重癥醫學科);孫鵬(吉林省傳染病醫院介入科);陶傳敏(四川大學華西醫院實驗醫學科);王蓮芝(哈爾濱市胸科醫院結核科);王玉光(首都醫科大學附屬北京中醫醫院呼吸科);王璞(重慶醫科大學附屬第一醫院呼吸與危重癥醫學科);王凌偉(深圳市呼吸疾病研究所呼吸與危重癥醫學科);王可(廣西醫科大學附屬第一醫院呼吸與危重癥醫學科);伍健林(大連大學附屬中山醫院放射科);仵倩紅(陜西省結核病防治院結核科);吳桂輝(成都市公共衛生臨床醫療中心結核科);謝汝明(首都醫科大學附屬北京地壇醫院放射科);夏黎明(華中科技大學同濟醫學院附屬同濟醫院放射科);熊焰(北京大學第一醫院病理科);薛新穎(首都醫科大學附屬北京世紀壇醫院呼吸科);楊澄清(武漢市肺科醫院呼吸科);張培澤(深圳市第三人民醫院結核科);周紅梅(南方科技大學醫院呼吸科);曾誼(南京市第二醫院結核科);周新華(首都醫科大學附屬北京胸科醫院放射科);周暉(中南大學湘雅醫院放射科);朱曉萍(同濟大學附屬東方醫院呼吸科);趙亞濱(中國醫科大學附屬第一醫院呼吸科)
利益沖突所有作者聲明不存在利益沖突
志謝蘭州大學循證醫學學院陳耀龍教授對共識編制提供了指導與幫助,北京大學第一醫院眼科楊柳教授提供了有價值的病例圖片資料,在此一并致以由衷的感謝!

