雷公藤紅素遺傳毒性研究
黃 鶴, 張 莉, 涂如霞, 吳思瀾, 李恒華
(重慶市中藥研究院,重慶市藥物安全評價中心,重慶 400065)
雷公藤紅素,又名南蛇藤素,是一種醌甲基三萜,主要存在于衛(wèi)矛科雷公藤屬及南蛇藤屬植物中,是一個具有多種生物活性的天然產(chǎn)物[1-2]。雷公藤紅素具有顯著的抗炎、免疫抑制、抗腫瘤、抑制血管生成、誘導細胞凋亡、神經(jīng)保護等作用[3-8],具有較大的研究和開發(fā)價值。但雷公藤紅素的毒性也不容忽視,有研究表明其對斑馬魚胚胎具有心臟毒性[9],對膽管細胞具有毒性[10],對造血系統(tǒng)也有一定的損傷[11],其毒性機制不甚清楚,尚未見相關文獻報道雷公藤紅素是否具有致基因突變和染色體畸變的遺傳毒性。因此,本研究根據(jù)藥物遺傳毒性研究技術指導原則規(guī)定,通過鼠傷寒沙門氏菌回復突變試驗(Ames試驗)、體外培養(yǎng)中國倉鼠肺(CHL)細胞染色體畸變實驗和小鼠骨髓嗜多染紅細胞微核實驗進行檢測,為雷公藤紅素研究開發(fā)提供理論依據(jù)。
1 材料
1.1 菌株 組氨酸缺陷型鼠傷寒沙門菌TA97a、TA98、TA100、TA102、TA1535,購自美國Moltox公司,實驗前進行菌株鑒定,均符合規(guī)定標準。
1.2 細胞 中國倉鼠肺(CHL)細胞,購自中國科學院上海生命科學研究院,實驗前檢測無支原體污染。
1.3 動物 選用性成熟雄性昆明小鼠60只,7~8周齡,SPF級,體質(zhì)量30~40 g,由重慶市中藥研究院實驗動物研究所提供,實驗動物生產(chǎn)許可證號SCXK(渝)2017-0003。實驗在本單位藥物安全性評價中心屏障環(huán)境動物實驗設施進行,并經(jīng)本單位實驗動物福利倫理委員會審核批準。
1.4 試劑與藥物 雷公藤紅素(北京融誠鑫德科技發(fā)展有限公司,批號L-003-170611)。環(huán)磷酰胺、ICR191、2-硝基芴(美國Sigma公司,批號WXBC7023V、SLBV4070、S43858V);絲裂霉素(美國Apexbio公司,批號A4452);疊氮鈉(成都麥卡希化工有限公司,批號150309002);2-氨基芴、D-生物素、L-組氨酸鹽酸鹽一水物(上海阿拉丁生化科技股份有限公司,批號J1311022、D1524076、H1518057);1,8-二羥基蒽醌[西格瑪奧德里奇(上海)貿(mào)易有限公司,批號WXBB0392V];二甲基亞砜(DMSO)、秋水仙堿(北京鼎國昌盛生物技術有限責任公司,批號93D00104、77010150);α-MEM(美國HyClone公司,批號SH30 265.01);0.25%Trypsln-EDTA、青霉素鏈霉素混合液(美國Genview公司,批號811120101100、811200101100);0.4%臺盼蘭染液、NADP-Na2(北京索萊寶科技有限公司,批號20181127、410F024);胎牛血清[賽爾博克斯生物制品(香港)貿(mào)易發(fā)展有限公司,批號P252018];肝微粒體酶(S9)(美國Moltox公司,批號3533);底層培養(yǎng)基、頂層培養(yǎng)基、營養(yǎng)肉湯、營養(yǎng)瓊脂(青島日水生物技術有限公司,批號20180816、20180816、20180426、20180724);葡萄糖-6-磷酸二鈉(山東西亞化學股份有限公司,批號F09443)。體外細菌試驗中雷公藤紅素用DMSO配制,陽性藥用DMSO或滅菌水配制或稀釋,溶劑對照為同體積DMSO;細胞實驗中雷公藤紅素用DMSO溶解,再加細胞培養(yǎng)液稀釋,陽性藥均用滅菌水配制,溶劑對照為含等濃度DMSO的細胞培養(yǎng)液;小鼠實驗中雷公藤紅素用0.5%羧甲基纖維素鈉(CMC-Na)溶液配制,陽性藥用0.9%氯化鈉溶液配制,溶劑對照為等體積0.5%CMC-Na溶液。
1.5 儀器 1384A2生物安全柜、IGS180生化培養(yǎng)箱、4111CO2培養(yǎng)箱、ST16R高速冷凍離心機(美國Thermo Fisher Scientific公司);Scan 300菌落計數(shù)儀(法國Interscience公司);GR85DA立式高溫高壓滅菌器[致微(廈門)儀器有限公司];HWS-26電熱恒溫水浴鍋(上海一恒科學儀器有限公司);細胞用超純水機(重慶市安特生環(huán)保設備有限公司);SW-CJ-2FD雙人單面垂直凈化工作臺(蘇州安泰空氣技術有限公司);IX71倒置熒光顯微鏡、CX31光學顯微鏡(日本Olympus公司)。
2 方法
按照2018年《藥物遺傳毒性研究技術指導原則》設計要求,分別應用鼠傷寒沙門氏菌回復突變試驗、體外培養(yǎng)CHL細胞染色體畸變實驗和小鼠骨髓微核實驗檢測雷公藤紅素的遺傳毒性[12]。
2.1 Ames試驗 選用5株鼠傷寒沙門氏菌突變型菌株(TA97a、TA98、TA100、 TAl02和TAl535),試驗前對菌株進行遺傳特性鑒定,均符合要求。根據(jù)前期劑量篩選實驗結果,本試驗選擇雷公藤紅素的劑量為2 000、400、80、16、3.2 μg/mL,另設陰性對照組、溶媒對照組(DMSO)和陽性對照組。陽性對照組不加S9時,TA97a加入1 μg/皿的ICR191,TA98加入5 μg/皿的2-硝基芴,TA100和TA1535加入1.5 μg/皿的疊氮鈉,TA102加入0.5 μg/皿的絲裂霉素;加S9時,TA97a、TA98、TA100加入10 μg/皿的2-氨基芴,TA102加入50 μg/皿的1,8-二羥基蒽醌,TA1535加入200 μg/皿的環(huán)磷酰胺,每皿給藥體積為0.1 mL,設3個平行皿,37 ℃培養(yǎng)48 h,計數(shù)每皿的回復突變菌落數(shù)。至少在一個菌株上,在有或無代謝活化系的情況下,供試品多誘發(fā)的回復突變菌落數(shù)出現(xiàn)質(zhì)量劑量依賴性的增加和/或在一個或多個質(zhì)量濃度組上出現(xiàn)可重復性的增加(回復突變菌落數(shù)均數(shù)比相應菌株的陰性對照菌落均數(shù)增加1倍以上),可判定為陽性結果。
2.2 染色體畸變實驗 根據(jù)細胞毒性預實驗結果,本實驗在無或有S9代謝活化系統(tǒng),暴露4 h條件下,雷公藤紅素劑量為300、150、75、37.5 μg/mL;在無S9代謝活化系統(tǒng),暴露24 h條件下,雷公藤紅素劑量為180、90、45、22.5 μg/mL;同時另設陰性對照組(α-MEM培養(yǎng)液)、溶媒對照組(DMSO 10 μL/mL,以α-MEM培養(yǎng)液為溶媒)和陽性對照組(加S9時為1.25 mg/mL環(huán)磷酰胺,不加S9時為12.5 μg/mL絲裂霉素),給藥體積均為0.1 mL,設2個平行培養(yǎng)瓶,在37 ℃、5% CO2培養(yǎng)箱中培養(yǎng)至24 h,終止培養(yǎng)前2 h,加入50 μg/mL秋水仙堿0.1 mL,使染色體停滯在分裂中期,培養(yǎng)結束后收集細胞,臺盼藍染色并計數(shù)細胞,并計算各劑量組相對群體倍增數(shù)(RPD),以反應細胞毒性情況。群體倍增數(shù)(PD)=[log(處理后的細胞數(shù)/處理前的細胞數(shù))]/log2;RPD=(處理組的倍增數(shù)/對照組的倍增數(shù))×100%;細胞抑制率=100%-RPD。剩余細胞懸液離心后棄上清液,保留細胞沉淀物,經(jīng)低滲、固定、制片、Giemsa染色,油鏡觀察300個中期分裂相細胞,分別記錄各組含有結構畸變?nèi)旧w的細胞數(shù)和畸變類型,計算染色體畸變率。受試物所誘發(fā)的染色體畸變率呈劑量依賴性增加,或出現(xiàn)可重復性增加,可判定為陽性結果。
2.3 小鼠骨髓微核實驗 用7~8周齡健康KM雄性小鼠60只,按體質(zhì)量隨機分為6組,每組10只,分別為溶媒對照組(0.5% CMC-Na),環(huán)磷酰胺組(40 mg/kg),雷公藤紅素100、50、25、12.4 mg/kg組。雷公藤紅素各劑量組及溶媒對照組每天灌胃給藥1次,容量為0.2 mL/10 g,連續(xù)3 d;環(huán)磷酰胺組于第3天腹腔注射給藥1次,給藥體積為0.1 mL/10 g。末次給藥后約24 h,進行股骨骨髓采樣并制作涂片,甲醇固定,姬姆薩染色,油鏡下觀察。每只小鼠計數(shù)4 000個多染紅細胞,并計算微核率;同時計數(shù)500個骨髓紅細胞[多染紅細胞(PCE)加正染紅細胞(NCE)],求出多染紅細胞/總紅細胞的比值,即PCE/(PCE+NCE)。受試物所誘發(fā)的微核率呈劑量依賴性升高,或某一劑量組在某一測試點呈現(xiàn)可重復性升高,可判定為陽性結果。
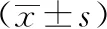
3 結果
3.1 Ames試驗 各培養(yǎng)皿上背景菌苔生長良好,2次試驗中各菌株自發(fā)回復突變菌落數(shù)(陰性對照組)均在正常范圍內(nèi),陽性對照組回復突變菌落數(shù)均高于陰性對照組2倍以上(P<0.05,P<0.01),提示本試驗體系可靠。在加或不加S9代謝活化系統(tǒng)條件下,雷公藤紅素1 000 μg/皿劑量作用于各菌株均有紅色沉淀產(chǎn)生,影響結果觀察,不計入統(tǒng)計;雷公藤紅素在個別劑量下表現(xiàn)出一定的細菌毒性(回復突變菌落數(shù)降低)(P<0.05,P<0.01)。在有或無代謝活化系統(tǒng)的情況下,雷公藤紅素各劑量組回復突變菌落數(shù)均未見有可重復劑量相關性升高,個別劑量作用下某些菌株回復突變菌落數(shù)有一定增加,但未超過陰性對照組回復突變菌落數(shù)的2倍,且在以往Ames試驗對照范圍內(nèi),未見劑量相關性升高,故無毒理學意義。因此,0.32~200 μg/皿的雷公藤紅素均未引起所有測試菌株基因突變,Ames試驗結果為陰性。具體結果見表1~3。

表1 雷公藤紅素對鼠傷寒沙門氏菌突變型菌株回復突變菌落數(shù)的影響(平行試驗一)(個/皿,

表2 雷公藤紅素對鼠傷寒沙門氏菌突變型菌株回復突變菌落數(shù)的影響(平行試驗二)(個/皿,

表3 陽性對照藥物及劑量
3.2 體外培養(yǎng)CHL細胞染色體畸變實驗 高劑量雷公藤紅素表現(xiàn)出明顯的細胞毒性,見表4。在有或無S9代謝活化系統(tǒng)暴露4 h和無S9代謝活化系統(tǒng)暴露24 h,與陰性對照組比較,陽性對照組染色體畸變率均升高(P<0.01),表明試驗系統(tǒng)可靠;溶媒對照組、雷公藤紅素各劑量組染色體結構畸變率無明顯變化(P>0.05),雷公藤紅素個別劑量有統(tǒng)計學差異(P<0.05,P<0.01),但未見重復性劑量依賴性升高,故無毒理學意義。結果表明,雷公藤紅素未引起CHL細胞染色體結構畸變率升高,染色體畸變試驗結果為陰性,見表5。
3.3 小鼠骨髓微核實驗 環(huán)磷酰胺組小鼠骨髓微核率高于溶媒對照組(P<0.01),顯示本實驗體系可靠。實驗期間,小鼠出現(xiàn)腹瀉癥狀,雷公藤紅素劑量越高,腹瀉動物數(shù)越多,同時隨給藥時間的延長,腹瀉小鼠數(shù)也增多。雷公藤紅素劑量為100、50、25 mg/kg時,腹瀉次數(shù)分別為20、21、6次。與溶媒對照組比較,雷公藤紅素100、50、25、12.4 mg/kg組小鼠體質(zhì)量均降低(P<0.05,P<0.01),劑量越高,給藥時間越長,體質(zhì)量降低幅度越大,這與雷公藤紅素引起的動物腹瀉情況一致;雷公藤紅素100、50、25 mg/kg組小鼠PCE/(PCE+NCE)值降低(P<0.01),提示雷公藤紅素對骨髓有抑制作用;雷公藤紅素各劑量組小鼠骨髓微核率無明顯變化(P>0.05)。結果表明,各劑量雷公藤紅素均未引起骨髓細胞染色體完整性損害或?qū)е氯旧w分離異常,微核實驗結果為陰性,見表6~8。
4 討論
近年來,雷公藤紅素的抗腫瘤作用使其成為研究熱點之一。目前抗腫瘤藥物大都具有明顯的細胞毒性,并且很多都具有潛在的遺傳毒性,可引起人體體細胞和生殖細胞不可逆轉(zhuǎn)的遺傳損傷[13-14]。雷公藤紅素是否具有遺傳毒性,目前尚未見研究報道,而遺傳毒性研究是藥物非臨床安全性評價的重要內(nèi)容,它與其他毒理學研究尤其是致癌性研究、生殖毒性研究有著密切的聯(lián)系,是藥物進入臨床試驗及上市的重要環(huán)節(jié)[15-18],因此,本研究采用目前公認檢測受試物致突變的幾種檢測方法,分別從體外到體內(nèi),在微生物、離體細胞和整體動物水平上系統(tǒng)評價雷公藤紅素的遺傳毒性。

表4 各劑量雷公藤紅素的細胞毒性

表5 雷公藤紅素對CHL細胞染色體畸變的影響

表6 雷公藤紅素對小鼠體質(zhì)量的影響

表7 雷公藤紅素對小鼠體質(zhì)量增長的影響

表8 雷公藤紅素對小鼠骨髓微核的影響
Ames試驗是經(jīng)典的檢測基因突變的方法之一,主要通過檢測組氨酸靶基因中的堿基置換或移碼突變來評價受試物的致突變性,從基因水平反映了遺傳物質(zhì)受損傷狀況[19]。本研究結果顯示,在加或不加S9的條件下,3.2~200 μg/皿雷公藤紅素均未引起細菌回復突變數(shù)有意義的增加,試驗結果為陰性,提示雷公藤紅素對鼠傷寒沙門氏菌無致突變性。染色體畸變實驗通過制備細胞中期分裂相染色體標本,在光鏡下直接觀察染色體數(shù)目和形態(tài)的變化,以檢測細胞染色體的損傷情況[20-21]。本研究表明,22.5~180 μg/mL(接觸24 h,不加S9)以及37.5~300 μg/mL(接觸4 h,加或不加S9)的雷公藤紅素均未引起CHL細胞染色體畸變率有意義的升高,實驗結果為陰性,提示雷公藤紅素對哺乳動物培養(yǎng)細胞染色體無致畸變作用。小鼠微核實驗是用于快速檢測化學毒物損傷細胞染色體和干擾細胞有絲分裂的方法,微核的產(chǎn)生與染色體斷裂及紡錘體受損有關,微核率大小可間接反映染色體受損情況,能檢測受試物導致染色體完整性的改變和分離,改變兩種遺傳終點[21-22]。本研究發(fā)現(xiàn),灌胃給予100、50、25、12.4 mg/kg雷公藤紅素均未引起骨髓嗜多染紅細胞微核率有意義的增高,實驗結果為陰性,提示雷公藤紅素無致小鼠股骨骨髓嗜多染紅細胞微核形成作用,不會影響細胞染色體完整性及有絲分裂進程。
綜上所述,本研究采用Ames試驗、染色體畸變實驗和體內(nèi)微核實驗這3個經(jīng)典實驗組合進行雷公藤紅素的遺傳毒性評價,結果提示,其不具有潛在的致基因突變和染色體畸變的遺傳毒性,與很多抗腫瘤藥物相比,顯示出一定的優(yōu)勢,具有極大的開發(fā)潛力。本研究為雷公藤紅素進一步開發(fā)利用提供了毒理學依據(jù),但雷公藤紅素作用靶點尚未完全闡明,其相關毒性以及具體機制有待更進一步深入研究。

