具有特殊免疫表型的乳腺腺肌上皮瘤
徐夢微,韓 銘,郭雙平,2
1 臨床資料
本例讀片資料由空軍軍醫大學西京醫院病理科提供,通訊讀片編號A-9。
患者女性,28歲,體檢發現右側乳腺包塊20余天。乳腺超聲:右側乳腺2點鐘方向距離乳頭3 cm處腺體層內可見一大小1.3 cm×0.7 cm×0.9 cm的混合回聲區,邊界尚清,形態尚可,內實性部分形狀不規則,方向平行于皮膚,距離皮層3 mm(圖1)。雙側腋窩未見形態異常淋巴結回聲。超聲提示:右側乳腺混合性結節,BI-RADS 4A類(低度可疑,惡性風險2%~10%,建議活檢)。雙側腋窩未見形態異常淋巴結。乳腺鉬靶:兩側乳腺呈不均勻致密型(C類),部分腺體呈片狀密度增高影,左側乳腺內下象限小點狀鈣化影。
眼觀:右側乳腺包塊穿刺活檢標本,灰白色條索樣組織3條,大小1 cm×0.3 cm×0.1 cm。右側腋窩淋巴結穿刺活檢標本:灰白色條索樣組織3條,大小0.2 cm×0.2 cm×0.1 cm。右側乳腺包塊切除標本:灰白、灰黃色不整形組織,大小4 cm×3 cm×1.5 cm,切面見一囊腔,囊內見一乳頭狀腫物,大小0.9 cm×0.8 cm×0.6 cm。
腫瘤細胞圍繞纖維血管軸心呈乳頭狀排列,細胞大小相對較一致,胞膜界限清,胞質豐富嗜酸性或透亮,細胞核多形性、成角,部分細胞胞質內可見黏液,核仁明顯(圖2)。術中冷凍標本低倍鏡下見腫瘤呈囊實性分布,與周圍組織界限欠清,無明顯包膜,實性區腫瘤細胞呈多結節狀或分葉狀排列,瘤細胞胞質豐富,嗜酸性或透亮,以透亮細胞為主(圖3),其間散在少許腺管樣結構,腺上皮為單層立方或柱狀,囊性區為擴張的導管,外周包裹厚的纖維性被膜,管腔內見腫瘤細胞呈乳頭狀或小葉狀增生,增生的細胞圍繞大小不一和被擠壓的小管生長,病變周邊可見小灶典型的上皮-肌上皮雙相性結構,肌上皮增生,細胞胞質豐富,嗜酸性或透亮,細胞核多形性,形態較溫和,核分裂象未見(圖4)。
免疫表型:腺上皮E-cadherin和p120細胞膜陽性,CK7和CK5/6(圖5)彌漫一致陽性,ER、PR、SOX10、GATA-3均陰性,HER-2(0,陰性)。肌上皮CK5/6(圖5)、p63(圖6)和p40彌漫一致陽性,SMA、S-100、SOX10均陰性,導管肌上皮細胞Calponin陽性(圖7),Ki-67增殖指數局部約5%。
特殊染色:PAS陽性,D-PAS陰性,提示腫瘤細胞胞質內富含糖原。FISH檢測:未發現MAML2基因斷裂(圖8)。臨床轉歸:隨訪時間6個月,患者預后較好,無復發。
2 結果
2.1 出片單位診斷乳腺腺肌上皮瘤(adenomyepithelioma, AME)。
2.2 診斷依據(1)瘤細胞呈多結節狀、巢團狀、片狀或乳頭狀排列,部分瘤細胞在擴張的導管內生長,瘤巢內可見小管結構。(2)瘤細胞大小相對較一致,胞膜界限較清,胞質豐富嗜酸性或透亮,細胞核多形性、成角,部分細胞胞質內可見黏液,核仁明顯,未見核分裂象。(3)瘤周可見乳腺導管及小葉結構,邊界較清。(4)腫瘤缺乏間質成分,僅有纖細的纖維結締組織或纖維血管分割。(5)同時具有腺上皮和肌上皮雙相性分化的特征。該腫瘤具有腺肌上皮瘤的組織學形態和免疫表型。
3 討論
WHO(2019)乳腺腫瘤分類中將AME明確定義為由明顯的、呈實性增生的肌上皮細胞組成的病變,增生的肌上皮細胞形態不一。AME患者多為中老年女性,發病年齡較廣,平均58歲[1-2]。臨床表現多無癥狀,常為查體發現或偶爾觸及無痛性腫塊,偶爾會出現疼痛或乳頭溢液[3-4]。AME在年輕患者中并不常見,本例患者為28歲年輕女性。目前,已有男性AME患者的文獻報道[5-6]。
AME影像學往往表現為分葉的輪廓,局部可發生囊性變,大多數位于乳房中央。鉬靶檢查AME通常呈圓形或分葉狀的致密腫塊,有或無鈣化緣。超聲表現為單側乳腺單發、實性的、界限清楚的圓形結節,最大徑0.3~7 cm[7]。
AME的組織學特點是腺腔內襯立方形或低柱狀上皮細胞,構成管狀或乳頭狀結構,有時被推擠到腺腔的邊緣,腔內常有分泌物。肌上皮細胞通常為梭形、多角形或漿細胞樣,胞質豐富,嗜酸性或透亮。肌上皮細胞增生呈巢狀、乳頭狀、小葉狀、腺管狀、小囊狀結構,細胞無異型性,核分裂象一般<2個/10 HPF。根據AME鏡下結構不同,AME可分為三種組織學亞型:小葉型、腺管型和梭形細胞型。本例組織學歸屬于小葉型AME。AME常伴皮脂腺化生、大汗腺化生及鱗狀上皮化生,但常常為局灶性表現。
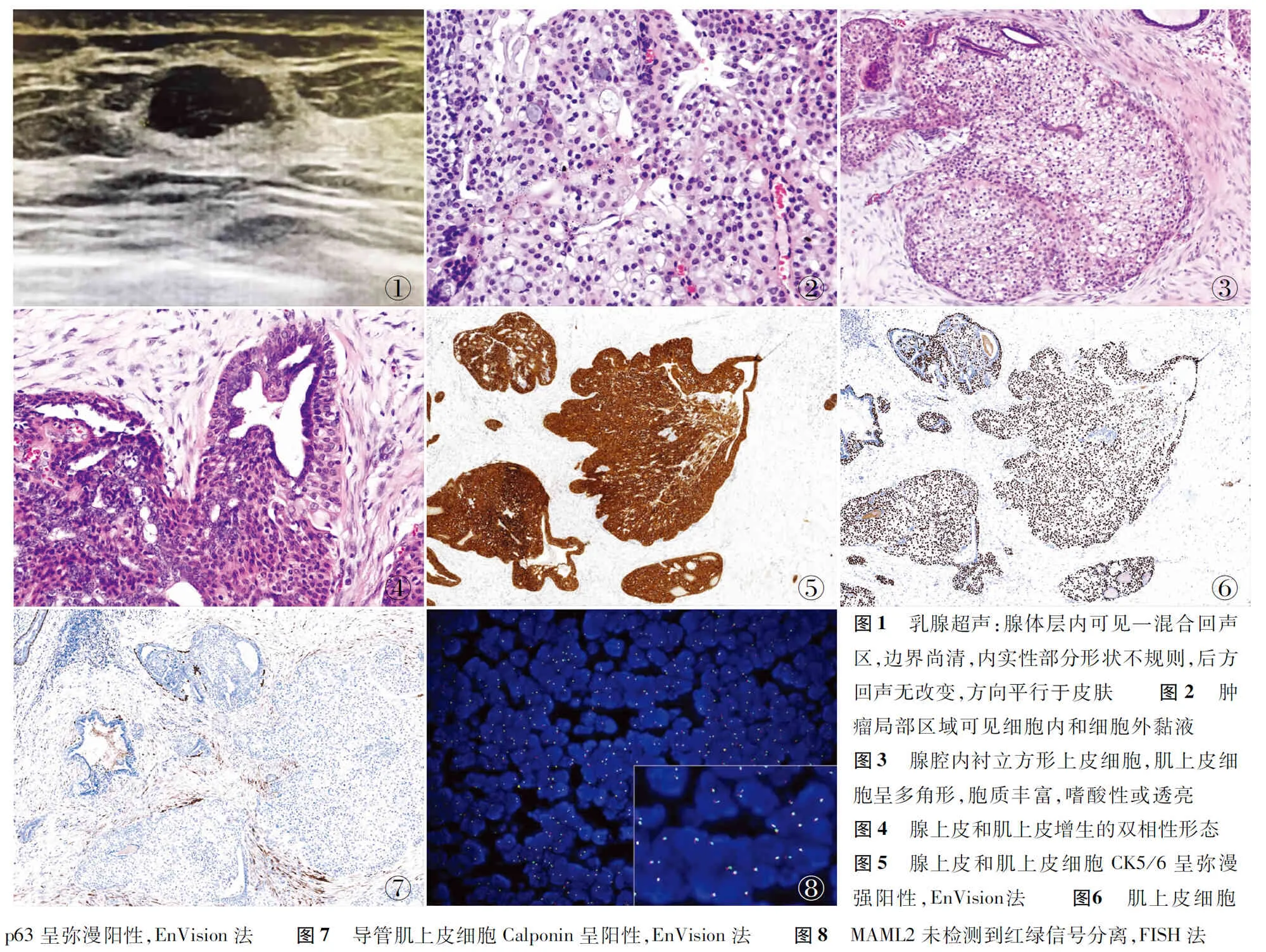
①②③④⑤⑥⑦⑧圖1 乳腺超聲:腺體層內可見一混合回聲區,邊界尚清,內實性部分形狀不規則,后方回聲無改變,方向平行于皮膚 圖2 腫瘤局部區域可見細胞內和細胞外黏液 圖3 腺腔內襯立方形上皮細胞,肌上皮細胞呈多角形,胞質豐富,嗜酸性或透亮 圖4 腺上皮和肌上皮增生的雙相性形態圖5 腺上皮和肌上皮細胞CK5/6呈彌漫強陽性,EnVision法 圖6 肌上皮細胞
AME的腺上皮細胞表達上皮性標志物EMA、CK7;肌上皮細胞表達SMA、Calponin、S-100、p63等,但表達可出現差異性;CK5/6除肌上皮表達外,部分腺上皮也可表達;腺上皮可表達ER和PR,肌上皮不表達或局灶弱表達ER和PR。本例彌漫表達CK5/6、p63、p40,但SMA、Calponin不表達,與典型的AME免疫表型有差異。然而,AME可有不同的肌上皮細胞免疫組化標記的表達模式,甚至出現無法預測的表達模式,腺上皮細胞CK5/6可彌漫一致性表達,如本例表達CK5/6;這也是造成AME診斷困難的原因之一。
AME中ER不同表達模式的腺肌上皮瘤,具有不同的分子遺傳學特征。ER+AME檢測到PIK3CA或AKT1激活突變;ER-AME檢測到HRAS(Q61R或Q61K)熱點突變(約占26%),PIK3CA或PIK3R1突變[8]。
絕大多數經典型AME預后良好,導管內生長或多結節狀生長的AME可復發,偶見無惡性形態學或Ki-67高增殖指數的AME發生遠處轉移的報道[9]。
AME的診斷較為困難,需與以下腫瘤或病變進行鑒別。(1)導管內乳頭狀瘤:是起源于中央或外周導管的良性病變,由腺上皮及肌上皮圍繞纖維血管軸心呈乳頭狀排列。當AME以乳頭狀結構為主時,較難與伴肌上皮增生的導管內乳頭狀瘤鑒別。AME具有比導管內乳頭狀瘤更明顯的肌上皮層,病變內腺體和小管周圍的肌上皮細胞即使未行免疫組化輔助檢查,也比較容易識別,且肌上皮細胞通常由細胞質透亮的立方形到多邊形細胞或明顯的梭形細胞組成。相比之下,導管內乳頭狀瘤的肌上皮細胞可以不明顯,也可以局灶增生,但在病變周圍常可見經典的乳頭狀瘤結構。(2)透明細胞汗腺瘤:有文獻報道乳腺透明細胞汗腺瘤可在乳頭、乳暈下區域或乳腺深部組織中發現。本例超聲提示腫瘤距離皮層較近(約3 mm),需與其進行鑒別。透明細胞汗腺瘤可伴皮膚破潰,組織學表現為一致的嗜酸性細胞或糖原豐富的透亮細胞形成小葉結構,導管擴張形成囊性區域;間質纖維化,廣泛的透明變性,可見鱗狀分化及黏液細胞化生。免疫組化標記CK5/6、p63、GATA-3均陽性,SOX10胞質透亮多角形細胞陰性,而腺上皮細胞陽性。約50%病例可檢測到t(11; 19)易位,導致CRTCI-MAML2基因融合[10]。本例在實性結節或擴張的管腔內均可見腺樣或小管狀結構,周圍圍繞透亮或嗜酸性的肌上皮細胞,形成典型的上皮-肌上皮雙相分化結構,且GATA-3、SOX10呈陰性,在透明細胞汗腺瘤中腺上皮細胞中SOX10陽性、透明細胞中SOX10陰性;而本例腫瘤的兩種細胞SOX10均陰性[10]。另FISH未檢測到MAML2基因斷裂,可以將其與乳腺透明細胞汗腺瘤進行鑒別。(3)黏液表皮樣癌:本例少數腫瘤細胞胞質內含有黏液,易與黏液表皮樣癌引起混淆。其腫瘤細胞可呈乳頭狀囊性的生長方式,也可有CK5/6、p63陽性的透明細胞,本例具有上皮-肌上皮兩種細胞形態,FISH檢測MAML2基因未見斷裂有助于鑒別。(4)鱗狀細胞癌:通常表現為囊性病變,囊腔襯覆具有不同程度核異型和多形性的鱗狀細胞。腫瘤細胞呈片狀、條索狀和巢狀浸潤至周圍間質,并引起明顯的間質反應,炎細胞浸潤通常較顯著。(5)富于糖原的透明細胞浸潤性癌:腫瘤通常邊界既可以清晰,也可以呈浸潤性,具有實性、粉刺樣或乳頭狀形態,由一致性的邊界清晰、多角形細胞組成。透明或細顆粒狀胞質含有PAS陽性糖原,并易被淀粉酶消化,核染色質豐富、團塊狀,核仁顯著[11]。本例病變形成雙相分化模式,免疫組化顯示透亮細胞肌上皮標志物(p63、CK5/6)陽性,可資鑒別。(6)多形性腺瘤:組織學與涎腺的多形性腺瘤相似,非常罕見,常發生在乳暈下,而不是乳腺周圍,多數呈實性,邊界清楚,由不同比例的上皮、肌上皮構成,可見腺管結構,與AME的主要鑒別點為前者腫瘤間質可見多少不等的黏液樣、軟骨樣或玻璃樣變物,常可見上皮與間質的過渡[12]。
總之,AME是一種罕見的乳腺良性腫瘤,具有復發、轉移和惡變的可能性。其診斷要點:(1)由肌上皮細胞圍繞腺上皮的小腔隙而形成的雙相性腫瘤;(2)常有不同程度肌上皮細胞增生;(3)肌上皮細胞可為梭形、上皮樣及富含糖原的透明細胞;腺上皮細胞立方或低柱狀,胞質嗜酸性,位于腺腔內側,形成管狀或乳頭狀結構;(4)細胞無異型性,核分裂象罕見(≤2個/10 HPF);間質可硬化或梗死。因AME與其他多種乳腺良性和惡性病變形態學相似,組織結構、細胞組成和間質變化異質性顯著造成診斷困難,且本例與透明細胞汗腺瘤、導管內乳頭狀瘤伴肌上皮增生等鑒別也存在一定難度。詳盡的組織學檢查、免疫組化和分子檢測有助于AME的正確診斷,避免誤診。

