非布司他聯合秋水仙堿對急性痛風性關節炎患者的臨床觀察
徐牡丹
福建省立金山醫院,福建省福州市 350000
急性痛風性關節炎(Acute gouty arthritis,AGA)是由高尿酸血癥引起的一種急性關節炎,其屬于晶體相關性關節炎。痛風是由長期的嘌呤代謝紊亂和血清尿酸(SUA)升高引起,而嘌呤代謝的最終產物是尿酸[1]。若患者無臨床癥狀,且血尿酸濃度高于正常水平,則在醫學上稱之為“高尿酸血癥”。當血液尿酸濃度達到一定的飽和溶解度時,該物質最后會形成晶體并在軟組織中積累,最終會引發體內的炎癥反應[2]。痛風可以由飲食、天氣變化引起,如溫度和氣壓變化,以及創傷引起。臨床表現為第一跖趾關節出現紅、腫、熱、痛以及功能性障礙。若不及時治療,會給患者的身心健康帶來嚴重影響,嚴重者甚至會導致關節變形[3]。基于研究各種藥物對治療痛風性關節炎的了解,臨床醫生在選擇尋找一種更有效、理想的方式治療,同時要減少治療后機體的不良反應。因此,本文通過非布司他聯合秋水仙堿對AGA患者的臨床療效及對氧化應激的影響進行探究,報道如下。
1 資料與方法
1.1 一般資料 選取 2021年1月—2022年1月到我院診治的AGA患者94例,按隨機數字表法分成對照組(47例)和聯合組(47例)。對照組中男32例,女15例,年齡40~69歲,平均年齡(48.79±5.92)歲,病程1~8年,平均病程(3.72±0.68)年;聯合組中男31例,女16例,年齡41~68歲,平均年齡(48.82±6.01)歲,病程1.5~7年,平均病程(3.69±0.66)年。兩組患者一般資料對比,差異均無統計學意義(P>0.05),有可比性。本研究通過我院倫理委員會批準且患者均知曉同意并簽署知情同意書。納入標準:(1)均符合《痛風性關節炎診斷標準》且符合有關臨床癥狀;(2)均未采用降尿酸治療;(3)無嚴重臟器損傷者;(4)無其他合并風濕性疾病。排除標準:(1)對本研究藥物過敏者;(2)患有免疫、血液、中樞神經系統疾病者;(3)惡性腫瘤者;(4)患者有放化療藥物等因素引起的AGA;(5)在治療過程中服用影響SUA代謝的藥物。
1.2 方法 對照組給予非布司他(江蘇恒瑞醫藥股份有限公司)口服,劑量為40mg/d,3次/d,治療24周。聯合組在對照組的基礎上口服秋水仙堿(廣東彼迪藥業有限公司)每2h服用0.5mg,24h內不超過6mg,停服72h后每日服用量為0.5~1.5mg,分次服用,連續用藥7d。
1.3 觀察指標 (1)對比兩組在治療前及治療后 4、8、12、16周SUA的水平;(2)對比兩組治療前后3-硝基絡氨酸修飾蛋白(3-NT)與血清8-羥基脫氧鳥苷(8-OHdG)的氧化應激標志物水平;(3)對比兩組治療前后的血脂指標,包括血清甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)水平、總膽固醇(TC);(4)對比兩組治療前后血清腫瘤壞死因子 α (TNF-α)、轉化生長因子β(TGF-β)及γ-干擾素(IFN-γ)水平;(5)對比兩組臨床療效,評價標準:顯效:患者紅、腫、痛等臨床癥狀改善較為明顯;有效:患者臨床癥狀有所改善;無效:患者臨床癥狀無改善情況甚至加重。
1.4 檢測方法 分別抽取患者治療前后晨起空腹狀態下的肘靜脈血5ml分成2份,室溫靜置10min,后用離心機分離出血清,于低溫冰箱保存待測,一份送檢進行SUA水平檢測,一份采用由上海酶聯生物科技有限公司提供的試劑盒,用酶聯免疫吸附法進行3-NT、8-OHdG、TNF-α、TGF-β及 IFN-γ水平檢測,步驟均按試劑盒說明書進行嚴格操作。
2 結果
2.1 兩組治療前后不同時段SUA水平對比 治療前兩組SUA水平對比無統計學差異(P>0.05);治療后,兩組各時間段SUA水平均有所降低,且聯合組各時間段SUA水平比對照組低(P<0.05),見表1。
表1 兩組治療前后不同時段血清SUA水平對比
2.2 兩組治療前后血清8-OHdG與3-NT的水平對比 治療前,兩組8-OHdG與3-NT水平對比無統計學差異(P>0.05);治療后,兩組8-OHdG與3-NT水平均有所降低,且聯合組8-OHdG與3-NT水平比對照組低(P<0.01),見表2。

表2 兩組治療前后血清8-OHdG與3-NT水平對比
2.3 兩組治療前后的血脂指標對比 治療前,兩組血脂指標對比無統計學差異(P>0.05);治療后,兩組TG、LDL、TC水平均有所降低,HDL水平有所升高,且聯合組血清 TG 水平低于對照組,HDL水平高于對照組(P<0.05),而兩組TC與LDL水平比較無統計學差異(P>0.05),見表3。
表3 兩組治療前后的血脂指標對比
2.4 兩組血漿TNF-α、TGF-β及 IFN-γ水平對比 治療前,兩組TNF-α、TGF-β及 IFN-γ水平對比無統計學差異(P>0.05);治療后,兩組的TGF-β、IFN-γ、TNF-α水平均有所降低,且聯合組的TGF-β、IFN-γ、TNF-α水平均比對照組低(P<0.05),見表4。

表4 兩組血漿TNF-α、TGF-β及 IFN-γ水平對比
2.5 兩組療效比較 聯合組的總有效率為95.74%,明顯高于對照組的78.72%,差異有統計學意義(χ2=6.114,P=0.013<0.05),見表5。
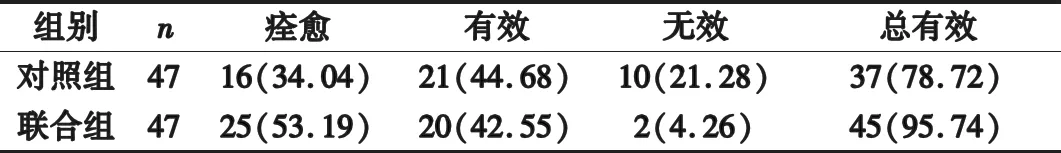
表5 兩組療效比較[n(%)]
3 討論
隨著社會發展和生活水平提高,人類平均壽命延長,但不良的飲食習慣、生活習慣,導致AGA患病率不斷增加且趨于年輕化,男性多于女性,超過50%的痛風患者超重或肥胖[4]。AGA由體內嘌呤代謝紊亂而引發的晶體性關節病。嚴重影響患者身心健康,臨床一般采用非甾體類藥物治療,秋水仙堿也是常用于治療AGA的藥物之一。
非布司他是一種黃嘌呤氧化酶(XO)抑制劑,用于長期治療伴有痛風癥狀的高尿酸血癥,是屬于抑制尿酸生成的一類新藥,主要適用于痛風緩解期控制尿酸的水平,對抑制XO的活性以及對血清尿酸的降低有著明顯作用,適用于具有痛風癥狀的高尿酸血癥的長期治療藥物。但常伴有肝功能異常、皮疹、惡心等不良反應[5]。秋水仙堿將細胞內的微管中主要的成分微管蛋白黏合,防止微管聚合,抑制紡錘體的形成,防止與細胞支架有絲分裂,也會停止中性粒細胞球的活動,因為紡錘體不能形成,染色體不能到達赤道板,可引起純粹的炎癥或抗炎作用[6]。因此,秋水仙堿能抑制炎癥細胞,削弱白細胞活性,發揮吞噬作用,使乳酸的形成減少,抑制了尿酸鹽的晶體堆積,以此來達到最終的減少炎癥反應以及迅速鎮痛的目的。在《2016 年中國痛風診療指南》[7]中有提到,適量的采用秋水仙堿治療初期痛風性關節炎,可預防AGA的發作,因此,秋水仙堿也可用于AGA的預防治療。在臨床應用中若單獨采用秋水仙堿治療AGA時,大部分服用的患者可在短時間內得到止痛效果,在止痛的時間上明顯優于其他類藥物,但單獨使用時藥劑量較大,而秋水仙堿本身的毒副作用較大,患者治療后會出現嚴重的毒副反應,而臨床研究證實,患者不良反應發生情況與用藥劑量成正比,因此,多數患者單獨使用秋水仙堿治療AGA時因接受不了其造成的不良反應而停止用藥[8]。
近年來,臨床醫學深入研究XO抑制劑等藥物治療AGA,但因止痛效果沒有秋水仙堿迅速,因此,采用適當劑量的秋水仙堿聯合XO抑制劑等藥物治療AGA的一類治療已成為新的研究方案,已有不少臨床實驗驗證,效果較好[9]。本文結果顯示,治療前,兩組SUA水平對比無統計學差異,治療后,聯合組各時間段SUA水平比對照組低,與張艷等[10]人的研究相符。本文結果還顯示,治療前,兩組血清水平無統計學差異,治療后,聯合組8-OHdG與3-NT水平均比對照組低。有報道提出非布司他聯合秋水仙堿均可有效降低血脂指標。本文結果顯示,治療后,聯合組血清 TG 水平比治療前低,HDL水平明顯比治療前高,而TC與LDL水平比較無統計學差異,與上述報道相符。本文結果顯示,治療后,聯合組的TGF-β、IFN-γ、TNF-α水平比對照組低;聯合組的總有效率為95.74%,明顯高于對照組的78.72%。通過各項指標說明表示非布司他聯合秋水仙堿可以有效治療AGA。
綜上所述,非布司他聯合秋水仙堿可以降低SUA、 8-OHdG 與 3-NT的水平,同時可以降低血脂,可有效抑制炎癥,治療效果佳,值得推廣與應用。

