人EGFL7真核表達載體的構建及穩定轉染EA.hy926細胞系的建立
丁 悅,黃為民,唐麗君
(南方醫科大學南方醫院新生兒科,廣東 廣州 510515)
支氣管肺發育不良(broncho-pulmonary dysplasia,BPD)是極低出生體重兒長期氧療、機械通氣常見的肺部并發癥,有較高的致殘率及死亡率[1],存活兒常遺留肺功能損傷及神經系統后遺癥[2],是早產極低體重兒并發癥中救治耗費最高的疾病。隨著肺表面活性物質及無創呼吸機等的應用[3-4],BPD在病理特征表現上,以肺泡以及肺微血管不良發育為基礎[5]。調控肺血管發育的生長因子紊亂可導致肺血管發育受阻進而影響肺泡正常發育。人類表皮生長因子樣結構域7(EGFL7)是一種血管內皮特異分泌的新型蛋白,在高氧致新生大鼠BPD中表達下調,有可能對BPD的發生發展有影響[6]。基于此,本研究建立針對人的真核表達EGFL7的載體,在此基礎上進一步評價該載體是否能穩定地轉染EA.hy926細胞系,從而為探究EGFL7對BPD的影響提供參考借鑒。
1 材料與方法
1.1 材料EA.hy926細胞購自廣州勵德生物科技有限公司,胎牛血清購自美國Gibco公司;質粒提取試劑盒、G418購自美國invitrogen公司;DNA凝膠回收試劑盒購自美國OMEGA公司;免抗人EGFL7多克隆抗體購自美國santa cruz公司;β-actin抗體購于美國Affinity公司;實時熒光定量PCR(RT-PCR)試劑盒購于QIAGEN公司。
1.2 方法
1.2.1 RT-PCR擴增mTSARG3基因開放閱讀框設計EGFL7引物,擴增含EGFL7開放閱讀框的822bp序列,瓊脂糖凝膠通過電泳儀(美國伯樂公司,型號:164-5050)進行電泳,然后對收回后的膠進行分析。
1.2.2 pEGFP-N1-EGFL7重組質粒的構建及鑒定利用HindⅢ以及BamHI對已經純化后的PCR產物和pEGFP-N1質粒進行雙酶切,將其轉化成為E coli DH5ɑ的感受態細菌,借助藥物篩選后以獲得顯示為陽性的克隆,通過PCR擴增并進一步雙酶切鑒定獲得的陽性克隆,在進行測序后就可以具體對載體命名為pEGFP-N1-EGFL7。
1.2.3 pEGFP-N1-EGFL7在EA.hy26細胞系中的瞬時轉染EA.hy926細胞融合至80%~90%時,將pEGFP-N1-EGFL7質粒通過電轉儀(日本BEX公司,型號:BEX系列CUY21EDIT Ⅱ型)轉染EA.hy926細胞。熒光顯微鏡下觀察轉染情況。
1.2.4 建立穩定轉染人EGFL7的EA.hy926細胞系篩選G418濃度即細胞全部死亡的最低濃度(500 μg/mL)。EA.hy926細胞轉染后48 h,改含G418的DMEM培養基培養,從中篩選出克隆物質,為獲得單克隆的細胞系對上述克隆物進行擴增培養。將pEGFP-N1空白質粒導入EA.hy926細胞中,并將此細胞作為陰性對照組。
1.2.5 RT-PCR檢測轉染細胞中EGFL7基因使用Trizol試劑盒進行RNA提取,利用微量分光光度法測定RNA含量及純度。利用瓊脂糖凝膠電泳的檢測方式,對18S RNA、28S RNA進行測定,測定的內容主要是證實RNA序列完整性。借助逆轉錄的方式,合成cDNA的第一鏈,利用這種參考模板做熒光定量RT-PCR工作。實時(Real-time)PCR數據采用2-△CT相對定量方法處理。
1.2.6 免疫印跡法(WB)鑒定EGFL7蛋白表達總蛋白加入到10 μL的5 × 樣品緩沖液(比例為4∶1),煮沸后進行十二烷基硫酸鈉聚丙烯酰胺凝膠電泳,轉膜,50 g.L-1 BSA室溫封閉2 h后加入EGFL7抗體(稀釋濃度為l∶400),4 ℃冷庫孵育過夜,用含TwEEN20的TBST在搖床上充分洗滌PVDF膜,每次10 min,前后共3次。然后加入經l∶10 000稀釋的二抗,將稀釋好的二抗置入22 ℃~26 ℃室溫下,搖床上持續搖晃約60 min,借助TBST洗滌PVDF膜3次,利用電化學發光法測定并且做顯色處理,之后針對結果予以吸光度的掃描檢查。
1.2.7 統計學方法用SPSS 21.0統計學軟件進行數據處理。數據均進行正態檢驗,兩樣本間比較采用t檢驗;兩樣本以上之間的比較,則檢驗方差是否齊性,若方差齊性,則采用方差分析,組內多重間比較行LSD檢驗,反之則用Welch檢驗。P<0.05表示差異有統計學意義。
2 結果
2.1 RT-PCR擴增mTSARG3基因開放閱讀框結果從臍靜脈內皮細胞的cDNA文庫中擴增EGFL7的開放閱讀框,電泳分析瓊脂糖凝膠發現:819bp為基因片段的大小,這一結果與預期的基本一致,見圖1。
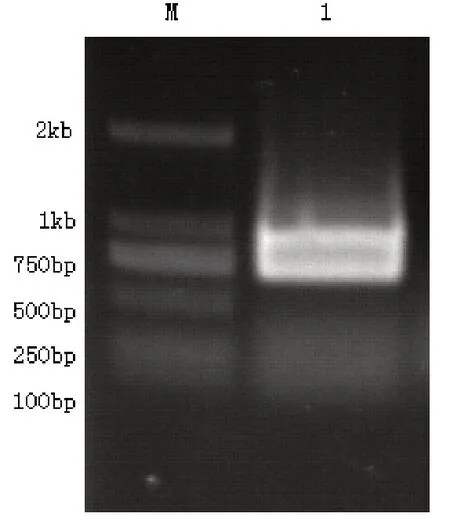
圖1 泳道M:DL1kb DNA Marker
2.2 pEGFP-N1-EGFL7重組質粒雙酶切及測序鑒定pEGFP-N1-EGFL7重組質粒1、2借助雙酶切下7kd左右、819bp左右條帶(圖2),經測序后證實DNA序列與GenBank中EGFL7序列一致,表明重組質粒構建成功。
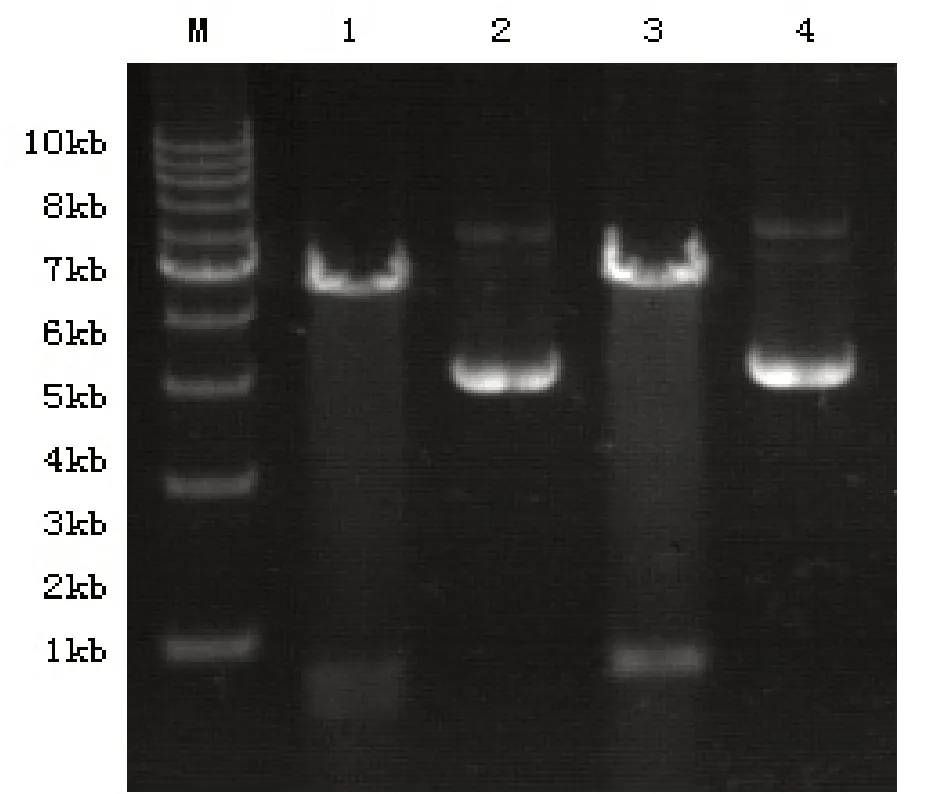
圖2 泳道M:1kb DNA 梯度標志
2.3 穩定轉染細胞系的鑒定
2.3.1 RT-PCR檢測EGFL7mRNA設對照質粒轉染的EA.hy926細胞EGFL7mRNA相對表達量(relativequantity,RQ)為l,N1-EA.hy926和hEGFL7-EA.hy926兩組差異有統計學意義(t=-5.975,P=0.028),見表1。
表1 不同細胞組間EGFL7mRNA的比較( ±s)

表1 不同細胞組間EGFL7mRNA的比較( ±s)
組別 例數 2△△CT值 t值 P值N1-EA.hy926 3 1.0124±0.0472 -5.975 0.028 hEGFL7-EA.hy926 3 8.6167±2.2337
2.3.2 WB檢測EGFL7蛋白量hEGFL7-EA.hy926組EGFL7蛋白量明顯高于空白對照組和N1-EA.hy926組,經過統計學方法,差異均有統計學意義(P<0.001),見圖3、表2。

圖3 轉染細胞的EA.hy926蛋白表達
表2 不同細胞組間EGFL7蛋白表達量的比較( ±s)
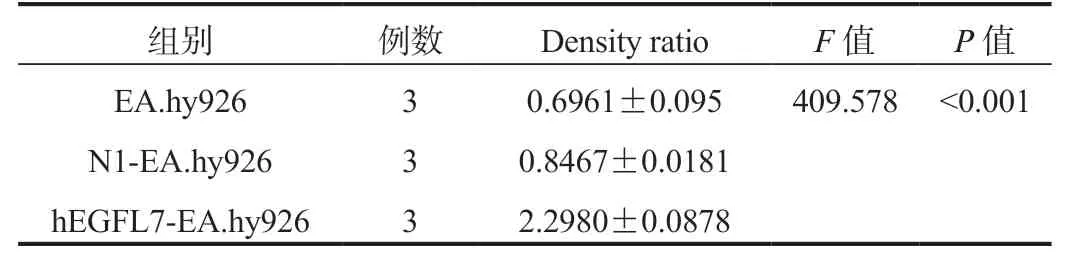
表2 不同細胞組間EGFL7蛋白表達量的比較( ±s)
注:方差齊(P=0.107),故采用方差分析,組內多重比較采用LSD法,EA.hy926與N1-EA.hy926兩組間差異無統計學意義(P=0.051);hEGFL7-EA.hy926組明顯高于EA.hy926組和N1-EA.hy926組(P<0.001)。
組別 例數 Density ratio F值 P值EA.hy926 3 0.6961±0.095 409.578<0.001 N1-EA.hy926 3 0.8467±0.0181 hEGFL7-EA.hy926 3 2.2980±0.0878
3 討論
BPD是早產兒比較嚴重的慢性呼吸系統疾病,可導致患兒長時間脫氧困難,對肺部及氣道造成持續的慢性損傷,嚴重者可出現肺動脈高壓甚至死亡[1]。即使存活,后期可能因感染或哮喘等原因反復住院從而導致預防不良。BPD的確切病因及機制尚未明確。因此,迫切需了解BPD的發生機制從而尋求有效的防治措施減少早產兒BPD發生率。肺血管發育紊亂及肺泡化阻滯是BPD發生發展的關鍵事件。既往學者們關注的主要領域是肺泡化損傷,但對BPD的預防及治療并未取得明顯成效。近年來認為BPD是由于肺微血管發育不良導致肺泡發育異常的“血管發育障礙假說”[7]。因此,目前認為肺血管分泌的多種因子在肺微血管和肺泡正常發育中起重要作用。探索血管生長因子在BPD中的作用可望為BPD的防治開辟新的途徑。EGFL7是新近發現的在肺血管形成和生成的過程中均起重要作用的蛋白,在血管內皮細胞中特異表達,通過自主分泌或者旁邊組織分泌刺激血管生成[8]。EGFL7可以抑制平滑肌細胞遷移,促進血管內皮細胞遷移、黏附、增殖在正常血管管腔形成中發揮了關鍵作用[9]。EGFL7敲除小鼠會出現外周出血、循環發育缺陷[10]。EGFL7過表達則導致血管結構異常及血管穩態受損[9]。這提示EGFL7是血管發育中的關鍵蛋白,其是否參與了BPD的發病過程,國內外報道較少。
我們從人的臍靜脈內皮細胞cDNA文庫中獲得擴增EGFL7的ORF,經過雙酶切將其克隆到pEGFP-N1中,得到重組表達質粒pEGFP-N1-EGFL7。利用電穿孔法最終建立穩定轉染的EA.hy926細胞系。使用RT-PCR及蛋白質印跡法檢測EGFL7在穩定轉染EA.hy926細胞系中的基因及蛋白水平。這一結果顯示:研究成功地建立了穩定整合pEGFP-N1-EGFL7載體的EA.hy926細胞系。我們前期研究發現:新生鼠在60%的氧氣中持續暴露14 d可以模擬BPD的發生發展過程,通過建立此模型我們觀察到肺部EGFL7基因和蛋白表達水平明顯低于正常組,下調值同肺部微血管的密度降低有緊密相關性,這一結果則提示EGFL7可能同肺部的微血管發育存在障礙有較大聯系[6]。此外,在高氧的暴露下,血管內皮細胞的EGFL7蛋白表達量明顯低于正常組并且高氧組的內皮細胞凋亡明顯增加,EGFL7蛋白表達增加可避免血管內皮細胞發生凋亡[11]。高表達EGFL7是否可減少內皮細胞凋亡進而促進血管發育,需深入研究明確。EGFL7在多種炎癥及血管生成中也扮演了重要的角色。在EGFL7敲除的體外血管模型中,EGFL7敲除后會抑制血管生成,同時血管屏障功能受損并導致炎癥反應[12]。EGFL7敲除鼠可導致神經系統免疫反應,重組EGFL7蛋白治療則可減輕上述炎癥反應[13]。在脂多糖誘導的炎癥反應中,鼠肺組織血管內皮細胞中的EGFL7表達減少,上調EGFL7可減少白細胞在內皮細胞的黏附[14]。這表明EGFL7有可能通過減輕炎癥反應增加血管生成。肺部高表達EGFL7是否能減輕炎癥反應促進血管及肺泡發育進而發揮對BPD的保護作用,國內外尚未見報道。
綜上所述,本研究通過建立能高表達EGFL7蛋白的EA.hy926細胞系,為下一步在體內外實驗中探討EGFL7在BPD中的作用及機制奠定基礎。

