深度學習重建算法優化能譜CT低單能量圖像質量及檢測肝臟低對比度小病灶能力
呂培杰,劉娜娜,王落桐,Francesca Rigiroli,Daniele Marin,高劍波*
(1.鄭州大學第一附屬醫院放射科,河南 鄭州 450052;2.通用電氣醫療集團CT影像研究中心,北京 100176;3.哈佛大學醫學院貝斯以色列女執事醫療中心放射科,美國 馬薩諸塞 22015;4.杜克大學醫學中心放射科,美國 北卡羅來納 27708)
隨著碘X射線衰減能力變強,能譜CT低單能量成像(<70 keV)對比度逐漸增加[1],但所伴隨的高噪聲可致圖像質量降低,影響檢測與診斷肝臟低對比度小病灶(如肝轉移灶);而常規重建算法,包括濾波反投影(filtered back projection,FBP)和基于混合模型的自適應統計迭代重建(adaptive statistical iterative reconstruction V,ASIR-V)等均無法有效解決低能級圖像的噪聲問題[2]。近期有研究[2-4]表明深度學習圖像重建(deep learning imaging reconstruction,DLIR)可顯著減低腹部CT圖像噪聲、提高對比度并保持圖像紋理不變,進而改善圖像質量。以往DLIR技術多用于常規混合能量CT圖像,少見用于單能量CT圖像的研究[5-7]。本研究觀察以DLIR算法優化能譜CT低單能量圖像質量、提高檢測肝臟低對比度小病灶能力的可行性。
1 資料與方法
1.1 研究對象 納入2020年3月—2021年3月30例于鄭州大學第一附屬醫院接受上腹部增強CT掃描的肝臟疾病患者,男16例、女14例,年齡21~72歲、平均(55.6±14.2)歲;體質量指數20.10~35.45 kg/m2,平均(25.81±3.72)kg/m2;共58個病灶,包括肝囊腫30個、肝臟轉移瘤28個,均經病理或臨床及6個月以上影像學隨訪證實,直徑0.51~3.00 cm,平均(2.13±0.81)cm。納入標準:①年齡≥18歲;②病灶門脈期呈局灶性低對比度,即病灶與周圍肝實質CT值比值<1,且0.5 cm<直徑≤3 cm。排除標準:圖像資料不完整或質量差而影響診斷。本研究經院倫理委員會批準(批號:2017-KY-02)。
1.2 儀器與方法 采用GE Revolution 256排CT機,囑患者仰臥,行上腹部雙期CT增強掃描,以雙筒高壓注射器經肘靜脈以3.0 ml/s流率注射非離子型對比劑碘海醇(350 mgI/ml,1.3~1.5 ml/kg體質量),采用Smart Prep技術觸發監測腹主動脈,達到閾值(100 HU)后延遲12 s開始動脈期掃描,完成30 s后行門脈期掃描。掃描參數:動脈期,管電壓120 kVp,自動管電流100~700 mA,螺距1.375;門脈期,管電壓80 kVp和140 kVp,管電流350~570 mA,螺距1.375,轉速0.5秒/周,噪聲指數10 HU,FOV 50 cm×50 cm。分別采用DLIR算法(重建強度為高水平)和基于混合模型的ASIR-V算法(重建百分比為60%)重建層厚和層間距均為1.25 mm的40、50、60及70 keV的門脈期單能量圖像。
1.3 圖像分析 將所有圖像傳輸至GE AW4.7影像工作站,由1名具有3年以上工作經驗的放射科醫師于門脈期肝門層面的肝臟、門靜脈主干、背部肌肉和肝臟病灶內放置類圓形ROI,測量CT值及標準差(standard deviation,SD);于前腹壁皮下脂肪內獲取圖像噪聲值(像素平均值的SD)[8]。保證同一能級不同算法之間、同一算法不同能級圖像間ROI一致,對各參數均測量3次,取平均值,分別計算肝臟和門靜脈相對于背部肌肉及肝臟病灶相對于周圍正常肝實質的對比噪聲比(contrast-to-noise ratio,CNR):CNR肝臟/門靜脈=(CT肝臟/門靜脈-CT背景肌肉)/SD,CNR肝臟病灶=(CT肝臟病灶-CT周圍肝實質)/SD周圍肝實質。
由另2名具有14年以上工作經驗、且不知曉患者及圖像信息的放射科醫師共同評估CT圖像,預設窗寬和窗位分別為400 HU和40 HU,可根據需要適當調整,采用5分法對圖像總體質量、病灶顯著性和診斷信心進行主觀評分(表1)[9-10],≥3分為滿足診斷標準。

表1 肝臟CT圖像質量主觀評分標準
1.4 統計學分析 采用Graphpad Prism 8.0.2統計軟件進行數據分析。以±s表示符合正態分布的計量資料;主觀評分結果為等級資料,以中位數(上下四分位數)表示。采用配對t檢驗或配對Wilcoxon秩和檢驗比較相同能級不同算法圖像之間各指標;以單因素方差分析或Friedman檢驗比較相同算法不同能級圖像(Geisser-Greenhouse校正,兩兩比較Turkey法)。P<0.05為差異有統計學意義。
2 結果
2.1 客觀評估 40~70 keV能級下,相比ASIR-V圖像,DLIR圖像的CNR肝臟、CNR門靜脈及CNR肝臟病灶分別增加36.33%~44.45%、36.00%~42.96%及13.15%~16.91%(P均<0.05);DLIR圖像噪聲均顯著減少(P均<0.05),減少幅度約26.71%~29.23%。不同能級下,2種算法間各指標變化率差異均無統計學意義(P均>0.05),見表2及3。DLIR圖像噪聲最大值位于40 keV,與ASIR-V圖像50 keV能級下噪聲相當(t=1.05,P=0.320)。除CNR肝臟外,不同能級間DLIR圖像各指標兩兩比較差異均有統計學意義(P均<0.05);所有能級圖像中,40 keV能級下DLIR圖像的CNR門靜脈與CNR肝臟病灶最高(P均<0.05),噪聲亦高于其他能級圖像(P均<0.05),見圖1。
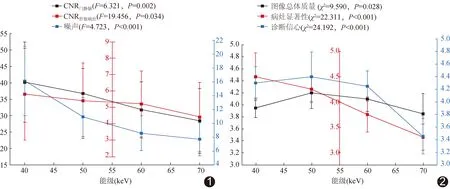
圖1 不同能級DLIR圖像的CNR門靜脈、CNR肝臟病灶及噪聲變化趨勢 圖2 不同能級DLIR圖像總體質量、病灶顯著性及診斷信心評分變化趨勢
2.2 主觀評估 40~70 keV條件下,DLIR圖像質量均可滿足臨床診斷標準,但20.00%(8/40)40 keV ASIR-V圖像無法滿足標準;40~60 keV能級下,相比ASIR-V圖像,DLIR圖像總體質量、病灶顯著性及診斷信心評分分別增加14.58%~34.26%、10.89%~14.46%及18.18%~21.89%(P均<0.05)。不同能級下,2種算法病灶顯著性評分變化率差異無統計學意義(P>0.05),見表2、4。不同能級DLIR圖像間各評分總體比較差異均有統計學意義(P均<0.05),40 keV DLIR圖像總體質量和診斷信心評分與50、60 keV圖像比較差異均無統計學意義(P均>0.05),而病灶顯著性評分高于50~70 keV圖像(P均<0.05),見圖2、3。
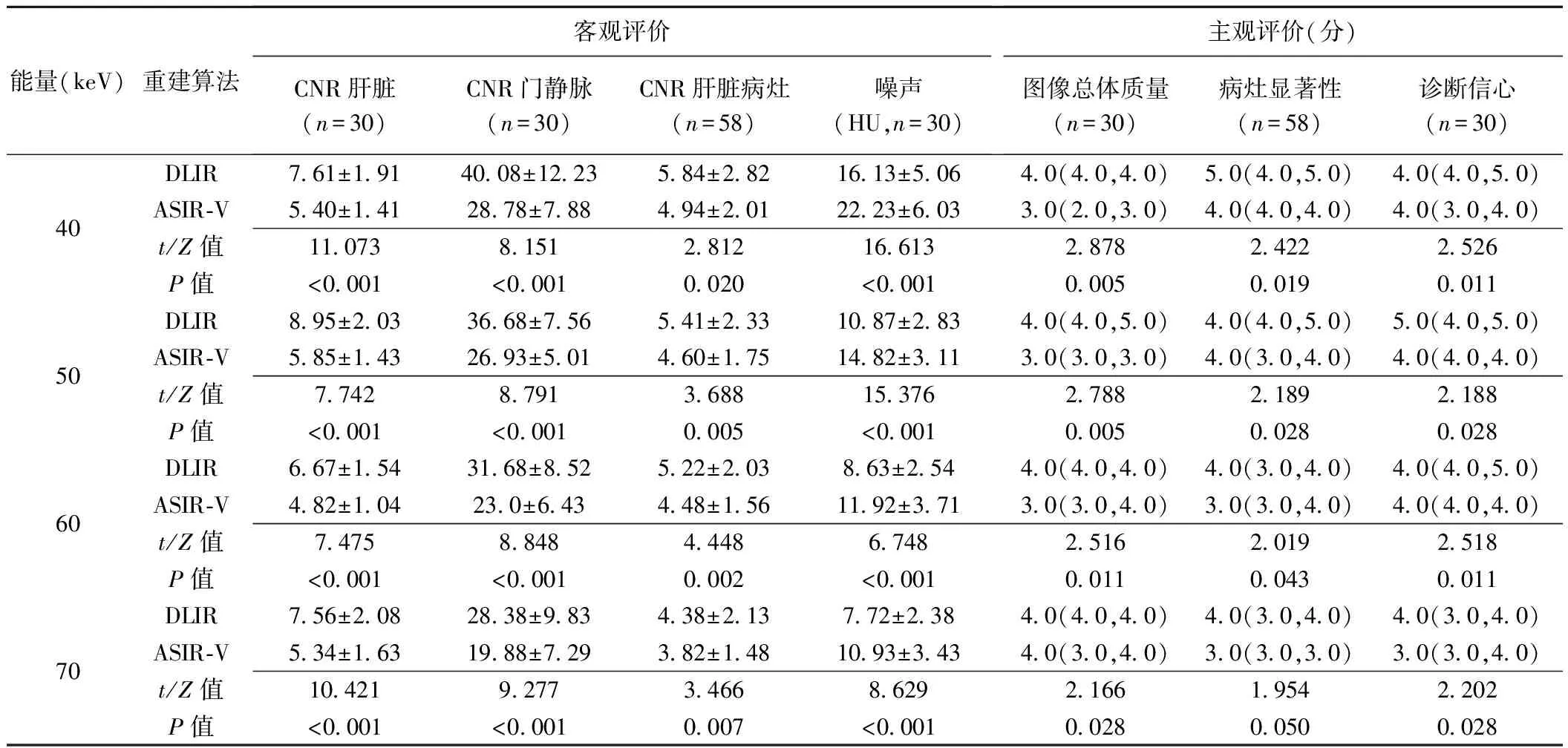
表2 不同重建算法各能級上腹部CT圖像客觀及主觀質量評價結果
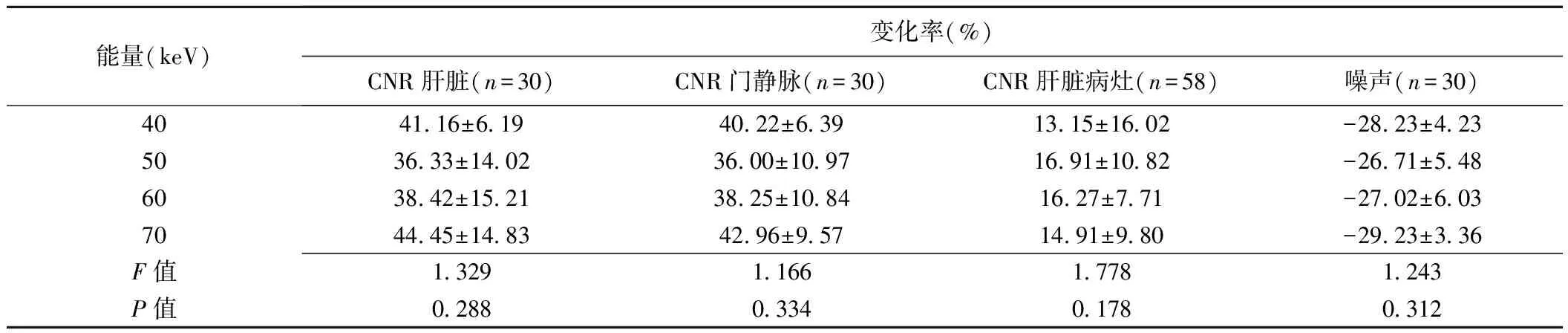
表3 相比ASIR-V重建圖像,各能級上腹部CT DLIR重建圖像CNR和噪聲變化率
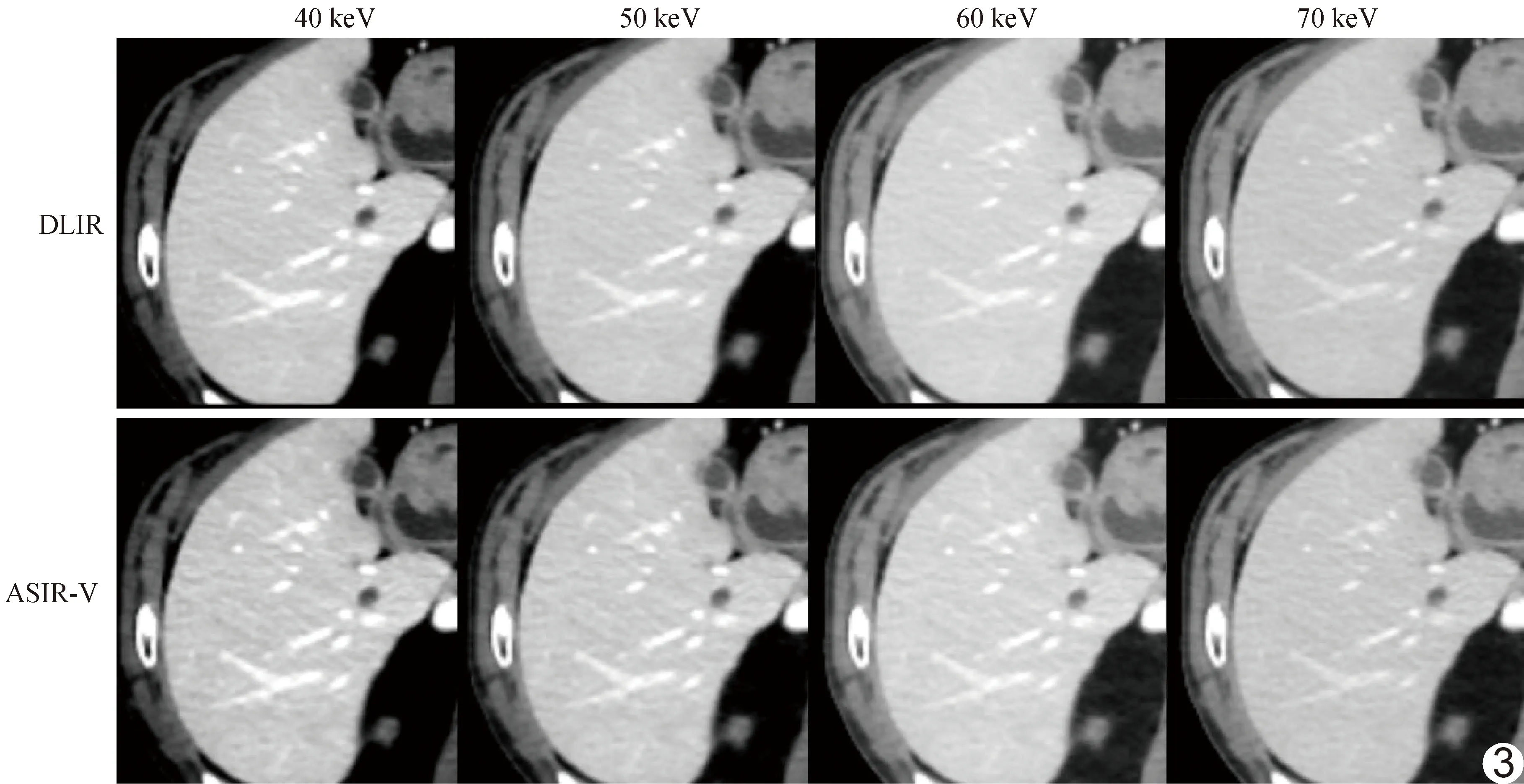
圖3 患者男,72歲,肝轉移癌(直徑0.55 cm) 相同能級下,相比ASIR-V圖像,DLIR圖像噪聲、圖像紋理及圖像總體質量均顯著改善,40 keV DLIR圖像噪聲高于其他能級,但CNR亦高,且病灶解剖細節清晰(箭)
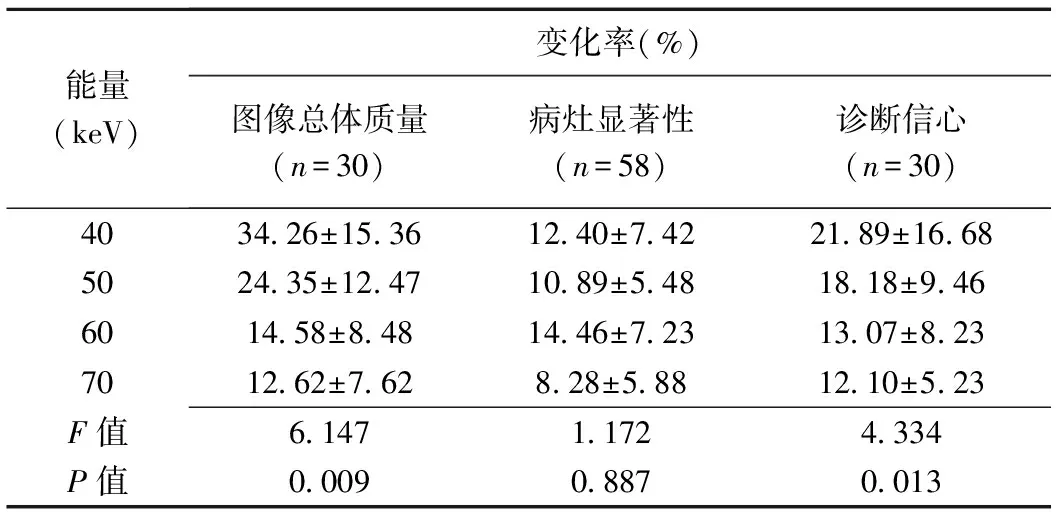
表4 相比ASIR-V重建圖像,各能級上腹部CT DLIR重建圖像主觀評分變化率
3 討論
新一代基于深度學習算法的DLIR圖像重建技術可獲得與高輻射劑量FBP圖像相匹配的噪聲紋理和空間分辨率特征,且降噪能力與現有常規迭代技術相當或更高[11-12]。本研究中,與ASIR-V圖像相比,各單能量DLIR圖像水平降噪效果更明顯、圖像對比度更佳,與既往臨床研究[13]結果相符。另外,本研究進一步發現,不同單能量之間,DLIR相對ASIR-V的降噪比例及CNR提升比例無顯著差異,表明DLIR客觀優化效果未受單一能級變化的影響;雖然DLIR圖像總體質量評分均顯著高于ASIR-V圖像[7,13],但各能級圖像表現不盡相同,40 keV能級下,DLIR相對于ASIR-V單能量圖像的優化率顯著高于其他能級,可能與原40 keV噪聲高于其他能級有關;在不改變圖像紋理的條件下,DLIR降噪優化效果更佳。
各能級DLIR單能量圖像的CNR肝臟病灶均顯著高于ASIR-V圖像,提升幅度為13.15%~16.91%,尤以40 keV DLIR圖像的CNR肝臟病灶最高;分析原因,一方面與40 keV碘匯聚能力最大有關,另一方面,40 keV聯合DLIR降噪后,噪聲已降至臨床可接受的50 keV ASIR-V圖像的水平[14]。本研究中40 keV DLIR圖像總體質量、病灶顯著性及診斷信心評分均大于或相當于其他能級圖像,提示40 keV可視為平衡肝臟病灶對比度和總體圖像質量的最佳能級水平。
綜上所述,DLIR技術可顯著減少低能量圖像噪聲,提高檢測肝臟低對比度小病灶的能力及診斷信心,提升圖像總體質量,其中40 keV為最佳單能量水平。但本研究樣本量小,且來自單一中心,僅采用60% ASIR-V和高強度水平DLIR,未納入其他重建水平,亦未評估診斷病灶的準確性,有待擴大樣本量進一步觀察。

