ARMS-PCR技術在玫瑰果鑒別中的應用
邵婕,楊正修,鄒強,陸崢飛,李凡*
1. 康寶萊蕾碩(湖南)天然產物有限公司(長沙 410100);2. 康寶萊全球測試中心HP1實驗室(托倫斯 90502)
玫瑰果(Rosa canina)在世界上有著悠久的藥食兩用歷史。玫瑰果中多酚、黃酮、維生素C等活性物質含量豐富,具有抗氧化、抗癌、抗輻射和抑菌等多種藥理作用[1]*。但玫瑰果原料品種繁多,薔薇屬果實的化學成分、抗氧化能力和個體酚類物質含量存在顯著差異[2]*。刺玫果(Rosa duvarica)和玫瑰果屬于同一植物屬,兩者不僅在外觀上非常相似,活性物質也非常相似,主要包括黃酮、多糖、三萜等[3]*。由于化學成分的相似性,常見的化學鑒定方法難以對二者進行區分,使得玫瑰果摻假特別是混合摻假的檢測具有挑戰性。擴增阻滯突變系統-聚合酶鏈式反應(amplification refractory mutation system-PCR,ARMSPCR)技術[4]*常用于遺傳疾病[5]*、基因分型[6]*和微生物學[7]*等許多快速檢測研究領域,在植物鑒定和分析化學中的應用鮮有報道。
試驗通過對玫瑰果和刺玫果基因組序列的比較分析,建立一種基于特征SNP位點的ARMS-PCR方法,可用于鑒定玫瑰果和刺玫果。
1 材料與方法
1.1 材料與設備
化學標準品Isoquercetin(ChromaDex ASB-00009505-025)。
植物對照藥材(Botanical Reference Material,BRM):玫瑰果果實BRM(Lot 00030792-473,ASB-00030792-005,ChromaDex. Inc);刺玫果果實BRM(Lot 121255-201203,121255,購自National Institute of Food and Drug Control,NIFDC)。
植物材料:從中國原料市場采購11份玫瑰果用于驗證。
Automatic TLC Sampler 4(Chromacim,Moirans,法國);硅膠板(60 F254,20×10 cm,Merck,德國);CAMAG TLC可視化儀(Chromacim,Moirans,法國);DNeasy mericon Food Kit;Qubit 3.0熒光計(Thermofisher,廣州,中國);C1000 Touch(BIORAD,上海,中國);Integrated DNA Technologies(Thermofisher,廣州,中國);AmpliTaq GoldTM*360 Master Mix(Thermo Fisher,立陶宛)。
1.2 高效薄層色譜(high-performance thin layer chromatography,HPTLC)
樣品處理:稱取500 mg玫瑰果或刺玫果果實BRM到15 mL試管中,加入10 mL甲醇,渦旋30 s。超聲處理15 min。將一部分樣品通過0.45 μm濾膜過濾到HPLC進樣瓶中。
使用Automatic TLC Sampler 4將樣品噴涂到預制硅膠板上,Isoquercetin作為化學標準品噴涂到預制硅膠板上。用流動相(乙酸乙酯/乙酸/甲酸/超純水100/11/11/26)展開,使用10%硫酸進行顯色。用CAMAG TLC可視化儀和Vision cats軟件拍攝照片。
1.3 DNA提取
DNA提取過程均根據制造商的說明使用DNeasy mericon Food Kit進行。過程:將50~100 mg玫瑰果或刺玫果果實BRM,1 mL Food Lysis Buffer和2.5 μL Proteinase K加入離心管中,在60 ℃下孵育30 min,并以2 500×g離心5 min;取700 μL上清液于新的離心管中,加入500 μL氯仿,渦旋15 s,并將混合物以14 000×g離心15 min;將350 μL上清液轉移到新的離心管中,加入350 μL PB Buffer,將混合液轉移到吸附柱中,以17 000×g離心1 min;棄去收集管中溶液;向吸附柱中加入500 μL AW2 Buffer,并以17 000×g離心1 min;將收集管中的溶液再次倒出,并將吸附柱以17 000×g離心2 min;將吸附柱放入新的離心管中,加入100 μL TE緩沖液,并將其以17 900×g離心2 min;使用Qubit 3.0熒光計進行定量。
1.4 DNA Barcode序列采集及植物鑒定
使用2對引物對玫瑰果和刺玫果gDNA(genomic DNA)進行擴增,擴增體系包含10 μL AmpliTaq GoldTM*360 Master Mix、2 μL引物混合物(每種引物5 μmol/L)、5 μL gDNA和3 μL Free-Nuclease Water。在C1000 Touch上進行PCR擴增,反應條件為95 ℃預變性5 min,95 ℃變性30 s(58 ℃退火30 s,72 ℃延伸30 s)×35,72 ℃終末延伸3 min。RbcL-F:5’-TGTAAAACGACGGCCAGTATGTCACCACAAACAGAAAC-3’;RbcL-R:5’-CAGGAAACAGCTATGACCGTAAAA TCAAGKCCACCRCG-3’;ITS2-F:5’-TGTAAAACGACGGCCAGTATCCGATACTTGGTGTGAAT-3’;ITS2-R:5’-CAGGAAACAGCTATGACCGACGCTTCTCCAGACTACAAT-3’。獲得RbcL與ITS2基因片段,通過sanger測序獲取序列信息。引物由Integrated DNA Technologies(Thermofisher,廣州,中國)合成。
雙盲試驗:將11份玫瑰果市場樣品與14份刺玫果果實BRM由試驗人員1隨機編排順序并編號,通過DNA barcode技術對25個樣品進行鑒定。提取25個樣品gDNA后,通過RbcL和ITS2這2對引物對gDNA進行PCR擴增,擴增體系包含10 μL AmpliTaq GoldTM*360 Master Mix、2 μL引物混合物(每種引物5 μmol/L)、5 μL gDNA和3 μL Free-Nuclease Water。在C1000 Touch上進行PCR擴增,反應條件為95 ℃預變性5分鐘,95 ℃變性30 s(58 ℃ 退火30 s,72 ℃延伸30 s)×35,72 ℃終末延伸3 min。瓊脂糖凝膠電泳檢測擴增結果后進行Sanger測序,確認樣品種屬信息。試驗人員2通過ARMS-PCR對25個樣品進行鑒別。
1.6 ARMS-PCR
使用AmpliTaq GoldTM*360 Master Mix對玫瑰果與刺玫果的gDNA進行擴增,擴增體系包含10 μL AmpliTaq GoldTM*360 Master Mix、2 μL引物混合物(每種引物5 μmol/L)、5 μL gDNA和3 μL Free-Nuclease Water。在C1000 Touch上進行PCR擴增,反應條件為95 ℃預變性5 min,95 ℃變性30 s(58 ℃退火30 s,72 ℃延伸30 s)×35,72 ℃終末延伸3 min。原始DNA洗脫用于PCR反應,無需調整濃度。每次運行都包括陽性對照和陰性對照,PCR產品在帶有DNA染料的2%瓊脂糖凝膠中可視化。各基因及其引物的擴增引物序列詳見表1。引物由Integrated DNA Technologies合成。

表1 ARMS-PCR引物信息表
1.7 生物信息學分析
從NCBI(https://www.ncbi.nlm.nih.gov/)下載所有序列,從NCBI下載的所有序列在MEGA X中使用ClustalW默認設置進行比對,引物設計使用Primer 3.0 plus(https://www.primer3plus.com/)。DNA條形碼序列使用CodonCode Aligner和APE軟件進行分析。Sanger測序結果在NCBI上進行比對。
1.8 統計學分析
雙盲試驗所獲得的試驗數據通過POI(probability of identification)進行分析[8]*。
2 結果與分析
2.1 HPTLC鑒別玫瑰果和刺玫果
通過HPTLC方法檢測玫瑰果和刺玫果,玫瑰果果實含有Isoquercetin[9]*,以Isoquercetin作為化學標準品,其位置和可見度如圖1所示。Rf值為0.59。玫瑰果和刺玫果HPTLC指紋圖譜非常相似,兩者之間的主要區別是檢測到的條帶的相對密度。因此,HPTLC難以區分玫瑰果和刺玫果。

圖1 玫瑰果和刺玫果HPTLC指紋圖譜
2.2 玫瑰果與刺玫果DNA barcode序列采集及引物設計
由于植物中ITS和rbcL區域的選擇壓力小、變異大,因此選擇該區域進行ARMS-PCR分析可更有效地區分遺傳關系密切的物種。通過DNA barcode方法獲取玫瑰果和刺玫果的ITS2和RbcL基因片段,Sanger測序得到序列信息(表2)。

表2 玫瑰果及刺玫果ITS2和RbcL序列信息
為驗證ARMS-PCR區分玫瑰果和刺玫果的可行性,根據3個不同的SNP位點分別設計P1、P2和P3這3種方案。P1方案的設計基于RbcL區域序列,而P2和P3方案的設計基于ITS2區域序列(圖2)。
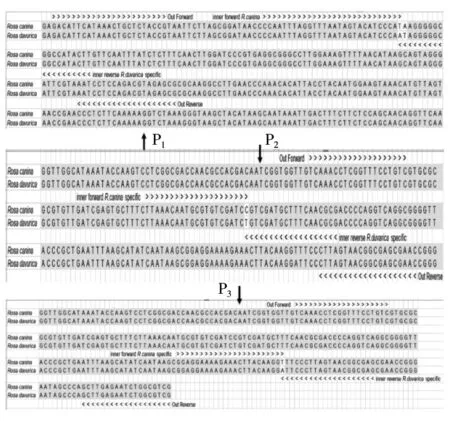
圖2 候選ARMS-PCR引物在RbcL(P1)和ITS2區域(P2和P3)中的位置
以P2方案為例,分析ARMS-PCR的工作原理(圖3)。基于SNP位置設計4條引物(表1)Outer F,Outer R,Inner F和Inner R,為玫瑰果和刺玫果提供不同長度的PCR片段。Outer F和Outer R配對從基因組DNA中擴增出1個182 bp的片段作為內參,Inner F和Inner R分別作為玫瑰果和刺玫果的特異性引物。玫瑰果DNA存在時,Inner F與玫瑰果的DNA模板之間形成完美匹配,Inner F與Outer R配對擴增出1段135 bp的片段。只有當Inner R與刺玫果的DNA模板之間形成完美匹配時,Inner R才能與Outer F配對擴增出1段86 bp片段。DNA模板中只存在玫瑰果DNA時,可以得到1條182 bp的內參條帶和1條135 bp的特異性條帶。DNA模板中只存在刺玫果DNA時,可以得到1條182 bp的內參條帶和1條86 bp的特異性條帶。當DNA模板中同時存在玫瑰果和刺玫果DNA時,可以得到1條182 bp的內參條帶,1條135 bp的特異性條帶和1條86 bp的特異性條帶。
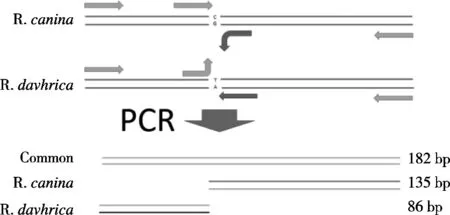
圖3 ARMS-PCR的P2設計示意圖

接表2
2.3 ARMS-PCR條件優化
為從P1、P2和P3中篩選最佳的試驗方案,使用玫瑰果和刺玫果果實BRM,通過DNA提取和PCR擴增,2%瓊脂糖凝膠電泳結果顯示,P1方案針對玫瑰果和刺玫果進行擴增,其擴增產物一致,均為1條100 bp左右的條帶,P3方案針對玫瑰果和刺玫果均得到兩條200 bp左右的條帶,P1和P3方案均無法區分玫瑰果和刺玫果。P2方案針對玫瑰果可得到1條182 bp的內參條帶和1條135 bp的特異性條帶,針對刺玫果可得到1條182 bp的內參條帶和1條86 bp的特異性條帶,可明顯區分玫瑰果和刺玫果。結果表明P2方案優于P1和P3方案,可以達到預期結果(圖4)。

圖4 3種設計的ARMS-PCR的驗證結果
由于設計的4條引物的退火溫度不同,設計梯度PCR試驗。從圖5(A)可以看出,最佳退火溫度為58℃。PCR的循環數決定擴增產物的產量,循環數太多會易出現非特異條帶。為避免非特異性條帶干擾,分別測試25 cycles和28 cycles的擴增效率,從圖5(B)可以看出,28 cycles和25 cycles均無非特異性條帶,但28 cycles電泳信號強度優于25 cycles,表明28 cycles優于25 cycles。
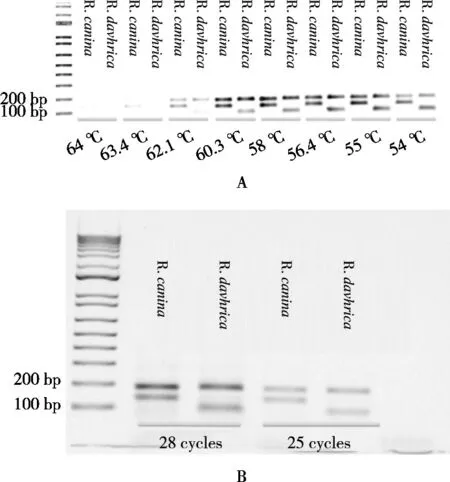
圖5 ARMS-PCR條件優化
2.4 ARMS-PCR驗證
為驗證ARMS-PCR玫瑰果鑒定的準確性,通過雙盲試驗測試玫瑰果市場樣品和刺玫果果實BRM,25個樣品經DNA barcode技術進行鑒定。ARMS-PCR結果表明(圖6),S-1,S-3,S-6,S-8,S-9,S-10,S-12,S-15,S-16,S-17,S-21,S-22,S-24,S-25這14個樣品被鑒定為刺玫果,S-2,S-4,S-5,S-7,S-11,S-13,S-14,S-18,S-19,S-20,S-23這11個樣品被鑒定為玫瑰果。該結果與DNA barcode方法結果完全一致。基于POI統計分析,該測定對于鑒別玫瑰果和刺玫果果實原材料具有大于0.9(95%CI)的識別概率。
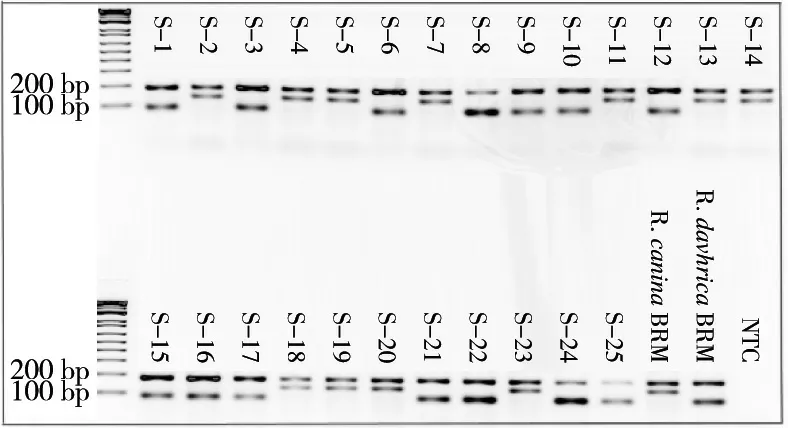
圖6 ARMS-PCR驗證市場25批樣品
2.5 玫瑰果中刺玫果的最低檢測限確認
為進一步探索ARMS-PCR的檢出限,將玫瑰果和刺玫果BRM粉末按質量比10/90,20/80,30/70,40/60,50/50,60/40,70/30,80/20和90/10進行混合。從這些混合材料中提取DNA用于擴增。結果顯示(圖7A),100%玫瑰果電泳結果僅有1條182 bp的內參條帶和1條135 bp的特異性條帶,添加10%~90%刺玫果后,電泳結果顯示多1條86 bp的刺玫果特異性條帶,且隨著刺玫果添加量的升高,135 bp的玫瑰果特異性條帶強度降低。為確認刺玫果的最低檢測限,對10%的刺玫果進行重復驗證,結果如圖7(B)所示。結果顯示,10次重復結果一致,均可檢出86 bp的刺玫果特異性條帶。綜上所述,該方法對玫瑰果中刺玫果的最低檢測限為10%。
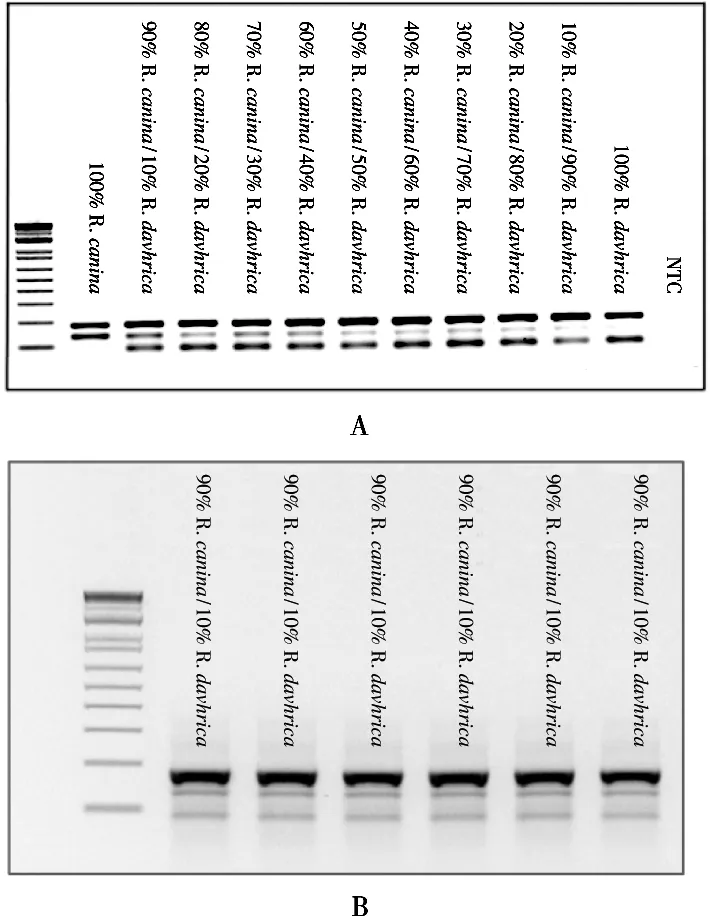
圖7 ARMS-PCR最低檢測限測定
3 結論與討論
建立一種基于特征SNP位點的ARMS-PCR方法,并應用于玫瑰果及其近緣種刺玫果的鑒定。該方法對玫瑰果和刺玫果的最低檢測限為10%。試驗方法客觀、分辨率高。與DNA Barcode方法相比,檢測周期短,無需測序,結果以圖位差異的形式呈現,易于進行判斷。
為確保目標序列的擴增和鑒定,高質量DNA的獲取極為重要。植物材料中蛋白質、脂肪、多糖、多酚等物質含量較高,這些物質可能抑制PCR擴增。因此,在DNA提取過程中盡可能地去除這些物質非常重要。此外,植物的加工過程也會影響DNA的最終產量、純度以及完整性。
基于DNA技術的植物鑒定方法通常只能得到種屬、基因型等信息,而無法獲得植物中活性物質的鑒定及定量信息。這些信息通常需要化學方法提供,如LC、LC-MS、GC-MS、NMR。在組學時代,基因組學、蛋白質組學和代謝組學相輔相成,從而能夠對各種復雜的植物原料進行全面鑒定。

