周期蛋白依賴性激酶4/6抑制劑相關肺毒性的文獻分析 Δ
趙 俊 ,劉廣偉 ,林玉燕 ,張小蕾 ,倪倍倍 [.青島大學附屬醫院藥學部,山東 青島 66003;.廣州中醫藥大學深圳醫院(福田)藥學部,廣東 深圳 58000]
周期蛋白依賴性激酶(cyclin-dependent kinases,CDK)4/6抑制劑為一類新型抗腫瘤藥物,用于激素受體陽性(hormone-receptor-positive,HR+)、人表皮生長因子受體2陰性(human epidermal growth factor receptor 2-negative,HER2-)的不可切除或復發乳腺癌的管理,并與標準內分泌療法聯合用于晚期HR+乳腺癌的治療。目前口服CDK4/6抑制劑[包括哌柏西利(palbociclib)、瑞博西利(ribociclib)和阿貝西利(abemacilib)]已被美國FDA批準用于HR+/HER2-晚期乳腺癌的治療[1―3],為乳腺癌患者帶來了新的希望。與此同時,上述3種藥物治療其他癌癥的臨床試驗也在全球各地開展,大多數都是CDK4/6抑制劑與其他藥物 (如酪氨酸激酶抑制劑、表皮生長因子受體抑制劑、HER2抑制劑、磷脂酰肌醇3-激酶抑制劑等)聯合用藥,未來其臨床應用可能會拓展到非小細胞肺癌[4]、肝癌[5]等多種癌癥的治療。然而,隨著該藥臨床使用與研究的深入,研究者們發現其安全性不可忽視。2017年,Ahsan等[6]在學術會議上報道了哌柏西利相關肺毒性的罕見不良反應,此后國外陸續有該類藥物相關肺毒性的報道。其中,間質性肺疾病(inter‐stitial lung disease,ILD)可導致肺間質纖維化病變,是一種具有潛在致命性的炎癥性肺疾病,已經列入該類藥物的藥品說明書[1―3]。目前,阿貝西利、哌柏西利已在我國上市,但相關肺毒性的詳細情況在其說明書中并未提及,且搜索中國知網、萬方數據、維普網截至2022年4月30日收錄的文獻,尚未見該藥相關肺毒性的報道。為便于國內臨床工作者了解該類藥物相關肺毒性的臨床特點,本研究擬收集國外報道的該類藥物相關肺毒性的案例進行分析,擬為國內合理使用該類藥物提供參考。
1 資料與方法
1.1 檢索策略
計算機檢索PubMed、Web of Science、SpringerLink、中國知網、萬方數據與維普網等數據庫,采用主題詞與自由詞相結合的方式進行檢索,檢索詞為“palbociclib”“ribociclib”“abemacilib”“CDK4/6 inhibitor”“induced”“case report”“adverse drug reaction”“side effect”“safety”“associated”“related”“lung”“interstitial lung disease”“pneumonia”,檢索時間截至2022年4月30日。
1.2 文獻納入與排除標準
文獻納入標準為:(1)文獻類型為國內外公開發表的臨床病例報告;(2)明確肺毒性為CDK4/6抑制劑所致;(3)結局指標報告了藥品不良反應(adverse drug reaction,ADR)的發生或提供了可統計的ADR發生的數據。
文獻排除標準為:(1)干預措施受其他藥物干擾而無法判斷ADR歸屬;(2)資料不完整導致無法分析;(3)重復發表的文獻;(4)動物實驗;(5)藥物基礎研究;(6)綜述等。
1.3 方法
采用回顧性分析的方法,對納入文獻的信息進行提取。由2位研究者按照納入與排除標準獨立進行文獻初步篩選,再在研究小組內討論決定納入的文獻,采用Ex‐cel 2013軟件記錄數據信息,提取數據后交叉核對,并進行統計描述和分析。
2 結果
2.1 病例一般情況
共檢索出170篇文獻,按照納入與排除標準剔除158篇,最終共收集到符合要求的文獻12篇,均為國外報道;涉及患者13例,包含美國3例,日本3例,印度2例,以色列、西班牙、法國、澳大利亞、沙特阿拉伯各1例。除2017年Ahsan等報道的1例之外,本次收集的案例最早報道時間為2018年,而2020年以后報道的案例有9例。13例患者均為女性,年齡在43~89歲之間,平均年齡62.54歲,其中使用哌柏西利的8例,使用阿貝西利的3例,使用瑞博西利的2例。有5例患者聯合使用氟維司群,6例患者聯合使用來曲唑,1例患者聯合使用阿那曲唑,1例患者聯合使用戈舍瑞林與氟維司群。13例患者中有12例出現腫瘤轉移,包括6例骨轉移[4例使用唑來膦酸,1例使用地舒單抗,1例未提及骨轉移用藥(病例13)]、2例肺轉移、1例肝轉移、1例肺轉移+肝轉移、1例縱隔淋巴結轉移、1例錐體轉移。13例患者的原患疾病及合并用藥情況見表1。
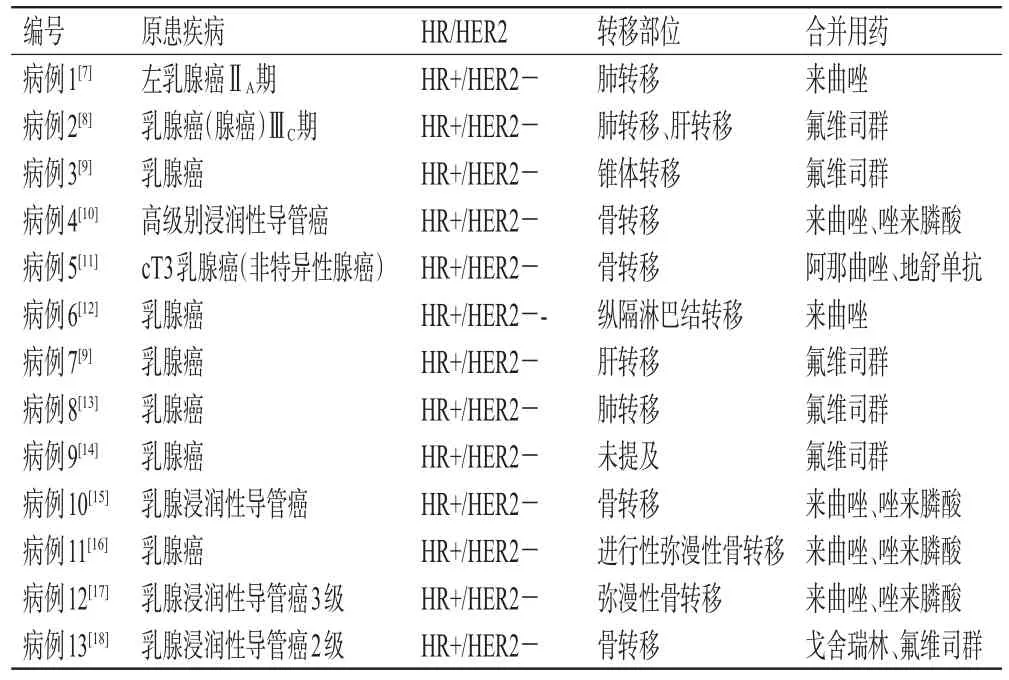
表1 13例患者的原患疾病及合并用藥情況
2.2 CDK4/6抑制劑相關肺毒性的臨床特點
2.2.1 發生時間 13例患者發生肺毒性的時間為用藥后1周~15個月。其中,使用哌柏西利的8名患者發病時間為用藥后1周~15個月,使用阿貝西利的3名患者發病時間為2周~1年,使用瑞博西利的2名患者發病時間為4周~4個月。具體見表2。
2.2.2 臨床表現 13例患者除病例5沒有臨床癥狀和縱隔淋巴結細胞學示上皮樣肉芽腫,余12例患者均以呼吸困難、胸悶、氣短、干咳等癥狀為主訴入院。這12例患者中僅有1例(病例4)提及發熱,最高37.7 ℃,其余均無發熱表現。13例患者肺部CT掃描顯示肺多發間質影、肺磨玻璃影、片狀多灶性磨玻璃密度影、雙側肺浸潤、雙側肺周邊磨玻璃樣混濁和結節性實變、雙側肺野多發斑片狀融合磨玻璃影、雙側肺中下區不均勻混濁等。具體見表2。
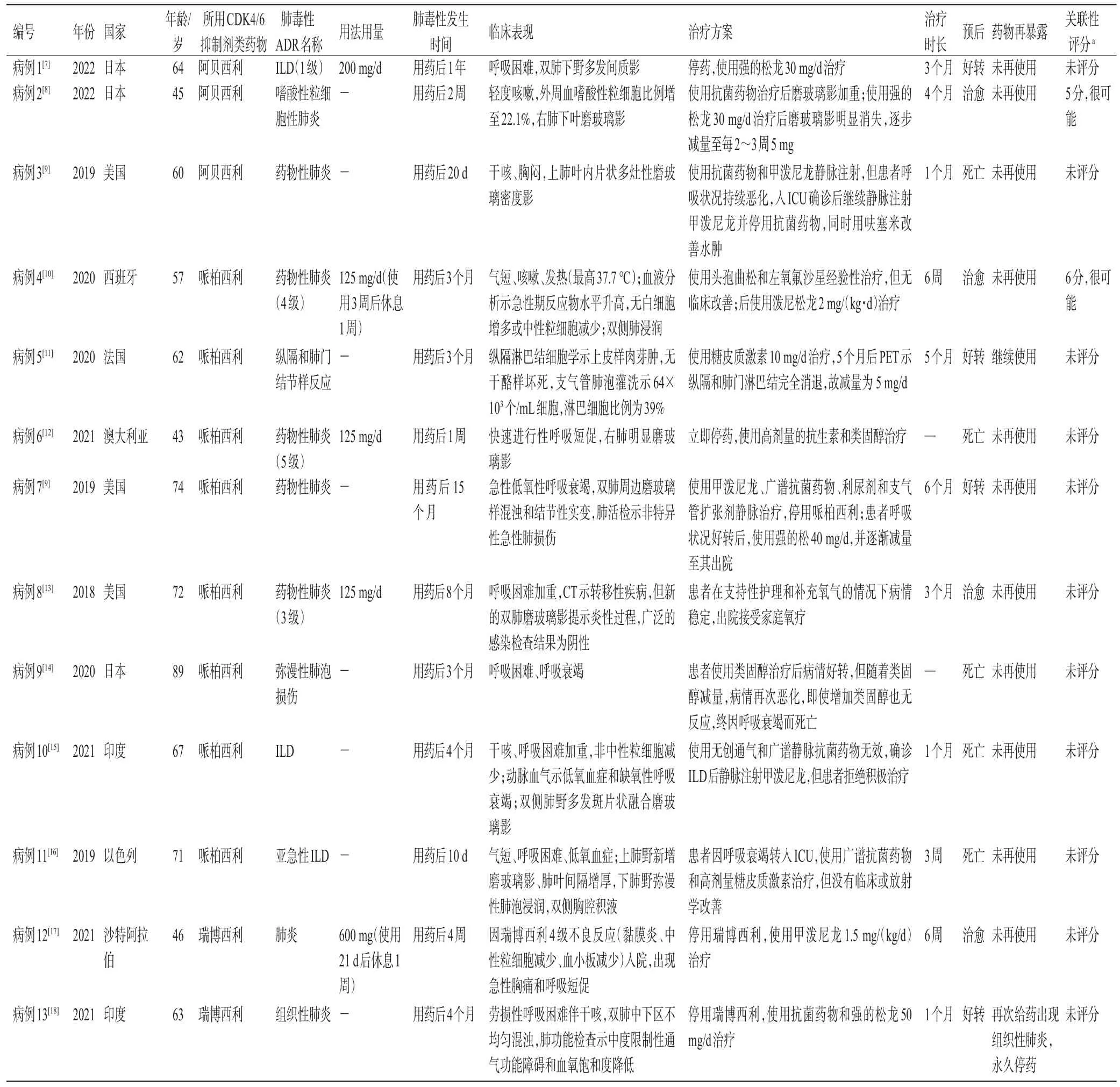
表2 13例患者使用CDK4/6抑制劑后的肺毒性發生情況
2.2.3 治療與轉歸 治療時長最短為3周,最長為6個月。除病例8使用鼻導管吸氧和支持性護理,未提及其他治療方案外,有4例患者(病例1、5、9、12)直接使用類固醇治療,有7例患者(病例2~4、6、10~11、13)起始使用廣譜抗菌藥物治療但未能改善病情甚或病情加重。診斷為肺毒性ADR后的治療措施包括停藥、靜脈使用全身類固醇、吸氧、利尿等。有8例患者好轉或康復,5例患者因病情惡化死亡。5例死亡患者的起病時間在用藥后1周~4個月不等,死亡時間在肺毒性發生后1個月內,其中4例使用哌柏西利,1例使用阿貝西利;5例中有4例(病例3、6、10、11)均接受過廣譜抗菌藥物與類固醇的聯合治療,但病情急劇惡化,余1例(病例9)在類固醇減量后病情惡化。病例3因低氧血癥和高碳酸血癥加重死亡;病例6因嚴重呼吸衰竭和肺功能下降死亡;病例9因呼吸衰竭死亡;病例10拒絕積極治療,因呼吸衰竭死亡;病例11積極治療無改善,因呼吸衰竭死亡。
2.2.4 藥物再暴露 有1例患者(病例13)再次使用瑞博西利又出現藥物相關肺毒性,臨床予以永久停止該類藥物使用。1例縱膈和肺門結節樣反應患者(病例5)繼續使用哌柏西利,未再出現肺毒性相關癥狀。余11例患者均未再使用CDK4/6抑制劑類藥物。
3 討論
藥物相關肺毒性通常被懷疑與暴露于某些藥物、用藥后導致新的肺部毒性癥狀出現以及停用藥物后患者卻出現癥狀緩解有關[19]。藥物相關肺毒性的發生機制包括劑量依賴毒性和免疫介導毒性,細胞毒性或免疫毒性均可獨立或合并發生,成為藥物相關肺毒性的病因[20]。癌癥化療藥物通常被描述為藥物相關肺毒性和組織性肺炎的病因[21]。
目前的乳腺癌臨床實踐指南建議將芳香化酶抑制劑和CDK4/6抑制劑聯合用于絕經后HR+轉移性或復發性乳腺癌的內分泌治療[22]。隨著CDK4/6抑制劑在乳腺癌治療中的廣泛應用,其安全性問題也引起了學者們的重視,已出現該類藥物相關肺毒性的報道[6]。這提示臨床為改善患者預后,有必要早期發現和治療CDK4/6抑制劑引起的肺毒性。
就納入本研究的病例來看,13例患者中有8例使用了哌柏西利,3例使用了阿貝西利,2例使用了瑞博西利,表明現已上市的3種CDK4/6抑制劑均有可能導致藥物相關肺毒性。本研究中哌柏西利的肺毒性發生比例相對較高,可能是因為該藥應用于臨床時間較早、臨床使用率較高且被研究得最多[23]。此外,肺毒性發生時間的長短可能與多種因素相關,如患者年齡、性別、體質量指數、種族、免疫狀態、疾病分期等[24―25]。就本研究來看,肺毒性在用藥后1周~15個月均有可能發生,而3種CDK4/6抑制劑的肺毒性發生時間沒有明顯差異。
本研究中,13例患者中有12例均以呼吸困難、胸悶、氣短、干咳、乏力等癥狀為主訴入院,僅有1例發生低熱(最高37.7 ℃),其余患者均無發熱表現。由此可見,CDK4/6抑制劑的肺毒性起病較為隱匿且為非特異性,易與其他類型肺部疾病相混淆,可能從無癥狀的影像學改變進展到呼吸衰竭,進程較為兇險。據報道,癌癥治療中的藥物性ILD的癥狀通常是非特異性的,最常見的是干咳、乏力和胸痛[26],與本研究納入的病例報道一致。目前,已有文獻報道的ADR標志物涉及皮膚、胃腸道、腎臟、血液、肌肉骨骼等多個系統[27],但肺毒性的預測尚無可用的生物標志物,要想確定CDK4/6抑制劑誘導的肺毒性必須依賴于臨床醫師排除肺部感染、淋巴管炎癌變和心源性肺水腫的診斷[19]。這提示臨床醫師一旦發現使用CDK4/6抑制劑的患者出現呼吸困難、低燒、咳嗽、乏力、胸痛等癥狀,應進行仔細評估并對癥治療。本研究中僅有2例患者進行了不良事件關聯性評估,余11例均未提及關聯性評分。用于評估不良事件因果關系的算法——計分推算法可以幫助統一不同觀察者的不同臨床印象,明確ADR與用藥的關聯程度,從而得出最終的實證診斷結果[28]。臨床藥師作為醫療團隊的一員,應幫助臨床醫師正確執行不良事件因果關系算法,從而確定可疑藥物,減少ADR的發生。
本研究中,13例患者中有5例死亡,占總納入病例數的38.46%,比例較高。其中使用哌柏西利者4例、阿貝西利者1例,分別診斷為藥物性肺炎、彌漫性肺泡損傷、ILD等。死亡時間最短為用藥后1周,最長為用藥后4個月,均在確診治療后1個月內死亡。其中,病例9為一位89歲的高齡患者,確診后開始使用類固醇治療時病情有所好轉,隨著類固醇減量,病情再次惡化,后期即使增加類固醇也無好轉,最終因呼吸衰竭死亡。根據《CDK4/6抑制劑治療激素受體陽性人表皮生長因子受體2陰性晚期乳腺癌的臨床應用共識》,可以遵循以下原則進行治療:(1)若為1級無癥狀,無需調整劑量,根據臨床指征采用適當的藥物干預和監測;(2)若為2級有癥狀,暫停給藥直至恢復至≤1級,降低1個劑量,如果2級再次出現,終止治療;(3)若為3或4級ILD或非感染性肺炎,終止治療[29]。
在納入的13例患者中,有11例均未再使用CDK4/6抑制劑類藥物;1例(病例13)再次使用該類藥物又出現藥物相關肺毒性,須永久停止使用該類藥物治療;1例縱隔和肺門結節樣反應患者(病例5)繼續使用該類藥物,未再出現肺毒性相關癥狀。所納入病例的肺毒性ADR發生級別均較高,需停藥處理。雖然確診病例停用可疑藥物并開始使用類固醇治療[30],但仍可能有難以挽救而死亡的情況發生。
據文獻報道,目前針對新型抗腫瘤藥物(免疫檢查點抑制劑)引起的肺炎主要的管理方法是采用皮質類固醇進行治療[31],CDK4/6抑制劑相關性肺炎可以參考該方案。一旦做出正式診斷,應即刻開始給予高劑量(通常為1~4 mg/kg)的強的松或等量皮質類固醇:對于較低級別(2級)的ILD,強的松劑量為1 mg/(kg/d);對于較高級別(3~4級)的ILD,強的松劑量為2~4 mg/(kg·d)[32]。
本研究納入的1例縱隔和肺門肉芽腫形成的病例(病例5)為該類藥物的首次報道。雖然乳腺癌介導的免疫失調可引起肉芽腫形成[33],但該患者在治療3個月后的第1次PET掃描中未見縱隔和肺門有18氟-脫氧葡萄糖攝取,表明可能是藥物相關的肉芽腫。這提示在使用CDK4/6抑制劑時,應注意區分藥物相關的肉芽腫與免疫失調介導、疾病轉移性進展產生的結節,這也是臨床判斷的一個難點。本研究發現,CDK4/6抑制劑引起的肉芽腫一般為非干酪性肉芽腫,此類肉芽腫經激素治療效果良好,可以繼續使用該類藥物。
綜上所述,CDK4/6抑制劑可引發相關肺毒性反應,有導致患者死亡的可能。臨床工作者在使用該類藥物時應注意其肺毒性的嚴峻性,須早期判斷、及時停藥,并盡早采用給予患者全身類固醇、吸氧等治療措施。但由于本研究納入的文獻均為國外病例報道,且病例數量有限,可能給研究結果帶來一定的偏倚,CDK4/6抑制劑相關肺毒性的具體發生特點及詳細規律還需更多國內外相關研究加以驗證。

