原發免疫性血小板減少癥發生艾曲泊帕治療相關動脈血栓形成1例并文獻復習
陶 紅 陳侃侃 陳秋妮 史玉葉 張麗娟 何正梅 王春玲
南京醫科大學附屬淮安第一醫院血液科,江蘇淮安 223300
免疫性血小板減少癥(primary immune thrombocytopenia,ITP)是一種以免疫介導的血小板破壞過多、生成減少為特征的獲得性出血性疾病[1]。患者可表現為無癥狀,也可表現為輕微的黏膜皮膚出血,嚴重有危及生命的出血[2]。根據最新指南,血小板計數小于30×109/L,可啟動治療[3]。艾曲泊帕是一種口服的促血小板生成素受體激動劑(thrombopoietin receptor agonist,TPO-RA),與巨核細胞上的血小板生成素受體結合從而增加血小板的產生[4],以劑量依賴的方式增加復發或難治性ITP患者的血小板計數[5]。然而,有研究顯示艾曲泊帕治療相關的血栓栓塞發生的風險升高[6],包括靜脈和動脈血栓,但其病理生理和危險因素尚未很好闡明。本文就南京醫科大學附屬淮安第一醫院(我院)收治的1例老年慢性ITP患者在艾曲泊帕治療期間并發3次動脈血栓事件予以報道,并復習相關文獻,以提高對本病及治療的認識。
1 病例資料
患者男性,82歲,因“血小板減少1年余,意識不清4 h”于2021-09-13入住我院。患者2020年8月因多次血常規提示血小板單系明顯減少,在本市某三甲醫院行骨髓檢查提示,有核細胞增生活躍,粒、紅、巨三系增生伴巨核系成熟抑制,抗核抗體、抗可溶性核抗原抗體未見異常,抗凝脂抗體陰性,診斷原ITP,給予丙種球蛋白(山東泰邦,國 藥 準 字 S20013001,規 格:2.5 g∶50 ml/支)400 mg/(kg·d)×5 d聯合醋酸潑尼松(辰欣藥業股份有限公司,國藥準字 H37021900,規格:5 mg/片)1 mg/(kg·d)治療后血小板計數升至正常,因醋酸潑尼松減量至20 mg/d時血小板計數不能維持安全范圍(血小板計數≤20×109/L),于2020-09-12改用艾曲泊帕(英國葛蘭素史克公司,批準文號 H20065432,規格:25 mg/片)25 mg qd長期口服維持治療,血小板計數基本維持在正常范圍,期間予口服阿司匹林(拜耳醫藥保健有限公司,國藥準字J20130078,規格:100 mg/片)100 mg/d。2020-10-24因“右下肢皮溫低伴靜息痛1周”入住我院血管外科,查血常規,白細胞計數7.03×109/L,血紅蛋白106 g/L,血小板計數422×109/L,CT檢查報告(2020-10-26,圖1):右側股動脈下段血栓,于2020-10-27日在全身麻醉下行右下肢動脈取栓術,術后患者右下肢足背及脛后動脈搏動可,術后繼續口服艾曲泊帕25 mg qd,并加用抗凝藥物利伐沙班(吉林省博大偉業制藥有限公司,國藥準字 H20213352,規格:10 mg/片)10 mg/d長期口服,期間監測血小板計數維持在正常范圍。2021-06-01因“右足踝后側疼痛1周”,再次入住我院血管外科,查血常規,白細胞計數5.73×109/L,血紅蛋白141 g/L,血小板計數248×109/L,下肢動脈CT血管造影檢查(2021-06-07,圖2):右下肢動脈血栓閉塞,繼續予以利伐沙班抗凝、阿司匹林抗血小板、擴管等藥物保守治療,患者右下肢癥狀明顯緩解,院外減量口服艾曲泊帕12.5 mg qd,并持續予以利伐沙班抗凝、阿司匹林抗血小板治療,期間監測血小板計數維持在正常范圍。既往史:患者既往有高血壓病史10年,長期口服非洛地平降壓治療,血壓控制基本正常;否認有吸煙史,否認既往有其他血栓病史。此次因患者突發意識不清4 h,急送我院,查體:意識淺昏迷,查體欠合作,測血壓160/70 mmHg(1 mmHg=0.133 kPa),全身皮膚未見明顯瘀點瘀斑,對答不準確,雙側瞳孔等大等圓,直徑2.5 mm,對光反射遲鈍,左側鼻唇溝淺,聽診心肺未聞及異常,腹軟,肝脾肋下未及,左側肢體肌張力減低,左側肢體疼痛刺激無收縮,右側肢體疼痛刺激可見活動,左側腱反射(+++),右側腱反射(++),左側巴賓斯基征陽性,腦膜刺激陰性。進一步查血常規:白細胞計數9.62×109/L,血紅蛋白137 g/L,血小板計數185×109/L;頭顱CT血管造影檢查(2021-09-13,圖3)提示:右側大腦中動脈閉塞。2021-09-14給予顱內血管血栓去除術、腦動脈內溶栓術,并予康復治療,病情穩定后給予持續抗凝及抗血小板聚集治療,艾曲泊帕減量至12.5 mg qod口服,隨訪至今(2021-12-30)暫未再次出現血栓事件,期間監測血常規提示血小板計數基本維持于正常范圍。
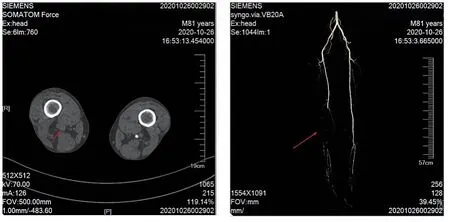
圖1 2020-10-26下肢CT血管造影檢查
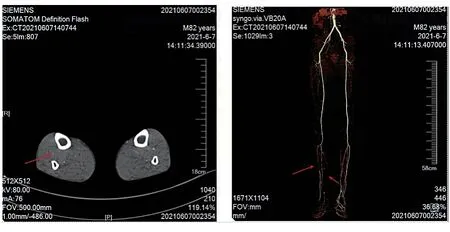
圖2 2021-06-07下肢CT血管造影檢查

圖3 2021-09-13頭顱CT血管造影檢查
2 討論
ITP患者以血小板減少為主要特點,出血為主要表現,但有研究報道ITP患者的血栓事件發病率有升高趨勢,Rodeghiero[7]研究發現ITP患者動脈血栓發生率為1.14%~4.1%。也有學者研究ITP血栓發生情況,結果提示ITP合并動脈血栓發生率為1.12%,并發現ITP本身也可能是可伴發血栓的一類疾病,年齡、吸煙、高血壓病、糖尿病、脾切除、抗磷脂抗體陽性等為血栓發生的危險因素[8-10]。Ito等[11]研究發現ITP患者10年累積血栓發生率為10%,單因素分析顯示,吸煙、高血壓、男性、血栓形成史、房顫與血栓的發生顯著相關,多因素分析發現吸煙和房顫是獨立的危險因素。Ekstrand等[12]研究發現年齡和男性是ITP合并動脈血栓形成最重要的危險因素。ITP患者本身由于未成熟血小板(immature platelet fraction,IPF)的升高,血小板的異常激活,也進一步增加了血栓形成的風險[13]。在ITP發病過程中幼稚巨核細胞增加導致凝血因子過度表達,導致高凝狀態,亦有助于血栓形成[14]。
本研究中ITP患者為老年男性,有高血壓病史,本身即存在血栓形成的危險因素,使用艾曲泊帕治療后,并發3次血栓事件,提示艾曲泊帕的使用可能進一步促使血栓事件的發生。艾曲泊帕屬于TPO-RA,主要通過裂解、氧化及與葡萄糖醛酸結合等途徑代謝,其中參與葡萄糖醛酸化的主要代謝酶為UGT1A1和UGT1A3,參與其氧化代謝的主要是CYP1A2和CYP2C8。通過上調慢性ITP患者糖蛋白Ⅵ(glycoprotein Ⅵ,GPⅥ)的表達來增強血小板黏附,還可通過與血小板生成素受體結合,誘導巨核細胞分化,從而促進血小板的產生[15],主要用來治療ITP和再生障礙性貧血。艾曲泊帕的藥代動力學特點存在種族差異性,可能與不同種族人群間的基因多態性和等位基因的頻率差異有關,研究顯示,中國和高加索人群相比,CYP1A2、UGT1A3酶活性更低[16-17];亞裔和非亞裔人群相比,CYP2C8及UGT1A1的酶活性更低[18-19]。所以針對亞裔人群,艾曲泊帕的清除率相對較低,是否提示低清除率與血栓發生率相關有待進一步探究,對于亞裔患者的給藥劑量在臨床實踐中亦有待進一步研究。
隨著TPO-RA的應用,有研究發現,相對于對照組,艾曲泊帕可導致血栓發生率升高,且大部分血栓事件發生在使用艾曲泊帕治療后的第一年[20]。盡管確切的病理機制尚不明確,但艾曲泊帕治療后血小板的過度活化可能是原因之一[15]。然而因缺乏足夠的證據,針對使用促血小板生成素受體激動劑艾曲泊帕治療的ITP患者血栓風險是否增加,各個研究結論不一[7]。目前還沒有大型的臨床隨機研究將接受促血小板生成素受體激動劑治療的ITP患者與對照組ITP患者進行比較,以檢測血栓形成率的臨床相關差異。
本例患者出院后持續減量口服艾曲泊帕維持血小板計數并持續口服利伐沙班抗凝、阿司匹林抗血小板聚集治療,至末次隨訪未再出現血栓事件,但是否可以提示適度的減量口服艾曲泊帕,使血小板計數波動在一定水平,并同時使用抗凝藥物治療可以減輕艾曲泊帕的血栓風險仍不清楚。在ITP背景下,關于動脈血管疾病的管理及治療證據尚缺乏,現有的文獻也主要局限于病例報告和一些小型病例研究。對于既往有血栓病史的ITP患者,應避免使用TPO-RA,需優先考慮其他治療策略[21]。在ITP患者開始TPO-RA治療前,需仔細評估血栓風險,血栓形成時需進行取栓、溶栓、抗凝等治療,如同時合并血小板計數低下,有可能會加重出血,故權衡利弊,綜合患者的年齡、基礎疾病、有無合并癥及出血風險等進行個體化治療可能為當前主要的治療策略。

