菟絲子總黃酮中擬雌激素作用的活性成分篩選 Δ
岳 霞,宋 輝,徐 媛,劉迪施,孫向明 ,李文蘭(哈爾濱商業(yè)大學(xué)藥學(xué)院,哈爾濱 150076)
菟絲子為旋花科植物南方菟絲子Cuscuta australisR.Br.或菟絲子Cuscuta chinensisLam.的干燥成熟種子,其用藥歷史悠久,為補益類常用中藥[1],具有補腎益精、安胎明目等多種功效[2]。近年來,多項研究發(fā)現(xiàn)菟絲子在激素調(diào)節(jié)[3]、保肝明目[4]、保護(hù)心腦血管[5]、抗癌[6]和抗衰老[7]等方面表現(xiàn)出一定的藥理療效。菟絲子植物分布廣泛,主要分布于黑龍江、內(nèi)蒙古、甘肅、山東等地,學(xué)者們從菟絲子中已提取出多類化學(xué)成分,如黃酮類、生物堿類、木質(zhì)素類、有機酸類和其他成分等[8―9]。
當(dāng)婦女進(jìn)入更年期后,各類雌激素指標(biāo)驟然下降,從而出現(xiàn)月經(jīng)失調(diào)、煩悶易怒、入睡困難等更年期癥狀,雌激素替代療法可以使更年期癥狀得到明顯改善;但長期使用人工合成的雌激素易對身體造成極大的損傷,如心腦血管損傷、腎臟損傷以及其他疾病等[10]。為此,科學(xué)家們不斷尋求更為安全、有效的雌激素替代物。目前,國內(nèi)外已有多種關(guān)于選擇性雌激素受體調(diào)節(jié)劑和其他輔助藥的報道,其中尤為重要的一類藥物就是植物雌激素[11―12],其被認(rèn)為是一種更安全、更有前途的雌激素替代品。
本課題組前期研究表明,菟絲子醇提物有顯著的擬雌激素活性,且其擬雌激素活性成分多為黃酮類[13]。本研究首先對菟絲子總黃酮的擬雌激素作用進(jìn)行驗證,建立10批菟絲子總黃酮的指紋圖譜;然后以小鼠子宮系數(shù)、子宮內(nèi)膜厚度為指標(biāo)對共有峰進(jìn)行活性檢識,再采用超高效液相色譜串聯(lián)四極桿飛行時間質(zhì)譜(UPLC?Q?TOF?MS)技術(shù)對菟絲子總黃酮成分進(jìn)行表征,明確菟絲子總黃酮中擬雌激素作用的活性成分,以期為植物雌激素類藥物的開發(fā)提供參考。
1 材料
1.1 主要儀器
本研究所用主要儀器有LE2O4E/O2型電子分析天平(瑞士Mettler Toledo公司),Acquity型超高效液相色譜(UPLC)儀、PGA495型質(zhì)譜儀(美國Waters公司),CKX53型倒置顯微鏡(日本Olympus公司),YN?02B1型生物組織包埋機(深圳市永年科技有限公司)等。
1.2 主要藥品與試劑
綠原酸、山柰酚、槲皮素、異鼠李素、槲皮苷、芹菜素對照品(批號分別為 20160312、20130621、20151225、20160615、20150813、20170224,純度≥98%)均購自中國食品藥品檢定研究院;金絲桃苷對照品(純度≥98%,批號111521?201903)購自上海金穗生物有限公司;戊酸雌二醇(陽性對照藥,批號20191038)購自拜耳醫(yī)藥保健有限公司;蘇木素染液、伊紅染液(批號分別為20190504、20190103)購自北京索萊寶生物科技公司。菟絲子藥材(編號S1~S10)購自不同的菟絲子種植基地,經(jīng)哈爾濱商業(yè)大學(xué)藥學(xué)院曲中原教授鑒定為旋花科植物南方菟絲子C.australisR.Br.或菟絲子C.chinensisLam.的干燥成熟種子,其藥材產(chǎn)地信息見表1。

表1 菟絲子藥材產(chǎn)地信息
1.3 動物
本研究所用動物為雌性未成年ICR小鼠,體質(zhì)量為(10±2) g,購自長春國家生物產(chǎn)業(yè)基地實驗動物中心,動物生產(chǎn)許可證號為SCXK(吉)?2020?0002。本實驗經(jīng)哈爾濱商業(yè)大學(xué)實驗動物倫理委員會批準(zhǔn),批準(zhǔn)號為HSDYXY?2020005。
2 方法與結(jié)果
2.1 樣品的制備
2.1.1 陽性對照藥混懸液的制備 取戊酸雌二醇適量,用蒸餾水配制質(zhì)量濃度為0.01 mg/mL的混懸液,備用。
2.1.2 供試品溶液的制備 分別稱取10個不同產(chǎn)地菟絲子藥材適量,粉碎過篩,按文獻(xiàn)[13]方法制備總黃酮浸膏(以蘆丁計,總黃酮的純度為29.84%~31.68%)。取菟絲子總黃酮浸膏1 g,用80%甲醇溶解并定容于10 mL容量瓶中,從中取1 mL溶液轉(zhuǎn)移至5 mL容量瓶中,以80%甲醇定容,過0.22 μm微孔濾膜,即得供試品溶液,備用。
2.1.3 對照品溶液的制備 分別精密稱取綠原酸、金絲桃苷、山柰酚、槲皮素、槲皮苷、異鼠李素、芹菜素對照品適量,以80%甲醇溶解,并定容于10 mL容量瓶中,過0.22 μm微孔濾膜,即得混合對照品溶液。
2.2 菟絲子總黃酮擬雌激素作用考察
2.2.1 分組與給藥 將小鼠隨機分為空白對照組、陽性對照組(戊酸雌二醇,0.075 mg/kg,劑量根據(jù)本課題組前期預(yù)實驗結(jié)果設(shè)置)和不同產(chǎn)地(S1~S10)菟絲子總黃酮組(8 g/kg,以菟絲子生藥量計,劑量根據(jù)本課題組預(yù)實驗結(jié)果設(shè)置),每組10只。給藥組小鼠灌胃相應(yīng)藥物,空白對照組灌胃等體積蒸餾水,每天早晚各給藥1次,連續(xù)4 d。
2.2.2 小鼠子宮系數(shù)和子宮內(nèi)膜厚度的檢測 末次給藥1 h后,將各組小鼠脫頸處死,剖取子宮,稱定質(zhì)量,并計算子宮系數(shù)(子宮系數(shù)=子宮質(zhì)量/體質(zhì)量×100%)。將子宮置于10%甲醛溶液中固定1~2 d,再進(jìn)行組織包埋、切片、染色、脫水、膠封,采用顯微鏡觀察小鼠子宮特征變化,并測量子宮內(nèi)膜厚度。采用SPSS 19.0軟件對數(shù)據(jù)進(jìn)行統(tǒng)計分析,數(shù)據(jù)均以±s表示,多組間比較采用單因素方差分析,組間兩兩比較采用LSD?t檢驗。檢驗水準(zhǔn)α=0.05。結(jié)果顯示,與空白對照組相比,陽性對照組和S1~S10菟絲子總黃酮組小鼠子宮系數(shù)和子宮內(nèi)膜厚度(S3、S7菟絲子總黃酮組除外)均顯著增加(P<0.05或P<0.01)。空白對照組子宮內(nèi)膜上皮、間質(zhì)、腺體無增生,肌層排列緊密,子宮內(nèi)膜壁薄,無明顯增厚及突出。陽性對照組和S1~S10菟絲子總黃酮組小鼠子宮內(nèi)膜增厚明顯,內(nèi)膜上皮由低柱狀形態(tài)進(jìn)展為高柱狀形態(tài),內(nèi)膜間質(zhì)疏松。結(jié)果見圖1~圖3。

圖1 各組小鼠子宮系數(shù)的檢測結(jié)果(±s,n=10)
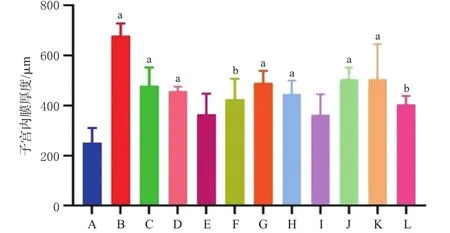
圖2 各組小鼠子宮內(nèi)膜厚度的檢測結(jié)果(±s,n=10)

圖3 各組小鼠子宮HE染色結(jié)果 (×200)
2.3 不同產(chǎn)地菟絲子總黃酮的指紋圖譜建立
2.3.1 色譜條件 色譜柱為Agilent Eclipse Plus C18R RHD(3.0 mm×150 mm,1.8 μm);保護(hù)柱為ACQUITY UPLC R BEH C18;柱溫為 40 ℃;流速為 0.3 mL/min;進(jìn)樣量為2 μL;流動相為0.1%甲酸溶液(A)?乙腈溶液(B),梯度洗脫(0~2 min,10%B→19%B;2~5 min,19%B;5~6 min,19%B→44%B;6~14 min,44%B→60%B;14~19 min,60%B→95%B;19~20 min,95%B→100%B)。
2.3.2 質(zhì)譜條件 采用電噴霧離子源,電壓為3.0 kV,溫度為100 ℃,去溶劑氣溫度為400 ℃,去溶劑氣流速為800 L/h,錐孔氣流速為50 L/h。采用正負(fù)離子模型進(jìn)行掃描,掃描范圍為m/z50→1 200,碰撞能為20~45 mV。
2.3.3 精密度試驗 取“2.1.2”項下供試品溶液適量,按“2.3.1”“2.3.2”項下色譜與質(zhì)譜條件連續(xù)進(jìn)樣6次,正離子模式選取13號峰(槲皮素)作為參照峰,負(fù)離子模式選取23號峰(槲皮素)作為參照峰,記錄各共有峰相對峰面積和相對保留時間。結(jié)果顯示,兩種模式下各共有峰相對峰面積的RSD均小于3.0%,相對保留時間的RSD均小于2.5%(n=6),表明儀器精密度良好。
2.3.4 重復(fù)性試驗 按“2.1.2”項下方法制備6份供試品溶液,按“2.3.1”“2.3.2”項下色譜與質(zhì)譜條件進(jìn)行檢測,正離子模式選取13號峰作為參照峰,負(fù)離子模式選取23號峰作為參照峰,記錄各共有峰相對峰面積和相對保留時間。結(jié)果顯示,兩種模式下各共有峰相對峰面積的RSD均小于3.0%,相對保留時間的RSD均小于2.5%(n=6),表明方法重復(fù)性良好。
2.3.5 穩(wěn)定性試驗 取“2.1.2”項下供試品溶液適量,于室溫放置0、3、6、8、12、24 h時按“2.3.1”“2.3.2”項下色譜與質(zhì)譜條件進(jìn)行檢測,正離子模式選取13號峰作為參照峰,負(fù)離子模式選取23號峰作為參照峰,記錄各共有峰相對峰面積和相對保留時間。結(jié)果顯示,兩種模式下各共有峰相對峰面積的RSD均小于3.0%,相對保留時間的 RSD均小于3.0%(n=6),表明樣品穩(wěn)定性良好。
2.3.6 指紋圖譜的建立 取“2.1.2”項下供試品溶液適量,按“2.3.1”“2.3.2”項下色譜與質(zhì)譜條件進(jìn)樣分析,記錄色譜圖。采用《中藥色譜指紋圖譜相似度評價系統(tǒng)(2004A版)》對10批不同產(chǎn)地菟絲子總黃酮的指紋圖譜進(jìn)行分析,生成正負(fù)離子模式下的對照指紋圖譜(R)和疊加指紋圖譜。如圖4所示,正、負(fù)離子模式下分別標(biāo)出28、33個共有峰。
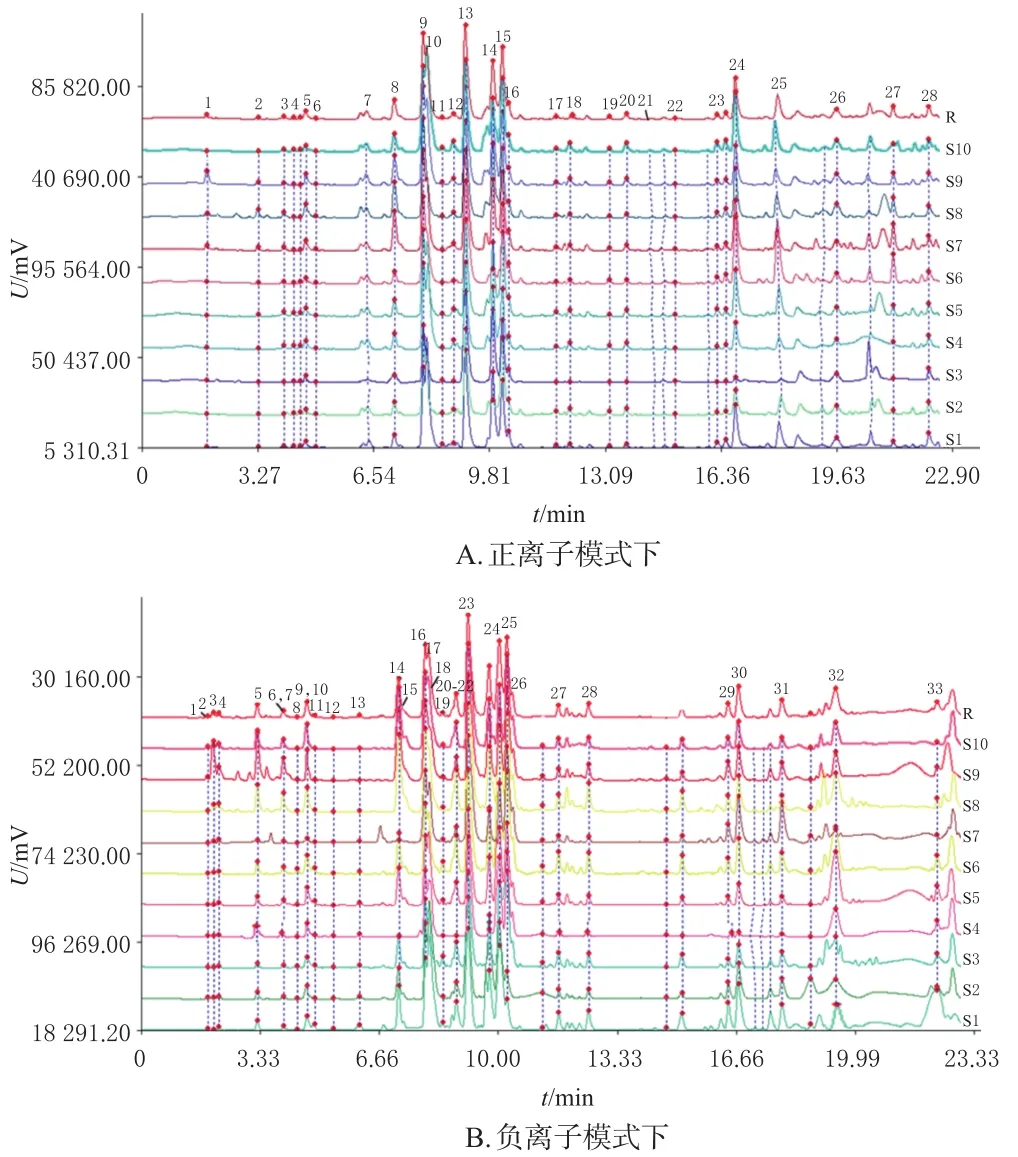
圖4 正負(fù)離子模式下不同產(chǎn)地菟絲子總黃酮的疊加指紋圖譜及對照圖譜(R)
2.4 不同產(chǎn)地菟絲子總黃酮的譜?效相關(guān)性分析
2.4.1 雙變量相關(guān)性分析 采用SPSS 19.0軟件進(jìn)行分析,將10批不同產(chǎn)地菟絲子總黃酮的共有峰相對峰面積進(jìn)行均值化處理后,以小鼠子宮系數(shù)、子宮內(nèi)膜厚度為變量,進(jìn)行雙變量相關(guān)性分析,并計算Pearson相關(guān)系數(shù),其絕對值越大表明相關(guān)性越好。結(jié)果顯示,在正離子模式下,有10個共有峰與菟絲子總黃酮的擬雌激素作用相關(guān)(P<0.05),分別是7、10、12~16、18、22、26號峰。在負(fù)離子模式下,有14個共有峰與菟絲子總黃酮的擬雌激素作用有關(guān)(P<0.05),分別是2、5、8、9、12、16、19、22~28號峰。
2.4.2 灰色關(guān)聯(lián)度分析 采用DPS軟件進(jìn)行分析,將10批不同產(chǎn)地菟絲子總黃酮的共有峰相對峰面積進(jìn)行均值化處理后,以此為子序列,再以小鼠子宮系數(shù)、子宮內(nèi)膜厚度為母序列,可得到子序列與相應(yīng)母序列的關(guān)聯(lián)度,將其按從大到小的順序排列級組成關(guān)聯(lián)序,通過關(guān)聯(lián)度排序結(jié)果,判斷各子序列對母序列的“貢獻(xiàn)”程度。通常認(rèn)為關(guān)聯(lián)度>0.5即存在關(guān)聯(lián),關(guān)聯(lián)度越大關(guān)聯(lián)性越好[14―15]。本研究選擇關(guān)聯(lián)度大于0.6的成分作為高度相關(guān)的成分。結(jié)果顯示,正離子模式下,有19個共有峰的關(guān)聯(lián)性較強,分別是3、5、7~17、19、20、24~26、28號峰。負(fù)離子模式下,有21個共有峰的關(guān)聯(lián)性較強,分別是2、5、7~9、11~17、19~26、31號峰。
2.4.3 綜合分析 將“2.4.1”“2.4.2”項下正負(fù)離子模式下的結(jié)果取交集發(fā)現(xiàn),正離子模式下的7、10、12~16、26號峰及負(fù)離子模式下2、5、8、9、12、16、19、22~26號峰所代表的成分與菟絲子總黃酮的擬雌激素作用高度相關(guān)。
2.5 菟絲子總黃酮成分的表征
由于樣本S9在正、負(fù)離子模式下所呈現(xiàn)的化學(xué)成分均較為全面,因此取S9樣品的供試品溶液和“2.1.3”項下混合對照品溶液,按“2.3.1”“2.3.2”項下色譜與質(zhì)譜條件進(jìn)樣分析,即得菟絲子總黃酮供試品溶液及混合對照品的總離子流圖(圖5)。采用Waters Masslynx V 4.1軟件對正、負(fù)離子模式下的總離子流圖進(jìn)行處理,獲取各共有峰的保留時間及一、二級質(zhì)譜信息,根據(jù)精確的準(zhǔn)分子離子峰的m/z初步判斷化合物的相對分子質(zhì)量、元素組成和分子式,并與對照品及自建數(shù)據(jù)庫中各化學(xué)成分的信息進(jìn)行比對,同時參考各類化合物的裂解規(guī)律[16―20],根據(jù)碎片離子信息推測化合物。結(jié)果見表2。

圖5 菟絲子總黃酮供試品溶液及混合對照品的總離子流圖

表2 菟絲子總黃酮中各色譜峰的化學(xué)成分分析結(jié)果
由表2可知,菟絲子總黃酮中共有16個擬雌激素活性成分,分別為5,7,3′,4′?四甲氧基黃酮、6?O?(反式)對香豆酰基?呋喃果糖?(2→1)?吡喃葡萄糖苷、蘆丁、山柰酚?3,7?雙葡萄糖苷、芹菜素?7?O?葡萄糖苷、金絲桃苷、紫云英苷、槲皮苷、槲皮素、芹菜素、山柰酚、異鼠李素、杜鵑黃素、異槲皮苷、山柰酚?3?呋喃阿拉伯糖苷、2,6?十八碳二炔酸。
3 討論
目前,可利用乳腺癌細(xì)胞增殖率、動物血清中雌激素含量、雌激素受體的蛋白和mRNA表達(dá)水平、子宮系數(shù)、子宮內(nèi)膜厚等指標(biāo)來評價擬雌激素作用[21―22]。結(jié)合本課題組前期預(yù)實驗結(jié)果,發(fā)現(xiàn)采用小鼠子宮系數(shù)和子宮內(nèi)膜厚度這2個指標(biāo)進(jìn)行評價,可更好地反映雌激素樣效果。本研究結(jié)果發(fā)現(xiàn),不同產(chǎn)地菟絲子總黃酮的擬雌激素活性均較好。進(jìn)一步在正負(fù)離子模式下建立不同產(chǎn)地菟絲子總黃酮的指紋圖譜,發(fā)現(xiàn)在正、負(fù)離子模式下共有28、33個共有峰。結(jié)合雙變量相關(guān)性分析和灰色關(guān)聯(lián)度分析發(fā)現(xiàn),正離子模式下的7、10、12~16、26號峰及負(fù)離子模式下2、5、8、9、12、16、19、22~26號峰所代表的成分與菟絲子總黃酮的擬雌激素作用高度相關(guān)。經(jīng)化學(xué)成分鑒定發(fā)現(xiàn),這16個成分分別為5,7,3′,4′?四甲氧基黃酮、6?O?(反式)對香豆酰基?呋喃果糖?(2→1)?吡喃葡萄糖苷、蘆丁、山柰酚?3,7?雙葡萄糖苷、芹菜素?7?O?葡萄糖苷、金絲桃苷、紫云英苷、槲皮苷、槲皮素、芹菜素、山柰酚、異鼠李素、杜鵑黃素、異槲皮苷、山柰酚?3?呋喃阿拉伯糖苷、2,6?十八碳二炔酸。相關(guān)研究發(fā)現(xiàn),蘆丁能夠提高雌性青春期大鼠雌二醇、孕酮水平,促進(jìn)催乳素、生長激素分泌,上調(diào)乳腺組織中雌激素受體、孕激素受體、催乳素受體和生長激素受體的表達(dá)量,促進(jìn)乳腺發(fā)育[23]。也有研究表明,槲皮素在雌激素相關(guān)疾病中的作用機制呈多元化,主要包括抗氧化作用,調(diào)控雌激素代謝,調(diào)節(jié)雌激素受體及其下游信號通路等[24]。
綜上所述,本研究從菟絲子總黃酮中篩選出16種擬雌激素作用的化學(xué)成分,可為植物雌激素類藥物的開發(fā)提供參考。

