5種單克隆抗體預防視神經脊髓炎譜系疾病復發的有效性網狀Meta分析及安全性評價 Δ
關茗元 ,王婷 ,段冉冉 ,李瑩 (.鄭州大學第一附屬醫院藥學部,鄭州 45005;.鄭州大學第一附屬醫院神經內科,鄭州 45005)
視神經脊髓炎譜系疾病(neuromyelitis optica spec‐trum disorder,NMOSD)是一種發作于中樞神經系統,由免疫介導的嚴重脫髓鞘及軸突損傷累及視神經和脊髓導致的炎性疾病,其臨床特征包括急性發作的雙側或短時間內相繼出現的視神經炎或橫貫性脊髓炎[1]。一項2021年的研究搜集了33篇相關領域文獻,發現NMOSD在不同地域及人群中的發病率為每年0.037/100 000~10/100 000,符合WHO關于罕見病發病率0.65‰~1‰的標準[2]。NMOSD的自然病程是反復發作和累積殘疾所致的逐步惡化,將給患者帶來不可逆的殘疾,并可造成其生命質量的下降[3]。可見,選用適宜的藥物治療方案對于預防疾病復發、減少疾病反復發作致神經功能障礙累積、有效改善患者生命質量有著十分積極的作用。
本研究納入的5種預防NMOSD復發的藥物選自《中國視神經脊髓炎譜系疾病診斷與治療指南(2021年版)》,分別為:(1)薩特利珠單抗,一種人源化免疫球蛋白G(immunoglobulin G,IgG)2亞型重組抗白細胞介素6受體(interleukin?6 receptor,IL?6R)單克隆抗體,為A級推薦;(2)利妥昔單抗,一種人鼠嵌合型白細胞分化抗原20(cluster of differentiation 20,CD20)單克隆抗體,為A級推薦;(3)托珠單抗,一種以IL?6R為靶點的單克隆抗體,為B級推薦;(4)伊奈利珠單抗:一種人源化的IgG亞型CD19單克隆抗體,為A級推薦;(5)依庫珠單抗:一種人源化的IgG2/4單克隆抗體,用作終端補體蛋白C5抑制劑,為A級推薦[4]。
就罕見病而言,能夠納入臨床研究的受試者非常有限,“頭對頭”研究或以安慰劑為對照的直接比較研究開展難度較高;同時,由于結局指標及分析方法的不一致,間接比較的應用亦存在一定難度。基于Gibbs采樣的貝葉斯網狀Meta分析是一種較為可靠的間接比較方法,可通過參數取樣迭代來獲取效應量及其他相關參數的后驗分布[5]。基于此,本研究擬通過該方法實現對上述5種單克隆抗體預防NMOSD復發有效性的間接比較,并進行安全性評價,以期為醫療決策提供證據。
1 資料與方法
1.1 納入與排除標準
根據 PICOS(population,intervention,comparison,outcomes and study)方法定義文獻的納入標準,并結合國際藥物經濟學與結果研究學會(International Society for Pharmacoeconomics and Outcomes Research,ISPOR)的方法學指導原則[6]來判斷納入文獻是否能夠開展間接比較研究。
1.1.1 研究對象 本研究納入診斷為NMOSD的患者,診斷標準參考文獻[1,7-8]。
1.1.2 干預措施 本研究納入使用上述5種單克隆抗體作為干預措施的研究。
1.1.3 對照措施 本研究納入使用安慰劑或其他可進行間接比較的治療方案。
1.1.4 結局指標 參考抗多發性硬化(multiple sclerosis,MS)藥物的無疾病活動證據3 (no evidence of disease activity?3,NEDA?3)治療目標[9]和已有研究的結局設計,采用以下4個指標作為本研究納入文獻的結局提取和間接比較對象:(1)復發風險評價方面,選用以首次復發為結局指標得到的風險比(hazard ratio,HR);(2)復發率評價方面,選用年復發率(annualized relapse rate,ARR);(3)殘疾進展評價方面,選用治療前后擴展殘疾狀態量表(expanded disability status scale,EDSS)評分變化;(4)安全性評價方面,選用不良事件(adverse event,AE)與嚴重不良事件(serious adverse event,SAE)報告情況。
1.1.5 研究類型 本研究納入隨機對照試驗(rando?mized controlled trial,RCT)。
1.1.6 排除標準 本研究的排除標準包括:(1)結局數據不完整或不能納入統計分析的文獻;(2)重復發表的文獻及會議摘要;(3)非中、英文文獻。
1.2 文獻檢索策略
英文文獻通過檢索Embase、Medline、PubMed數據庫獲取,并結合檢索臨床試驗注冊數據庫ClinicalTrials.gov、UMIN Clinical Trials Registry進行補充;中文文獻通過檢索中國知網獲取,并結合檢索中國臨床試驗注冊中心進行補充。檢索時限為各數據庫建庫起至2022年4月。采用主題詞與自由詞結合的方式進行檢索。中文檢索詞包括:視神經脊髓炎、利妥昔單抗、托珠單抗、伊奈利珠單抗、薩特利珠單抗、依庫珠單抗、臨床試驗等;英文檢索詞以Embase數據庫為例,具體檢索策略見圖1。

圖1 Embase數據庫檢索策略(示例)
1.3 文獻篩選、資料提取
2位研究者從數據庫中將文獻標題、摘要、作者等信息導出至EndNote 20軟件,并獨立對文獻進行篩選、資料提取及交叉核對,如產生分歧則咨詢第3位研究者協助判斷。如有多項文獻對同一研究進行報告,則僅保留涵蓋所有指標的文獻。若數據有缺失則發送郵件咨詢通信作者。
1.4 納入研究的偏倚風險評價
根據Cochrane風險偏倚評估工具對各項研究的隨機序列產生、分配隱藏、參與者與受試者盲法、結果評估盲法、結局完整性、是否選擇性報告以及其他偏倚共7個維度進行評估[10]。
1.5 統計學方法
1.5.1 數據的轉換 對于僅報告Kaplan?Meier曲線的研究,使用Machin等[11]發表的方法進行適宜的數據轉換,以獲取HR及相應的95%置信區間(confidence inter‐val,CI)。
1.5.2 模型的選取及應用 應用OpenBUGS(3.2.3 rev1012版本)軟件進行統計分析,模型代碼來自Dias等[12]和Woods等[13]研究中的隨機效應模型。視輸入變量的取值范圍對研究間模糊先驗標準差(SD)進行調整。通過監控總殘差(totresdev)評價模型的擬合水平,并通過監控SD評價研究間差異。根據Salanti等[14]描述的方法繪制累積概率曲線圖(cumulative ranking probability plots)并計算累積排序概率曲線下面積(surface under the cumulative ranking curve,SUCRA),從而獲得各干預措施對結局指標的干預效果排序,其值越大,說明干預效果越具有優勢。模型使用3條馬爾可夫鏈進行模擬,迭代次數為100 000次,退火次數為50 000次,通過Auto Cor圖形監控鏈的收斂水平,以圖形末端趨向于0且視覺觀察不能識別任一條鏈的迭代過程表示收斂水平較高,收斂性良好。同時,計算結局指標的比較結果及95%可信區間(credible interval,CrI)。
1.5.3 安全性評價 不良反應發生風險方面,如文獻提供了統計學檢驗結果則以文獻的報告為標準,如未提供則應用SPSS 25軟件計算AE及SAE的RR及95%CI,并進行χ2檢驗,如觀察輸出雙側P<0.05則說明差異有統計學意義。
2 結果
2.1 文獻檢索結果
共檢索出相關文獻507篇,經過逐層篩選后,最終納入文獻 8篇[15―22],涉及7項RCT,793例患者。在研究Cree等[21]中,EDSS評分指標取自Marignier等[22]的研究成果,其余指標取自Cree等[21]的研究,后文以Cree等表示。檢索流程及結果如圖2所示。
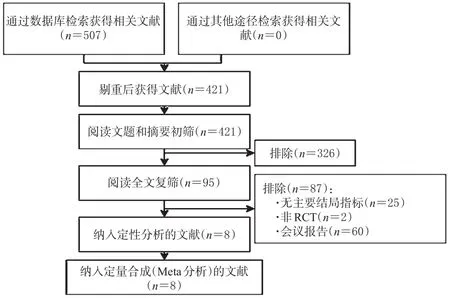
圖2 文獻篩選流程及結果
2.2 納入研究的基本特征與偏倚風險評價結果
納入研究的基本特征見表1,偏倚風險評價結果見表2。
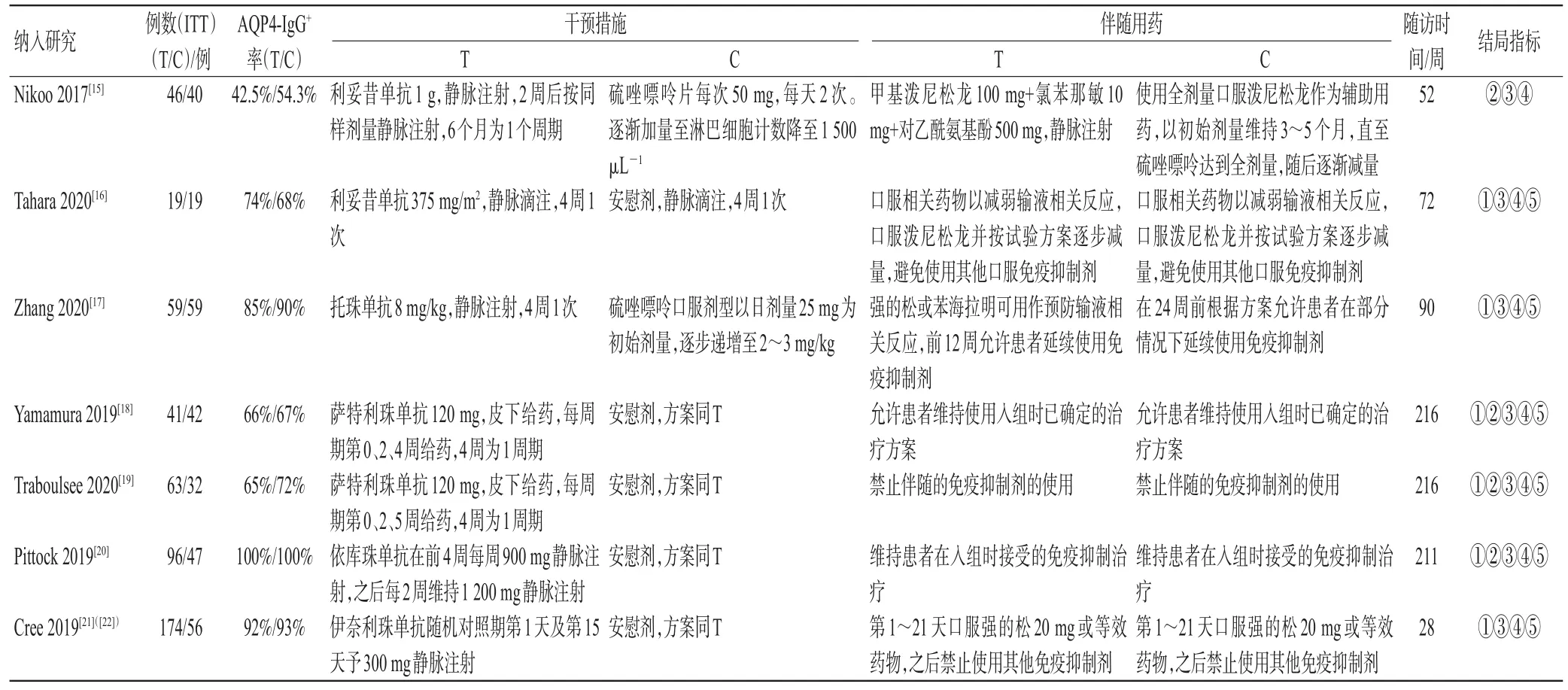
表1 納入研究的基本特征
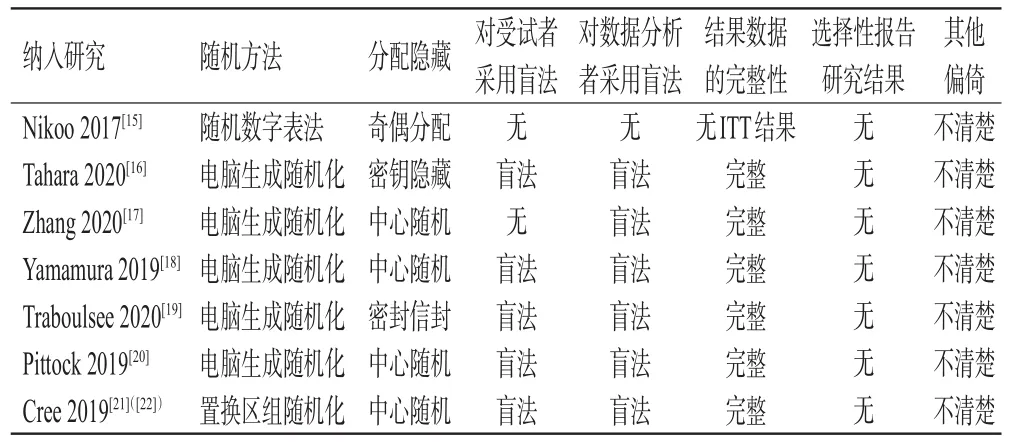
表2 納入研究的偏倚風險評價
2.3 網狀Meta分析結果
2.3.1 鏈的收斂性評估及一致性檢驗 納入研究的3項結局指標經100 000次迭代后,Auto Cor圖形曲線末端趨向于0并到達穩定,提示馬爾可夫鏈收斂性良好。各項干預措施間缺乏直接比較,未能形成閉環,故采用一致性模型進行比較[23―24]。
2.3.2 各指標直接比較結果 直接比較結果表明,5種單克隆抗體與其對照組比較,在降低復發風險、減緩殘疾進展和降低ARR方面差異均有具有統計學意義。對Yamamura等[18]和Traboulsee等[19]進行直接Meta分析,結果顯示,兩組患者的復發風險[HR=0.42,95%CI(0.25,0.72),P=0.76]和 ARR[MD=-0.22,95%CI(-0.36,-0.08),P=0.84]兩項指標的定量合成無統計學異質性;在殘疾進展指標上則異質性較大(P=0.02),遂采用隨機效應模型,結果顯示,試驗組與對照組比較,差異無統計學意義[MD=-0.26,95%CI(-0.73,0.21),P=0.270 3]。
2.3.3 復發風險的網狀Meta分析結果 共6項RCT[16―21]報告了以復發為結局指標的 Kaplan?Meier曲線,其中Tahara等[16]僅報告了Log?rank檢驗的結果,使用Mantel?Haenszel法進行數據轉換得到 HR 為 0.12,SE(lgHR)為0.76。Zhang等[17]的結果由于缺乏一致的對照所以無法進行間接比較。網狀關系圖如圖3A所示。計算SUCRA(圖4A)得到以下排序:依庫珠單抗(92.00%,為SUCRA,下同)>利妥昔單抗(72.84%)>伊奈利珠單抗(50.29%)>薩特利珠單抗(33.36%)。網狀Meta分析結果如圖5所示。
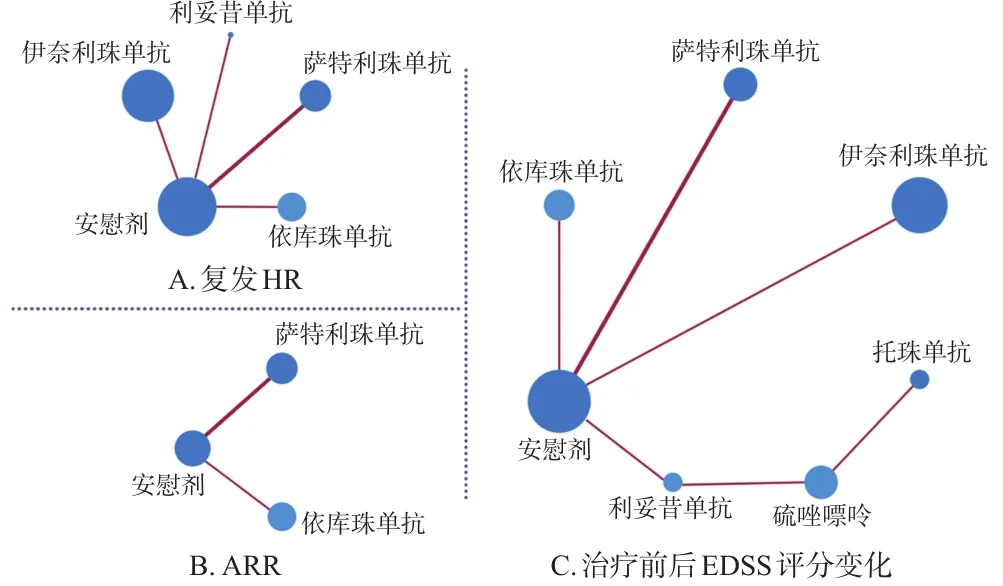
圖3 納入研究復發HR、ARR、EDSS評分的網狀關系圖

圖4 各結局指標的累積概率排序圖
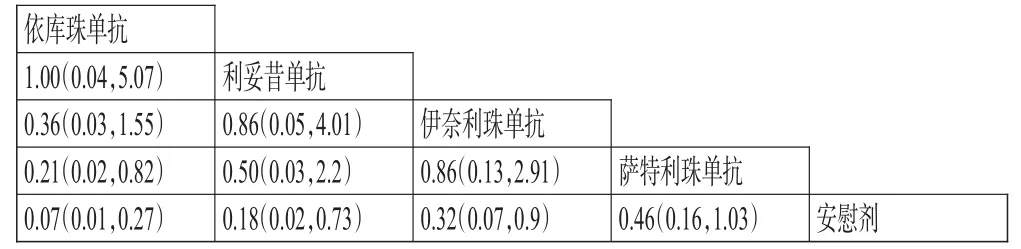
圖5 4種單克隆抗體預防NMOSD復發風險的網狀Meta分析結果[HR(95%%CrI)]
2.3.4 ARR的網狀Meta分析結果 共4項RCT[15,18―20]報告了試驗組與對照組患者的ARR及CI,其中Nikoo等[15]的結果由于缺乏一致的對照組無法進行間接比較。網狀關系圖如圖3B所示,網狀Meta分析結果如圖6所示。計算SUCRA(圖4B)得到以下排序:依庫珠單抗(76.32%)>薩特利珠單抗(60.30%)。

圖6 2種單克隆抗體預防NMOSD復發ARR的網狀Meta分析結果[MD(95%%CrI)]
2.3.5 EDSS評分的網狀Meta分析結果 共7項RCT[15―21]報告了試驗組與對照組的EDSS評分變化均值及標準差,其中有關薩特利珠單抗的2項研究選取了其所報告的第72周結局同基線的EDSS差值,其余均使用研究結局時采集的EDSS差值。網狀關系圖如圖3C所示,網狀Meta分析結果如圖7所示。計算SUCRA(圖4C)得到以下排序:依庫珠單抗(63.87%)>薩特利珠單抗(63.44%)>伊奈利珠單抗(53.73%)>利妥昔單抗(53.49%)>托珠單抗(40.64%)。
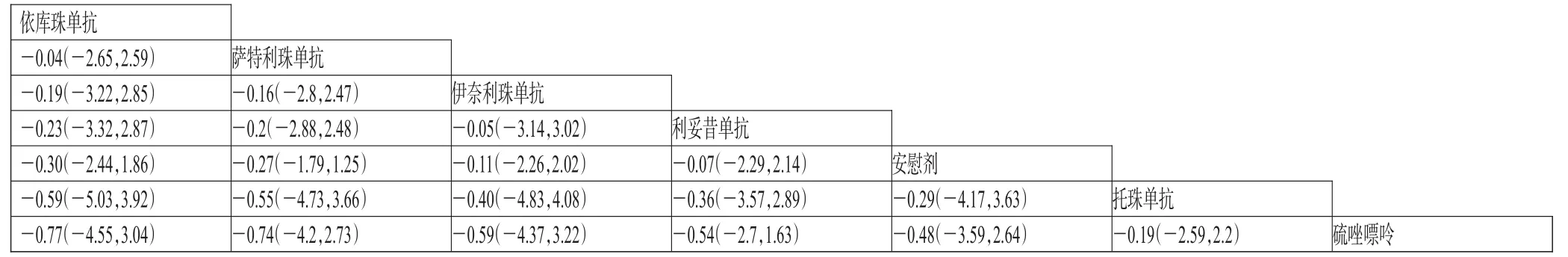
圖7 5種單克隆抗體預防NMOSD復發EDSS評分的網狀Meta分析結果[MD(95%%CrI)]
2.4 不良反應發生情況
納入的7項RCT[15―21]均報告了 AE。其中,Nikoo等[15]僅報告了AE個案,無法進行統計分析;Tahara等[16]將AE分為3個等級;Zhang等[17]將AE分為5個等級;Pittock等[20]將AE分為4個等級;Cree等[21]報告了總體AE及SAE的發生情況;2項薩特利珠單抗相關研究均報告了總體AE及SAE的發生情況[18―19]。
對總體AE及SAE的發生情況進行χ2檢驗,結果顯示,利妥昔單抗組與安慰劑組、托珠單抗組與硫唑嘌呤組、依庫珠單抗組與安慰劑組、伊奈利珠單抗組與安慰劑組、薩特利珠單抗組與安慰劑組患者總體AE及SAE發生風險比較,差異均無統計學意義(P>0.05)。
對于不同分級和單項AE,先計算RR再進行χ2檢驗。結果顯示,試驗(托珠單抗)組患者第3級AE發生率顯著低于對照(硫唑嘌呤)組[RR=0.42,95%CI(0.20,0.89),χ2=5.81,P=0.02],該分級意義為“嚴重或具有醫學意義但不會立即危及生命;導致住院或延長住院時間;致殘;自利性生活活動受限”。試驗(利妥昔單抗)組患者輸液反應[RR=8.00,95%CI(1.10,58.46),χ2=8.58,P=0.01]、惡心嘔吐[RR=6.00,95%CI(0.79,45.63),χ2=5.76,P=0.05]的發生風險均顯著高于對照(安慰劑)組;試驗(托珠單抗)組患者白血球減少癥[RR=0.17,95%CI(0.06,0.47),χ2=17.34,P<0.01]、惡心 [RR=0.42,95%CI(0.20,0.89),χ2=5.81,P=0.02]的發生風險均顯著低于對照(硫唑嘌呤)組;試驗(依庫珠單抗)組患者上呼吸道感染[RR=2.29,95%CI(1.02,5.14),χ2=4.68,P=0.03]的發生風險顯著高于對照(安慰劑)組。
3 討論
NMOSD曾被認為是MS的一種亞型。隨著研究的深入,根據其免疫學特征,學者將其歸納為獨立的臨床疾病,而病理生理學的研究則證實,NMOSD與MS的細胞免疫介導不同,其為體液免疫介導[7]。研究指出,約70%~80%的NMOSD患者呈AQP4?IgG陽性,約20%~25%的AQP4?IgG陰性患者血清中存在髓鞘少突膠質細胞糖蛋白(myelin oligodendrocyte glycoprotein,MOG)抗體[4]。
本研究結果顯示,與參與間接比較的其他單克隆抗體相比,依庫珠單抗在降低NMOSD患者復發風險、降低ARR及改善殘疾進展這3項指標上的SUCRA值均為最高。在降低EDSS評分方面,3種以NMOSD為適應證的藥物(依庫珠單抗、薩特利珠單抗、伊奈利珠單抗)的SUCRA值均高于托珠單抗、利妥昔單抗。安全性方面,總體AE及SAE的發生風險與對照組比較,差異均無統計學意義。對于不同分級與單項AE中有顯著性差異的項目,對比藥品說明書與已有文獻報告,未發現有不一致。
本研究有以下幾項局限性:(1)已有研究證明,NMOSD的發病與人種及性別相關,但本研究未能基于人種和性別進行亞組分析。(2)NMOSD的治療常會伴隨甾體類藥物及其他免疫抑制劑的使用,且納入研究對隨機分配后的伴隨用藥所采取的措施存在差別,但本研究并未采用對患者進行進一步分層的方法。現已有Wingerchuk等[25]對依庫珠單抗、薩特利珠單抗和伊奈利珠單抗按伴隨用藥措施進行分層,并以復發HR為主要指標開展了一項網狀Meta研究,但此方法進一步稀釋了受試人群,加大了組內偏倚。(3)本研究未能根據患者的免疫學特征進行分層級的討論。(4)暫時難以根據長期隨訪結果對藥品安全性進行全面評估。
本研究可能存在以下偏倚:(1)部分研究未進行適宜的隨機化及盲法處理;(2)納入的研究數及受試者群體總量較少;(3)未能進行進一步的敏感性分析及亞組分析;(4)部分數據轉換可能會降低間接比較的效力;(5)部分指標的基線水平(如入組時的EDSS評分)并不均衡,且由于指標定義不一致,未能就確認殘疾進展(confirmed disability progression,CDP)進行間接比較。
綜上所述,根據現有RCT結合間接比較方法可得,依庫珠單抗用于預防NMOSD復發在復發HR、ARR、EDSS評分變化3種結局指標上的效果均為最優;在改善殘疾進展方面,依庫珠單抗、薩特利珠單抗和伊奈利珠單抗效果優于托珠單抗、利妥昔單抗。安全性方面,部分不同分級及單項AE存在顯著性差異,但未發現其與已有的文獻及藥品說明書的報告結果不一致。但受研究數量以及質量所限,上述結論仍須通過納入更多高質量的臨床試驗進一步驗證。

