質(zhì)量源于設(shè)計(jì)在注射液工藝研究中的應(yīng)用
*路婷婷 池芳澤 楊保姣 高培培 劉清梁
(華潤雙鶴藥業(yè)股份有限公司 北京 100111)
國際上,藥品質(zhì)量管理模式已經(jīng)從生產(chǎn)與檢驗(yàn)相結(jié)合的模式發(fā)展成為設(shè)計(jì)(研發(fā))模式,ICH成員國率先采用質(zhì)量源于設(shè)計(jì)(QbD)方法進(jìn)行藥品研發(fā)和注冊(cè)申請(qǐng),從源頭設(shè)計(jì)開始抓最終質(zhì)量,強(qiáng)調(diào)過程控制和風(fēng)險(xiǎn)評(píng)估,注重建立控制策略和持續(xù)改進(jìn)。這些理念和方法對(duì)于全面提升我國藥品質(zhì)量,真正實(shí)現(xiàn)藥品的有效、安全和穩(wěn)定,有著十分重要的借鑒和引導(dǎo)作用。本文即基于QbD理念,進(jìn)行注射液產(chǎn)品的工藝開發(fā)[1-2]。
1.確定項(xiàng)標(biāo)產(chǎn)品關(guān)鍵質(zhì)量屬性(CQAs)
在研發(fā)過程中應(yīng)用質(zhì)量源于設(shè)計(jì)(QbD)理念來進(jìn)行生產(chǎn)工藝的開發(fā),以確保產(chǎn)品安全、有效和質(zhì)量可控。確定藥品的關(guān)鍵質(zhì)量屬性(CQAs)和擬控制策略,見表1[3-5]。

表1 目標(biāo)產(chǎn)品的關(guān)鍵質(zhì)量屬性(CQAs)


續(xù)表
2.生產(chǎn)工藝開發(fā)過程
小容量注射劑,采用該劑型常規(guī)生產(chǎn)工藝,生產(chǎn)過程主要包括:稱量、配制、過濾、灌封、滅菌、燈檢、包裝、入庫。我們重點(diǎn)對(duì)配制、過濾、灌封和滅菌等關(guān)鍵步驟的參數(shù)進(jìn)行研究[6-9]。
3.工藝流程圖
工藝流程圖以一種穩(wěn)定性和溶解性較好的小分子化合物注射液為例,以說明常規(guī)的注射液制備流程。

圖1 注射液工藝流程
4.生產(chǎn)工藝對(duì)產(chǎn)品關(guān)鍵質(zhì)量屬性的影響評(píng)估
首先對(duì)整個(gè)藥品生產(chǎn)工藝進(jìn)行風(fēng)險(xiǎn)評(píng)估,以確定可影響成品藥品關(guān)鍵質(zhì)量屬性的高風(fēng)險(xiǎn)工藝步驟。對(duì)每一工藝步驟進(jìn)行風(fēng)險(xiǎn)評(píng)估以確定潛在的高風(fēng)險(xiǎn)工藝變量。這些變量可能影響已確定的中間產(chǎn)品的關(guān)鍵質(zhì)量屬性,并最終影響藥品的關(guān)鍵質(zhì)量屬性[10-11]。生產(chǎn)工藝的初始風(fēng)險(xiǎn)評(píng)估、依據(jù)及擬控制策略見表2。
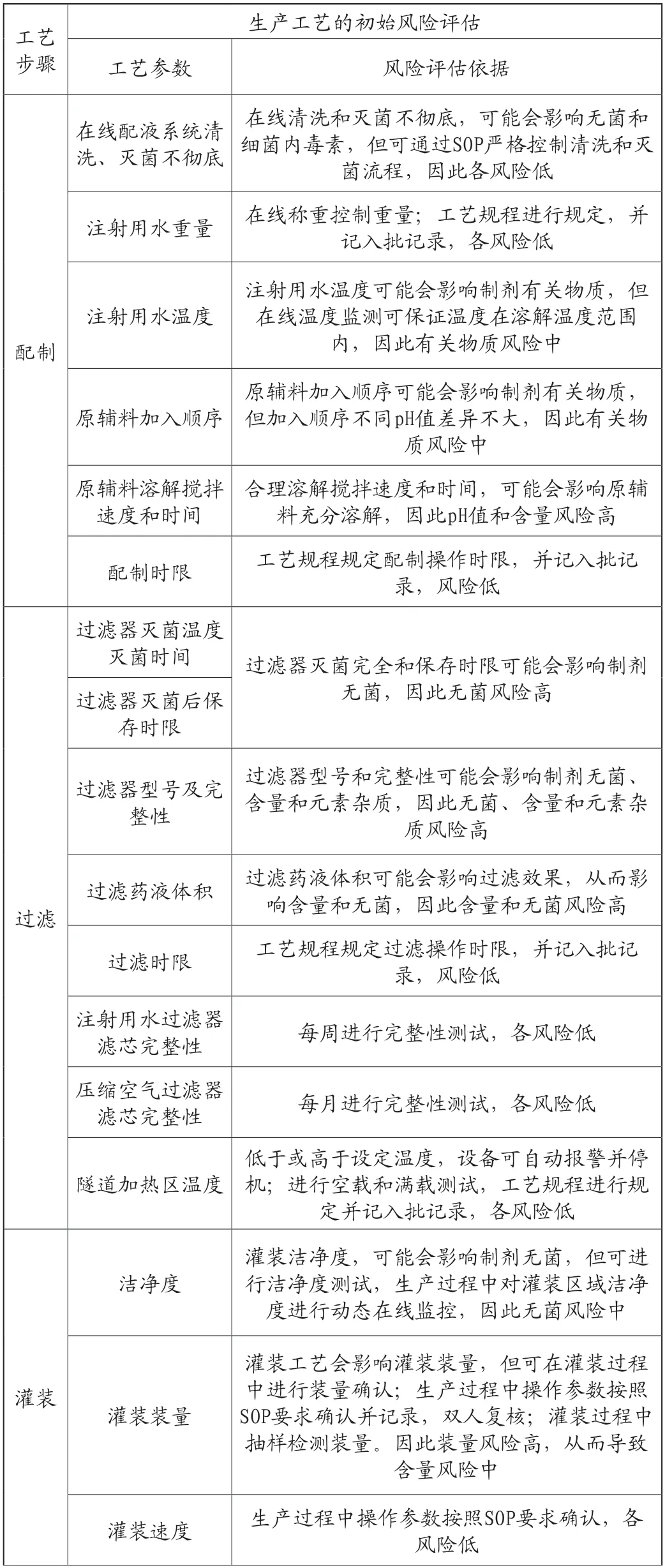
表2 生產(chǎn)工藝的初始風(fēng)險(xiǎn)評(píng)估

續(xù)表
通過風(fēng)險(xiǎn)評(píng)估,確認(rèn)配制、過濾、灌封和滅菌為關(guān)鍵工藝步驟,后續(xù)開展相應(yīng)研究。
5.確定的關(guān)鍵工藝參數(shù)
生產(chǎn)工藝中配制、過濾系統(tǒng)、灌封和滅菌工藝的關(guān)鍵工藝參數(shù)見表3。
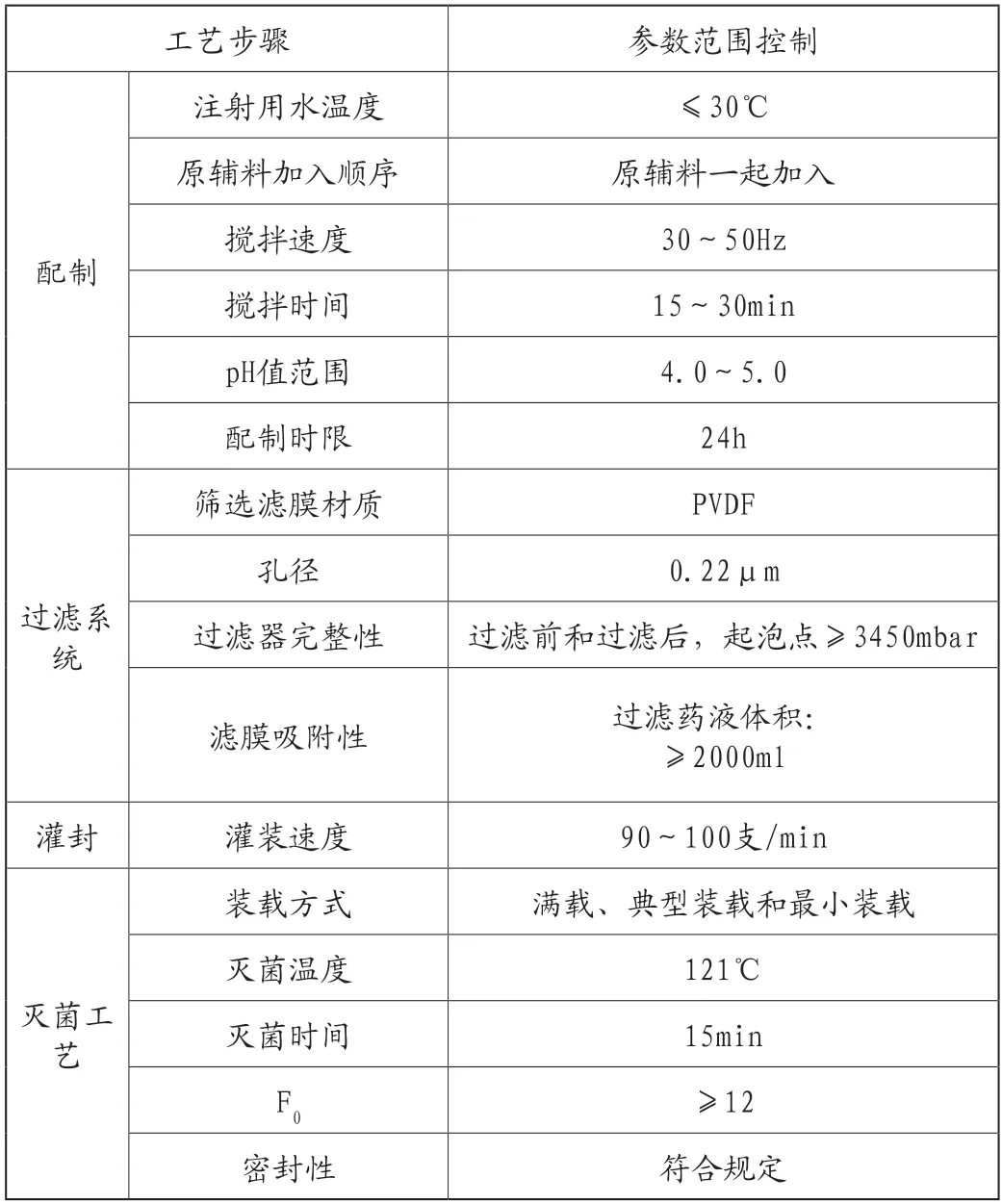
表3 工藝研究
6.藥物性質(zhì)對(duì)注射液工藝的影響
根據(jù)藥物不同的性質(zhì),注射液工藝參數(shù)需要進(jìn)行調(diào)整,如,不同藥物過濾體積會(huì)不同;藥液黏度不同裝量不同則灌裝速度也不同;穩(wěn)定性不同的藥物滅菌方式、滅菌溫度和時(shí)間不同;復(fù)雜注射液工藝相較復(fù)雜,如為了改善原料的溶解性增加表面活性劑,增加乳化等制備工藝。因此,注射液制備工藝需要根據(jù)藥物性質(zhì),給藥目的等制定合理的工藝參數(shù)。
7.討論
在注射液處方工藝中應(yīng)用QbD理念,確定產(chǎn)品的關(guān)鍵質(zhì)量屬性,基于風(fēng)險(xiǎn)評(píng)估,采用過程控制策略,如控制輸入物料關(guān)鍵質(zhì)量屬性(CMAs)和控制關(guān)鍵工藝參數(shù)(CPP)保障產(chǎn)品質(zhì)量,進(jìn)一步說明產(chǎn)品是設(shè)計(jì)出來的,不是檢驗(yàn)出來的。

