電性分析:促進化學學科理解的重要手段
——以鈉、氯相關知識的教學為例
劉 瑩 趙 拯
(1.江陰市第二中學 江蘇 無錫 214400;2.江蘇省江陰高級中學 江蘇 無錫 214443)
一、問題的提出
在《普通高中化學課程標準(2017年版)》中,明確地提出要進一步增進化學學科理解,并將化學學科理解定義為:教師對化學學科知識及其思維方式和方法的一種本原性、結構化的認識,它不僅是對化學知識的理解,還包括對具有化學學科特質的思維方式和方法的理解。[1]增進化學學科理解是落實學生學科核心素養的重要目標,是提升學科教學專業化水平的重要依據。如何通過培育學生的核心素養來提升其學科理解力是非常值得研究的課題。眾所周知,高中元素化合物知識內容豐富、反應眾多、轉化復雜、應用廣泛。如果沒有形成化學學習方法,往往呈散點式學習,所學知識孤立、分散,缺少知識間的聯系與對比,缺乏概念與理論之間的融合促進,無法揭示其內在本質規律,自然就無法形成化學核心素養,而大部分教師對此認識不足,主要原因就是學科理解不夠。近年來,應用于真實化學問題情境的高考化學試題呈不斷上升趨勢,但師生對于該試題的解答卻往往不得要領,表層原因是元素化合物知識學習不得要領,深層次原因在于對化學反應過程的本質認識不深、思維訓練不足。受到有機反應機理中電性分析的啟發,筆者嘗試對高一鈉和氯元素相關知識進行再設計,從學科理解角度來啟發研究學習的新視角,共同提高師生對化學學科的深度理解。
二、研究思路
化學原理和化學知識是相互聯系、相互促進、螺旋式上升的。化學原理性知識是化學元素知識的內在本質表現,只有對原理性知識有深入理解,才能立體地掌握化學元素化合物基本性質;化學知識的遷移應用是化學元素知識的外在實用體現,表現出化學知識學習的意義和價值。在有機化學學習過程中,東北師范大學的鄭長龍團隊就通過醛的結構與性質進行學科理解研究。[2]其中一個重要的觀點,就是從電子云角度和鍵的極性來預測和驗證醛類性質。根據學生已有的知識水平,我們將電子云、分子極性等知識簡化為電性作用,同時利用氧化還原反應和離子反應的相關內容知識,在一定層面上解釋和預測化學變化中的一些原理性知識。化學學習是累積、遞進式進行的,在教學設計時,筆者采用整本書整體設計,采用“左顧右盼,瞻前顧后”的方式進行備課,具體為學習鈉和氯元素相關性質時,回顧運用前面學過的氧化還原、離子反應等相關知識,也為后續的元素原子性質和化學鍵等內容積累素材;同時在類似知識之間進行比較,尋找相同點與不同點,從而整體認識物質的性質。
三、教學過程主要片段
在進行高一必修1 的教學時,全教研組對全書內容通讀研究,厘清內在邏輯性,特別在物質分類與轉化、氧化還原反應和離子反應等知識的教學時,就考慮到后續元素化合物知識的需求,同時將最后一章的元素周期律相關內容在講授元素性質時有意識地滲透。在教學實踐中,我們在學習離子反應、電解質時,花了較多時間來建立微粒電性模型。具體設計如下:
1.氯化鈉是如何溶于水的?初步建立微粒電性模型
氯化鈉固體溶于水,學生的直觀感受集中在固體體積變小并消失上。如果這樣描述實驗現象,思維仍停留在宏觀層面。在電解質概念學習時,以氯化鈉為例,教師通常聚焦于溶液中自由移動的鈉離子與氯離子,認為電離是在水的作用下氯化鈉離解成氯離子和鈉離子,通過電離方程式書寫后就結束了該內容的教學。在初三化學學習時,學生已具備氯化鈉由氯離子和鈉離子組成的基本認識。在高中教學時,我們不僅要將眼光放在氯離子和鈉離子上,更需要關注到水分子的作用,要啟發學生關注微觀層面,結合圖像從微觀層面來想象鈉離子和氯離子是怎么被水分子“抬”入溶液。根據教材圖片信息提示(見圖1),引導學生觀察水分子在鈉離子和氯離子周圍的取向,將之類比于磁鐵的磁性作用,建構水分子電性模型:氧原子吸引電子能力比氫原子強,所以在氧原子一邊顯負電性,氫一頭顯正電性,化合價的正負性與之呼應。根據電性的信息,對水分子建構一邊帶正電,一邊帶負電的微粒電性模型,見圖2:
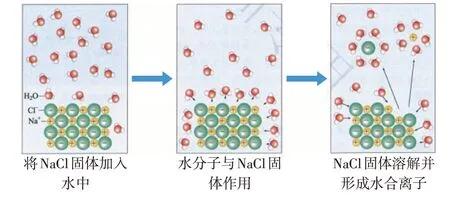
圖1 氯化鈉固體溶于水的微觀表征
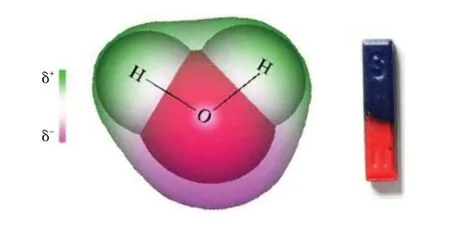
圖2 氯化鈉固體溶于水的微觀表征
該模型能很好地從微觀層面解釋氯化鈉在水中的電離機制。那這個模型是否具有一定的科學性呢?那就帶領學生用摩擦毛皮的塑料棒吸引細水流實驗來驗證(如圖3所示)。我們繼續擴展:如何解釋氯化氫極易溶于水?氯化氫中由于氯原子和氫原子對電子吸引力不同,氯原子端顯負電,氫原子端顯正電,在水分子的電性作用下發生“撕裂”成自由移動的陰陽離子。

圖3 水流在電性作用下偏轉
評析:宏觀辨識與微觀探析是化學核心素養的重要組成部分。在高中教學中,要注意培養學生從宏觀層面深入到微觀層面的認識視角。通過整本書的設計,我們認為,在水分子電性模型上花精力是值得的,因為后續很多內容都能通過微粒電性模型來解釋與推理。雖然氯化鈉溶于水并不是難點,但其中水分子作用及其機理卻是值得深入研究的。鑒于學生認知,水分子微粒電性模型時,顯得相對粗糙,甚至不夠嚴謹,但模型構建主要揭示其關鍵要素,忽略次要因素。如何判斷模型的優劣,關鍵在于能否解釋現象,解決問題。
2.進一步厘清并補充適量的原理性知識,為學生的積極建構提供足夠的支持
在學習鈉和氯相關性質知識之前,復習回顧1-18號元素符號和原子核外電子排布式。再針對原子核外電子排布,介紹因發現了六種稀有氣體,1904年的諾貝爾化學獎授予了英國化學家威廉·拉姆塞的化學史。為什么稀有氣體的發現如此重要呢?因為稀有氣體揭示了各種元素原子核外電子得失趨向的問題。我們知道,化學變化往往是最外層電子發生轉移。為此,我們介紹電子式,讓學生明確電子式的特點和意義。明確原子間可以通過電子轉移形成相對穩定的水分子、氯氣、氯化氫和氯化鈉等物質。
評析:化學是在分子、原子角度研究物質組成和性質的學科。原子最外層電子與化學性質密切相關,根據這個邏輯很順暢地引入電子式,并通過這種化學用語來表示常見的物質。其中,諾獎的引入以及稀有氣體的單原子分子的事實,讓學生感受到電子式的意義與價值。雖然這部分內容是安排在必修1 第四章“物質結構和元素周期律”中,但教學中將之提前引入并應用,并不感覺到突兀。當然,也只介紹最常見且馬上需要的物質電子式,學生學習難度并不大。事實上,電子式的提前引入和應用,也為后續化學鍵提供了大量事實性的素材,有利于化解化學鍵過于抽象的問題。
3.鈉相關化學反應原理的研究,初步運用微粒電性模型來表示物質的反應
結構決定性質,這是化學學科的大概念。根據鈉原子的結構示意圖,預測金屬鈉具有很強的還原性。根據鈉與氧氣反應的實驗現象,得出鈉與氧氣反應生成氧化鈉、過氧化鈉。在此基礎上,師生合作寫出鈉與氧原子的電子式來表示形成氧化鈉和過氧化鈉的過程。通過符號表征,深刻觀察到鈉與氧原子之間的電子轉移情況。觀察氧化鈉的電子式,氧化鈉中O2-離子,與水接觸時即發生電性作用分裂為兩個OH-,電子式表示如下:。這樣推理是否有道理呢?進行實驗,氧化鈉加水再滴入酚酞變紅,確實發生了反應。接著進行過氧化鈉與水反應的實驗,感受到試管壁發燙,滴加酚酞,溶液先變紅后褪色,并產生使帶火星的木條復燃的氣體。有了前面模型推演的基礎,師生共同合作進行了電子式推理,分析如下實驗過程中有氫氧根生成,使酚酞變紅;過氧化氫的氧化性使酚酞漂白而褪色;反應放熱過氧化氫受熱分解。
評析:在鈉與氧氣的反應中,師生合作練習電子式的表示方式。針對氧化鈉,借助水分子的微粒電性模型,與氧化鈉中的O2-離子發生作用,預測并通過實驗驗證,說明了微粒電性模型的有效性,同時與電子式的符號表征得到印證。對于現象相對復雜的過氧化鈉與水的反應,我們先實驗演示,再用電子式的電性作用推理,與實驗現象進行互相驗證,初步形成了用電子式結合微粒電性模型研究化學反應的方法。整個過程,學生既感覺到具有很大的挑戰性,又體驗到明顯的成就感,這對于激發學生勤于思考、樂于探究,具有很好的引領作用。
4.深入探索氯氣與水反應機理,提升對電性作用模型遷移應用能力
通過前面的探索,我們堅定了化學學習是有規律的,規律是可以探索的。教師的重要作用是提供工具,啟迪方法,激勵自主探究。下面進一步研究氯氣溶于水的實驗。首先提出問題:氯化氫在水中溶解度極大,但為什么氯氣的溶解度就不大呢?寫出兩種氣體的電子式,氯化氫對外顯電性作用,而氯氣分子Cl Cl,由于電荷均勻分布,所以不像氯化氫那樣對外顯電性,根據微粒電性作用很容易解釋氯氣在水中的溶解度相對比較小的原因。將氯氣通入水中形成飽和溶液,在其中滴加硝酸銀溶液,有白色沉淀析出,說明氯氣與水發生了反應。這就與氯氣不顯電性,難以與水分子作用產生認知沖突了。教師啟發:鐵塊沒有磁性,但如果被磁鐵吸引,也有可能產生磁性。那么氯氣分子在水分子電性的“誘擾”下,氯分子可能在端點上顯示少量的電性,在這少量電性的作用下,水分子帶負電性的部分就會與正電性部分的氯原子作用,并形成HOCl(習慣上寫成HClO,即次氯酸),另一個氯原子轉化為Cl-,水中一個氫原子轉化為H+,電性模型分析:。當然水分子對氯分子的“誘擾”作用是微弱的,自然氯氣與水反應程度也很微弱。而產物氯離子也是帶有負電性,次氯酸中的氯原子又與氧共用電子,共用電子偏向氧原子而帶正電性(化合價為+1),那么,兩個不同的氯之間同樣會有電性作用,反向結合成氯氣的趨勢,而且一旦兩個氯結合成氯氣,次氯酸剩余部分就生成負電的OH-,溶液中的H+與OH-迅速結合成水分子。這種對于反應本質的研究,對于后期可逆反應的建構具有極大的促進作用,還有一個額外收獲就是意識到體系的酸堿性在一定程度上也會影響反應的進行。理論必須要通過實踐檢驗才能有生命力。同樣通過實驗來驗證,將潔廁劑(主要成分是濃鹽酸)和84 消毒液(主要成分是NaClO)混合,就會發生上述反應,很明顯產生有毒氣體氯氣。
評析:在傳統的教學中,大家比較推崇實驗探究來分析氯水的成份,通過實驗中各成分共存來說明該反應是可逆反應。這種推理是有一定的瑕眥的,因為無法反駁該反應速率小的假說。而這里通過電性作用進行研究,不僅成功地克服了反應物與生成物共存是速率還是限度的問題,而且還能為深入研究次氯酸是怎么分解的,是如何漂白的,以及為什么氯水長時間放置最終會轉變為稀鹽酸的一系列問題打下基礎。如何把握好這一系列的問題契機,都顯示出教師對課堂的把控能力,顯示出教師對核心素養的認識層次以及教師對化學學科的理解力。
四、結語
分子電性模型作為學習化學的重要認知工具,通過簡單易懂的原理,在化學反應的機理認識和結果解釋過程中發揮了非常有意義的作用。有研究認為:基于預測的認識過程會讓大腦釋放多巴胺,促進前額皮層的活動,大腦體驗到這種活動的價值,會付出更多的努力投入到認識活動中。[3]我們的這種教學方式,極大地激發了學生的研究熱情。在教學實踐中,在建構電性分析模型后,學生馬上主動地進行反應過程的預測,不斷嘗試,不斷提問,享受著探索的樂趣。教師更多的是要發現培養學生核心素養的契機,不失時機地提出疑問,鼓勵科學探究,訓練化學思維,并且在與學生一起探索的過程中,不斷提升化學學科理解力。

