抗除草劑棉花GV-2 的分子特征和遺傳穩(wěn)定性分析
陸國清 馬彩霞 孫國清 郭惠明 程紅梅

摘要:分子特征和遺傳穩(wěn)定性是我國轉(zhuǎn)基因植物安全評價流程所需考察的重要數(shù)據(jù)。利用基因組測序技術(shù)對抗除草劑棉花GV-2 的T-DNA 插入位點、拷貝數(shù)及側(cè)翼序列進行解析,并采用實時熒光定量PCR(quantitative real time polymerase chain reaction,qRT-PCR)、Southern雜交、膠體金試紙及ELISA(enzyme linkedimmunosorbent assay)方法對連續(xù)3代(T3~T5)GV-2轉(zhuǎn)化體中目的基因的表達的穩(wěn)定性進行驗證。結(jié)果表明,轉(zhuǎn)化體GV-2中T-DNA以單拷貝形式插入到陸地棉A06染色體2 092 124~2 092 194 bp之間,造成棉花基因組中70 bp DNA的缺失。轉(zhuǎn)化體特異性PCR及Sanger測序結(jié)果進一步驗證了插入位點的正確性。此外,目的基因及其表達蛋白在不同世代轉(zhuǎn)化體中均可穩(wěn)定遺傳,為轉(zhuǎn)基因棉花GV-2轉(zhuǎn)化體的安全評價提供了有效的支撐。
關(guān)鍵詞:轉(zhuǎn)基因棉花;抗除草劑;G10evo;分子特征;遺傳穩(wěn)定性doi:10.13304/j.nykjdb.2021.0581
中圖分類號:S562 文獻標(biāo)志碼:A 文章編號:10080864(2023)01004208
轉(zhuǎn)基因植物的分子特征主要是指在基因水平、轉(zhuǎn)錄水平和翻譯水平考察外源插入序列的整合和表達情況[1],這些是我國轉(zhuǎn)基因植物安全評價管理要求中必須提供的信息,對于轉(zhuǎn)基因材料的風(fēng)險監(jiān)管至關(guān)重要。其中,目的基因在植物基因組中的整合情況是考察的重點。分析外源插入序列整合情況的方法包括轉(zhuǎn)化體特異性聚合酶鏈?zhǔn)椒磻?yīng)(polymerase chain reaction,PCR)、Southern雜交等,其中轉(zhuǎn)化體特異性PCR 的實現(xiàn)要基于PCR的染色體步移技術(shù)或高通量的基因組測序技術(shù)獲得外源序列在植物基因組中的整合位點和側(cè)翼序列。染色體步移是劉耀光院士于1995年發(fā)明的一種用于分析T-DNA插入位點的技術(shù),即熱不對稱交錯PCR (thermal asymmetric interlacedPCR,TAIL-PCR),TAIL-PCR是一種用來分離與已知序列鄰近的未知DNA 序列的分子生物學(xué)技術(shù)[2-5]。
基因組測序技術(shù)作為近年來解析轉(zhuǎn)基因植物分子特征的新方法,已經(jīng)在多種植物上得到應(yīng)用,尤其是糧食作物。Williams-carrier等[6]利用高通量測序技術(shù)開發(fā)出一套適于玉米轉(zhuǎn)座突變插入位點檢測的新方法,該方法為玉米中表型驅(qū)動的突變標(biāo)簽鑒定提供了新的工具,同時也適用于其他具有高拷貝轉(zhuǎn)座子的植物。Siddique等[7]利用新一代測序技術(shù)鑒定了轉(zhuǎn)基因玉米IE09S034的分子特征。Kovalic 等[8]和Guo等[9]分別利用基因組測序技術(shù)分析了轉(zhuǎn)基因大豆(MON17903、MON87704以及GE-J16、ZH10-6)的分子特征。研究表明,利用全基因組測序技術(shù)成功鑒定了水稻轉(zhuǎn)化事件的插入位點及側(cè)翼序列[10-12]。Inagaki等[13]利用高通量測序技術(shù)成功分析確定了22個擬南芥轉(zhuǎn)化事件中T-DNA的插入位點及側(cè)翼序列。然而,該方法在轉(zhuǎn)基因棉花分子特征檢測方面的應(yīng)用鮮見報道。
遺傳穩(wěn)定性在我國轉(zhuǎn)基因植物安全評價過程中主要是考察目的基因整合的穩(wěn)定性、表達的穩(wěn)定性以及目標(biāo)性狀表現(xiàn)的穩(wěn)定性[1]。Southern雜交由于其結(jié)果直觀,是檢測目的基因整合穩(wěn)定性的首選方法。實時熒光定量PCR(qRT-PCR)和酶聯(lián)免疫法(enzyme linked immunosorbent assay,ELISA)在檢測目的基因轉(zhuǎn)化體不同世代中轉(zhuǎn)錄和翻譯水平表達的穩(wěn)定性方面具有靈敏、高效的優(yōu)勢。對于抗除草劑這一目標(biāo)性狀,我國《轉(zhuǎn)基因生物新品種培育重大專項成果認定指南》中明確指出,轉(zhuǎn)化體至少能夠耐受目標(biāo)除草劑的劑量要達到農(nóng)業(yè)生產(chǎn)上推薦劑量的4倍以上,因而,抗除草劑轉(zhuǎn)化體不同世代的目標(biāo)性狀穩(wěn)定性也是其是否具有產(chǎn)業(yè)化前景的重要前提。
G10evo 基因是已經(jīng)在玉米和大豆中獲得成功應(yīng)用的抗除草劑基因[1415]。棉花轉(zhuǎn)化體GV-2是通過農(nóng)桿菌介導(dǎo)的方法將G10evo 基因?qū)腌孀置?12中獲得的獨立轉(zhuǎn)化事件,具有良好的除草劑抗性[16]。該轉(zhuǎn)化體已于2016年完成了農(nóng)業(yè)轉(zhuǎn)基因植物安全評價的中間實驗環(huán)節(jié),本研究利用基因組測序技術(shù)對GV-2 的T-DNA 插入位點、拷貝數(shù)及側(cè)翼序列進行解析,并采用qRT-PCR、Southern 雜交、膠體金試紙及ELISA 方法對連續(xù)3代GV-2轉(zhuǎn)化體(T3~T5)中目的基因轉(zhuǎn)錄和表達的穩(wěn)定性進行驗證,同時也對不同世代轉(zhuǎn)化體的除草劑抗性開展鑒定,為轉(zhuǎn)基因棉花GV-2轉(zhuǎn)化體安全評價提供有效的支撐。
1 材料與方法
1.1 試驗材料
供試植物材料包括源于珂字棉312的轉(zhuǎn)化受體材料R15以及通過農(nóng)桿菌介導(dǎo)法將G10evo 基因?qū)隦15獲得的抗除草劑棉花GV-2,由本實驗室創(chuàng)制。轉(zhuǎn)化質(zhì)粒是以pCambia2301為基礎(chǔ)的植物表達質(zhì)粒,包含2 個分別由木薯葉脈花葉病毒PCsVMV 啟動子和花椰菜花葉病毒CaMV35S 啟動子驅(qū)動的G10evo 基因、1個由CaMV35S啟動子驅(qū)動的卡那霉素抗性選擇標(biāo)記基因(nptII)[16]。
主要試劑:植物DNA和總RNA提取試劑盒購自天根生化科技(北京)有限公司;反轉(zhuǎn)錄試劑盒、熒光定量PCR相關(guān)試劑盒購自北京全式金生物技術(shù)有限公司;G10-EPSPS膠體金試紙條、ELISA試劑盒購自上海佑隆生物科技有限公司;農(nóng)達、41%草甘膦異丙胺鹽水劑,由美國孟山都公司生產(chǎn);其余一般化學(xué)試劑均購自北京博艾生物技術(shù)有限公司。引物由六合華大基因科技有限公司合成。
1.2 試驗方法
1.2.1 GV-2的基因組測序及插入位點分析 全基因組測序委托北京利百加生物技術(shù)有限公司完成。利用片段化的GV-2 基因組DNA 構(gòu)建文庫,構(gòu)建好的文庫采用PE150 雙末端測序法在Illuminia Nova Seq 6000 平臺進行測序,測序深度為30× 。用BWA 軟件將clean reads 與棉花(NBI_Gh_v1.1.fa)參考基因組比對,根據(jù)比對結(jié)果確定reads 的insert size 峰值為340 bp,變幅296~383 bp。去除雙端都比對上的reads,保留單端比對上的reads以及雙端都未比對上的reads,用BWA 軟件將保留的reads 與T-DNA 插入序列及棉花基因組比對以獲得插入位點及其側(cè)翼序列。
1.2.2 轉(zhuǎn)化體特異PCR 根據(jù)基因組測序獲得插入位點兩端的側(cè)翼序列及T-DNA 的LB 和RB 序列,設(shè)計特異的轉(zhuǎn)化體PCR 引物詳見表1。PCR程序為:94 ℃ 5 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃30 s,35個循環(huán);72 ℃ 8 min。PCR產(chǎn)物測序后與插入位點側(cè)翼序列進行比對分析。
1.2.3 熒光定量PCR分析 參照試劑盒說明書,分別提取R15及T3~T5代GV-2的根、莖、葉、花組織的總RNA,反轉(zhuǎn)錄成cDNA,通過qRT-PCR法分析目的基因在GV-2不同世代植株中轉(zhuǎn)錄水平的表達穩(wěn)定性。熒光定量特異性檢測引物及方法參照文獻[16]。
1.2.4 Southern雜交分析 參照Clarke[17]的方法,分別選取R15及GV-2 T3~T5代植株的幼嫩葉片組織,采用CTAB 法提取并純化植物基因組DNA。分別選擇Hind Ⅲ和Spe Ⅰ對基因組DNA進行酶切,通過Southern雜交分析目的基因和標(biāo)記基因在GV-2中的插入表達情況。以G10evo 的353 bp序列片段和nptII 的337 bp序列片段作為探針進行Southern雜交[18]。
1.2.5 目的蛋白的定性與定量分析 于花期分別對R15和轉(zhuǎn)基因GV-2(T3~T5)植株的根、莖、葉、花進行取樣,利用G10-EPSPS膠體金快速檢測試紙條定性檢測目的基因的表達,確定在GV-2不同世代的植株中目的蛋白的穩(wěn)定性及表達情況;利用ELISA試劑盒對GV-2不同世代植株中目的蛋白進行定量檢測,分析不同組織中目的蛋白表達水平。分析方法參照試劑盒說明。
1.2.6 目標(biāo)性狀鑒定 采用盆栽方式,在裝有營養(yǎng)土的花盆中種植R15 及T3~T5 代GV-2 棉花種子。待棉花長至2葉1心期,在晴朗的天氣,采用手持式噴壺噴施20 mL·L-1農(nóng)達,使葉面全部噴濕15 d后觀察植株生長情況。每個材料處理5盆,每盆不少于5株。
2 結(jié)果與分析
2.1 GV-2 的插入位點分析及轉(zhuǎn)化體特異PCR
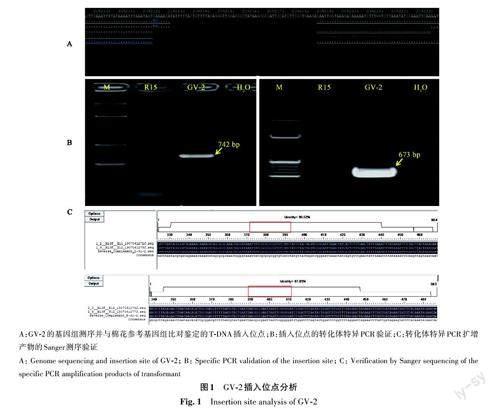
對GV-2進行基因組測序并與棉花參考基因組比對,結(jié)果(圖1)表明,該轉(zhuǎn)化體僅有1個插入位點,位于陸地棉A06 染色體2 092 124~2 092 194 bp之間,T-DNA的插入刪除了原序列中70 bp堿基(圖1A)。經(jīng)檢索,插入位點區(qū)域無已知編碼基因,在陸地棉已發(fā)表的轉(zhuǎn)錄組中(包括根、莖、葉、花、果實、種子等各種組織器官)均無轉(zhuǎn)錄表達痕跡,因此外源基因插入不影響基因組原有功能。利用插入位點側(cè)翼序列及T-DNA左、右邊界序列設(shè)計的轉(zhuǎn)化體特異引物,能夠分別擴增出插入位點左邊界742 bp和右邊界673 bp的目的片段(圖1B),Sanger測序證明,T-DNA左、右邊界的側(cè)翼序列與參考基因組的序列一致(圖1C),進一步證實了基因組測序獲得的GV-2插入位點及側(cè)翼序列的正確性。
2.2 目的基因轉(zhuǎn)錄水平的穩(wěn)定性
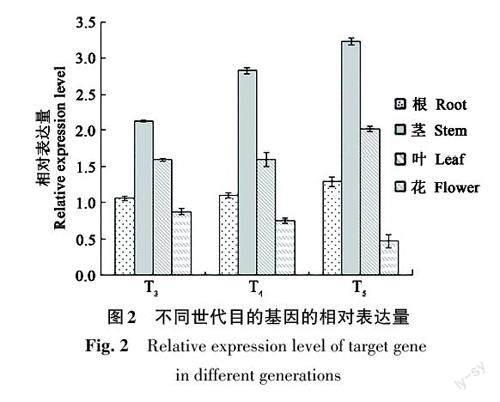
利用qRT-PCR對轉(zhuǎn)基因棉花GV-2不同世代植株的目的基因轉(zhuǎn)錄穩(wěn)定性進行檢測,結(jié)果(圖2)表明,目的基因在不同世代的植株中均可以穩(wěn)定轉(zhuǎn)錄;而在對照R15中未檢測到。由此證明,GV-2的草甘膦抗性是由G10evo 基因產(chǎn)生,其轉(zhuǎn)錄可以在不同世代間穩(wěn)定遺傳。
2.3 目的基因在不同世代的整合穩(wěn)定性
分別采用Hind Ⅲ 和Spe Ⅰ 對R15 和GV-2T3~T5 代基因組DNA 進行酶切,利用目的基因(G10evo)及標(biāo)記基因(nptⅡ)的探針進行雜交,雜交探針在對應(yīng)基因的相對位置如圖3所示。雜交結(jié)果(圖3B和C)表明,目的基因經(jīng)2種酶切后分別獲得約22和24 kb的條帶,標(biāo)記基因分別獲得約3和7 kb的條帶。根據(jù)插入位點側(cè)翼序列的酶切位點預(yù)測Southern雜交時預(yù)計產(chǎn)生的條帶與實際結(jié)果相吻合,表明目的基因與標(biāo)記基因均以單拷貝的形式整合到棉花基因組中,且能夠在GV-2中穩(wěn)定遺傳(T3~T5)。
2.4 目的蛋白翻譯水平的穩(wěn)定性
用膠體金試紙條及ELISA的方法分別定性和定量檢測不同世代GV-2中目的蛋白的表達。膠體金試紙條定性檢測結(jié)果(圖4A)顯示,目的蛋白在GV-2連續(xù)3個世代的不同器官中均有表達,而對照R15中未檢測到目的蛋白。根據(jù)ELISA試劑盒提供的標(biāo)準(zhǔn)品制備標(biāo)準(zhǔn)曲線,定量檢測結(jié)果(圖4B和C)表明,目的蛋白在莖中的表達量最高,T3~T5代分別為3.30、3.26、3.82 μg·L-1;在葉片中的表達量為2.15、2.13、3.25 μg·L-1;在根中的表達量較低,為0.12~1.12 μg·L-1;在花中表達量最低,T3~T5代分別為0.09、0.08和0.44 μg·L-1。不同世代相同器官中目的蛋白含量差異不顯著,進一步表明目的蛋白可以在不同世代及不同器官中穩(wěn)定表達。
2.5 目標(biāo)形狀的穩(wěn)定性
對R15和轉(zhuǎn)基因棉花GV-2不同世代植株幼苗按照說明書推薦劑量4倍稀釋液噴施,進行草甘膦抗性檢測,結(jié)果(圖5)表明,轉(zhuǎn)基因棉花GV-2不同世代植株生長狀態(tài)良好,不同世代間差異不顯著;對照R15死亡。由此表明,轉(zhuǎn)基因棉花GV-2草甘膦抗性強、遺傳穩(wěn)定性高。
3 討論
抗除草劑轉(zhuǎn)基因作物的研究和推廣在全球農(nóng)業(yè)生產(chǎn)過程中一直處于非常重要的位置。根據(jù)國際農(nóng)業(yè)生物技術(shù)應(yīng)用服務(wù)組織(InternationalAgricultural Biotechnology Application ServiceOrganization,ISAAA)統(tǒng)計,截至2017 年5 月21日,共有328 個抗除草劑轉(zhuǎn)化事件(這些抗除草劑轉(zhuǎn)化事件均被相關(guān)國家授權(quán)直接食用、作為添加劑或用于栽培),其中棉花(Gossypiumhirsutum)、大豆(Glycine max)、油菜(Brassicanapus)和玉米(Zea mays)的抗除草劑轉(zhuǎn)化事件300 個,占抗除草劑轉(zhuǎn)化事件總數(shù)的91.46%,抗除草劑棉花轉(zhuǎn)化事件39 個。其中,單一抗除草劑性狀的轉(zhuǎn)化事件只有5 個,分別是19-51a(杜邦,抗磺酰脲類除草劑)、GHB614(拜耳,抗草甘膦)、LLCotton25(拜耳,抗草銨膦)、MON1445 和MON88913(孟山都,抗草甘膦)[19]。由此可見,轉(zhuǎn)基因抗除草劑棉花轉(zhuǎn)化事件在全球轉(zhuǎn)基因抗除草劑作物中的占比很小,并且基本被跨國公司壟斷。截至目前,我國轉(zhuǎn)基因抗除草劑棉花轉(zhuǎn)化事件還沒有完成全部安全評價流程。隨著全基因組測序技術(shù)在水稻、玉米、大豆等作物轉(zhuǎn)基因分子特征檢測中的成功應(yīng)用,將其應(yīng)用于抗除草劑轉(zhuǎn)基因棉花轉(zhuǎn)化體插入位點及側(cè)翼序列的鑒定也將為加快抗除草劑棉花新品種的培育提供有力的技術(shù)支撐。
本實驗室培育的抗除草劑棉花GV-2是通過農(nóng)桿菌介導(dǎo)的方法將外源基因?qū)腙懙孛轗15(選育自珂字棉312的易轉(zhuǎn)化品系)中,通過除草劑篩選測試及多代自交獲得的純合且抗性穩(wěn)定的轉(zhuǎn)化體。研究利用高通量全基因組測序結(jié)合生物信息學(xué)分析,鑒定出GV-2 中T-DNA 的插入位點及其側(cè)翼序列,結(jié)果表明T-DNA以單拷貝的形式插入到陸地棉A06 染色體2 092 124~2 092 194 bp 之間,同時刪除了原序列中無功能的70 bp片段。基因組測序數(shù)據(jù)中部分讀序比對到載體骨架上,但數(shù)量很少,推測這可能是由于建庫過程中質(zhì)粒污染所致[20]。轉(zhuǎn)化體特異性PCR 及擴增產(chǎn)物的Sanger 測序印證了基因組測序分析結(jié)果,Southern雜交再次證明了T-DNA在陸地棉中的單拷貝整合,至此GV-2 的分子特征得到成功解析。
本研究還利用qRT-PCR、Southern 雜交以及ELISA 等技術(shù)對目的基因的遺傳穩(wěn)定性進行了分析。在轉(zhuǎn)錄水平上,目的基因在各器官的表達量存在一定差異,在莖和葉中的轉(zhuǎn)錄水平較高,而在根和花器官中的轉(zhuǎn)錄水平較低,分析其原因可能是由于T-DNA 中含有2 個G10evo 基因的表達盒(圖3A),其中木薯葉脈花葉病毒啟動子的組成表達型是由不同組織特異性結(jié)構(gòu)域引起的,而其中最高啟動子表達區(qū)域位于維管組織和葉肉細胞中[21]。目的基因在不同世代間的轉(zhuǎn)錄沒有顯著差異,說明其在轉(zhuǎn)錄水平的表達非常穩(wěn)定。此外,GV-2連續(xù)3代材料的Southern雜交均一致反映出T-DNA的單拷貝插入形式,說明目的基因在不同世代間整合的穩(wěn)定性良好。膠體金試紙條檢測結(jié)果說明目的蛋白在不同世代GV-2中穩(wěn)定表達,ELISA定量分析不但印證了定性檢測結(jié)果還發(fā)現(xiàn),目的蛋白在莖和葉中的含量較高,而在花和根中較低,這一結(jié)果與基因轉(zhuǎn)錄水平的變化趨勢相一致,且目的蛋白在不同世代間無顯著差異。草甘膦抗性檢測反映GV-2棉花目標(biāo)性狀在不同世代間均非常穩(wěn)定,表明該轉(zhuǎn)化體在生產(chǎn)應(yīng)用方面具有巨大潛力。總之,本研究為加快抗除草劑棉花的安全評價提供了有力的支撐,為我國抗除草劑棉花新品種突破跨國公司的壟斷奠定了基礎(chǔ)。
參考文獻
[1] 劉培磊,徐琳杰,葉紀(jì)明,等.我國農(nóng)業(yè)轉(zhuǎn)基因生物安全管理
現(xiàn)狀[J].生物安全學(xué)報,2014,23(4):297-300.
LIU P L, XU L J, YE J M, et al .. Administration on the
biosafety of agricultural GMOs in China [J]. J. Biosafety, 2014,
23(4):297-300.
[2] LIU Y G, WHITTIER R F. Thermal asymmetric interlaced
PCR: automatable amplification and sequencing of insert end
fragments from P1 and YAC clones for chromosome walking [J].
Genomics, 1995, 25(3):674-681.
[3] LIU Y G, MITSUKAWA N, OOSUMI T, et al .. Efficient
isolation and mapping of Arabidopsis thaliana T-DNA insert
junctions by thermal asymmetric interlaced PCR [J]. Plant J.,
1995, 8(3):457-463.
[4] LIU Y G, CHEN Y. High-efficiency thermal asymmetric
interlaced PCR for amplification of unknown flanking
sequences [J]. Biotechniques, 2007, 43(5):649-652.
[5] TAN J T, GONG Q Z, YU S C, et al .. A modified highefficiency
thermal asymmetric interlaced PCR method for
amplifying long unknown flanking sequences [J]. Genet.
Genomics, 2019, 46(7):363-366.
[6] WILLIAMS-CARRIER R, STIFFLER N, BELCHER S, et al ..
Use of Illumina sequencing to identify transposon insertions
underlying mutant phenotypes in high-copy mutator lines of
maize [J]. Plant J., 2010, 63(1):167-177.
[7] SIDDIQUE K, WEI J J, LI R, et al .. Identification of T-DNA
insertion site and flanking sequence of a genetically modified
maize event IE09S034 using next-generation sequencing
technology [J]. Mol. Biol., 2019, 61(9):694-702.
[8] KOVALIC D, GARNAAT C, GUO L, et al .. The use of next
generation sequencing and junction sequence analysis
bioinformatics to achieve molecular characterization of crops
improved through modern biotechnology [J]. Plant Genome,
2012, 5(3):149-163.
[9] GUO B F, GUO Y, HONG H L, et al.. Identification of genomic
insertion and flanking sequence of G2-EPSPS and GAT transgenes
in soybean using whole genome sequencing method [J/OL]. Front.
Plant Sci., 2016, 12(7): 1009 [2021-06-15]. https://doi.org/
10.3389/fpls.2016.01009.
[10] WAHLER D, SCHAUSER L, BENDIEK J, et al .. Next-generation
sequencing as a tool for detailed molecular characterisation of
genomic insertions and flanking regions in genetically modified
plants: a pilot study using a rice event unauthorised in the EU [J].
Food Anal. Methods, 2013, 6(6):1718-1727.
[11] PARK D, PARK S H, BAN Y W, et al .. A bioinformatics
approach for identifying transgene insertion sites using whole
genome sequencing data [J]. BMC Biol., 2017, 17(1):67-71.
[12] PARK D, KIM D, JANG G, et al.. Efficiency to discovery
transgenic loci in GM rice using next generation sequencing whole
genome re-sequencing [J]. Genomics Inform., 2015, 13(3):81-85.
[13] INAGAKI S, HENRY I M, LIEBERMAN M C, et al .. Highthroughput
analysis of T-DNA location and structure using
sequence capture [J/OL]. PloS One, 2015, 10(10): e0139672
[2021-06-15]. https//doi.org/10.1371/journal.pone.0139672.
[14] 孫紅煒,徐曉輝,李凡,等.轉(zhuǎn)基因玉米雙抗12-5-21的抗蟲性
及對草甘膦的耐受性 [J].生物安全學(xué)報, 2021, 30(1):43-49.
SUN H W, XU X H, LI F, et al .. Insect resistance and
glyphosate tolerance of transgenic maize double-resistance
12-5-21 [J]. J. Biosafety, 2021, 30(1):43-49.
[15] 李娜,曹越平.轉(zhuǎn)基因大豆SHZD32-01對草甘膦的抗性及草
甘膦除草效果研究 [J].大豆科學(xué),2018,37(3):408-414.
LI N, CAO Y P. Study on the resistance of genetically modified
soybean SHZD32-01 to glyphosate and the herbicidal effect of
glyphosate [J]. Soybean Sci., 2018, 37(3):408-414.
[16] 陸國清,王春玲,郝宇瓊,等.轉(zhuǎn)G10eve 基因棉花的獲得及草
甘膦抗性初探[J].棉花學(xué)報, 2018,30(1):21-28.
LU G Q, WANG C L, HAO Y Q, et al .. Obtainment of G10eve
transgenic cotton and preliminary study on glyphosate
resistance [J]. Cotton Sci., 2018, 30(1):21-28.
[17] CLARKE J D. Cetyltrimethyl ammonium bromide (CTAB)
DNA miniprep for plant DNA isolation [J/OL]. Cold Spring
Harbor Protocols., 2009(3):pdb.prot5177 [2021-06-15]. https://
doi.org/10.1101/pdb.prot5177.
[18] GEBBIE L. Genomic southern blot analysis [J]. Mol. Biol.,
2014, 109(9):159-177.
[19] 王園園,王敏,相世剛,等.全球抗除草劑轉(zhuǎn)基因作物轉(zhuǎn)化事
件分析 [J].農(nóng)業(yè)生物技術(shù)學(xué)報, 2020, 46(11):1703-1710.
WANG Y Y, WANG M, XIANG S G, et al .. Analysis of global
herbicide-resistant transgenic crop transformation events [J]. J.
Agric. Biotechnol., 2020, 46(11):1703-1710.
[20] 馬碩,焦悅,楊江濤,等.基因組測序技術(shù)解析耐除草劑轉(zhuǎn)基因
水稻G2-7的分子特征[J].作物學(xué)報,2020,46(11):1703-1710.
MA S, JIAO Y, YANG J T, et al.. Genome sequencing technology
parsing herbicide resistant transgenic rice molecular characteristics
of the G2-7 [J]. Acta Agron. Sin., 2020, 46(11):1703-1710.
[21] B·貝達格爾, A·德科希科, R·N·比奇,等.木薯葉脈花葉
病毒啟動子及其應(yīng)用: ZL97197430.6. [P]. 19990915.
(責(zé)任編輯:張冬玲)

