燕麥根際土壤細菌多樣性對鹽脅迫的響應
李峰 殷叢培 殷冉 王凡 韓永亮 楊志敏 劉建成

摘要:為探究燕麥(Avena sativa L.)在不同鹽脅迫處理下根際土壤微生物的群落多樣性及變化特征,選取領袖(Souris,S)和愛沃(Everleaf,E)2個燕麥品種為試驗材料,分別設置0(Y0)、3(Y1)、6(Y2)和9(Y3) g?kg-1NaCl脅迫處理。采用高通量測序技術對不同鹽脅迫處理下燕麥根際土壤微生物進行測序,分析微生物群落多樣性及其與土壤鹽脅迫的相關性。結果表明,2個燕麥品種根際土壤細菌群落的多樣性在4種鹽脅迫處理下存在差異,其中S-Y2的群落豐度最高,S-Y3的多樣性最豐富。在不同分類水平上,細菌變形菌門(Proteobacteria)、放線菌綱(Actinobacteria)、根瘤菌目(Rhizobiales)、norank_c_Subgroup_6科和norank_c_Subgroup_6 屬的相對豐度較高。鹽脅迫影響燕麥根際微生物的群落組成,隨著鹽脅迫程度的增加,其菌落組成的相對豐度發生顯著變化。通過對操作分類單元(OTU)豐度的16S功能預測和COG、KEGG代謝通路數據庫對比發現,燕麥根際微生物的功能富集于新陳代謝、遺傳信息處理、環境信息處理、細胞過程和生物體系統等。由此表明,根際微生物在燕麥生長和響應鹽脅迫中起重要作用,為進一步挖掘和利用根際功能微生物奠定了理論基礎。
關鍵詞:燕麥;根際;16S;微生物群落結構;鹽脅迫doi:10.13304/j.nykjdb.2021.0906
中圖分類號:S512.6 文獻標志碼:A 文章編號:10080864(2023)01015313
鹽堿地是干旱和半干旱地區生態系統的重要組成部分,我國鹽漬化土地總面積占全國可利用土地面積的4.88%,約3 600 萬hm2[1]。工業進程的發展、農業化肥和農藥的不當施用等人類活動[2],致使我國每年約有1%~2% 的農業生產耕地鹽漬化[3]。過高的土壤鹽分不但會導致植物的離子滲透脅迫[4],還會引起氧化應激反應、營養失調和器官衰老,甚至死亡。大多數植物對鹽脅迫較為敏感,長久以來,通過對植物耐鹽相關生理和分子機制的研究來提高農作物耐鹽性、培育耐鹽作物品種是保障鹽漬區作物產量的基本手段[5]。
在鹽脅迫下,植物可能會啟動多種防御策略來降低鹽脅迫對自身造成的傷害,如形成能分泌鹽分的腺體[6],重建細胞離子、滲透和活性氧平衡[7]以及調節發育進程[8]等。植物的耐鹽性除由遺傳因素決定外[9],微生物在植物抵御逆境脅迫中也起到重要作用[1011]。植物根際微生物可以通過調節植物根系的離子穩態、產生植物激素、促進根系滲透物質積累、提高植物抗氧化活性和提高營養物質吸收等過程來改善植物的耐鹽性[12]。植物根際微生物群落結構多樣性具有特異性,同樣土壤環境中的不同植物和不同土壤環境中的同種植物其根際微生物菌落結構均存在差異[13]。因此,研究鹽脅迫下植物根際微生物菌落結構的變化,對了解根際微生物參與植物應對非生物脅迫的作用機理至關重要。
土壤細菌可以降低植物體內Na+含量[14],植物根際促生細菌(plant growth promoting rhizobacteria,PGPR)可以提高植物對K+的吸收以及對Na+的排斥,從而提高植物體內的K+/Na+ 值[15]。小麥(Triticum aestivum L.)種子接種Nesterenkoniarhizosphaerae wp-8,可通過調控幼苗的抗氧化系統緩解鹽脅迫對植株造成的損傷,促進幼苗生長和根系發育[16]。混合接種根瘤菌(Rhizobia leguminumRhOF125)、膠質類芽孢桿菌(Paenibacillusmucilaginosus BLA7)和草木犀劍菌(Ensifer melilotiRhOL1)能夠顯著提高蠶豆(Vicia faba L.)的耐鹽性,表明根際微生物對植物響應鹽脅迫有直接或間接的作用[17]。根際微生物在增強植物對鹽脅迫的適應性方面有重要作用,植物招募土壤有益菌以提高其抵御鹽脅迫的能力[18]。
燕麥是禾本科、燕麥屬,一年生特色糧飼兼用作物[19],具有一定的耐鹽堿能力,其耐鹽性的研究主要集中在種子萌發、幼苗生長和生理響應等方面,關于燕麥鹽脅迫下根際微生物變化的研究甚少。因此,本研究基于16S rRNA高通量測序分析不同鹽脅迫下燕麥根際土壤細菌群落結構的差異,旨在評價鹽脅迫對燕麥根際細菌群落組成的影響,為利用根際微生物提高作物的耐鹽性奠定理論基礎。
1 材料和方法
1.1 供試材料
以領袖(Souris,S)和愛沃(Everleaf,E)2 個飼用燕麥品種為供試材料,均由張家口市農科學院畜牧研究所提供。供試土壤采自河北省張家口市農業科學院畜牧研究所(40°68′N,114°93′E),土壤全碳20.31 g·kg-1、全氮0.98 g·kg-1、全鉀2.45 g·kg-1、速效氮163.5 mg·kg-1、速效磷1.53 mg·kg-1、速效鉀125.8 mg·kg-1,pH 7.4。
1.2 試驗設計和樣品采集
將取自田間耕層11—30 cm 的土壤風干,過1 mm 篩后裝盆(直徑11.5 cm,高9.7 cm),每盆裝土量為800 g,設置0 (Y0)、3(Y1)、6(Y2)和9 g?kg-1 NaCl(Y3)共4種鹽脅迫處理。挑選發育良好、籽粒飽滿、大小一致的種子,用75%的酒精消毒15 min,1%(質量分數)HgCl2消毒30 min,用蒸餾水反復沖洗干凈后浸泡10 h,于人工氣候箱內恒溫培養2 d,將發芽整齊、一致的幼苗移植到不同鹽處理的塑料盆中,每盆種植3株,置于25~28 ℃植物培養室中進行培養(光強600 μmol·m-2·s-1,光照12 h/黑暗12 h,相對濕度70%),采用隨機區組設計,每個處理設10盆重復。試驗使用土壤水分-溫度-鹽分記錄儀(浙江托普云農科技股份有限公司,TZS-ECW-GT)對土壤含鹽量和含水量進行監測,每2 d補充1次。
各處理均在處理21 d后,采用“抖根法”收集根際土壤樣品[20],樣品采集后及時裝入無菌塑封袋中,?80 ℃保存。將燕麥品種領袖在不同鹽脅迫下的土壤樣本分別命名為S-Y0、S-Y1、S-Y2和S-Y3;燕麥品種愛沃在不同鹽脅迫下的土壤樣本分別命名為E-Y0、E-Y1、E-Y2和E-Y3。
1.3 土壤DNA 的提取及高通量測序
采用試劑盒E.Z.N.A.? Soil DNA Kit (OmegaBio-tek, Norcross, GA, USA)提取燕麥根際土壤細菌總DNA。純化后采用1.5%瓊脂糖凝膠電泳和Nanodrop 2000 分光光度計(Thermo Scientific,Wilmington, USA)檢測DNA 的純度和含量。以提取的DNA 為模板,利用引物338F(5-ACTCCTACGGGAGGCAGCAG-3)和806R (5-GGACTACHVGGGTWTCTAAT-3)[21]對土壤細菌16S rRNA V3~V4區進行擴增。最后,在IlluminaMiSeq平臺(Illumina, San Diego, USA)進行雙末端測序。
1.4 數據分析
使用QIIME v1.8.0處理原始序列數據[22],進行操作分類單元(operational taxonomic units, OTU)的聚類分析[23],對OTUs代表序列進行物種注釋,并構建稀釋性曲線,計算 Alpha多樣性指數,包括Chao1指數、ACE指數、Shannon指數和Simpson指數[24]。通過非度量多維尺度(non-metric multidimensionalscaling, NMDS)和主坐標分析(principal co-ordinatesanalysis PCoA)進行β 多樣性分析。基于PICRUSt(phylogenetic investigation of communities byreconstruction of unobserved states)方法對樣本中微生物群落的功能組成進行預測[24] 。
2 結果與分析
2.1 根際微生物測序數據分析
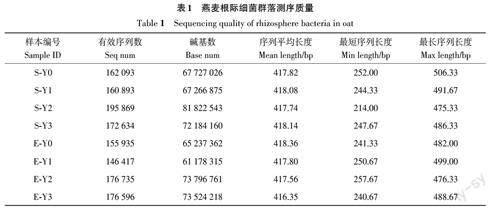
由表1可知,8個供試土壤樣本共獲得有效序列1 347 172條,其中樣本S-Y2的有效序列數最多,為195 869 條;樣本E-Y1 的有效序列數最少,為146 417條。不同處理樣本平均長度為416~419 bp,平均417.73 bp。
2.2 鹽脅迫對燕麥根際細菌Alpha多樣性的影響
稀釋性曲線可以用來比較不同樣本中微生物種類的豐富度,在抽取相同序列的條件下,S-Y1、S-Y2和E-Y0樣本的OTU數較多,說明S-Y1、S-Y2和E-Y0樣本中的豐富度較高(圖1A)。Sobs指數反映了樣本中細菌群落物種豐富度的實際觀測值,結果(圖1B)表明,不同脅迫處理表現為Y2>Y0>Y1>Y3,且不同處理間差異顯著(P<0.05),表明鹽脅迫對燕麥根際細菌群落的多樣性有顯著影響。維恩圖分析(圖1C)顯示,不同根際土壤樣本中共有的OTU為1 668個,其中樣本S-Y0和E-Y0特有OTU分別為264和220個;鹽處理后各樣本的OTU數量明顯下降,表明鹽脅迫對根際土壤細菌群落結構有顯著影響。
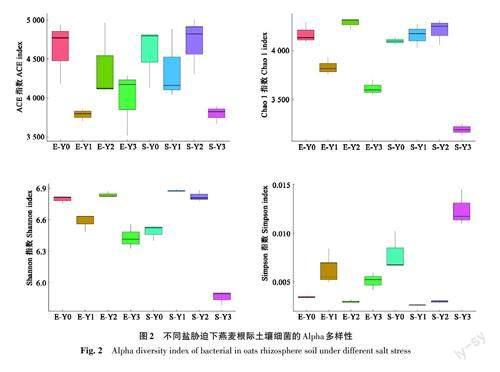
如圖2所示,鹽脅迫改變了燕麥根際細菌群落Alpha多樣性,不同指數在不同的品種間表現不一致。其中,ACE指數和Shannon指數的變化趨勢在品種E中基本相同,而在品種S中則不同;Chao 1指數和Simpson 指數的變化呈相反趨勢。由此表明,鹽脅迫對燕麥根際細菌群落的豐度和多樣性影響顯著。
2.3 鹽脅迫對燕麥根際細菌Beta 多樣性的影響
NMDS分析(圖3A)顯示,Y0和Y1根際土壤的細菌群落結構較為相似,Y2和Y3與其差異較大。PCoA 分析(圖3B)顯示,PC1(47.22%)和PC2(21.2%)分別由品種因子和鹽脅迫因子貢獻;不同處理的土壤樣本分布于不同象限,表明其細菌群落組成具有明顯差異。S-Y0和S-Y2與PC1和PC2均呈正相關;S-Y1、E-Y0和E-Y2與PC1呈正相關,與PC2呈負相關;E-Y3與PC1和PC均呈負相關;S-Y3與PC1呈負相關,與PC2呈正相關(圖3B)。說明鹽脅迫和品種均影響根際土壤微細菌的群落結構。
將供試樣本按品種和鹽脅迫程度進行分組,通過相似性分析(analysis of similarities ANOSIM),結果(圖3C 和D)表明,組間差異均達到顯著水平(P=0.001),其中品種分組的R值為0.210 4,鹽脅迫程度分組的R值則為0.535 3,表明鹽脅迫對燕麥根際土壤樣本細菌群落多樣性的影響更大。
2.4 鹽脅迫對燕麥根際細菌群落結構的影響
對測序結果進行注釋,共獲得7 095個OTU,歸屬33個門、97個綱、273個目、470個科、919個屬。
在門水平(圖4A), 變形菌門(Proteobacteria)、放線菌門(Actinobacteria)、酸桿菌門(Acidobacteria)、綠彎菌門(Chloroflexi)和擬桿菌門(Bacteroidetes)的相對豐度較高,分別為24.71%~50.8%、9.59%~20.29%、5.67%~17.30%、5%~11.66%和6.11%~14.99%,累計相對豐度平均為83.18%;其次為芽單胞菌門(Gemmatimonadetes)、厚壁菌門(Firmicutes)、髕骨細菌門(Patescibacteria)、藍藻細菌門(Cyanobacteria)和疣微菌門(Verrucomicrobia),相對豐度分別為2.55%~4.58%、0.93%~4.79%、1.49%~3.73%、0.85%~6.09%和0.66%~7.77%。鹽脅迫顯著提高了Proteobacteria、Bacteroidetes和Patescibacteria的相對豐度,而Actinobacteria、Acidobacteria、Chloroflexi、Gemmatimonadetes 和Verrucomicrobia的相對豐度顯著降低。其中,Proteobacteria在樣本S-Y3中的相對豐度較S-Y0顯著增加102.67%;Firmicutes 在S-1 和S-Y3 樣本中的相對豐度較S-Y0 分別顯著增加321.51% 和288.17%;Patescibacteria在S-Y2樣本中的相對豐度較S-Y0顯著增加145.39%;Gemmatimonadetes 在E-Y3 樣本中的相對豐度較E-Y0顯著降低65.55%。
在綱水平上(圖4B), 放線菌綱(Actinobacteria)、α- 變形菌綱(Alphaproteobacteria)、γ - 變形菌綱(Gammaproteobacteria)、擬桿菌綱(Bacteroidia)、Subgroup_6、芽單胞菌綱(Gemmatimonadetes)、δ-變形菌綱(Deltaproteobacteria)、Blastocatellia_Subgroup_4、綠彎菌綱(Chloroflexia)和厭氧繩菌綱(Anaerolineae)為優勢菌綱,相對豐度分別為9.59%~20.29%、11.82%~22.74%、9.11%~25.29%、5.84%~14.71%、3.13%~10.37%、2.55%~4.58%、2.48%~5.05%、1.57%~4.25%、1.55%~3.76% 和1.67%~4.32%,累計相對豐度的平均值為80.74%。其次是芽孢桿菌綱(Bacilli)、產氧光細菌綱(Oxyphotobacteria)、疣微菌綱(Verrucomicrobiae)、Saccharimonadia 和KD4-96,相對豐度分別為0.82%~4.63%、0.77%~5.97%、0.69%~7.77%、0.88%~2.16%和0.49%~1.63%。鹽脅迫顯著提高了Alphaproteobacteria、Gammaproteobacteria 和Bacteroidia的相對豐度,而Actinobacteria、Subgroup_6、Deltaproteobacteria 和Verrucomicrobiae 的相對豐度顯著降低。Actinobacteria、Gemmatimonadetes、Deltaproteobacteria、Chloroflexia、Bacilli 和KD4-96均在Y1處理下相對豐度最高。
在目水平上(圖4C), 根瘤菌目(Rhizobiales)、norank_c__Subgroup_6、Betaproteobacteriales、鞘脂單胞菌目(Sphingomonadales)、噬纖維菌目(Cytophagales)、假單胞菌目(Pseudomonadales)、微球菌目(Micrococcales)、Chitinophagales、芽孢桿菌目(Bacillales)和芽單胞菌目(Gemmatimonadales)為優勢菌目,相對豐度分別為5.29%~14.3%、3.1%~10.21%、3.19%~5.31%、3.24%~5.19%、2.86%~7.34%、0.36%~8.73%、1.53%~5.41%、2.08%~3.32%、0.82%~4.63% 和1.6%~2.87%,其相對豐度之和平均為42.14%;其次是熱微菌目(Thermomicrobiales)、黏球菌目(Myxococcales)、Pyrinomonadales、Propionibacteriales 和SBR1031,相對豐度分別為1.34%~3.11%、1.2%~2.52%、1.03%~2.67%、1.07%~2.99% 和1.30%~3.35%。
鹽脅迫顯著降低了norank_c_Subgroup_6 和Betaproteobacteriales 的相對豐度,而Rhizobiales、Pseudomonadales 和Cytophagales 的相對豐度顯著升高。Gemmatimonadales、Thermomicrobiales和Myxococcales在Y1處理下的相對豐度均顯著高于其他處理。
在科水平上(圖4D),norank_c_Subgroup_6、鞘脂單胞菌科(Sphingomonadaceae)、假單胞菌科(Pseudomonadaceae)、根瘤菌科(Rhizobiaceae)、芽單胞菌科(Gemmatimonadaceae)、芽孢桿菌科(Bacillaceae)、伯克氏菌科(Burkholderiaceae)、甲殼菌科(Chitinophagaceae)、Microscillaceae和梭菌科(Pyrinomonadaceae)為優勢菌科,相對豐度分別為3.1%~10.21%、3.24%~3%、0.36%~8.72%、2.02%~6.73%、1.6%~2.87%、0.59%~4.22%、1.57%~3.16%、1.65%~2.79%、1.5%~2.64% 和1.03%~2.67%,其樣本平均相對豐度均在2.03%以上,相對豐度之和平均為31.36%;其次是Devosiaceae、JG30-KF-CM45、類諾卡氏菌科(Nocardioidaceae)、微球菌科(Micrococcaceae)和鏈霉菌科(Streptomycetaceae),相對豐度分別為0.60%~6.59%、1.00%~2.46%、0.96%~2.72%、0.57%~4.28% 和0.81%~3.88%。鹽脅迫顯著降低了norank_c_Subgroup_6、Bacillaceae、Gemmatimonadaceae 和Burkholderiaceae 的相對豐度,而Pseudomonadaceae、Rhizobiaceae和Devosiaceae的相對豐度顯著升高,其中JG30-KF-CM45在Y1和Y2處理下的相對豐度顯著高于Y0和Y7處理。
在屬水平(圖5),其相對豐度均值排名前15的菌屬中,品種S中分別有8(Y0)、7(Y1)、8(Y2)和8(Y3)個屬的相對豐度高于品種E。在Y0、Y1、Y2處理下,norank_c__Subgroup_6、RB41 和節桿菌屬(Arthrobacter)均表現為在品種S中的相對豐度更高;在Y3處理下,norank_c_Subgroup_6 和RB41則表現為在品種E中的相對豐度更高。假單胞菌屬(Pseudomonas)在Y3處理下表現為在品種S中的相對豐度更高,而在Y0、Y1、Y2處理下均為在品種E 中的相對豐度更高;鞘脂單胞菌屬(Sphingomonas)和norank_f_Gemmatimonadaceae在不同處理下均表現為在品種E 中的相對豐度更高。
2.5 鹽脅迫下燕麥根際土壤細菌系統發生進化分析及功能預測
系統發生的推斷能夠揭示有關生物進化過程的順序,有助于了解生物進化歷史和機制。燕麥根際土壤細菌中最豐富的20個屬主要歸屬于變形菌門(Proteobacteria) 、放線菌門(Actinobacteria)、綠彎菌門(Chloroflexi)和芽單胞菌門(Gemmatimonadetes)等(圖6A),主要菌屬為norank_Subgroup_6 和假單胞菌屬 (Pseudomonas),其次是norank_Gemmatimonadaceae、RB41、芽孢桿菌屬(Bacillus)和鞘脂單胞菌屬(Sphingomonas)。
為了更好地了解燕麥根際細菌群落的作用,基于PICRUSt分析平臺進行功能預測,將獲得的OTU豐度表與相關數據庫進行比對,獲得相應的COG 及KO(kyoto encyclopedia of genes and genomes?ontology)功能信息及其豐度。
COG結果(圖6B)表明,一些代謝和基本生命活動相關功能的細菌菌群在所有鹽脅迫處理的土壤樣本中均有所富集,表明鹽脅迫影響了燕麥根際細菌微生物的代謝和生命活動。基因注釋結果中除功能未知外,氨基酸運輸代謝最多;其次為一般代謝、能量產生與轉化、細胞壁和細胞膜生物合成、信號轉導、轉錄、碳水化合物轉錄與運輸、無機離子的轉運和代謝;而染色質結構與動力學、RNA加工與修飾、細胞骨架和胞外結構較少。
運用PICRUSt軟件分析鹽脅迫下燕麥根際細菌代謝通路在3 個水平的信息及其豐度,結果(圖7A和7B)表明,一級代謝通路有6條,依次為新陳代謝(51.37%)、遺傳信息處理(15.66%)、環境信息處理(14.14%)、細胞過程(3.93%)、人類疾病(0.95%)、生物體系統(0.8%)和功能未分類基因(13.16%);二級代謝通路有41條,主要包括膜轉運(11.82%)、氨基酸代謝(10.97%)、糖代謝(10.29%)、復制和修復(6.8%)和能量代謝(5.82%);三級代謝通路有406條,主要包括次級代謝產物的生物和合成(ko 01 110)、不同環境中的微生物代謝(ko 01 120)、氨基酸生物合成(ko 01 230)、碳代謝(ko 01 200)、ABC 轉運蛋白(ko 02 010)、核糖體(ko 03 010)、雙組分系統(ko 02020)、嘌呤代謝(ko 00 230)、細菌的聚量效應(ko 02 024)和氧化磷酸化(ko 00 190)。
3 討論
隨著高通量測序技術的突破和生物信息學的發展,土壤微生物組學的研究得到了迅速發展,為研究土壤微生物、促進土壤健康和提高作物生產提供了有力的工具[25]。Fan等[26]發現,關鍵土壤微生物在維持土壤營養元素循環和作物高產方面具有重要作用。土壤微生物在土壤生態系統的調節、支持和供應功能中起著關鍵作用,是聯系陸地生態系統中地上和地下部分的關鍵紐帶[27]。
鹽脅迫對植物根際微生物群落結構有顯著的影響,本研究發現,鹽脅迫條件下土壤細菌樣本的OUT數量差異較大,表現為Y0>Y1>Y2>Y3,即隨著鹽脅迫程度的加劇,樣本中檢測到的OTU數量逐漸降低;稀釋曲線分析發現樣本E-Y0、S-Y1和S-Y2的細菌群落豐富度高于其他樣本;Sobs指數表現為Y2>Y0>Y1>Y3,且不同程度脅迫間存在顯著差異;多樣性分析表明鹽脅迫對燕麥根際細菌群落結構和多樣性有顯著影響,土壤微生物多樣性越高,其生態功能越強,有利于作物高產和抵御不良環境脅迫[28]。Alpha多樣性反映了土壤微生物的物種豐度及多樣性。本研究表明,樣本S-Y2的群落豐度最高,樣本S-Y3 的多樣性最豐富。
Beta多樣性用來描述不同樣本微生物群落間的差異,NMDS分析結果表明Y0和Y1處理下細菌的群落組成相似性較高,而Y2和Y3處理下細菌的群落組成差異較大。PCoA分析發現,各處理樣本分布于不同象限,表明各處理的細菌群落組成具有明顯差異。ANOSIM分析表明鹽脅迫、品種類型對根際土壤微生物菌群類型均有影響,且鹽脅迫對燕麥根際土壤細菌群落的多樣性的影響更顯著。Gao等[29]研究發現,低鹽脅迫對高粱(Sorghumbicolor L.)根際土壤細菌多樣性的抑制小于高鹽脅迫,不同品種間細菌多樣性差異不明顯。本研究也發現,不同鹽脅迫下燕麥根際土壤細菌多樣性及群落組成存在差異,鹽脅迫程度不同是造成燕麥根際土壤細菌群落多樣性差異的主要原因。
本研究表明,變形菌門(Proteobacteria)、放線菌門(Actinobacteria)、酸桿菌門(Acidobacteria)、綠彎菌門(Chloroflexi)、Bacteroidetes、芽單胞菌門(Gemmatimonadetes)、厚壁菌門(Firmicutes)、Patescibacteria、藍藻門(Cyanobacteria)和疣微菌門(Verrucomicrobia)為燕麥根際土壤細菌的主要優勢菌門,與前人研究結果一致[3031];在其他分類水平下,燕麥根際細菌優勢菌群與汪焱等[32]研究結果基本一致。鹽脅迫使燕麥根際土壤中變形菌門(Proteobacteria)的相對豐度顯著提高,在不同鹽脅迫處理中均為最優勢菌門。研究表明,變形菌門與土壤有機碳含量顯著相關,其豐度的增多可更有效地固定氮源[32]。在變形菌門內主要包含α-變形菌綱(α -proteobacteria) 、β - 變形菌綱(β-proteobacteria)、δ-變形菌綱(δ-proteobacteria)、ε-變形菌綱(ε-proteobacteria)、γ-變形菌綱(γ-proteobacteria)等。Valenzuela-encinas 等[34]研究發現,無論在高鹽還是低鹽土壤中,變形菌門的優勢類群都是γ-變形菌綱,而在中等鹽度土壤中優勢類群是α-變形菌綱。在本研究中,不同鹽脅迫下各樣本根際細菌的最優勢菌綱均為α-變形菌綱。α-變形菌綱常以胞內的生活方式作為植物互惠者或植物/動物病原體,并能在營養匱乏的生境中生長。無論鹽度高低,γ-變形菌綱的相對豐度均較高。酸桿菌門(Acidobacteria)在燕麥根際土壤中的相對豐度也較高,其門下菌類大多數為腐生菌,在有機物分解過程中起促進作用,具有共生固氮和解磷作用[35],也是世界上分布最廣、種類最豐富的細菌之一。綠彎菌門(Chloroflexi)能夠降解有機質,將糖和多糖發酵成有機酸,加快土壤中有機物的分解和吸收,具有較好的生物解磷作用,有助于硝酸鹽的分解[36]。放線菌門(Actinobacteria)可以在含有3.5% NaCl的培養基上生長[37],在有機物分解導電過程中有促進作用,以往從鹽土中分離的嗜鹽細菌大多屬于Actinobacteria。
芽孢桿菌屬(Bacillus)、假單胞菌屬(Pseudomonas)等能夠提高寄主對不同非生物脅迫環境的耐受性。Bacillus 為革蘭氏陽性菌,是嚴格需氧或兼性厭氧的有莢膜桿菌,該屬細菌的重要特性是能夠對不利條件產生具有特殊抵抗力的芽孢,芽孢是自然界已經發現的最具耐受性的細胞,處于休眠狀態的芽孢對熱、干燥、輻射、酸、堿和有機溶劑等具有極強的抵抗力,在作為植物促生菌或益生菌方面具有很大的潛力[38]。Pseudomonas 為直或稍彎的革蘭氏陰性桿菌,為無核細菌,以極生鞭毛運動,不形成芽孢,有極強分解有機物的能力,在植物促生與抗逆方面表現更突出,可增強植株對水分和營養的吸收,提高生長素、嗜鐵素、ACC脫氨酶等含量,參與調控植物諸多生理代謝功能,從而促進植物生長,提高植物的抗逆性[39],在提高棉花[40]、番茄[31]等植物的耐鹽性方面有重要作用。
本研究KEGG 代謝通路分析與COG 數據庫預測的結果基本一致。鹽脅迫影響了燕麥根際微生物群落的功能豐度譜,尤以次生代謝產物、聚糖和氨基酸代謝合成等相關功能基因豐度變化明顯。土壤微生物多樣性和生態系統功能多樣性呈顯著正相關,多樣化的土壤微生物群落能夠更好地改善農業生態系統[41]。
本研究發現,鹽脅迫是燕麥根際微生物群落組成顯著影響,優勢核心菌群可能在植物響應環境脅迫應答中起重要作用。應用核心菌種接種的微生物組工程技術可以直接調節微生物互作網絡,抑制有害微生物,同時招募功能微生物,從而提升作物抗逆性[15,18]。利用微生物間的互作,通過調控土壤微生物群落結構既能夠改良土壤,減少農藥和肥料的施用,又可以提高作物產量和抗逆性,降低農業生產中的資源消耗,緩解環境污染等問題,因此,利用微生物作為生物防治劑或生物修復劑在農業實踐中具有廣闊的應用前景。
參考文獻
[1] 李建國,濮勵杰,朱明,等.土壤鹽漬化研究現狀及未來研究
熱點[J].地理學報,2012,67(9):1233-1245.
LI J G, PU L J, ZHU M, et al .. The present situation and hot
issues in the salt-affected soil research [J]. Acta Geogr. Sin.,
2012, 67(9):1233-1245.
[2] MUNNS R, TESTER M. Mechanisms of salinity tolerance [J].
Ann. Rev. Plant Biol., 2008, 59(1):651-681.
[3] MEENA M D, YADAV R K, NARJARY B, et al .. Municipal
solid waste (MSW): strategies to improve salt affected soil
sustainability: a review [J]. Waste Manag., 2018, 84:38-53.
[4] YANG Y, GUO Y. Elucidating the molecular mechanisms
mediating plant salt-stress responses [J]. New Phytol., 2018,
217:523-39.
[5] 高玉坤,楊溥原,項曉冬,等.不同耐鹽高粱品種全生育期對
鹽脅迫的響應[J].華北農學報,2020,35(6):113-121.
GAO Y K, YANG P Y, XIANG X D, et al . Response of
different salt tolerant sorghum varieties to salt stress in the
whole growth period [J]. Acta Agric. Boreali-Sin., 2020, 35(6):
113-121.
[6] YUAN F, LENG B, WANG B. Progress in studying salt
secretion from the salt glands in recretohalophytes: how do plants
secrete salt? [J/OL]. Front Plant Sci., 2016, 7:977 [2021-09-10].
https://doi.org/10.3389/fpls.2016.00977.
[7] YANG Y, GUO Y. Unraveling salt stress signaling in plants [J].
J. Integr. Plant Biol., 2018, 60:796-804.
[8] KAZAN K, LYONS R. The link between flowering time and
stress tolerance [J]. J. Exp. Bot., 2015, 67:47-60.
[9] LOWRY D B, HALL M C, SALT D E, et al .. Genetic and
physiological basis of adaptive salt tolerance divergence
between coastal and inland Mimulus guttatus [J]. New Phytol.,
2009, 183:776-788.
[10] RODRIGUEZ P A, ROTHBALLER M, CHOWDHURY S P,
et al .. Systems biology of plant microbiome interactions [J].
Mol. Plant., 2019, 12:804-821.
[11] PAUL D, LADE H. Plant-growth-promoting rhizobacteria to
improve crop growth in saline soils: a review. [J]. Agron.
Sustain. Dev., 2014, 34:737-752.
[12] BADRI D V, VIVANCO J M. Regulation and function of root
exudates [J]. Plant Cell Environ., 2009, 32:666-681.
[13] CASTRILLO G, TEILXEIRA P, PAREDES S, et al .. Root
microbiota drive direct integration of phosphate stress and
immunity [J]. Nature, 2017, 543:513-518.
[14] LI H, LA S, ZHANG X, et al .. Salt-induced recruitment of
specific root-associated bacterial consortium capable of
enhancing plant adaptability to salt stress [J]. ISME J., 2021,
15:2865-2882.
[15] SERRANO R, RODRIGUEZ-NAVARRO A. Ion homeostasis
during salt stress in plants [J]. Curr. Opin. Cell Biol., 2001,
13(4):399-404.
[16] 王丹,趙亞光,張鳳華.耐鹽促生菌篩選、鑒定及對鹽脅迫小
麥的效應[J].麥類作物學報,2020,40(1):110-117.
WANG D, ZHAO Y G, ZHANG F H. Screening and
identification of salt-tolerant plant growth-promoting bacteria
and its promotion effect on wheat seedling under salt stress [J].
J. Triticeae Crops, 2020, 40(1):110-117.
[17] LOUBNA B, FATIMA E K, KHALID O, et al .. Phytobeneficial
bacteria improve saline stress tolerance in Vicia faba
and modulate microbial interaction network [J/OL]. Sci. Total
Environ., 2020, 729:139020 [2021-09-10]. https://doi.org/10.1016/j.
scitotenv.2020.139020.
[18] ZHAO S, LIU J, BANERJEE S, et al.. Biogeographical distribution
of bacterial communities in saline agricultural soil [J/OL].
Geoderma, 2019, 361(1):114095 [2021-09-10]. https://doi.org/
10.1016/j.geoderma.2019.114095.
[19] 陳曉晶,劉景輝,楊彥明,等.鹽脅迫對燕麥葉片生理指標和
差異蛋白組學的影響[J].作物學報, 2019, 45(9):1431-1439.
CHEN X J, LIU J H, YANG Y M, et al .. Effects of salt stress on
physiological indexes and differential proteomics of oat leaf [J].
Acta Agron. Sin., 2019, 45(9):1431-1439.
[20] CASTRILLO G, TEILXEIRA P, PAREDES S, et al .. Root
microbiota drive direct integration of phosphate stress and
immunity [J]. Nature, 2017, 543:513-518.
[21] MAGOC T, SALZBERG S L. FLASH: fast length adjustment of
short reads to improve genome assemblies [J]. Bioinformatics,
2011, 27:2957-2963.
[22] CAPORASO J G, KUCZYNSKI J, STOMBAUGH J, et al ..
QIIME allows analysis of high-throughput community sequencing
data [J]. Nat. Methods, 2010, 7:335-336.
[23] CHAO A, SHEN T J. Nonparametric prediction in species
sampling [J]. J. Agric. Biol. Environ. Statist., 2004, 9:253-269.
[24] BAI Y, M?LLER D B, SRINIVAS G, et al .. Functional overlap
of the Arabidopsis leaf and root microbiota [J]. Nature, 2015,
528:364-369.
[25] RAAIJMAKERS J M, MAZZOLA M. Soil immune responses [J].
Science, 2016, 352:1392-1393.
[26] FAN K, DELGADO-BAQUERIZO M, GUO X, et al ..
Biodiversity of key-stone phylotypes determines crop
production in a 4-decade fertilization experiment [J]. ISME J.,
2020, 15:550-561.
[27] DELGADO-BAQUERIZO M, MAESTRE F T, REICH P B,
et al .. Microbial diversity drives multifunctionality in terrestrial
ecosystems [J/OL]. Nat. Commun., 2016, 7: 10541 [2021-09-
10]. https://doi.org/10.1038/ncomms10541.
[28] CHEN Q L, DING J, ZHU Y G, et al .. Soil bacterial taxonomic
diversity is critical to maintaining the plant productivity [J/OL].
Environ. Int., 2020, 140:105766 [2021-09-10]. https://doi.org/
10.1016/j.envint.2020.105766.
[29] GAO Y K, CUI J H, REN G Z, et al .. Changes in the rootassociated
bacteria of sorghum are driven by the combined
effects of salt and sorghum development [J/OL]. Environ.
Microbiome, 2021, 16: 14 [2021-09-10]. https://doi.org/10.1186/
s40793-021-00383-0.
[30] YANG Y, SHAO T Y, LONG X H, et al .. Microbiome structure
and function in rhizosphere of Jerusalem artichoke grown in
saline land [J/OL]. Sci. Total Environ., 2020, 724(168):138259
[2021-09-10]. https://doi.org/10.1016/j.scitotenv.2020.138259.
[31] 蘭汝佳.根際耐鹽促生菌的篩選及其對番茄耐鹽性的調控
研究[D].南京:南京農業大學, 2019.
LAN R J. Screening of salt-tolerant rhizosphere-promoting
bacteria and its regulation on salt tolerance of tomato [D].
Nanjing: Nanjing Agricultural University, 2019.
[32] 汪焱,張英,蘇貝貝,等.高寒區不同地域燕麥根際土壤微生
物多樣性研究[J].草地學報,2020,28(2):358-366.
WANG Y, ZHANG Y, SU B B, et al .. Study on microbial
diversity of rhizosphere soil of oat in different areas in alpine
region [J]. Acta Agrestia Sin., 2020, 28(2):358-366.
[33] WAGG C, SCHLAEPPI K, BANERJEE S, et al .. Fungalbacterial
diversity and microbiome complexity predict
ecosystem functioning [J/OL]. Nat. Commun., 2019, 10:4841
[2021-09-10]. https://doi.org/10.1038/s41467-019-12798-y.
[34] VALENZUELA-ENCINAS C, NERIA-GONZ?LEZ I,
ALC?NTARA-HERN?NDEZ R J, et al .. Changes in the
bacterial populations of the highly alkaline saline soil of the
former lake Texcoco (Mexico) following flooding [J].
Extremophiles, 2009, 13(4):609-621.
[35] WARD N L, CHALLACOMBE J F, JANSSEN P H, et al ..
Three genomes from the phylum Acidobacteria provide insight
into their lifestyles in soils [J]. Appl. Environ. Microbiol.,
2009, 75(7):2046-2056.
[36] KRAGELUND C, LEVANTESI C, BORGER A. Identity
abundance and ecophysiology of filamentous Chloroflexi
species present in activated sludge treatment plants [J]. FEMS
Microbiol. Ecol., 2007, 59:671-682.
[37] MALDONADO L A, FENICAL W, JENSEN P R, et al ..
Salinispora arenicola gen. nov. sp. nov. and Salinispora tropica
sp. nov. obligate marine actinomycetes belonging to the family
Micromono sporaceae [J]. Int. J. Syst. Evol. Microbiol, 2005,
55(5):1759-1766.
[38] VARDHARAJULA, ALI S Z, GROVER M, et al .. Droughttolerant
plant growth promoting Bacillus spp.: effect on growth,
osmolytes, and antioxidant status of maize under drought stress [J].
J. Plant Interact., 2011, 6(1):1-14.
[39] RAJKUMAR M, BRUNO L B, BANU J R. Alleviation of
environmental stress in plants: the role of beneficial
Pseudomonas spp. [J]. Crit. Rev. Environ. Sci. Technol., 2017,
47(6):372-407.
[40] EGAMBERDIEV D, JABBOROV D, HASHEM A. Pseudomonas
induces salinity tolerance in cotton (Gossypium hirsutum) and
resistance to Fusarium root rot through the modulation of indole-3-
acetic acid [J]. Saudi J. Biol. Sci., 2015, 22(6):773-779.
[41] FR?C M, HANNULA S E, BE?KA M, et al .. Fungal
biodiversity and their role in soil health [J/OL]. Front.
Microbiol., 2018, 9:707 [2021-09-10]. https://doi.org/10.3389/
fmicb.2018.00707.
(責任編輯:張冬玲)

